文档内容
2024-2025学年高二化学下学期月考试卷
(考试时间:90分钟 试卷满分:100分)
出题人:杨辉峰 2025 03
可能用到的相对原子质量:H-1 O-16 Na-23 Ti-48 Cu-64 La-139
第Ⅰ卷(选择题 共40分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符
合题目要求。
1.我国在天宫空间站研制成一种铌合金,熔点超过 。已知铌元素与钒同
族,下列说法正确的是( )
A.基态时钒元素的未成对电子数为3 B.铌原子的第一电离能大于钒原子
C.铌与钒,均属于s区元素 D.铌与钒,最高正价均为
2.下列化学用语表达正确的是( )
A.基态硅原子的轨道表示式:
B.基态Cr的电子排布式:
C. 键形成的轨道重叠示意图:
D.C原子的核外能量最高的电子云图像如图:
3.冬奥会的成功举办离不开各种科技力量的支撑。下列说法正确的是( )
A.跨临界直冷制冰使用的 分子中存在1个σ键和1个π键
B.开幕式上,鸟巢上空绽放的璀璨焰火与原子核外电子跃迁释放能量有关
C.颁奖礼服内胆中添加的石墨烯是最薄且最坚硬的纳米材料,属于分子晶体
D.BF 和NH 化学键的类型和分子的极性都相同
3 3
4.下列有关物质结构与性质的比较正确的是( )
A.分子的极性: B.酸性:
C.键角: D.基态原子未成对电子数:
5.下列说法中正确的是( )
A.CH ,C H ,HCN都是含有极性键的非极性分子
4 2 2
第 1 页 共 9 页B.稳定性: 是因为氢键作用不同所导致
C. 分子中含有1个手性碳原子
D.无机含氧酸分子中有几个氢原子,它就属于几元酸
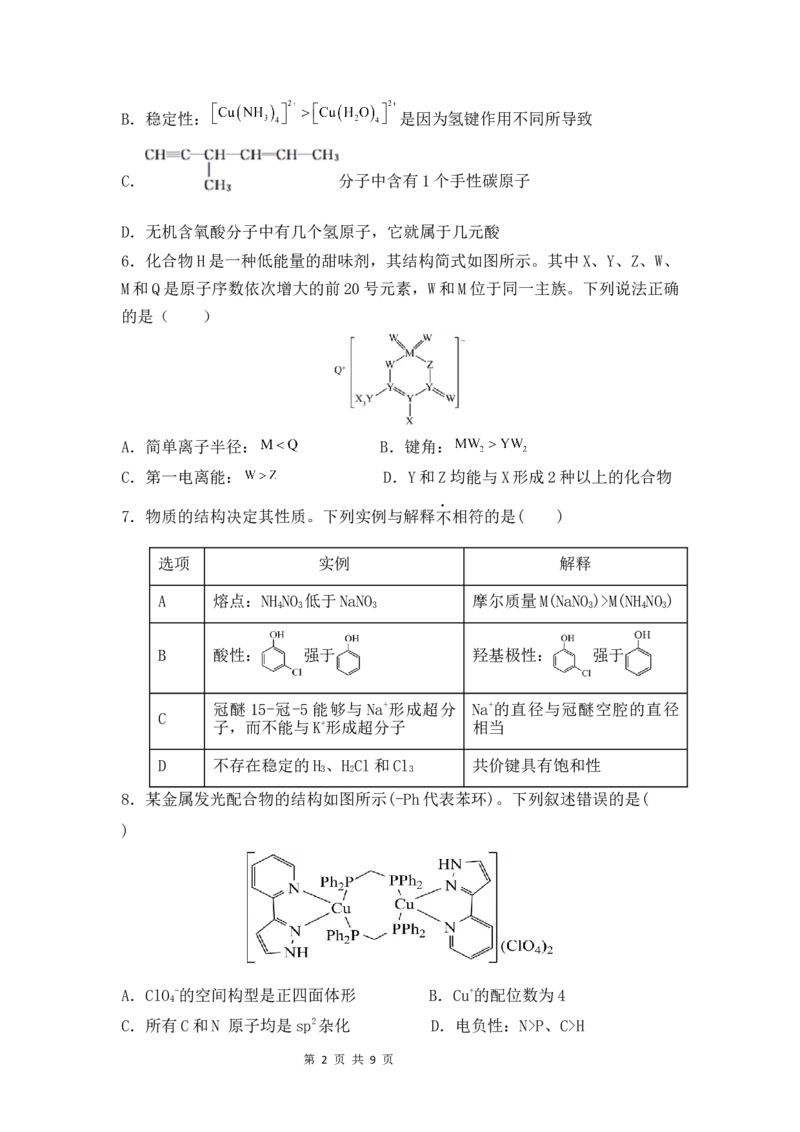
6.化合物H是一种低能量的甜味剂,其结构简式如图所示。其中X、Y、Z、W、
M和Q是原子序数依次增大的前20号元素,W和M位于同一主族。下列说法正确
的是( )
A.简单离子半径: B.键角:
C.第一电离能: D.Y和Z均能与X形成2种以上的化合物
7.物质的结构决定其性质。下列实例与解释不相符的是( )
选项 实例 解释
A 熔点:NH NO 低于NaNO 摩尔质量M(NaNO )>M(NH NO )
4 3 3 3 4 3
B 酸性: 强于 羟基极性: 强于
冠醚 15-冠-5 能够与 Na+形成超分 Na+的直径与冠醚空腔的直径
C
子,而不能与K+形成超分子 相当
D 不存在稳定的H 、H Cl和Cl 共价键具有饱和性
3 2 3
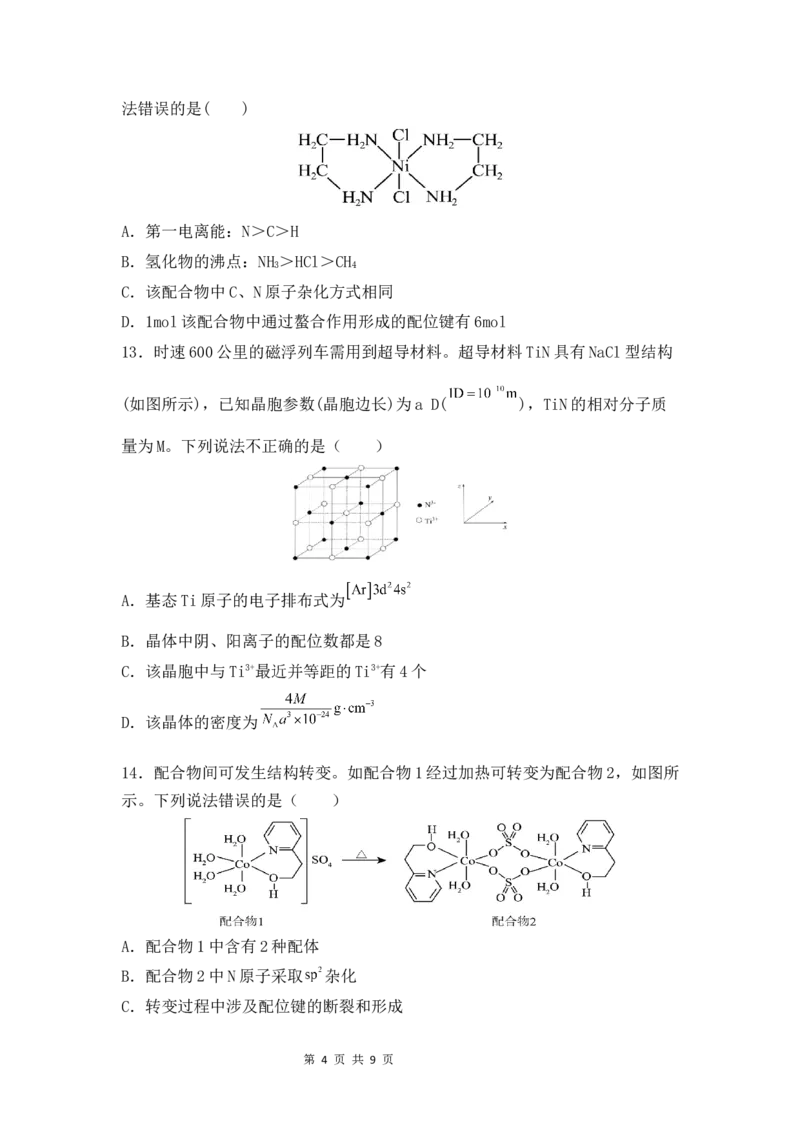
8.某金属发光配合物的结构如图所示(-Ph代表苯环)。下列叙述错误的是(
)
A.ClO -的空间构型是正四面体形 B.Cu+的配位数为4
4
C.所有C和N 原子均是sp2杂化 D.电负性:N>P、C>H
第 2 页 共 9 页9.关于分子的结构与性质,下列说法正确的是( )
A.SiF 和NH 均为非极性分子
4 3
B.CH O、BF 、SO 都是平面三角形的分子
2 3 2
C.四氟乙烯CF =CF 分子中C的杂化方式为sp3
2 2
D.等物质的量的[Cu(H O) ]2+与[Ag(NH ) ]+中所含的σ键数之比为3:2
2 4 3 2
10.观察下列模型,判断下列说法错误的是( )
二氧化
金刚石 碳化硅 石墨烯 C
60
硅
A.物质的量相同的金刚石和碳化硅,共价键个数之比为1∶1
B.SiO 晶体中Si和Si-O键个数比为1∶4
2
C.石墨烯中碳原子和六元环个数比为2∶1
D.C 晶体堆积属于分子密堆积
60
二、选择题:本题共5小题,每小题4分,共20分。每小题有个或两个选项符
合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.下列对实验现象或事实的解释正确的是( )
实验现象/事实 解释
往CuSO 溶液里滴加过量氨水得到深蓝色的透明溶 乙醇是极性较小的
4
A
液,再加入95%的乙醇析出深蓝色的晶体 溶剂
利用空腔大小适配的“杯酚”,借助甲苯和氯仿将C 超分子具有“自组
60
B
和C 分离 装”的特性
70
向稀的K [Fe(CN) ]溶液中滴加几滴KSCN溶液,溶液 结合Fe3+ 的能力:
3 6
C
颜色无明显变化 SCN-”“<”或“=”);基态钪( Sc)元素的原子核外电子的空间运动
状态共 种。
(2)化学上可用EDTA测定 和 的含量。EDTA的结构简式如图所示:
①EDTA中C原子的杂化轨道类型为 。若EDTA作为配合物中的配
体,它的配位原子为 。
②EDTA分子中不存在的化学键有 (填选项字母)。
第 5 页 共 9 页a.离子键 b.共价键 c.σ键 d.π键 e.配位键
17.(12分)回答下列问题。
(1)Cr3+基态核外M层电子排布式为 ;基态Ti原子核外
K、L层电子的电子云有 种不同的伸展方向。
(2) 的沸点比 高,原因是__________________
_____
___。
(3)1 mol [TiCl(NH ) ]Cl ·H O 含 σ 键数目为 。
3 5 2 2
(4)已知 和KCl的熔点分别是73.4℃和770℃,请分析两种物质熔点差异
的原因: 。
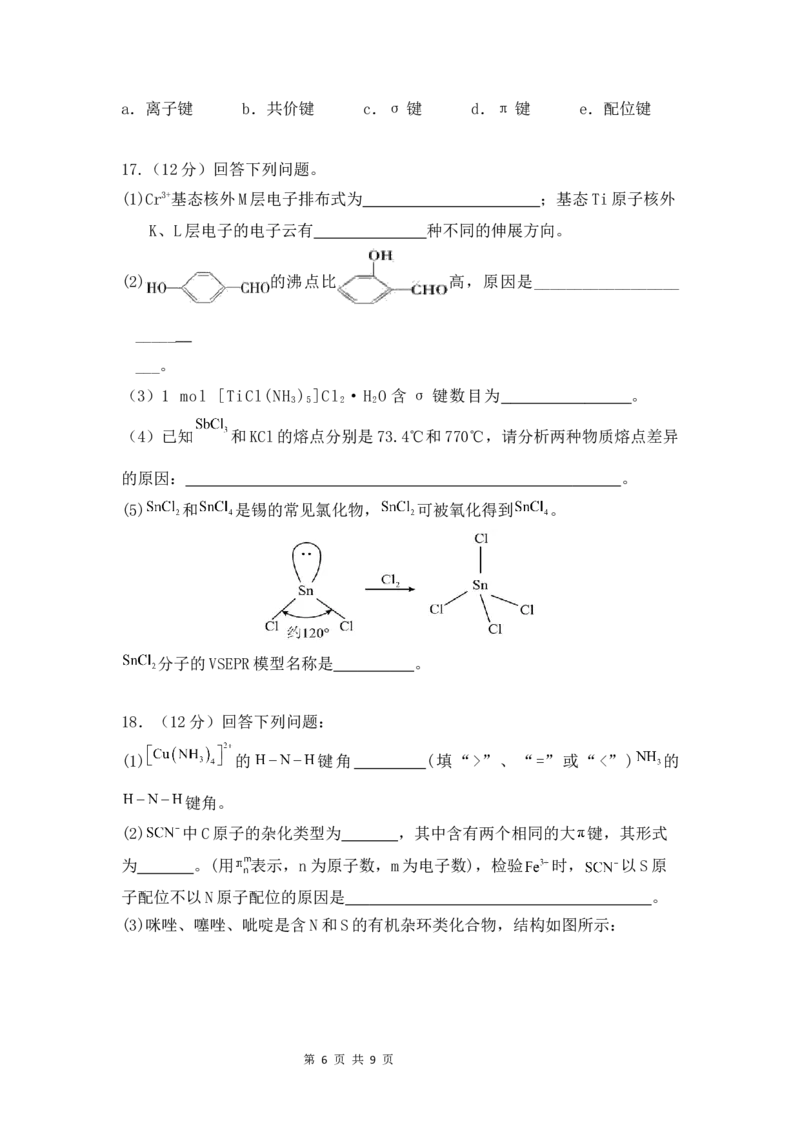
(5) 和 是锡的常见氯化物, 可被氧化得到 。
分子的VSEPR模型名称是 。
18.(12分)回答下列问题:
(1) 的 键角 (填“>”、“=”或“<”) 的
键角。
(2) 中C原子的杂化类型为 ,其中含有两个相同的大 键,其形式
为 。(用 表示,n为原子数,m为电子数),检验 时, 以S原
子配位不以N原子配位的原因是 。
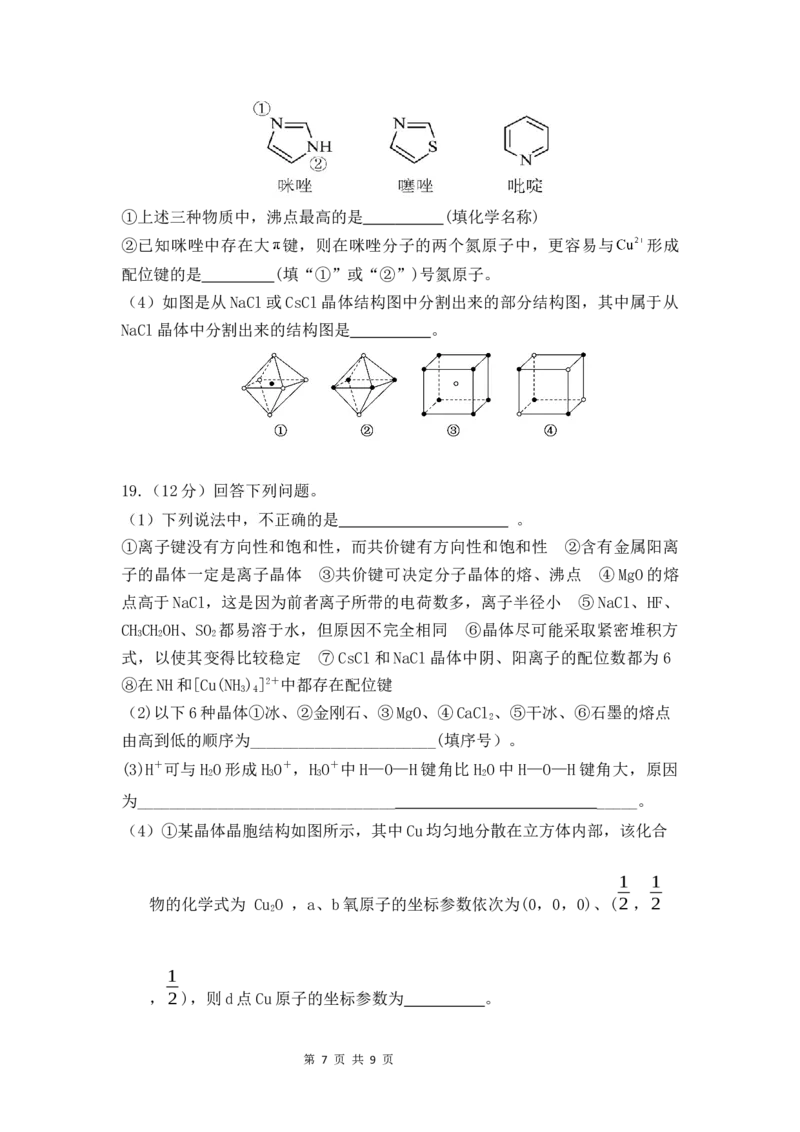
(3)咪唑、噻唑、呲啶是含N和S的有机杂环类化合物,结构如图所示:
第 6 页 共 9 页①上述三种物质中,沸点最高的是 (填化学名称)
②已知咪唑中存在大 键,则在咪唑分子的两个氮原子中,更容易与 形成
配位键的是 (填“①”或“②”)号氮原子。
(4)如图是从NaCl或CsCl晶体结构图中分割出来的部分结构图,其中属于从
NaCl晶体中分割出来的结构图是 。
19.(12分)回答下列问题。
(1)下列说法中,不正确的是 。
①离子键没有方向性和饱和性,而共价键有方向性和饱和性 ②含有金属阳离
子的晶体一定是离子晶体 ③共价键可决定分子晶体的熔、沸点 ④ MgO的熔
点高于NaCl,这是因为前者离子所带的电荷数多,离子半径小 ⑤ NaCl、HF、
CH CH OH、SO 都易溶于水,但原因不完全相同 ⑥晶体尽可能采取紧密堆积方
3 2 2
式,以使其变得比较稳定 ⑦ CsCl和NaCl晶体中阴、阳离子的配位数都为 6
⑧在NH和[Cu(NH ) ]2+中都存在配位键
3 4
(2)以下6种晶体①冰、②金刚石、③MgO、④CaCl 、⑤干冰、⑥石墨的熔点
2
由高到低的顺序为_______________________(填序号)。
(3)H+可与H O形成H O+,H O+中H—O—H键角比H O中H—O—H键角大,原因
2 3 3 2
为________________________________ _____。
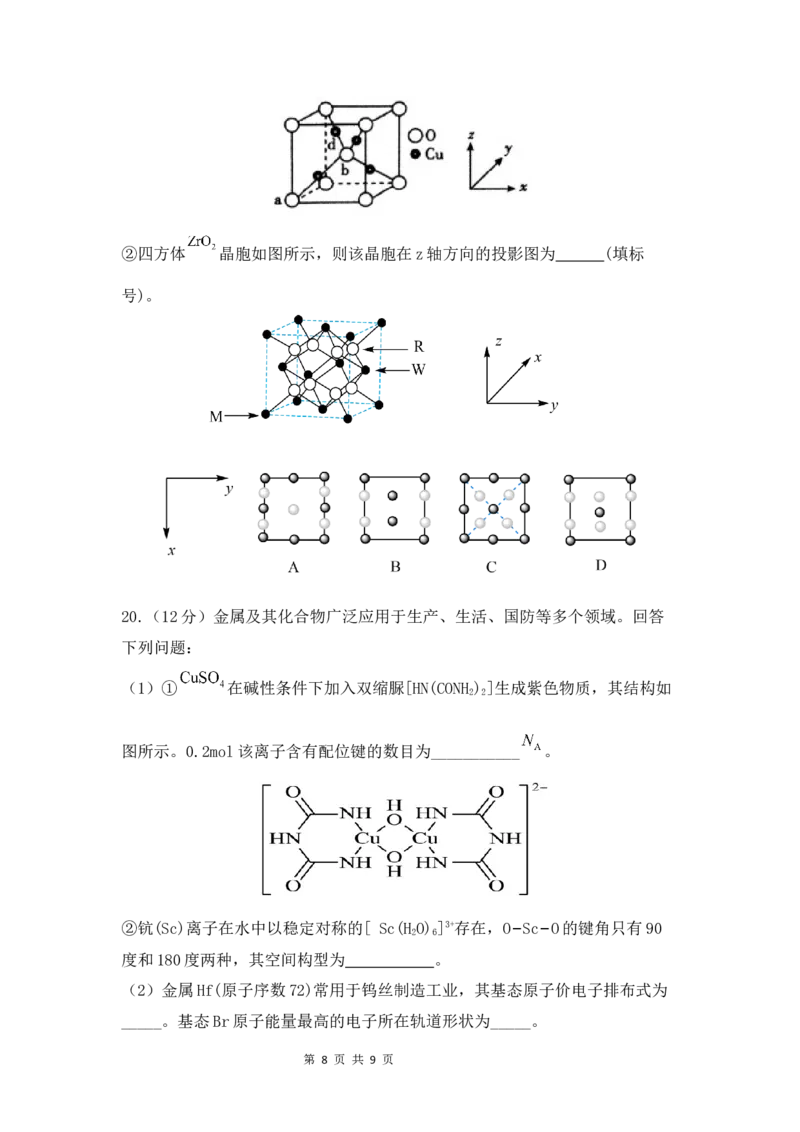
(4)①某晶体晶胞结构如图所示,其中Cu均匀地分散在立方体内部,该化合
1 1
物的化学式为 Cu O ,a、b氧原子的坐标参数依次为(0,0,0)、(2 ,2
2
1
,2 ),则d点Cu原子的坐标参数为 。
第 7 页 共 9 页②四方体 晶胞如图所示,则该晶胞在z轴方向的投影图为 (填标
号)。
20.(12分)金属及其化合物广泛应用于生产、生活、国防等多个领域。回答
下列问题:
(1)① 在碱性条件下加入双缩脲[HN(CONH ) ]生成紫色物质,其结构如
2 2
图所示。0.2mol该离子含有配位键的数目为___________ 。
②钪(Sc)离子在水中以稳定对称的[ Sc(H O) ]3+存在,O−Sc−O的键角只有90
2 6
度和180度两种,其空间构型为 。
(2)金属Hf(原子序数72)常用于钨丝制造工业,其基态原子价电子排布式为
_____。基态Br原子能量最高的电子所在轨道形状为_____。
第 8 页 共 9 页(3)金属Hf溴化物离子八面体钾盐晶胞结构如图,化学式为_____。已知晶胞
参数为anm,则该晶体的密度为 g⋅cm-3(写出计算表达式)
(设N 为阿伏加德罗常数的值,该化合物相对分子质量为M)。
A
第 9 页 共 9 页