文档内容
2024-2025学年高二化学下学期月考试卷参考答案
1.【答案】A【详解】A.钒元素为23号元素,基态时钒原子的价电子排布为
3d34s2,未成对电子数为3,故A正确;
B.铌元素与钒同族,同族元素从上往下第一电离能逐渐减小,所以铌原子的第
一电离能小于钒原子,故B错误;
C.铌与钒均为VB族元素,位于周期表的d区,故C错误;
D.铌与钒的价电子数均为5个,最高正价均为 ,故D错误;故选A。
2.【答案】D【解析】A.基态硅原子的电子排布式为1s22s22p63s23p2,轨道表
示式: ,故A错误;
B.Cr元素为24号元素,原子核外有24个电子,其电子排布式为
1s22s22p63s23p63d54s1,故B错误;
C.p-pπ键形成的轨道重叠示意图为 ,故C错
误;
D.C原子的核外能量最高的轨道为2p,电子云图像如图: ,故D正
确;故选D。
3.【答案】B【解析】A. 的结构式为O=C=O,1个 分子中含有2个σ键
和2个π键,故A错误;
B.焰火是原子核外电子由较高能量的激发态向较低能量的激发态乃至向基态跃
迁释放能量形成的,故B正确。
C.石墨烯是混合型晶体,故C错误;
D.BF 的化学键为极性共价键,中心B原子的价电子数为3,无孤对电子,为平
3
面三角形结构,为非极性分子,NH 的化学键为极性共价键,中心N原子的价电
3
子数为3,有1对孤对电子,为三角锥形,为极性分子,故D错误;综上所述,
答案为B。
4.【答案】D【详解】A.氧气为双原子分子,分子极性与键的极性一致,为非
极性分子,臭氧分子呈V形,正负电荷中心不重合,为极性分子,所以分子极
性 ,故A错误;
第 1 页 共 9 页B.F电负性较大,使羧基中的氢更容易电离,所以酸性CH COOHQ,A错误;
B. 是 ,空间结构为V形,键角约 ; 是 ,空间结构为直线
形,键角 ,所以键角 ,即 ,B错误;
C.同周期元素从左到右第一电离能呈增大趋势,但Z(N)的2p轨道为半充满稳
定结构,第一电离能N>O,即WP,电负性:N>P,C与H形成的
共价键中H为正价,C为负价,C的得电子能力大于H,电负性C>H,D正确;故
选C。
9.【答案】D【详解】A.NH 中N价层电子对数为 且含1个孤电子
3
对,空间构型为三角锥形,正负电荷中心不重合,为极性分子,SiF 中Si原子
4
的价层电子对数为 且不含孤电子对,为正四面体形,正负电荷中心
重合,为非极性分子,A项错误;
B.CH O分子中C原子的价层电子对数为 且不含孤电子对,BF
2 3
分子中B原子的价层电子对数为 且不含孤电子对,SO 分子中S原子
2
的价层电子对数为 且含1个孤电子对,为V形,因此并不都是平面
三角形的分子,B项错误;
C.四氟乙烯CF =CF 分子中存在碳碳双键,所以C的杂化方式为sp2,C项错
2 2
误;
D.[Cu(H O) ]2+中O原子是配体H O中的O原子,O的价层电子对数为4,则杂化
2 4 2
第 3 页 共 9 页类型为sp3杂化;配位键属于 键,一个水分子中有2个0-H 键,则
1mol[Cu(H O) ]2+中含有 键(4+2x4) =12mol,同理,1mol[Ag(NH ) ]+中所含的
2 4 3 2
σ键数为(2+3x2) =8mol,故等物质的量二者所含的σ键比为12:8=3:2,D正
确;故选D。
10.【答案】A【详解】A.假设金刚石和碳化硅的物质的量均为1mol,金刚石
中每个碳原子连接四根共价键,但每根共价键被两个环共用,因此每个碳原子
实际连接 根共价键,可知1mol金刚石中含有2molC-C键;1molSiC中有
1mol碳原子和1mol硅原子,每个原子通过共价键连接到其他原子,形成Si-C
键。由于每个共价键是两个原子共有的,因此每个原子独占的键数是总键数的
一半,即2mol,由于碳原子和硅原子的数量相等,因此总共有4molSi-C键;可
知物质的量相同的金刚石和碳化硅,共价键个数之比为1∶2,故A错误;
B. 晶体中1个硅原子形成4个共价键,Si和Si-O键个数比为1∶4,故B
正确;
C.石墨烯中1个六元环平均含有 个碳,则碳原子和六元环个数比为
2∶1,故C正确;
D. 晶体为分子晶体,其堆积属于分子密堆积,故D正确;故答案选A。
11.【答案】AC【详解】A.往CuSO 溶液里滴加过量氨水得到深蓝色的透明
4
Cu(NH ) SO 溶液,该溶液可以溶于水,加入乙醇,乙醇的极性小,Cu(NH ) SO
3 4 4 3 4 4
溶解度降低,析出深蓝色的晶体,A正确;
B.超分子具有“分子识别”的特性,利用空腔大小适配的“杯酚”与C 结
60
合,借助甲苯和氯仿将C 和C 分离,B错误;
60 70
C.向稀的K [Fe(CN) ]溶液中滴加几滴KSCN溶液,溶液颜色无明显变化,说明
3 6
结合Fe3+ 的能力:CN->SCN-,C中正确;
D.甲烷分子与水分子间不能形成氢键,通过范德华力结合,D错误;答案选
A。
12.【答案】AD【解析】A项,N原子电子排布为1s22s22p3,2p轨道上为半满状
态,因此氮的第一电离能相对较高;H原子电子排布为1s1,氢原子只有一个电
子,且原子半径非常小,其第一电离能相对较高;C原子电子排布为
1s22s22p2,2p轨道上的电子相对容易失去,因此碳的第一电离能相对较低,则
第一电离能:N>C>H,A错误;B项,NH 分子间可形成氢键,沸点高,HCl和
3
CH 为分子晶体,HCl分子量大,沸点高于CH ,B正确;C项,由该螯合物的结
4 4
第 4 页 共 9 页构可知,该配合物中C、N原子杂化方式均为sp3,C正确;D项,Ni-N键为通过
螯合作用形成的配位键,Ni提供空轨道,N提供孤电子对,则1mol该配合物中
通过螯合作用形成的配位键有4mol,D错误;故选AD。
13.【答案】BC【解析】A.Ti是22号元素,其基态原子电子排布式为
,A正确;
B.该晶胞的结构类似NaCl晶胞,晶体中阴、阳离子的配位数都是6,B错误;
C.从晶胞示意图可看出,与体心Ti3+最近并等距的Ti3+有12个,C错误;
D. 位于晶胞顶点和面心,晶胞中 数目为 , 位于晶胞内
部和棱上,晶胞中 数目为 ,故晶胞质量为 ,晶胞体积为
,所以该晶体密度为 ,D
正确;故选B。
14.【答案】D【详解】A.配合物1中, 中氧原子提供孤对电子,Co2+提供
空轨道形成配位键;配合物1右侧N、O分别提供一对孤电子,与Co2+形成配位
键,则配合物1中含有2种配体,A正确;
B.由配合物2的结构可知,N形成2个 键,一个配位键,故采取sp2杂化,B
正确;
C.转变过程中,配合物1中断裂2个 与Co2+形成的配位键,配合物2中,
中的O与Co2+形成2个配位键,涉及配位键的断裂和形成,C正确;
D.配合物1、2中Co都为+2价,Co的化合价没有发生变化,D错误;故选D。
15.【答案】BD【详解】A.由均摊法得,结构 1 中含有 Co 的数目为
,含有S的数目为 ,Co与S的原子个数比为9:8,因
此结构1的化学式为Co S ,故A正确;
9 8
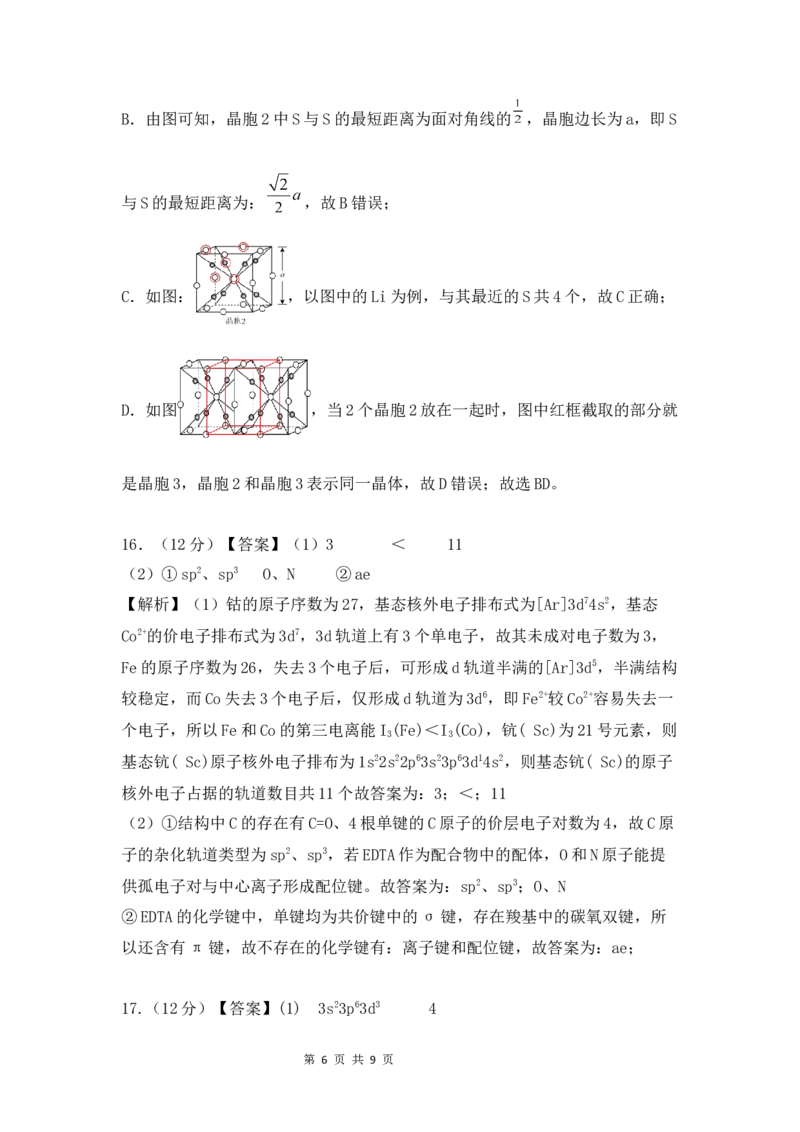
第 5 页 共 9 页B.由图可知,晶胞2中S与S的最短距离为面对角线的 ,晶胞边长为a,即S
与S的最短距离为: ,故B错误;
C.如图: ,以图中的Li为例,与其最近的S共4个,故C正确;
D.如图 ,当2个晶胞2放在一起时,图中红框截取的部分就
是晶胞3,晶胞2和晶胞3表示同一晶体,故D错误;故选BD。
16.(12分)【答案】(1)3 < 11
(2)①sp2、sp3 O、N ②ae
【解析】(1)钴的原子序数为27,基态核外电子排布式为[Ar]3d74s2,基态
Co2+的价电子排布式为3d7,3d轨道上有3个单电子,故其未成对电子数为3,
Fe的原子序数为26,失去3个电子后,可形成d轨道半满的[Ar]3d5,半满结构
较稳定,而Co失去3个电子后,仅形成d轨道为3d6,即Fe2+较Co2+容易失去一
个电子,所以Fe和Co的第三电离能I (Fe)<I (Co),钪( Sc)为21号元素,则
3 3
基态钪( Sc)原子核外电子排布为1s22s22p63s23p63d14s2,则基态钪( Sc)的原子
核外电子占据的轨道数目共11个故答案为:3;<;11
(2)①结构中C的存在有C=O、4根单键的C原子的价层电子对数为4,故C原
子的杂化轨道类型为sp2、sp3,若EDTA作为配合物中的配体,O和N原子能提
供孤电子对与中心离子形成配位键。故答案为:sp2、sp3;O、N
②EDTA的化学键中,单键均为共价键中的σ键,存在羧基中的碳氧双键,所
以还含有π键,故不存在的化学键有:离子键和配位键,故答案为:ae;
17.(12分)【答案】(1) 3s23p63d3 4
第 6 页 共 9 页(2) 存在分子间氢键,而 存在分子内氢键,分子间氢
键主要影响物质的熔沸点(升高)。
(3)23N
A
(4)因为 属于分子晶体,而KCl属于离子晶体。(5) 平面三角形
【解析】(2)水分子内的 O—H 键为化学键,氢键为分子间作用力;
存在分子间氢键,而 存在分子内氢键,而分子间氢键主
要影响物质的熔沸点(升高)。(3)H O、H O+中的O原子均采取sp3杂化,孤电子
2 3
对对成键电子对具有排斥作用,而孤电子对数多的 H O中排斥力大,键角小。
2
(4)从 和KCl的熔点分别是73.4℃和770℃可以判断出 属于分子晶
体,而KCl属于离子晶体,因为 属于分子晶体,而KCl属于离子晶体,分
子晶体中分子间作用力是范德华力,离子晶体中阴、阳离子间作用力为离子
键,离子键的键能大于范德华力,所以KCl熔点高于
(5)SnCl 的中心原子Sn的价层电子对数= ,因此SnCl 分子的VSEPR
2 2
模型名称是平面三角形。
18.(14分)【答案】(1) >
(2) sp杂化 S的电负性比N弱,更易提供孤对电子
(3) 咪唑 ① (4)①④
【详解】(1) 中N原子价层电子对数为4,无孤对电子,而 中
心N原子价层电子对数也为4,含一对孤对电子,孤电子对对成键电子对的斥力
大于成键电子对之间的斥力,因此 中的 的键角小于 的
键角;
第 7 页 共 9 页(2) 与CO 互为等电子体,也呈直线形结构,中心C原子采用sp杂化;
2
其中含有两个相同的大 键,形式为: ; 中S和N原子均存在孤对电
子,但N的电负性强于S,因此S原子更易提供孤对电子;
(3)①三者均为分子,但咪唑可形成分子间氢键,因此其沸点最高;
②由咪唑的结构简式可知其大 键应为 ,N①提供单电子形成大 键,而N②
提供一对孤对电子形成大 键,由此可知N②不含其他孤电子对,而N①存在一
对孤对电子,则①号氮原子更容易与 形成配位键。
19.(10分)(1) ⑥②③④①⑤ (2)②③⑦
(3)H O中氧原子上有2对孤电子对,H O+中氧原子上只有1对孤电子对,排斥力
2 3
较小
1 3 3
(4)① (4 ,4 ,4 ) ②C
20. (12分)(1) ①. 1.6 ②. 正八面体
(2)①. 5d26s2 ②. 哑铃形
(3)①. K [HfBr ] ②.
2 6
20.【解析】【小问1详解】根据图示可知,每个配离子中有8个配位键;钪
(Sc)离子在水中以稳定对称的[ Sc(H O) ]3+存在,其中O−Sc−O的键角只有90
2 6
度和180度两种,即钪(Sc)离子的前后左右上下与水中氧连接形成正八面体;
故答案为:正八面体;
【小问2详解】Hf为72号元素,位于第六周期第ⅣB族,其基态原子夹层电子
排布式为5d26s2,基态Br原子能量最高的电子位于 4p轨道,该轨道呈现哑铃
形;
小问3详解】根据图示可知[HfBr ]n-: ,K+:8,故其化学式为
【 6
第 8 页 共 9 页K [HfBr ],该晶体 密度为 。
2 6
的
第 9 页 共 9 页