文档内容
高二化学参考答案
【答案】
1. C
【解析】 龙虎纹四环铜鼓座 属青铜器 主要材质为铜合金 项正确
“ ” , ,A ;
木雕铁拐李 由木料雕制而成 主要成分是纤维素 项正确
“ ” , ,B ;
金扣玛瑙碗 玛瑙的主要成分为二氧化硅 不是硅酸盐 项错误
“ ” , ,C ;
犀角杯 犀角的化学成分主要是蛋白质 项正确
“ ” ,D 。
【答案】
2. B
【解析】 基态 原子的价层电子排布式为 电子排布图即轨道表示式 项正确
5 2 2-
Mn 3d4s, ,A ;CO3
的中心原子 是 杂化 无孤电子对 模型为平面三角形 应该为 项错
2
C sp , ,VSEPR , ,B
误 的电子式 项正确 分子中的 键是以 肩并肩 方式重叠的 项
;CO2 : ,C ;O2 p—pπ “ ” ,D
正确
。
【答案】
3. C
【解析】 标准状况下 不是气体 不是 项错误 环氧乙烷
,CH2Cl2 ,11.2L 0.5mol,A ;0.1mol
中含有共价键数目为 N 项错误 和环丁烷的最简式为 其式量
( ) 0.7 A,B ;CH3CH=CH2 CH2,
为 和环丁烷混合气体中碳原子数为 N 项正确 -1 的乙
14,28gCH3CH=CH2 2 A,C ;0.1mol·L
酸 未给体积无法计算数目 项错误
, ,D 。
【答案】
4. B
【解析】 该分子含有碳氯键 碳碳双键 醚键和羟基 种官能团 项错误 该分子含有碳碳双键
、 、 4 ,A ;
且双键上碳连接的原子团不相同 存在顺反异构 项正确 该物质最多与 反
, ,B ;1mol 1molNaOH
应 项错误 该物质分子中烃基所占比例大 且碳氯键 醚键都不是亲水基团 故该物质在水中
,C ; , 、 ,
的溶解度小 项错误
,D 。
【答案】
5. A
【解析】 是通过范德华力结合的 不含化学键 项错误 每个 的价电子数为 已
-
Ar19 , ,A ; Al 3,Al13
得到一个电子 - 含有价电子总数为 N 项正确 表现出超卤素的性质 因此
,1molAl13 40 A,B ;Al13 ,
与 能形成稳定的离子化合物 项正确 表现出碱土金属 如 的性质 因
Na Al13 NaAl13,C ;Al14 ( Ca) ,
此 与水反应的化学方程式为 项正确
Al14 Al14+2H2OAl14(OH)2+H2↑,D 。
【答案】
6. B
【解析】 根据题给信息和结构图可以推断 元素依次是 同周
,X、Y、Z、M、Q :C、O、F、Na、S。O、F
期 第一电离能 同主族 第一电离能 项正确 和 的中心原子均
, :OS,A ;CH4 H2O
是 杂化 有两个孤电子对 孤电子对对成键电子对斥力大 故甲烷分子的键角比水分子大
3
sp ,O , , ,
项错误 具有相同的核外电子排布 离子半径随着核电荷数增大而减小 项正
2- - +
B ;O 、F 、Na , ,C
确 的非金属性强于 最高价氧化物对应水化物的酸性 项正确
;S C, :Q>X,D 。
【答案】
7. C
【解析】 是极性键构成的双原子分子 是极性分子 项正确 与 通过配位键结合
+
HF , ,A ;HF H
高二化学参考答案 第 页(共 页)
1 6
{#{QQABKYQQogigAJJAAQhCAQkYCkMQkBCACSgGgBAEoAAAQRFABAA=}#}项正确 与 通过氢键 结合生成 每个 中只含 个 键
- - -
,B ;HF F HF2 , HF2 1 σ ,C
项错误 液态氟化氢分子间存在氢键 项正确 公众号:高中试卷君
; ,D 。
【答案】
8. B
【解析】 根据材料说明和六氟合铂酸氙的化学式 可知 六氟合铂酸氙中
+ -
([XeF] [Pt2F11] ) , Xe
的化合价为 价 项正确 结合图示 在第 步参与反应 在第 步又生成了 它是催化剂
-
+2 ,A ; ,F ① , ④ , ,
而 仅是反应的中间产物 项错误 第 步单质 转化成化合物 化合价有变化 属于
-
PtF7 ,B ; ② Xe XeF, ,
氧化还原反应 第 步 转化为 说明它得到了电子 也属于氧化还原反应 其它各步
-
, ③ PtF6 PtF6 , , 。
元素的化合价均无变化 项正确 根据材料说明和六氟合铂酸氙的化学式
+ -
,C ; ([XeF][Pt2F11] )
可知 六氟合铂酸氙是离子化合物 晶体属于离子晶体 项正确
, , ,D 。
【答案】
9. B
【解析】 过渡态是中间产物不稳定 能量较高 项正确 碘原子半径比氯原子大 碳碘键较易断
, ,A ; ,
裂 碘乙烷比氯乙烷更易发生水解反应 项错误 从该反应机理看 带负电荷的 进攻分子
-
, ,B ; , OH
中带正电荷的碳原子 说明 水溶液中实际参加反应的是 项正确 从上述反应机
-
, NaOH OH ,C ;
理可知 溶液中 也能发生类似反应生成 项正确
-
,NaCN CN CH3CH2CN,D 。
【答案】
10. D
【解析】 有机物 中所有碳原子都是 杂化 所有碳原子可能共平面 项正确 是碳
2
X sp , ,A ;Y→Z
碳双键的加成反应 项正确 中含有 能发生银镜反应 而 不可以 项正确 中
,B ;W —CHO , X ,C ;Z
苯环和 都能与氢气发生加成反应 有机物 最多可消耗 氢气 项错误
—CN ,1mol Z 5mol ,D 。
【答案】
11. D
【解析】 乙醇催化氧化产物中一般含有未反应完的乙醇 乙醇也能使酸性高锰酸钾溶液褪色
, ,
项错误 挥发出来的溴单质能与水反应生成氢溴酸 所以验证反应生成的 应先将气体通
A ; , HBr,
过四氯化碳 将挥发的溴单质除去 项错误 氯丁烷是非电解质不能直接电离出氯离子 检
, ,B ;1- ,
验 氯丁烷中氯元素 向 氯丁烷中加入氢氧化钠溶液 加热条件下水解 再加入硝酸酸化
1- , 1- , ,
的硝酸银 若产生白色沉淀 则含有氯元素 项错误 过程 超分子不溶于甲苯 通过过滤操作
, , ,C ; ① ,
分离得到 过程 不溶于氯仿 杯酚溶于氯仿 通过过滤操作分离得到 杯酚与氯仿互
C70, ②C60 , , C60,
溶 通过蒸馏操作分离 用 杯酚 可以分离 和 项正确
, , ( ) C60 C70,D 。
【答案】
12. C
【解析】 原子核外电子的空间运动状态有 种 项错误 的阴阳离子的空间构型
P 9 ,A ;NH4PF6
分别是正四面体和正八面体 项错误 离子晶体的离子半径大 离子键弱 熔点低 的阳离子
,B ; , , ,Y
体积大 半径比 大 项正确 中五元环成键方式类似苯 则 为 杂化形成 个杂化
+ 2
, Na ,C ;X , N sp 3
轨道 号 原子形成 个 键 存在 对孤电子对 则孤电子对在剩余的没有杂化的 轨道
。1 N 3 σ , 1 , 2p
上 号 原子形成 个 键 则孤电子对位于 杂化轨道上 项错误
2
。3 N 2 σ , sp ,D 。
【答案】
13. D
【解析】 从工作原理示意图可知 电极为负极 电极反应式为 生成的
- 2+
,Fe , Fe-2e Fe ,
在微生物的作用下发生反应 碳电极为正极 电极
2+ 2+ + +
Fe :3Fe +2NH4 N2↑+3Fe+8H , ,
反应式为 质子 经交换膜从甲室向乙室移动 项
- + - +
2NO3 +12H +10e N2↑+6H2O, (H ) ,A
错误 电池工作时 每转移 电子 生成 产生 但只有 移向
2+ + +
; , 6mol , 3molFe , 8molH , 6molH
乙室 故甲室 浓度增大 减小 项错误 碳电极为正极 电极反应式为
+ - +
, H pH ,B ; , 2NO3 +12H +
高二化学参考答案 第 页(共 页)
2 6
{#{QQABKYQQogigAJJAAQhCAQkYCkMQkBCACSgGgBAEoAAAQRFABAA=}#}项错误 根据上述反应式 理论上转移 电子 甲室产生
-
10e N2↑+6H2O,C ; , 6mol , 1mol
乙室产生 共产生标准状况下 项正确
N2 , 0.6molN2 , 22.4×1.6L=35.84LN2 ,D 。
【答案】
14. C
【解析】 随着盐酸的加入 减小 乙二胺溶液中由微粒 转为微粒 进一步转为
+ 2+
,pH , B BH BH2 ,
因微粒浓度减小 增大 由此推得曲线 为 曲线 为 曲线 为
+
pC , III pC(B), II pC(BH )、 I
2+ 根据 点c c + 则K
c
(BH
+
)
c
(OH
-
) c - -4.8 同理根
pC(BH2 ), c (B)= (BH ), b1= c = (OH )=10 ,
(B)
据 点 可求K
-7.6
项错误 由 到 到 水的电离程度依次增大 三点所对应
a , b2=10 ,A ; c b a, ,a、b、c
的溶液 点水的电离程度最大 项错误 点对应的溶液c 2+ c 根据K K
,a ,B ;b ,(BH2 )= (B), b1· b2=
c 2+ c2 -
(BH2 ) (OH ) -4.8 -7.6 -12.4c - -6.2 -1 项正确 当加入与
c =10 ×10 =10 ,(OH )=10 mol·L ,C ;
(B)
乙二胺等物质的量的盐酸时 此时溶液溶质为 根据电离平衡常数 电离生成
+ 2+
, BHCl, ,BH BH2
的程度大于水解生成 的程度 则c + c 2+ c 项错误
B , (BH )> (BH2 )> (B),D 。
【答案】 除标注外 每空 分 分 公众号:高中试卷君
15. ( , 2 ,14 )
分 分
6
(1)3d(1 ) 4(1 )
分 减弱
2
(2)①sp(1 ) ②N>C>H ③
减弱 分 氯原子为吸电子基 使得氨基 给出电子对的能力减弱 结合 的能力
+
(3) (1 ) , N , H
减弱
1 1 1 56+16×3+48 或 152 21
(4)① , , ②N -7 3 ( N 3×10 )
2 2 2 A×(a×10 ) A×a
【解析】 基态 的价电子排布式为 失去最外层 个电子 价电子排布式
6 2 2+
(1) Fe 3d4s, 2 ,Fe
为
6
3d;
卟啉分子中所有原子共平面 则 原子的杂化方式为
2
(2)① , N sp;
卟啉中各元素电负性大小顺序为
② N>C>H;
在酸性环境中 卟啉分子中部分 会与 形成配位键 部分 上无孤电子对 与其他原
+
③ , N H , N ,
子配位能力减弱
。
由于氯原子为吸电子基 使得氨基 给出电子对的能力减弱 结合 的能力减弱 故甘氨
+
(3) , N , H ,
酸的碱性减弱
。
根据晶胞结构 点的原子坐标参数为 是面心 点为 1 1 是体心 则
(4)① ,A (0,0,0),B ,B ,0, ,C ,
2 2
点的原子坐标参数为 1 1 1
C , , 。
2 2 2
立方晶胞顶角粒子占 面上粒子占 晶胞内部粒子为整个晶胞所有 一个晶胞中
② 1/8, 1/2, ,
含有 4+ 的个数为 1 2- 的个数为 1 2+ 的个数为 的摩尔质量为
Ti 8× =1,O 6× =3,Fe 1,FeTiO3
8 2
m
-1 晶胞参数a 故晶胞的密度 56+16×3+48 -3
152g·mol , nm, ρ=V=N -7 3g·cm 。
A×(a×10 )
【答案】 除标注外 每空 分 分
16. ( , 2 ,14 )
环己醇分子之间形成氢键而环己烯分子之间不能形成氢键
(1)
△ 没写沉淀符号不扣分 上口倒出 分
(2)FeCl3+3H2OFe(OH)3↓+3HCl( ) (1 )
高二化学参考答案 第 页(共 页)
3 6
{#{QQABKYQQogigAJJAAQhCAQkYCkMQkBCACSgGgBAEoAAAQRFABAA=}#}分
(3)c(1 )
(4)①c1→a1→b2
当加入最后半滴标准溶液时 溶液蓝色褪去 且半分钟不恢复原色
② , ,
③73.8%
(5)A
【解析】 环己醇沸点大于环己烯的主要原因除相对分子质量大外 还有环己醇分子之间形
(1) ,
成氢键而环己烯分子之间不能形成氢键
。
产生 的原因是 △ 因为有机层的密度比水小 产物
(2) HCl FeCl3+3H2OFe(OH)3↓+3HCl; ,
应该从分液漏斗的上口倒出
。
粗产品蒸馏提纯时 温度计测量的是蒸汽的温度 所以水银球应该放在蒸馏烧瓶的支管口
(3) , ,
处 若温度计水银球放在支管口以下位置 测得蒸汽的温度偏低 会导致收集的产品中混有低沸
, , ,
点杂质 若温度计水银球放在支管口以上位置 测得蒸汽的温度过高 会导致收集的产品中混有
; , ,
高沸点杂质 所以用 装置收集会导致收集到的产品中混有高沸点杂质 故选
; c , c。
硫代硫酸钠溶液呈碱性 用碱式滴定管盛放 滴定管用标准液润洗后 装入标准液至 刻
(4)① , , , “0”
度以上 尖嘴略向上倾斜挤压玻璃珠排出滴定管尖嘴部分的气泡 调整滴定管中的液面至 或
, , “0”
刻度以下 记录读数 然后将锥形瓶放于滴定管下 边滴边摇动锥形瓶 眼睛注视锥形瓶内颜
“0” , , , ,
色变化 直至滴定终点 记录读数 故排序为
, , , c1→a1→b2。
淀粉溶液遇碘变蓝 故用淀粉溶液作指示剂 滴定终点现象为当加入最后半滴标准溶液时 溶
② , , ,
液蓝色褪去 且半分钟不恢复原色
, 。
根据关系式 2- 得 反应溶液中n 1.000×24.00 即
③ I2~2S2O3 ,25.00mL (I2)= mol=0.012mol,
2000
过量 的物质的量为 则与环己烯反应 的物质的量为 环己烯与 反
Br2 0.12mol, Br2 0.18mol, Br2
应的比例是 则环己烯物质的量为 故样品中环己烯的质量分数为 82×0.18
1∶1, 0.18mol, ×
20.0
100%=73.8%。
元素分析仪用来确定有机物中元素组成 不能提供物质结构分析信息
(5) , 。
【答案】 除标注外 每空 分 分
17. ( , 2 ,15 )
邻氯苯甲醛 或 氯苯甲醛
(1) ( 2- )
(2)
高二化学参考答案 第 页(共 页)
4 6
OH
碳氯键 酯基 只写对一个得一分
CH COOH
、 ( )
Cl
分
(3)1(1 )
加成反应 分 取代反应 分
(4) (1 ) (1 )
(5)
Cl
CH COCl
(Et)3N
+CH3OH →
Cl
Cl
CH COOCH3
+HCl
Cl
{#{QQABKYQQogigAJJAAQhCAQkYCkMQkBCACSgGgBAEoAAAQRFABAA=}#}
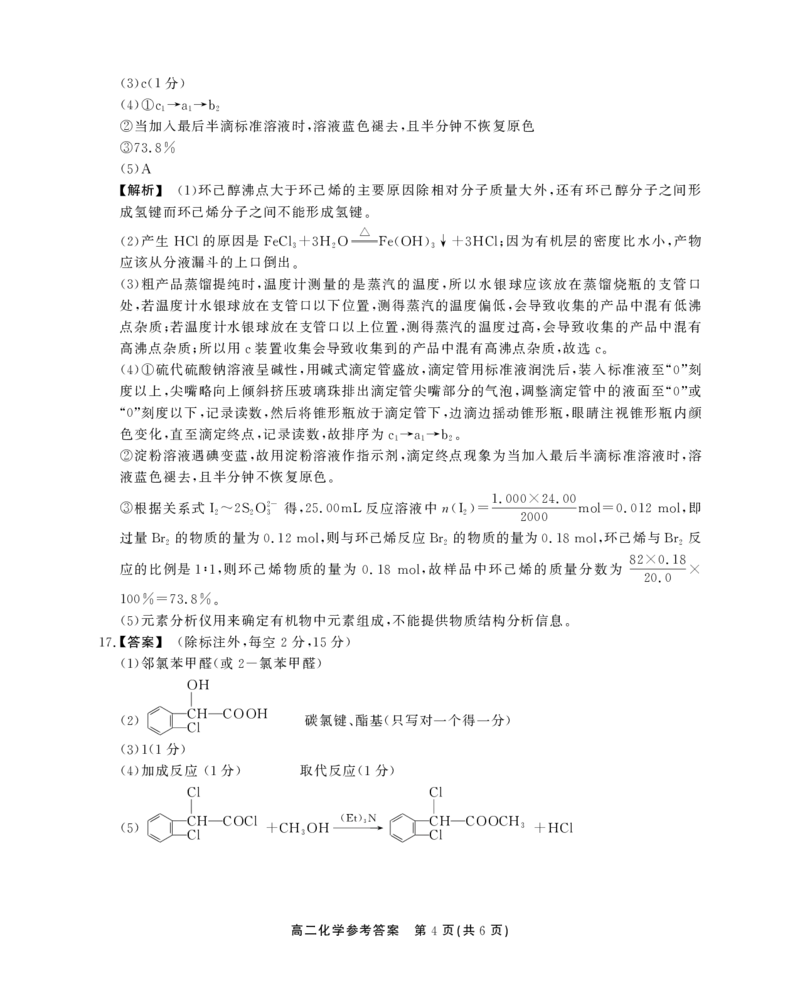
(6)17
高二化学参考答案 第 页(共 页)
5 6
SH
或
CH2NH2
NH2
任选一种即可
( )
CH2SH
【解析】 的化学名称为邻氯苯甲醛 或 氯苯甲醛
(1)A ( 2- )。
结合 的结构式和 的分子式 可推知 的结构简式为
(2) B、D C , C
OH
分子中
CH COOH
;E
Cl
所含官能团为碳氯键 酯基
、 。
分子中只有一个手性碳原子
(3)G 。
的反应类型为加成反应 的反应类型为取代反应
(4)A→B ,E→G 。
的化学方程式为
(5)D→E
Cl
CH COCl
(Et)3N
+CH3OH →
Cl
Cl
CH COOCH3
Cl
+HCl。
的分子式为 符合条件的 的同分异构体为 若苯环上有 个取代基
(6)F C7H9NS, F : 3 :—SH、
则有 种 若苯环上有 个取代基 或 有
—NH2、—CH3, 10 ; 2 :—CH2SH、—NH2 —CH2NH2、—SH,
种 若苯环上有 个取代基 则有 种 一共 种 其中核磁共振氢谱
2×3=6 ; 1 :—CH NH2 , 1 , 17 ;
SH
有 组峰的结构简式有
5
SH
或
CH2NH2
NH2
。
CH2SH
【答案】 除标注外 每空 分 分
18. ( , 2 ,15 )
K2 K
(1)+128 p1· p3
只选对一个得一分
(2)BD( )
反应 都是吸热反应 温度升高平衡正向移动 丙烷的转化率增大
(3)① Ⅰ、Ⅱ , ,
②36
大于 分
③ (1 )
只选对一个得一分
(4)①174 ②AC( )
【解析】 根据盖斯定律 反应 可由 而得 H -1 K K2 K
(1) , Ⅳ Ⅰ×2+Ⅲ ,Δ 4=128kJ·mol , p4= p1· p3。
改变 沸石颗粒大小 能改变反应物的接触面积 影响反应速率 项错误 根据题意
(2) RhIn4/ , , ,A ;
沸石催化剂改变反应的机理 能提高生成丙烯的选择性 项正确 催化剂不能改变平衡
RhIn4/ , ,B ;
转化率 项错误 射线衍射技术可测得晶体结构 项正确
,C ;X ,D 。
反应 都是吸热反应 温度升高平衡正向移动 丙烷的转化率增大
(3)① Ⅰ、Ⅱ , , 。
t 时 平衡时丙烷的转化率为 丙烯的选择性为 乙烯的选择性为 假设丙
② 1℃ , 60%、 80%、 20%。
烷进料为 平衡时各物质的量为丙烷 丙烯 乙烯 甲烷
1mol, 0.4mol、 0.48mol、 0.12mol、
氢气 气体总物质的量为 则各物质的体积分数为丙烷 丙烯
0.12mol、 0.48mol, 1.6mol, 0.25、
{#{QQABKYQQogigAJJAAQhCAQkYCkMQkBCACSgGgBAEoAAAQRFABAA=}#}氢气 可求得反应 的平衡常数K (0.3×100)×(0.3×100)
0.3、 0.3, Ⅰ p1= kPa=36kPa。
0.25×100
因为反应 都是气体分子数增大的反应 恒压条件下同时混入惰性气体 减小了丙烷的压
③ Ⅰ、Ⅱ , ,
强 平衡正向移动 丙烷的转化率增大
, , 。
E
由 经验公式 R k a C可知 -3 -3E C
(4)① Arrhenius :ln =-T+ ,237×10 =-4.0×10 a+ ,63×
-3 -3E C 解得E
10 =-5.0×10 a+ , a=174kJ/mol;
由 经验公式可知 速率常数k只与活化能和温度有关 催化剂能降低反应的活化
② Arrhenius , ,
能使速率常数增大 升温也能使速率常数增大 故答案为
, , AC。
高二化学参考答案 第 页(共 页)
6 6
{#{QQABKYQQogigAJJAAQhCAQkYCkMQkBCACSgGgBAEoAAAQRFABAA=}#}