文档内容
秘密 启用前 姓名 准考证号
★
年邵阳市高二联考试题卷
2024
化 学
本试卷共 页, 个小题。满分 分。考试用时 分钟。
8 18 100 75
注意事项:
答卷前 考生务必将自己的姓名 准考证号填写在答题卡上 将条形码横贴在答题卡
1. , 、 。
上 贴条形码区
“ ”。
作答选择题时 选出每小题答案后 用 铅笔在答题卡上对应题目选项的答案信息
2. , , 2B
点涂黑 如需改动 用橡皮擦干净后 再选涂其他答案 答案写在试题卷上无效
; , , 。 。
非选择题必须用黑色字迹的钢笔或签字笔作答 答案必须写在答题卡各题目指定区域
3. ,
内相应位置上 如需改动 先划掉原来的答案 然后再写上新答案 不准使用铅笔和涂改液
; , , ; 。
不按以上要求作答无效
。
保持答题卡的整洁 考试结束后 只交答题卡 试题卷自行保存
4. 。 , , 。
可能用到的相对原子质量
:H—1 C—12 N—14 O—16 Ca—40 Ni—59
Co—59 Ga—70
一、选择题:本题共 小题,每小题 分,共 分。在每小题给出的四个选项中,只有
14 3 42
一项是符合题目要求的。
化学与生产 生活有着密切联系 下列有关说法正确的是
1. 、 。
磷酸二氢钾是复合肥料,过量施用对环境无影响
A.
煤中含有苯、甲苯和粗氨水,可通过干馏得到上述产品
B.
海底可燃冰开发不当释放出的甲烷会造成温室效应的加剧
C.
“天宫”空间站使用石墨烯存储器,所用材料石墨烯与金刚石互为同分异构体
D.
下列化学用语错误的是
2.
中子数为 的硫原子符号:
34
A. 18 16S
的命名: 甲基丁烯
B. 2-
的共价键类型: 键
C.F2 p-pσ
·· ··
的电子式: [ ]
+ 2- +
D.Na2O2 Na ∶O··∶O··∶ Na
基本概念和理论是化学思维的基石 下列叙述错误的是
3. 。
洪特规则认为基态原子中填入简并轨道的电子总是先单独分占,且自旋平行
A.
理论认为 模型与分子的空间结构相同
B.VSEPR VSEPR
热力学理论认为化学反应总是向着自由能减小的方向进行,直到体系达到平衡
C.
同一化学反应,只要起始和终止的状态与量相同,加催化剂后,反应总的热效应一定
D.
不会发生改变
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 1 ( 8 )
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}用N 表示阿伏加德罗常数的值 下列叙述正确的是
4. A 。
时, 的氢氧化钡溶液中含有 N 个氢氧根离子
A.25℃ 1LpH=13 0.1 A
· -1 溶液中含有 - 的数目为 N
B.1L0.1mol L NaClO ClO 0.1 A
标准状况下, 氟化氢中含有 N 个氟化氢分子
C. 33.6L 1.5 A
完全转化为 - 时,转移的电子数为 N
D.3.3gNH2OH NO2 0.6 A
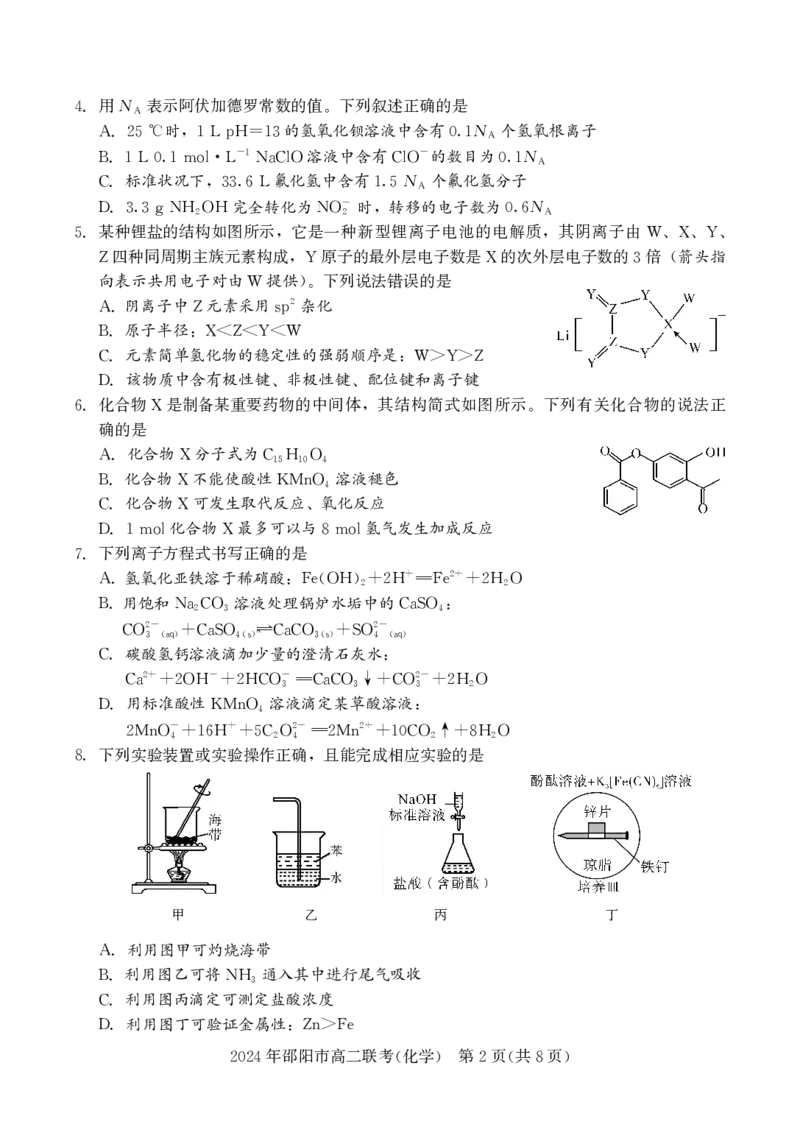
某种锂盐的结构如图所示 它是一种新型锂离子电池的电解质 其阴离子由
5. , , W、X、Y、
四种同周期主族元素构成 原子的最外层电子数是 的次外层电子数的 倍 (箭头指
Z ,Y X 3
向表示共用电子对由 提供) 下列说法错误的是
W 。
阴离子中 元素采用 杂化
2
A. Z sp
原子半径:
B. XY>Z
该物质中含有极性键、非极性键、配位键和离子键
D.
化合物 是制备某重要药物的中间体 其结构简式如图所示 下列有关化合物的说法正
6. X , 。
确的是
化合物 分子式为
A. X C15H10O4
化合物 不能使酸性 溶液褪色
B. X KMnO4
化合物 可发生取代反应、氧化反应
C. X
化合物 最多可以与 氢气发生加成反应
D.1mol X 8mol
下列离子方程式书写正确的是
7.
氢氧化亚铁溶于稀硝酸: ( )
+ 2+
A. FeOH 2+2H Fe +2H2O
用饱和 溶液处理锅炉水垢中的 :
B. Na2CO3 CaSO4
2-() () () 2-()
CO3 aq+CaSO4sCaCO3s+SO4 aq
碳酸氢钙溶液滴加少量的澄清石灰水:
C.
2+ - - 2-
Ca +2OH +2HCO3 CaCO3↓+CO3 +2H2O
用标准酸性 溶液滴定某草酸溶液:
D. KMnO4
- + 2- 2+
2MnO4+16H +5C2O4 2Mn +10CO2↑+8H2O
下列实验装置或实验操作正确 且能完成相应实验的是
8. ,
甲 乙 丙 丁
利用图甲可灼烧海带
A.
利用图乙可将 通入其中进行尾气吸收
B. NH3
利用图丙滴定可测定盐酸浓度
C.
利用图丁可验证金属性:
D. Zn>Fe
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 2 ( 8 )
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}类比 是化学学习的重要方法 下列客观事实和类比关系均正确的是
9.“ ” 。
在空气中燃烧生成 , 则 在空气中燃烧生成
A.Na Na2O2 Li Li2O2
过量的铁丝在稀硝酸中生成 ( ), 则过量的铁丝在氯气中燃烧生成
B. FeNO3 2 FeCl2
通入 ( )溶液无明显现象, 则 通入 ( )溶液无明显现象
C.CO2 BaNO3 2 SO2 BaNO3 2
溶液低温蒸干得到 ( ), 则 溶液低温蒸干得到 ( )
D.MgCl2 MgOH 2 AlCl3 AlOH 3
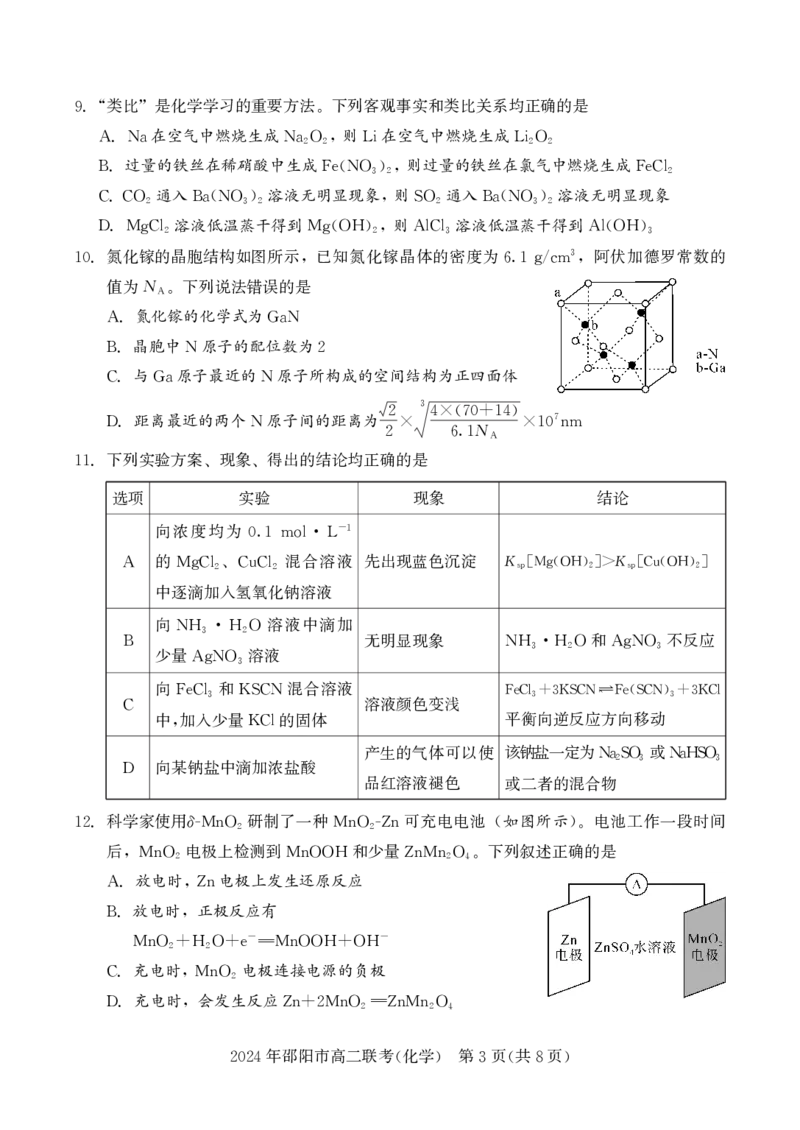
氮化镓的晶胞结构如图所示 已知氮化镓晶体的密度为 阿伏加德罗常数的
3
10. , 6.1g/cm ,
值为N 下列说法错误的是
A。
氮化镓的化学式为
A. GaN
晶胞中 原子的配位数为
B. N 2
与 原子最近的 原子所构成的空间结构为正四面体
C. Ga N
3 ( )
距离最近的两个 原子间的距离为 2 4×70+14 7
D. N × N ×10nm
2 6.1 A
下列实验方案 现象 得出的结论均正确的是
11. 、 、
选项 实验 现象 结论
向浓度均为
-1
0.1mol·L
的 混合溶液 先出现蓝色沉淀 K K
A MgCl2、CuCl2 sp[Mg(OH)2]> sp[Cu(OH)2]
中逐滴加入氢氧化钠溶液
向 溶液中滴加
NH3·H2O 无明显现象 和 不反应
B 少量 溶液 NH3·H2O AgNO3
AgNO3
向 和 混合溶液
FeCl3 KSCN 溶液颜色变浅 FeCl3+3KSCNFe(SCN)3 +3KCl
C 中 加入少量 的固体 平衡向逆反应方向移动
, KCl
产生的气体可以使 该钠盐一定为 或
向某钠盐中滴加浓盐酸 Na2SO3 NaHSO3
D 品红溶液褪色 或二者的混合物
科学家使用δ 研制了一种 可充电电池 (如图所示) 电池工作一段时间
12. -MnO2 MnO2-Zn 。
后 电极上检测到 和少量 下列叙述正确的是
,MnO2 MnOOH ZnMn2O4。
放电时, 电极上发生还原反应
A. Zn
放电时,正极反应有
B.
- -
MnO2+H2O+e MnOOH+OH
充电时, 电极连接电源的负极
C. MnO2
充电时,会发生反应
D. Zn+2MnO2ZnMn2O4
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 3 ( 8 )
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}碘循环工艺不仅能吸收 降低环境污染 同时还能制得氢气 具体流程如下
13. SO2 , , :
下列说法错误的是
该工艺中 和 的相互转化体现了 “碘循环”
A. I2 HI
反应器中,控制温度为 ,温度过低反应速率慢,温度过高水气化且增大
B. 20℃~100℃
碘的流失,反应速率也慢
膜反应器中,增大压强有利于提高 的平衡转化率
C. HI
碘循环工艺的总反应为:
D. SO2+2H2OH2+H2SO4
缓冲溶液是指加少量水稀释或外加少量酸 碱 自身 不发生显著变化的溶液 含
14. 、 , pH 。1L
乳酸 和 乳酸钠 的溶液就是一种缓冲溶液 该溶液的 为
1mol (HLac) 1mol (NaLac) , pH
下图是该缓冲溶液的 随通入 或加入 的物质的量变化的示意
3.85。 pH HCl(g) NaOH(s)
图 溶液体积保持 已知 下列说法错误的是
( 1L), lg3=0.48。
通过计算可得出, 点溶液的 值约为
A. a pH 3.37
根据图像可以判断, 点溶液已失去缓冲能力
B. b
该缓冲溶液中:c( )c( + ) c ( - ) c( - )
C. 2 HLac+ H =2 Lac + OH
当加入 ,且横坐标为 时,溶液中:c(
+
)c(
-
)
D. NaOH 0.5 Na < Lac
二、非选择题:本题共 小题,共 分。
4 58
分 亚硝酸钙 可作为混凝土防冻剂和钢筋阻锈剂的主要原料 熔点为
15.(14 ) Ca(NO2)2 。
易潮解 易溶于水 实验室中 某兴趣小组根据反应 Δ
390℃, , 。 , 2NO+CaO2Ca(NO2)2,
利用如下装置 (部分装置可重复选用)制备无水亚硝酸钙并测定产品的纯度 (夹持装置略)
。
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 4 ( 8 )
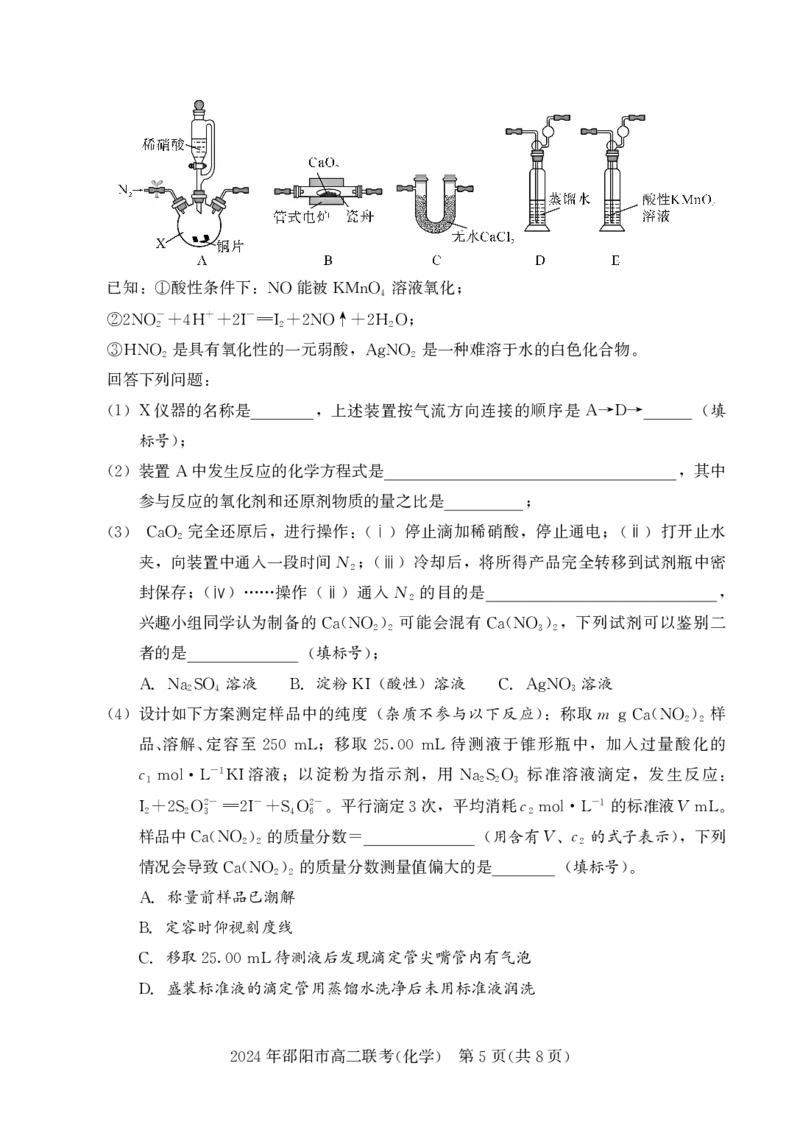
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}已知 酸性条件下 能被 溶液氧化
:① :NO KMnO4 ;
- + -
②2NO2+4H +2I I2+2NO↑+2H2O;
是具有氧化性的一元弱酸 是一种难溶于水的白色化合物
③HNO2 ,AgNO2 。
回答下列问题
:
仪器的名称是 上述装置按气流方向连接的顺序是 (填
(1)X , A→D→
标号)
;
装置 中发生反应的化学方程式是 其中
(2) A ,
参与反应的氧化剂和还原剂物质的量之比是
;
完全还原后 进行操作 停止滴加稀硝酸 停止通电 打开止水
(3) CaO2 , :(ⅰ) , ;(ⅱ)
夹 向装置中通入一段时间N 冷却后 将所得产品完全转移到试剂瓶中密
, 2;(ⅲ) ,
封保存 操作 通入N 的目的是
;(ⅳ)…… (ⅱ) 2 ,
兴趣小组同学认为制备的 可能会混有 下列试剂可以鉴别二
Ca(NO2)2 Ca(NO3)2,
者的是 (填标号)
;
溶液 淀粉 (酸性)溶液 溶液
A.Na2SO4 B. KI C.AgNO3
设计如下方案测定样品中的纯度 (杂质不参与以下反应) 称取m 样
(4) : gCa(NO2)2
品 溶解 定容至 移取 待测液于锥形瓶中 加入过量酸化的
、 、 250mL; 25.00mL ,
c -1 溶液 以淀粉为指示剂 用 标准溶液滴定 发生反应
1mol·L KI ; , Na2S2O3 , :
2- - 2-
平行滴定 次 平均消耗c
-1
的标准液V
I2+2S2O3 2I +S4O6 。 3 , 2mol·L mL。
样品中 的质量分数 (用含有V、c 的式子表示) 下列
Ca(NO2)2 = 2 ,
情况会导致 的质量分数测量值偏大的是 (填标号)
Ca(NO2)2 。
称量前样品已潮解
A.
定容时仰视刻度线
B.
移取 待测液后发现滴定管尖嘴管内有气泡
C. 25.00mL
盛装标准液的滴定管用蒸馏水洗净后未用标准液润洗
D.
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 5 ( 8 )
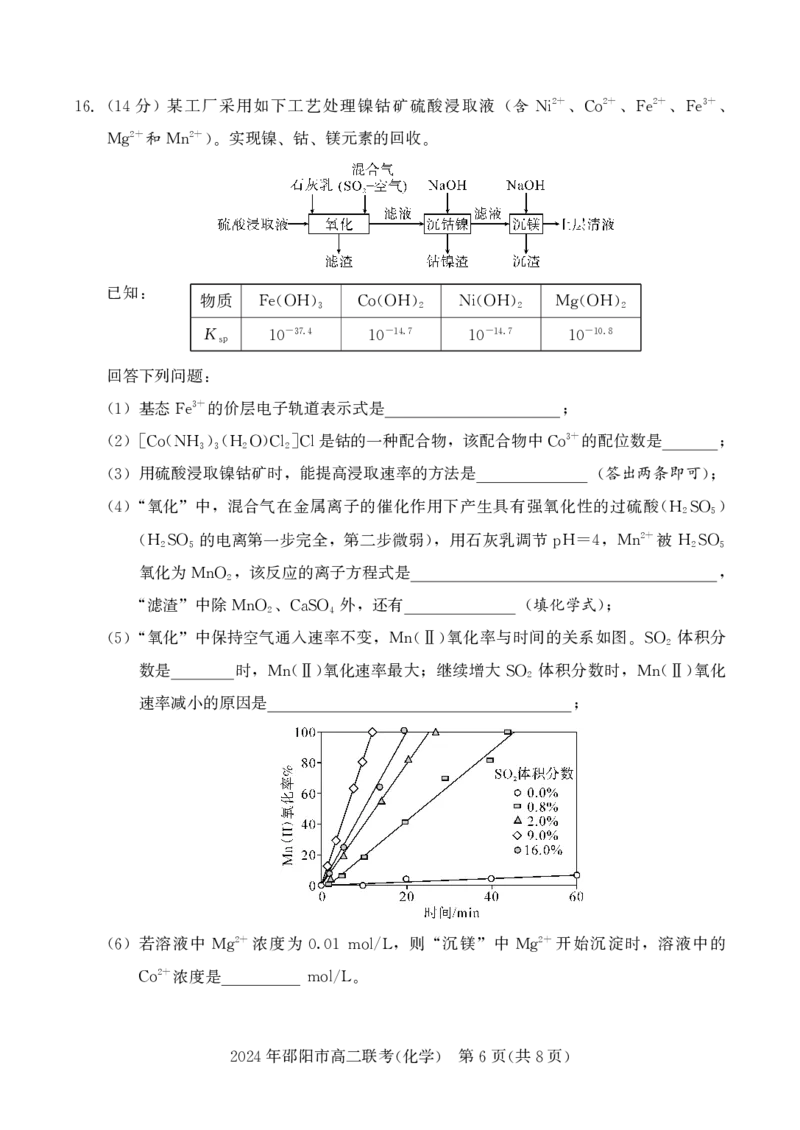
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}分 某工厂采用如下工艺处理镍钴矿硫酸浸取液 (含 、 、 、 、
2+ 2+ 2+ 3+
16.(14 ) Ni Co Fe Fe
和 ) 实现镍 钴 镁元素的回收
2+ 2+
Mg Mn 。 、 、 。
已知
: 物质
Fe(OH)3 Co(OH)2 Ni(OH)2 Mg(OH)2
K -37.4 -14.7 -14.7 -10.8
sp 10 10 10 10
回答下列问题
:
基态 的价层电子轨道表示式是
3+
(1) Fe ;
是钴的一种配合物 该配合物中 的配位数是
3+
(2)[Co(NH3)3(H2O)Cl2]Cl , Co ;
用硫酸浸取镍钴矿时 能提高浸取速率的方法是 (答出两条即可)
(3) , ;
氧化 中 混合气在金属离子的催化作用下产生具有强氧化性的过硫酸
(4)“ ” , (H2SO5)
的电离第一步完全 第二步微弱 用石灰乳调节 被
2+
(H2SO5 , ), pH=4,Mn H2SO5
氧化为 该反应的离子方程式是
MnO2, ,
滤渣 中除 外 还有 (填化学式)
“ ” MnO2、CaSO4 , ;
氧化 中保持空气通入速率不变 氧化率与时间的关系如图 体积分
(5)“ ” ,Mn(Ⅱ) 。SO2
数是 时 氧化速率最大 继续增大 体积分数时 氧化
,Mn(Ⅱ) ; SO2 ,Mn(Ⅱ)
速率减小的原因是
;
若溶液中 浓度为 则 沉镁 中 开始沉淀时 溶液中的
2+ 2+
(6) Mg 0.01mol/L, “ ” Mg ,
浓度是
2+
Co mol/L。
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 6 ( 8 )
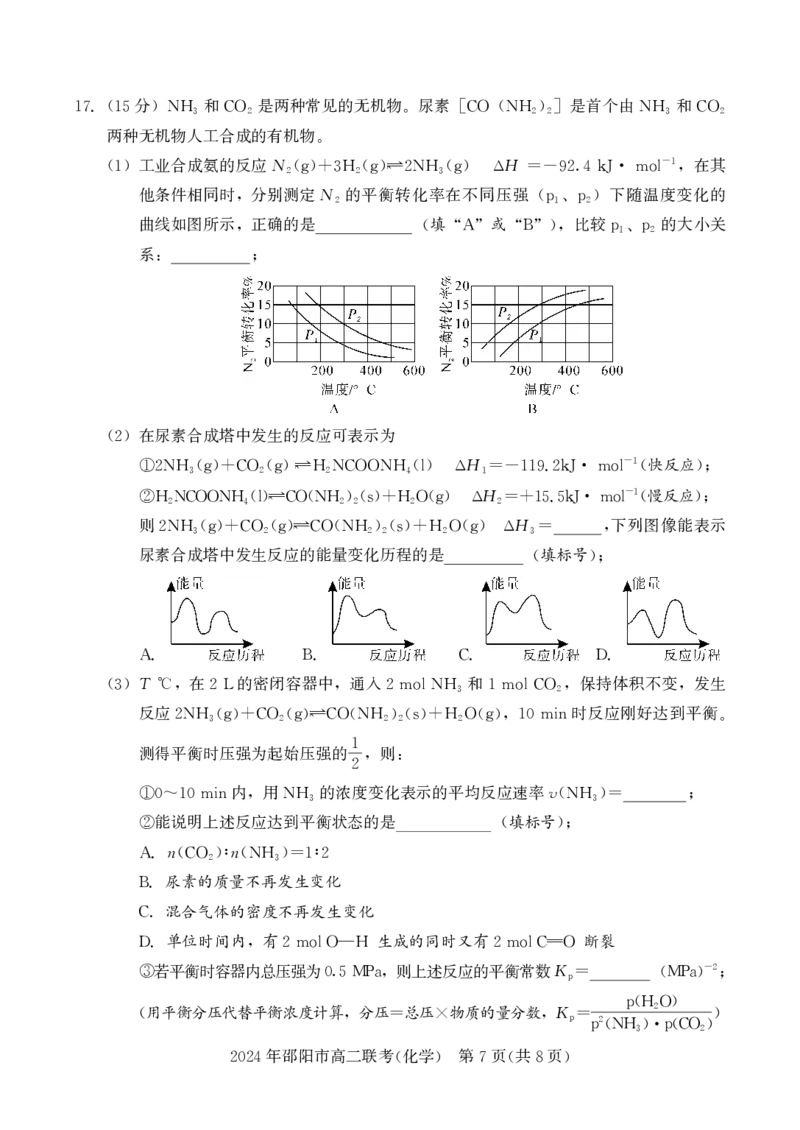
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}分 和 是两种常见的无机物 尿素 是首个由 和
17.(15 )NH3 CO2 。 [CO (NH2)2] NH3 CO2
两种无机物人工合成的有机物
。
工业合成氨的反应N H -1 在其
(1) 2(g)+3H2(g)2NH3(g) Δ =-92.4kJ· mol ,
他条件相同时 分别测定N 的平衡转化率在不同压强 下随温度变化的
, 2 (p1、p2)
曲线如图所示 正确的是 (填 “ ”或 “”) 比较 的大小关
, A B , p1、p2
系
: ;
在尿素合成塔中发生的反应可表示为
(2)
H -1 (快反应)
①2NH3(g)+CO2(g)H2NCOONH4(l) Δ 1=-119.2kJ· mol ;
H -1 (慢反应)
②H2NCOONH4(l)CO(NH2)2(s)+H2O(g) Δ 2=+15.5kJ·mol ;
则 H 下列图像能表示
2NH3(g)+CO2(g)CO(NH2)2(s)+H2O(g) Δ 3= ,
尿素合成塔中发生反应的能量变化历程的是 (填标号)
;
A. B. C. D.
T 在 的密闭容器中 通入 和 保持体积不变 发生
(3) ℃, 2L , 2molNH3 1molCO2, ,
反应 时反应刚好达到平衡
2NH3(g)+CO2(g)CO(NH2)2(s)+H2O(g),10min 。
测得平衡时压强为起始压强的1 则
, :
2
内 用 的浓度变化表示的平均反应速率v
①0~10min , NH3 (NH3)= ;
能说明上述反应达到平衡状态的是 (填标号)
② ;
n( )n( )
A. CO2∶ NH3 =1∶2
尿素的质量不再发生变化
B.
混合气体的密度不再发生变化
C.
单位时间内,有 生成的同时又有 断裂
D. 2molO H 2molCO
若平衡时容器内总压强为 则上述反应的平衡常数K
-2
③ 0.5MPa, p= (MPa) ;
( )
(用平衡分压代替平衡浓度计算,分压 总压 物质的量分数,K pH2O )
= × p= 2 ( )· ( )
p NH3 pCO2
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 7 ( 8 )
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}用惰性电极电解尿素 的碱性溶液可制取氢气 装置如图所示 写出
(4) [CO (NH2)2] , ,
该装置阳极的电极反应式
。
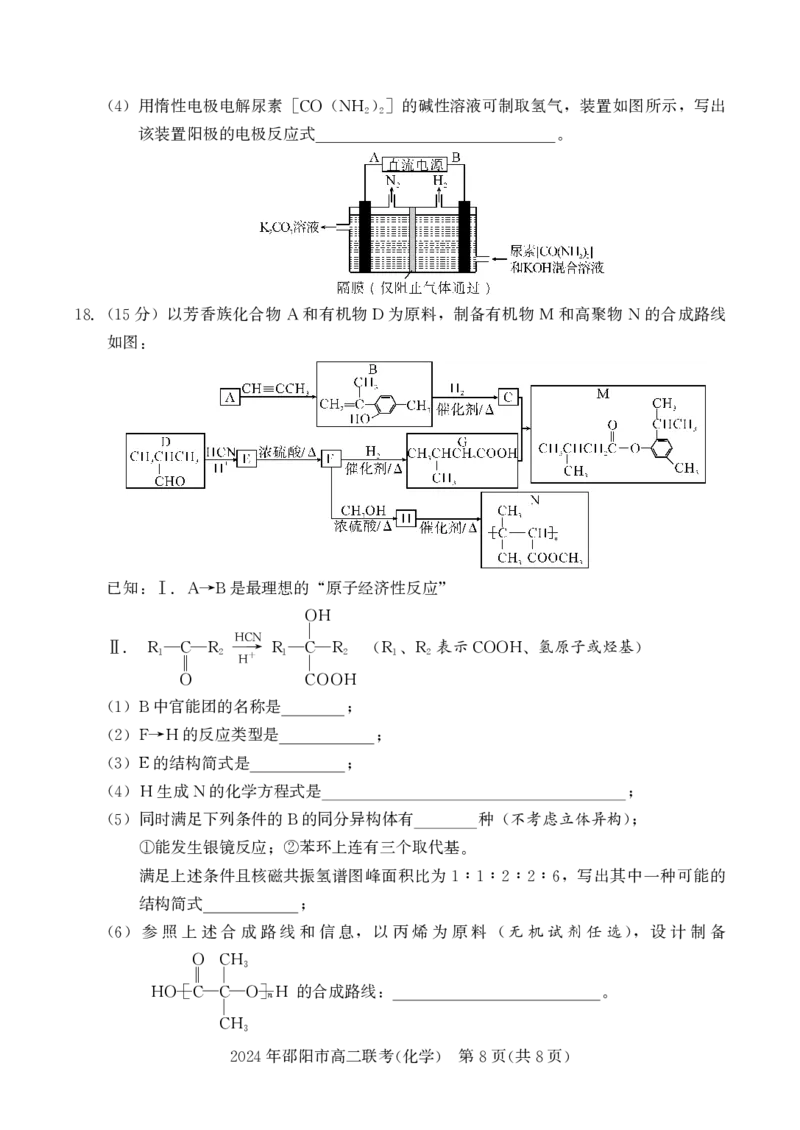
分 以芳香族化合物 和有机物 为原料 制备有机物 和高聚物 的合成路线
18.(15 ) A D , M N
如图
:
已知 是最理想的 原子经济性反应
:Ⅰ.A→B “ ”
Ⅱ. R1 C
O
年邵阳市高二联考 化学 第 页 共 页
2024 ( ) 8 ( 8 )
OH
HCN ( 、 表示 、氢原子或烃基)
R2 →+ R1 C R2 R1 R2 COOH
H
COOH
中官能团的名称是
(1)B ;
的反应类型是
(2)F→H ;
的结构简式是
(3)E ;
生成 的化学方程式是
(4)H N ;
同时满足下列条件的 的同分异构体有 种 (不考虑立体异构)
(5) B ;
能发生银镜反应 苯环上连有三个取代基
① ;② 。
满足上述条件且核磁共振氢谱图峰面积比为 写出其中一种可能的
1∶1∶2∶2∶6,
结构简式
;
参照上述合成路线和信息 以丙烯为原料 (无机试剂任选) 设计制备
(6) , ,
O
HOC
CH3
的合成路线
C OH : 。
CH3
{#{QQABYYKEggAAAJIAAAgCUQX6CAMQkBEAAQgOBEAIsAAAwBNABAA=}#}