文档内容
哈三中 2024—2025 学年度上学期
高二学年期中考试化学试卷
可能用到的相对原子质量C-12 O-16 F-19 Na-23
I卷(共45分)
一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
符合题目要求。)
1. 下列说法错误的是
A. 盐碱地(含较多 、 )不利于农作物生长,可以施加适量石膏降低土壤碱性
B. 血浆中 缓冲体系对稳定体系的酸碱度发挥着重要作用
C. 含氟牙膏可以将羟基磷灰石转化为氟磷灰石,达到预防龋齿的目的
D. 医疗上常用 作 射线透视肠胃的内服药剂,俗称“钡餐”
【答案】D
【解析】
【详解】A.盐碱地施加适量石膏,可以发生反应 ,得到的
显中性,可以降低由 引起的碱性,A正确;
B.缓冲溶液的作用就是用于调节溶液的酸碱性不产生大的波动,因此血浆中 缓冲体系对
稳定体系的酸碱度发挥着重要作用,B正确;
C.含氟牙膏可以将羟基磷灰石转化为氟磷灰石,促进牙釉质的再矿化,达到预防龋齿的目的,C正确;
D. 有毒,因此医疗上的钡餐通常采用难溶于胃酸的 ,不能使用易溶于胃酸的 ,D错
误;
故答案为:D。
2. 下列电离或水解方程式正确的是
A. B.
C. D.【答案】D
【解析】
【详解】A.亚硫酸氢钠是强电解质,在水中完全电离为钠离子和亚硫酸氢根离子,A错误;
B.多元弱酸根分步水解,以第一步为主,S2−+H
2
O⇌HS-+OH−,B错误;
C.一水合氨是弱电解质,微弱电离,用可逆符号,C错误;
D.铝离子水解,铝离子结合水电离的氢氧根产生氢氧化铝,D正确;
故答案选D。
3. 下列各离子组在溶液中能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】A
【解析】
【详解】A.给定各离子可以大量共存,A正确;
B. 与 会发生双水解的反应,不能大量共存,B错误;
C. 与 之间会发生离子反应, ,
不能大量共存,C错误;
D. 、 具有还原性, 具有氧化性,会发生氧化还原反应不能大量共存,D错误;
故选A。
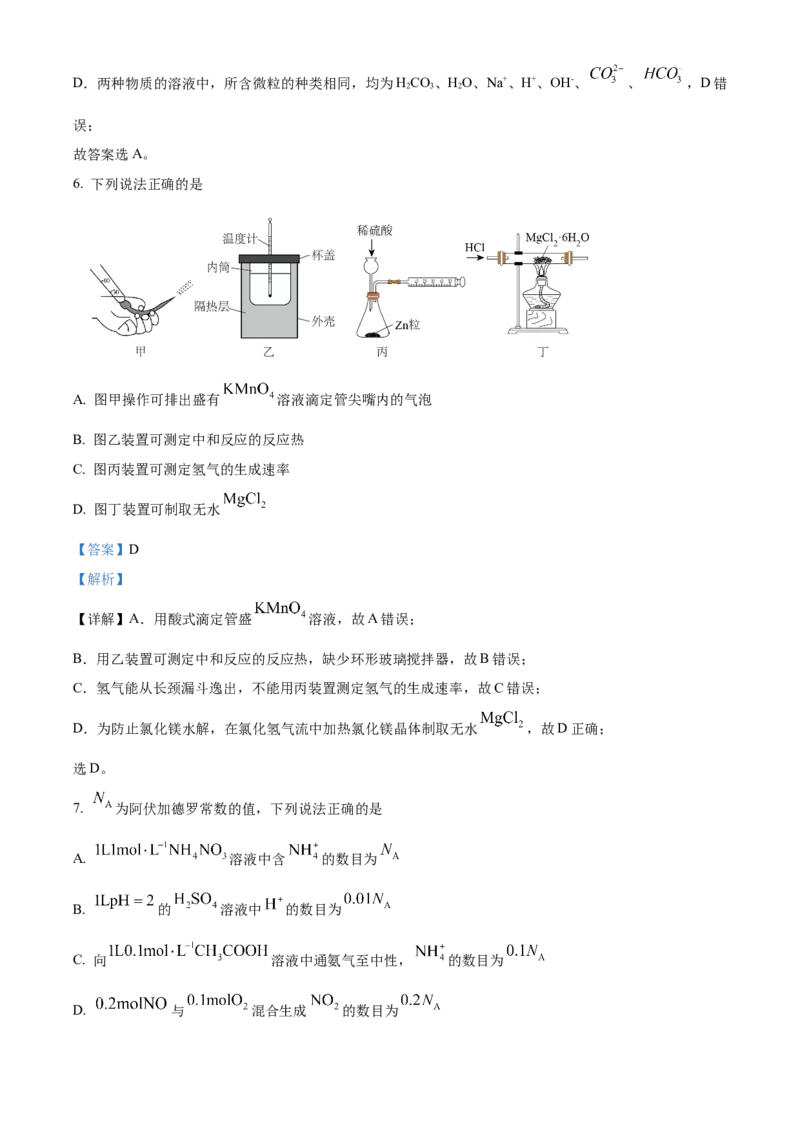
4. 化学反应均伴随着能量的变化,下列反应的能量变化规律与图示相符的有
①食物的腐败
②焦炭与水蒸气高温下反应
③盐酸与碳酸氢钠反应
④镁条溶于盐酸⑤氢氧化钡晶体与氯化铵反应
⑥铝热反应
⑦过氧化氢分解
⑧生石灰加水制熟石灰
A. ①②⑦ B. ②⑤⑦ C. ②③⑤ D. ③⑤⑥
【答案】C
【解析】
【分析】由图可知,图示反应为反应物总能量小于生成物总能量的吸热反应。
【详解】①食物的腐败是放出热量的放热反应,故不符合题意;
②碳与水蒸气高温下的反应是吸收热量的吸热反应,故符合题意;
③盐酸与碳酸氢钠发生的反应时吸收热量的吸热反应,故符合题意;
④镁条溶于盐酸发生的反应是放出热量的放热反应,故不符合题意;
⑤氢氧化钡晶体与氯化铵的反应是吸收热量的吸热反应,故符合题意;
⑥铝热反应是放出热量的放热反应,故不符合题意;
⑦过氧化氢分解是放出热量的放热反应,故不符合题意;
⑧生石灰加水制熟石灰是放出热量的放热反应,故不符合题意;
②③⑤符合题意,故选C。
5. 关于 和 的下列说法中,正确的是
A. 可用 溶液鉴别两种溶液
B. 蒸干 溶液或 溶液均可获得 固体
C. 室温下,二者饱和溶液的 差约为4,主要是由于它们的溶解度差异
D. 两种物质的溶液中,所含微粒的种类不相同
【答案】A
【解析】
【详解】A.HCl溶液滴入碳酸钠溶液中,开始生成碳酸氢钠,故开始不产生气泡,后生成的碳酸氢钠转
化为水和二氧化碳,有气泡冒出,将HCl溶液滴入碳酸氢钠溶液中,产生二氧化碳,有气泡冒出,现象不
同,可以用HCl溶液鉴别两种溶液,A正确;
B.蒸干NaCO 溶液或NaHCO 溶液均可获得NaCO 固体,B错误;
2 3 3 2 3
C.二者饱和溶液的pH差约为4,主要是由于碳酸根水解程度大于碳酸氢根,C错误;D.两种物质的溶液中,所含微粒的种类相同,均为HCO、HO、Na+、H+、OH-、 、 ,D错
2 3 2
误;
故答案选A。
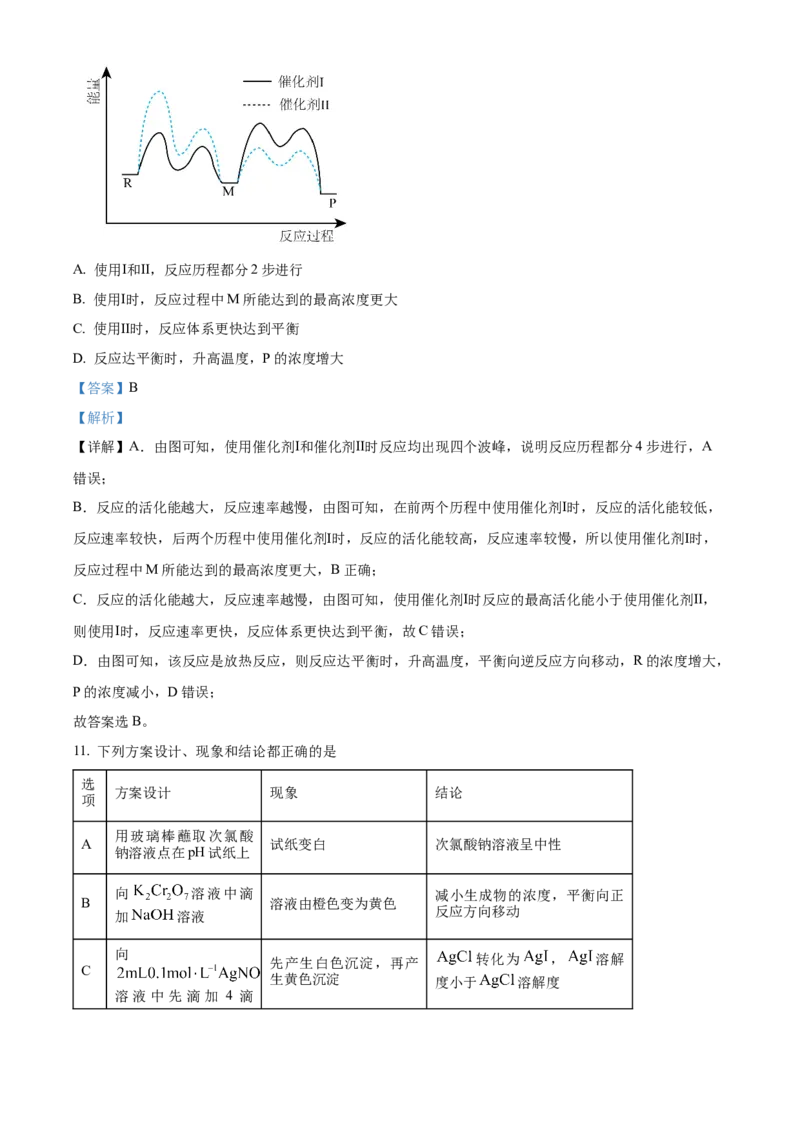
6. 下列说法正确的是
A. 图甲操作可排出盛有 溶液滴定管尖嘴内的气泡
B. 图乙装置可测定中和反应的反应热
C. 图丙装置可测定氢气的生成速率
D. 图丁装置可制取无水
【答案】D
【解析】
【详解】A.用酸式滴定管盛 溶液,故A错误;
B.用乙装置可测定中和反应的反应热,缺少环形玻璃搅拌器,故B错误;
C.氢气能从长颈漏斗逸出,不能用丙装置测定氢气的生成速率,故C错误;
D.为防止氯化镁水解,在氯化氢气流中加热氯化镁晶体制取无水 ,故D正确;
选D。
7. 为阿伏加德罗常数的值,下列说法正确的是
A. 溶液中含 的数目为
B. 的 溶液中 的数目为
C. 向 溶液中通氨气至中性, 的数目为
D. 与 混合生成 的数目为【答案】B
【解析】
【详解】A.该 溶液中溶质的物质的量为1mol,但 会发生水解,则 的数目小于N ,A
A
错误;
B.按pH的定义,该溶液中氢离子的物质的量为0.01mol,则氢离子的数目为0.01N ,B正确;
A
C.醋酸溶液通氨气至中性,溶液中溶质为醋酸铵、其物质的量为0.1mol,但铵离子和醋酸根离子均部分
水解,则铵根离子的数目小于0.1N ,C错误;
A
D. ,则一氧化氮和氧气恰好完全反应生成二氧化氮、其物质的量为0.2mol,但存在可
逆反应 ,故 的数目小于0.2N ,D错误;
A
答案选B。
8. 下列关于滴定实验叙述正确的是
A. 装标准液的滴定管滴定前有气泡,滴定后气泡消失,所得待测液浓度偏大
B. 用 标准溶液滴定未知浓度的 溶液,可用甲基橙作指示剂
C. 量取一定体积的待测液时,眼睛注视锥形瓶中溶液颜色变化
D. 用标准液润洗滴定管后,应将润洗液从滴定管上口倒出
【答案】A
【解析】
【详解】A.装标准液的滴定管滴定前有气泡,滴定后气泡消失,消耗标准液的体积读数偏大,则所得待
测液浓度偏大,A正确;
B.用NaOH标准溶液滴定未知浓度的CHCOOH溶液,恰好反应时溶液显碱性,应选择碱性范围内变色
3
的指示剂,甲基橙的变色范围为3.1~4.4,不能选用甲基橙作指示剂,应选择酚酞作指示剂,B错误;
C.量取一定体积的待测液时,视线与滴定管中凹液面相切,C错误;
D.用标准液润洗滴定管后,应将润洗液从滴定管下口放出,因滴定管尖嘴部分也需要润洗,D错误;
故选A。
9. 亚磷酸 是二元弱酸,室温下, , 。在浓度为 的
溶液中,下列说法正确的是
A. 该溶液中浓度最大的离子是B. 该溶液呈碱性
C. 该溶液中
D. 该溶液中
【答案】D
【解析】
【详解】A.亚磷酸 是二元弱酸, 的 溶液中 会发生水解和电离,则
溶液中c(Na+)>c( ),该溶液中浓度最大的离子是Na+,A错误;
B. 的 溶液中 的水解常数为
,说明 的水解程度小于电离程度,则溶
液呈酸性,B错误;
的
C.亚磷酸 是二元弱酸, 溶液中存在物料守恒:
,C错误;
D. 的 溶液中存在电荷守恒:
,D正确;
故选D。
10. 催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为其中一个中间产物。其它条件相同
时,下列说法正确的是A. 使用Ⅰ和Ⅱ,反应历程都分2步进行
B. 使用Ⅰ时,反应过程中M所能达到的最高浓度更大
C. 使用Ⅱ时,反应体系更快达到平衡
D. 反应达平衡时,升高温度,P的浓度增大
【答案】B
【解析】
【详解】A.由图可知,使用催化剂Ⅰ和催化剂Ⅱ时反应均出现四个波峰,说明反应历程都分4步进行,A
错误;
B.反应的活化能越大,反应速率越慢,由图可知,在前两个历程中使用催化剂Ⅰ时,反应的活化能较低,
反应速率较快,后两个历程中使用催化剂Ⅰ时,反应的活化能较高,反应速率较慢,所以使用催化剂Ⅰ时,
反应过程中M所能达到的最高浓度更大,B正确;
C.反应的活化能越大,反应速率越慢,由图可知,使用催化剂Ⅰ时反应的最高活化能小于使用催化剂Ⅱ,
则使用Ⅰ时,反应速率更快,反应体系更快达到平衡,故C错误;
D.由图可知,该反应是放热反应,则反应达平衡时,升高温度,平衡向逆反应方向移动,R的浓度增大,
P的浓度减小,D错误;
故答案选B。
11. 下列方案设计、现象和结论都正确的是
选
方案设计 现象 结论
项
用玻璃棒蘸取次氯酸
A 试纸变白 次氯酸钠溶液呈中性
钠溶液点在pH试纸上
向 溶液中滴 减小生成物的浓度,平衡向正
B 溶液由橙色变为黄色
反应方向移动
加 溶液
向
先产生白色沉淀,再产 转化为 , 溶解
C
生黄色沉淀 度小于 溶解度
溶液中先滴加 4 滴溶
液 , 再 滴 加 4 滴
溶液
用
溶液分别中和等体积
的 消耗的
D 酸性:
溶 液 和 溶液多
溶液
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.NaClO溶液具有强氧化性,能漂白pH试纸,不能用pH试纸测NaClO溶液的pH,NaClO属
于强碱弱酸盐,NaClO溶液呈碱性,A项错误;
B.在KCr O 溶液中存在平衡 +H O 2 +2H+,滴加NaOH溶液,OH-消耗H+,H+浓度减小,
2 2 7 2
平衡正向移动,溶液由橙色变为黄色,B项正确;
C.向2mL0.1mol/LAgNO 溶液中滴加4滴0.1mol/LKCl溶液,产生白色AgCl沉淀后AgNO 溶液过量,再
3 3
滴加4滴0.1mol/LKI溶液,过量的AgNO 溶液与KI直接反应产生黄色沉淀,不能说明AgCl转化成AgI,
3
不能比较AgCl和AgI溶解度的大小,C项错误;
D.用0.1mol/LNaOH溶液分别中和等体积的0.1mol/LH SO 溶液和0.1mol/LCH COOH溶液,HSO 消耗的
2 4 3 2 4
NaOH溶液多,说明HSO 的元数大于CHCOOH,不能比较HSO 、CHCOOH酸性强弱,D项错误;
2 4 3 2 4 3
答案选B。
人类的生长发育和社会可持续发展在很大程度上依赖于分子氮的固定,经过数十年几代科学家的努力,我
国固氮研究取得了世界瞩目的成绩。请完成下列两题。
12. 近期,华东师范大学合成了 催化剂,显示出优异的光催化固氮活性。光催化剂在紫外
线照射下产生光生电子 和光生空穴 ,反应历程如下图所示(*代表吸附在催化剂表面的物种)。下
列说法错误的是A. 反应过程中有非极性键的断裂和形成
B. 转化的过程可表示为:
C. 以 为催化剂时,决速步的能垒
D. 相同条件下,使用 催化剂时的平衡转化率更高
13. 固氮过程中可能会产生肼 ,肼常用于航天的燃料,也可催化氧化生产 :
,下列说法正确的是
A. 该反应不能自发进行
B. 容积一定,通入 使压强增大,可使平衡向逆反应方向移动
C. 催化剂提高了活化分子的百分数,使单位体积内有效碰撞次数增加从而反应速率加快
D. 保持其他条件不变,适当提高 的比值可以提高 的转化率
【答案】12. D 13. C
【解析】
【12题详解】
A.反应过程中氮氮三键断裂,氧氧双键形成,故存在非极性键的断裂和形成,A正确;
B.HO转化的过程可表示为:2HO+4h+=O +4H+,B正确;
2 2 2
C.决速步的化学反应速率最小,能垒最大,由图可知,以ZnS为催化剂时,决速步的能垒E =1.07eV,
正
C正确;
D.催化剂能够加快反应速率,不影响平衡移动,无法改变平衡转化率,D错误;
故答案选D;
【13题详解】
A.该反应△S>0,△H<0,在低温下能够自发进行,A错误;B.容积一定,通入N 使压强增大,不影响反应物、生成物浓度,不影响反应速率,平衡不移动,B错误;
2
C.化剂提高了活化分子的百分数,提高单位体积内的活化分子数,使单位体积内有效碰撞次数增加从而
反应速率加快,C正确;
的
D.保持其他条件不变,适当提高n(N H)/n(O) 比值可以提高O 的转化率,NH 的转化率降低,D
2 4 2 2 2 4
错误;
故答案选C。
14. T℃时, 和 (砖红色)都是难溶电解质,以
对 或 作图的沉淀平衡曲线如图所示。该温度下,下列说法正确的是
A. 阴影区域 和 都沉淀
B. 的饱和溶液中, 时,
C. 向含有 的 溶液中加入 ,白色固体逐渐变为砖红色
D. 用硝酸银滴定 ,指示剂 浓度在 左右时滴定误差较小
【答案】D
【解析】
【分析】由图可知,当pAg=0时,c(Ag+)=1mol/L,pCl=9.8,pCrO=11.72,K (Ag CrO)=c2(Ag+)•c(
4 sp 2 4
),K (AgCl)=c(Ag+)•c(Cl-),曲线①对应的溶度积常数K =10-11.72,数量级为10-12,曲线②对应的溶度积常
sp sp
数K =10-9.8,数量级为10-10,且K (AgCl)=1.6×10-10,所以曲线①线代表Ag CrO ,曲线②代表AgCl;所
sp sp 2 4
以K (Ag CrO)=10-11.72,K (AgCl)=10-9.8,据此分析解答。
sp 2 4 sp
【详解】A.纵坐标越大,银离子浓度越小,横坐标越大,阴离子浓度越小,故阴影区域AgCl和Ag CrO
2 4
都不沉淀,A错误;B.2pAg+pCrO=11.72,pCrO=4.45时,pAg= =3.635,B错误;
4 4
C.当溶液中有1.0mol/LKCl溶液时,则此时氯离子的浓度为1.0mol/L,pCl=0,由图可知,此时无法形成
Ag CrO,C错误;
2 4
D.由图可知,当KCrO 浓度在0.01mol/L左右时(pCrO =2)形成Ag CrO 所需要的银离子浓度约为10-
2 4 4 2 4
5mol/L,根据氯化银的溶度积可知此时氯离子浓度约为1.6×10-5mol/L,氯离子接近完全沉淀,滴定误差较
小,D正确;
故答案选D。
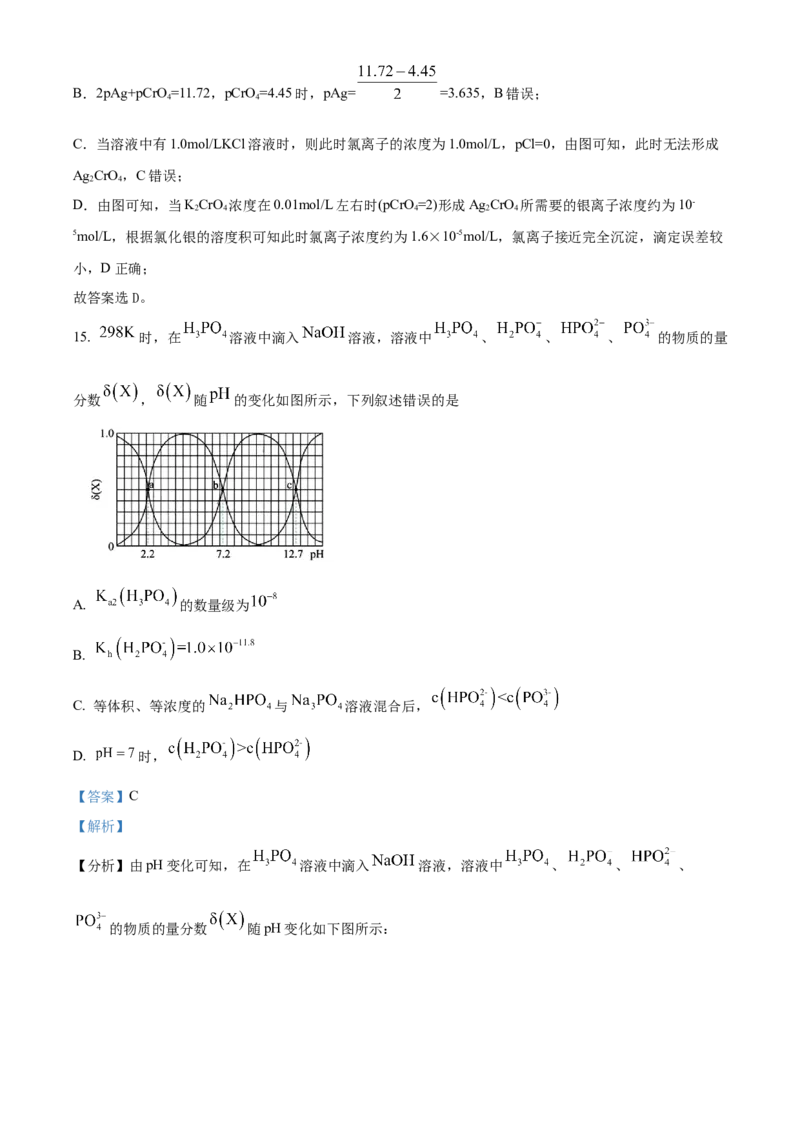
15. 时,在 溶液中滴入 溶液,溶液中 、 、 、 的物质的量
分数 , 随 的变化如图所示,下列叙述错误的是
A. 的数量级为
B.
C. 等体积、等浓度的 与 溶液混合后,
D. 时,
【答案】C
【解析】
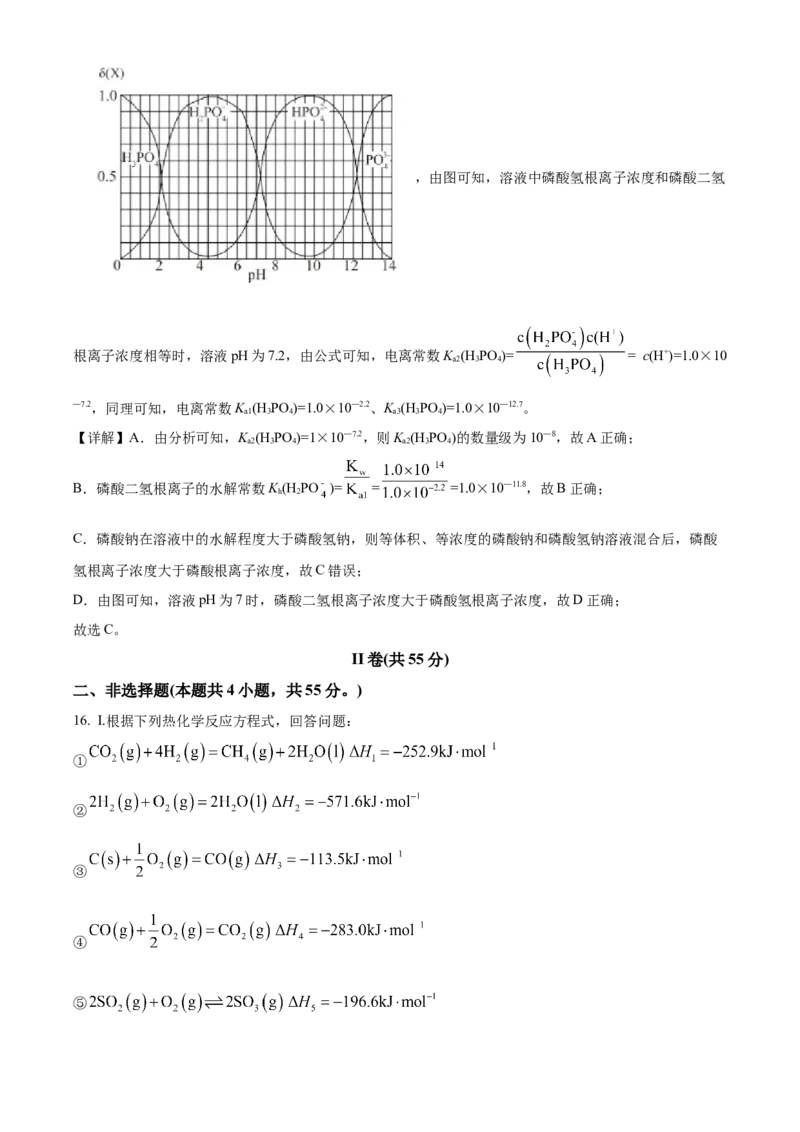
【分析】由pH变化可知,在 溶液中滴入 溶液,溶液中 、 、 、
的物质的量分数 随pH变化如下图所示:,由图可知,溶液中磷酸氢根离子浓度和磷酸二氢
根离子浓度相等时,溶液pH为7.2,由公式可知,电离常数K (H PO )= = c(H+)=1.0×10
a2 3 4
—7.2,同理可知,电离常数K (H PO )=1.0×10—2.2、K (H PO )=1.0×10—12.7。
a1 3 4 a3 3 4
【详解】A.由分析可知,K (H PO )=1×10—7.2,则K (H PO )的数量级为10—8,故A正确;
a2 3 4 a2 3 4
B.磷酸二氢根离子的水解常数K (H PO )= = =1.0×10—11.8,故B正确;
h 2
C.磷酸钠在溶液中的水解程度大于磷酸氢钠,则等体积、等浓度的磷酸钠和磷酸氢钠溶液混合后,磷酸
氢根离子浓度大于磷酸根离子浓度,故C错误;
D.由图可知,溶液pH为7时,磷酸二氢根离子浓度大于磷酸氢根离子浓度,故D正确;
故选C。
II卷(共55分)
二、非选择题(本题共4小题,共55分。)
16. I.根据下列热化学反应方程式,回答问题:
①
②
③
④
⑤(1)上述反应中,表示燃烧热的热化学方程式有_______(填序号),写出甲烷燃烧热的热化学方程式
_______。
(2)下列情况能说明反应⑤达到化学平衡状态的是_______。
A.
B. 、 、 三者的浓度之比为2:1:2
C. 的物质的量不再改变
D. 恒温恒容时,混合气体的密度不改变
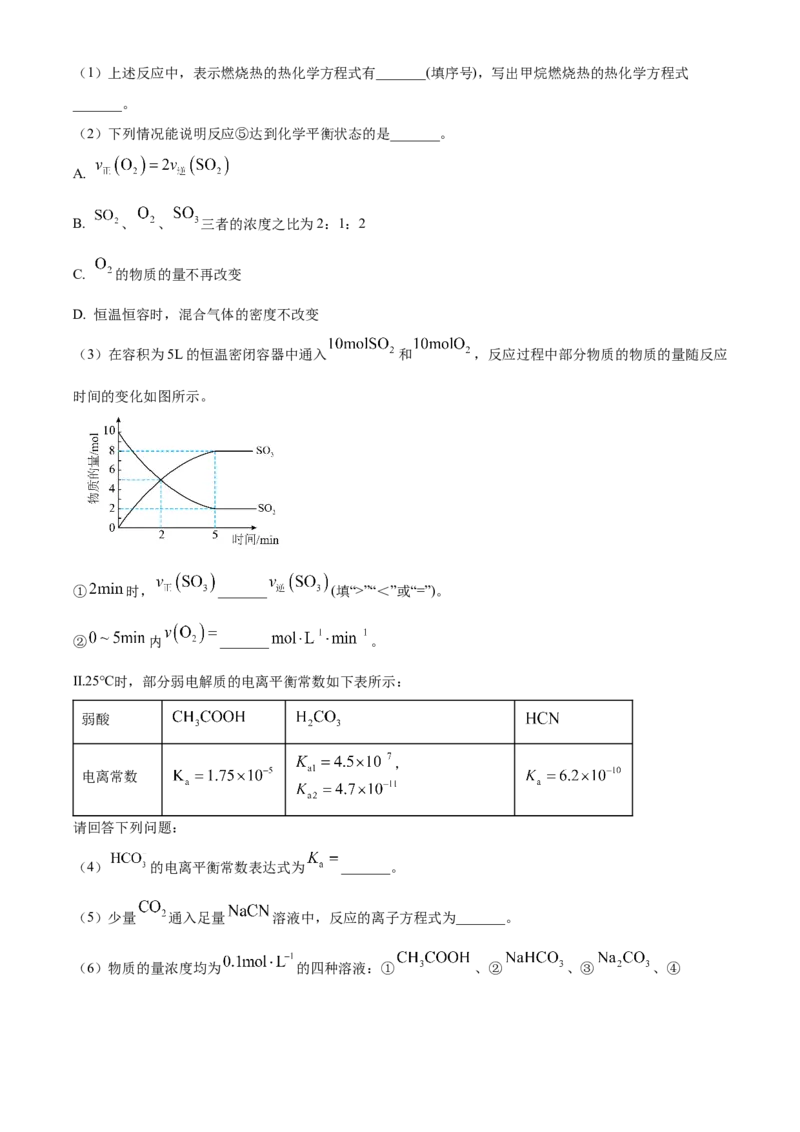
(3)在容积为5L的恒温密闭容器中通入 和 ,反应过程中部分物质的物质的量随反应
时间的变化如图所示。
① 时, _______ (填“>”“<”或“=”)。
② 内 _______ 。
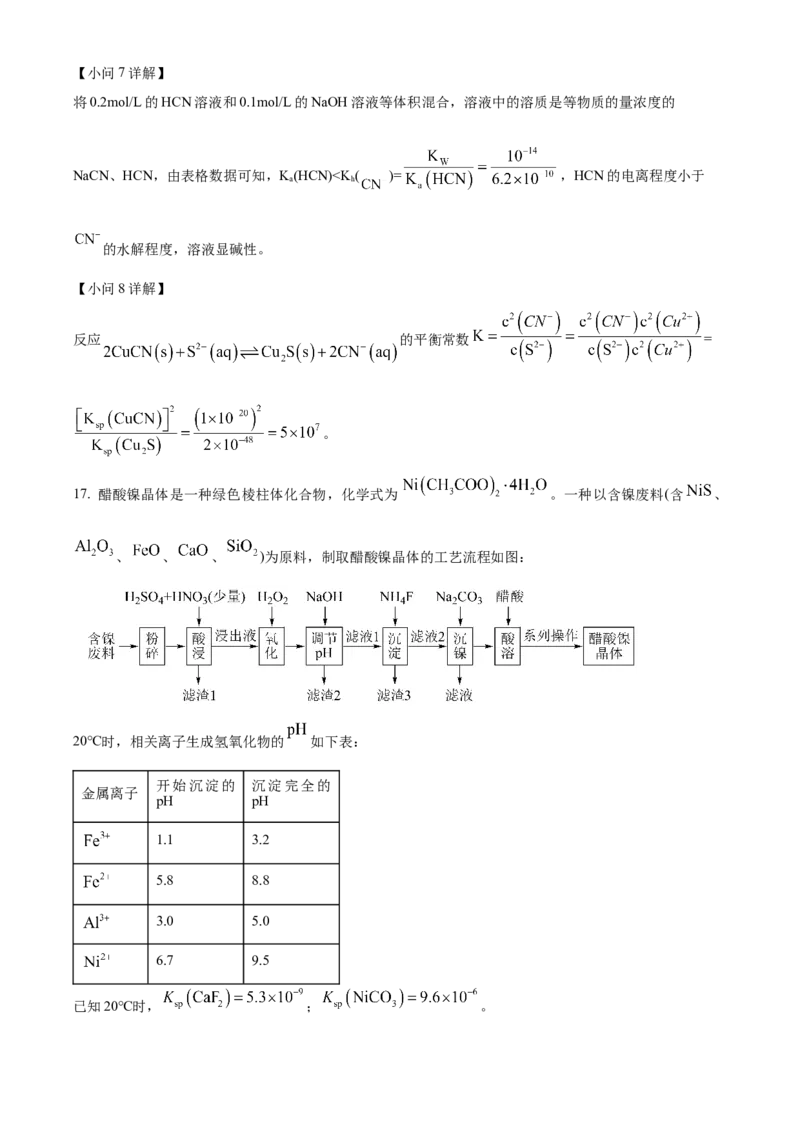
Ⅱ.25℃时,部分弱电解质的电离平衡常数如下表所示:
弱酸
,
电离常数
请回答下列问题:
(4) 的电离平衡常数表达式为 _______。
(5)少量 通入足量 溶液中,反应的离子方程式为_______。
(6)物质的量浓度均为 的四种溶液:① 、② 、③ 、④, 由小到大的排列顺序是_______(用序号表示)。
(7) 溶液与 溶液等体积混合后,溶液显_______性(填“酸”“碱”或
“中”)。
(8)已知 ℃时, ,则 ℃下,反应
的平衡常数 _______。
【答案】(1) ①. :④ ②. -890.3
(2)C
(3) ①. > ②. 0.16
(4)
(5)
(6)③>④>②>① (7)碱
(8)
【解析】
【小问1详解】
燃烧热是指在25℃,101kPa时,1mol纯物质完全燃烧生成稳定氧化物时所放出的热量,上述反应中,表
示燃烧热的热化学方程式是④ ;由盖斯定律可知,
② ×2-① 可 得 甲 烷 燃 烧 热 的 热 化 学 方 程 式 为 :
=-890.3 。
【小问2详解】
A.当 时反应达到平衡,v (O )=2v (SO )不能说明反应达到平衡,A不选;
正 2 逆 2B. 、 、 三者的浓度之比为2:1:2时,该反应不一定达到平衡状态,与反应初始物质的量和
转化率有关,所以不能据此判断平衡状态,B不选;
C. 的物质的量不再改变,说明说明正逆反应速率相等,反应达到平衡,C选;
D.恒温恒容时,该反应过程中气体总质量和总体积都是定值,混合气体的密度是定值,当混合气体的密
度不改变时,不能说明反应达到平衡,D不选;
故选C。
【小问3详解】
① 后, 的物质的量仍在减小, 的物质的量仍在增大,说明 时反应正向进行,
> ;
② 内 。
【小问4详解】
的电离平衡常数表达式为 。
【小问5详解】
酸的电离常数越大,酸性越强,由表格数据可知,酸性: > > ,少量 通入足量
溶液中,根据强酸制取弱酸的原理可知,生成HCN和NaHCO ,离子方程式为:
3
。
【
小问6详解】
物质的量浓度均为 的四种溶液中 是酸,溶液中氢离子浓度最大,pH最小,相同物
质的量浓度的钠盐溶液,对应的酸的酸性越弱,则酸根离子水解程度越大,其溶液的pH越大,由表格数
据可知酸性: > > ,则水解程度: > > ,则pH由大到小的顺序为
③>④>②>①。【小问7详解】
将0.2mol/L的HCN溶液和0.1mol/L的NaOH溶液等体积混合,溶液中的溶质是等物质的量浓度的
NaCN、HCN,由表格数据可知,K(HCN)