文档内容
2025 届高三第一学期期中考试检测卷
化学
全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上
的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非一
答题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
5.本卷主要考查内容:化学物质及其变化、物质的量、化学实验基础知识、金属及其化合物、
非金属及其化合物、元素及其化合物综合应用(60%),其余高考内容(40%)。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学处处呈现美。下列说法错误的是
A. 氮的固定,一定包含共价键的断裂和形成
B. 北宋名画“千里江山图”中水墨底颜料是墨汁,其主要成分为炭黑
C. 很多金属或它们的化合物在焰色试验中呈现出的特征焰色属于发射光谱的颜色
D. 绚丽多彩的晚霞是丁达尔效应带来的美景
2. 下列有关化学用语表示正确的是
A. CCl 的空间填充模型为
4
B. CO 的电子式为
2
C. Cu原子的简化电子排布式为[Ar]3d94s2
D. Cl 分子中的共价键的电子云图形为
23. 下列有关物质的性质与用途具有对应关系的是
A. 具有两性,可用作耐火材料
B. 青铜比纯铜熔点低、硬度大,古代用青铜铸剑
C. 能与酸反应,可用作铁磁性材料
D. 受热易分解,可用作抗酸药
的
4. 下列离子方程式与所给事实不相符 是
A. 通入氢氧化钠溶液:
B. 盐酸去除水垢中的 :
C. 利用覆铜板制作印刷电路板:
D. 用两个铜电极电解 溶液:
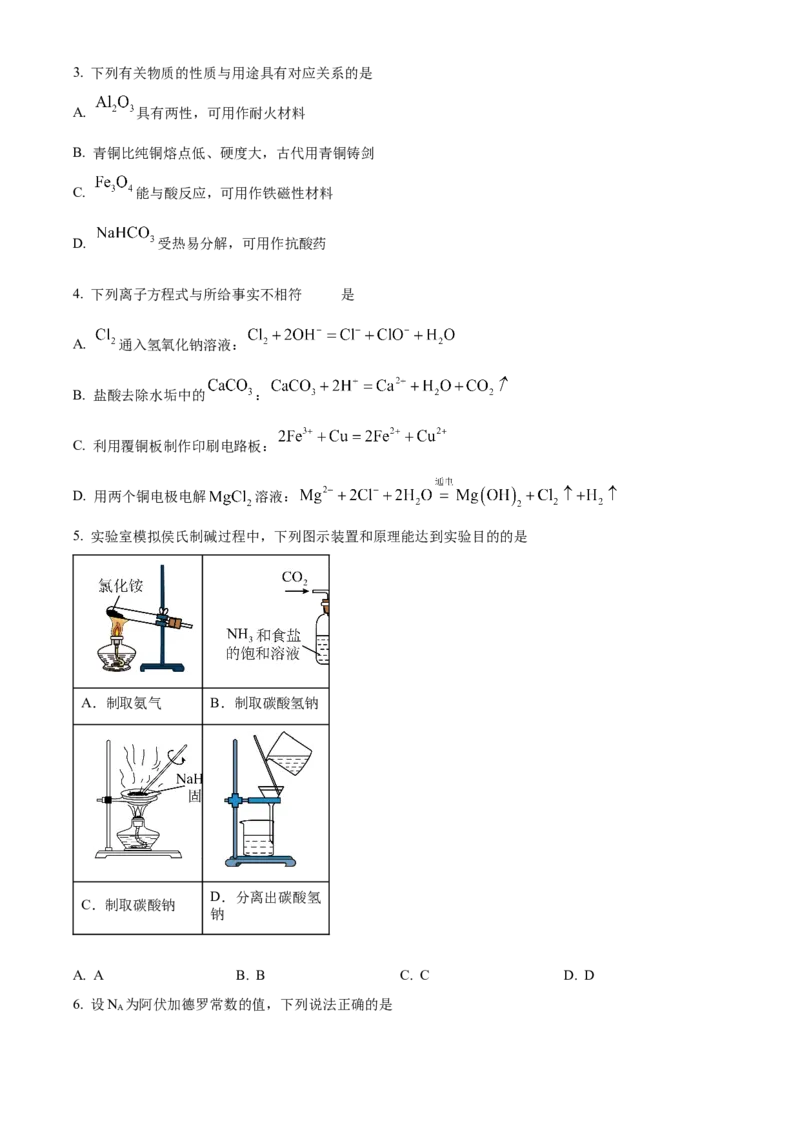
5. 实验室模拟侯氏制碱过程中,下列图示装置和原理能达到实验目的的是
A.制取氨气 B.制取碳酸氢钠
D.分离出碳酸氢
C.制取碳酸钠
钠
A. A B. B C. C D. D
6. 设N 为阿伏加德罗常数的值,下列说法正确的是
AA. 18g重水(DO)含有的中子数为10 N
2 A
B. 溶液中含有Fe3+数目小于0.2N
A
C. 晶体含有的离子总数为1.5 N
A
D. 标准状况下, 完全反应,转移的电子数一定为0.2N
A
7. ①向蓝色的 溶液中滴加酸性 溶液,溶液由蓝色变为淡黄色 ;
②向 溶液中滴加浓盐酸产生黄绿色气体 ,溶液变蓝;
③ (足量) 。
下列说法错误的是
A. ①中还原剂与氧化剂的物质的量之比为
B. 由①、②可知,酸性条件下氧化性;
C. ②中每生成 ,转移 电子
D. 向酸性 溶液中滴加少量 溶液,发生的反应为
8. 室温下,下列实验探究方案能达到探究目的的是
选
探究方案 探究目的
项
向 溶液中加入几滴新制的氯水,振荡,
A 还原性强于
再加 萃取,观察 层颜色变化
向 溶液中滴加过量的氯水;再加入淀粉
B 氧化性:
溶液,观察溶液颜色变化
将灼热的木炭投入热的浓硝酸中,有红棕色气 木炭在加热条件下能与浓硝酸
C
体产生 反应
向溶有 的 溶液中通入气体X,出现
D 气体X具有强氧化性
白色沉淀A. A B. B C. C D. D
9. 如下表所示,对陈述1和陈述2的正确性及两者间是否具有因果关系的判断都正确的是
选
陈述1 陈述2 判断
项
1
对,2
A 碳酸钠可用于治疗胃病 碳酸钠可与盐酸反应
对 ,
有
1
向滴有酚酞的水溶液中加入过氧化钠,溶液最终 过氧化钠与水发生化合反应生成氢 对,2
B
变红色 氧化钠 错 ,
无
1
对,2
C 金属钠具有强还原性 钠可置换出硫酸铜溶液中的铜
对 ,
有
1
对,2
D 碳酸氢钠可作为发酵粉用于烘焙糕点 碳酸钠溶解度比碳酸氢钠溶解度大
对 ,
无
A. A B. B C. C D. D
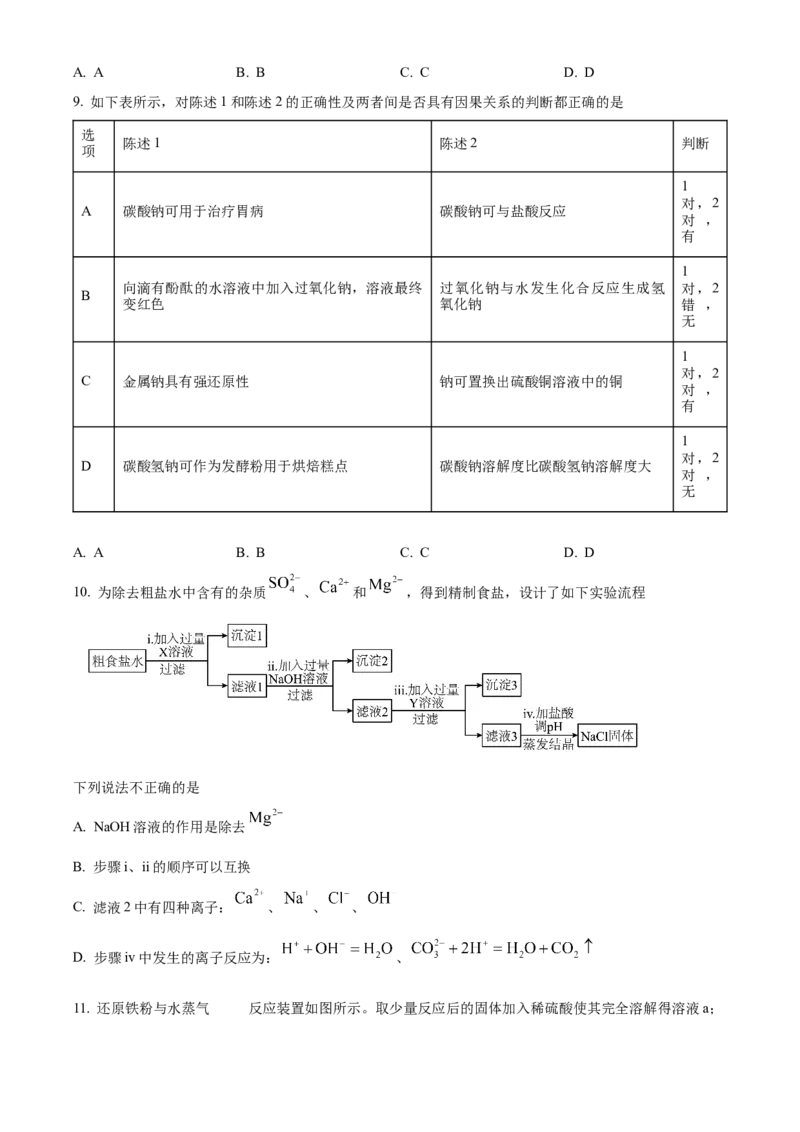
10. 为除去粗盐水中含有的杂质 、 和 ,得到精制食盐,设计了如下实验流程
下列说法不正确的是
A. NaOH溶液的作用是除去
B. 步骤i、ii的顺序可以互换
C. 滤液2中有四种离子: 、 、 、
D. 步骤iv中发生的离子反应为: 、
的
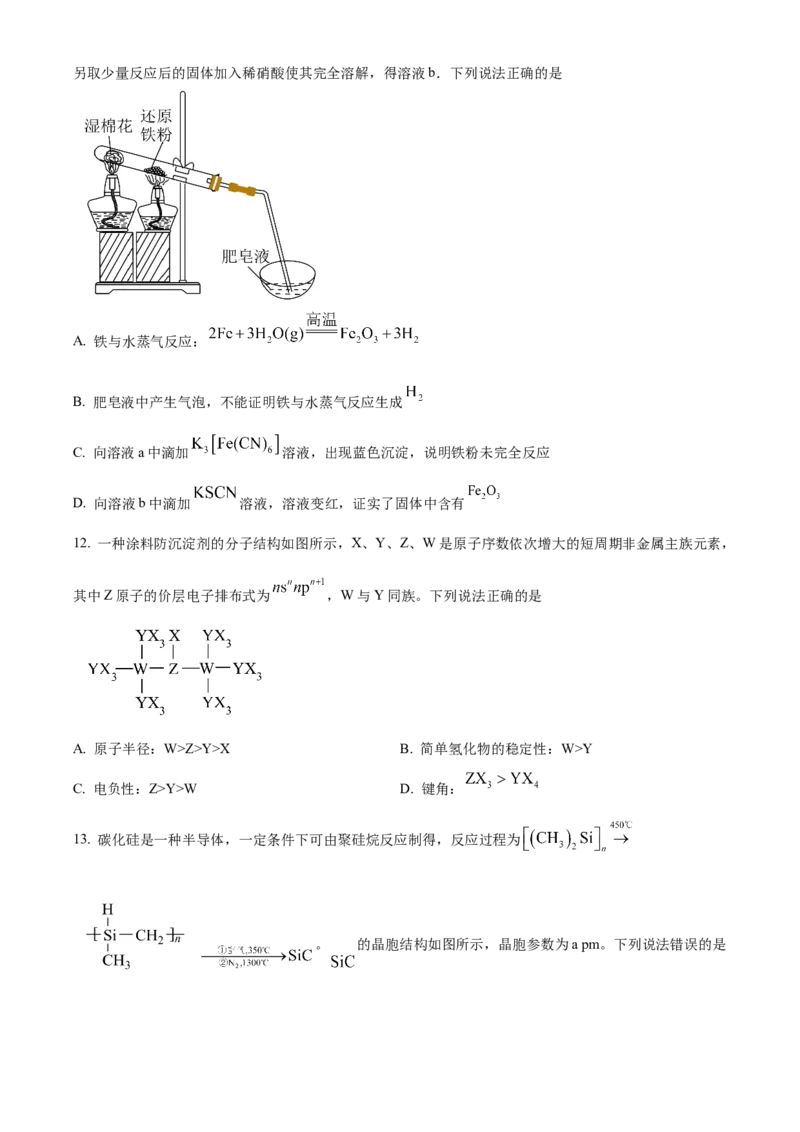
11. 还原铁粉与水蒸气 反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另取少量反应后的固体加入稀硝酸使其完全溶解,得溶液b.下列说法正确的是
A. 铁与水蒸气反应:
B. 肥皂液中产生气泡,不能证明铁与水蒸气反应生成
C. 向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉未完全反应
D. 向溶液b中滴加 溶液,溶液变红,证实了固体中含有
12. 一种涂料防沉淀剂的分子结构如图所示,X、Y、Z、W是原子序数依次增大的短周期非金属主族元素,
其中Z原子的价层电子排布式为 ,W与Y同族。下列说法正确的是
A. 原子半径:W>Z>Y>X B. 简单氢化物的稳定性:W>Y
C. 电负性:Z>Y>W D. 键角:
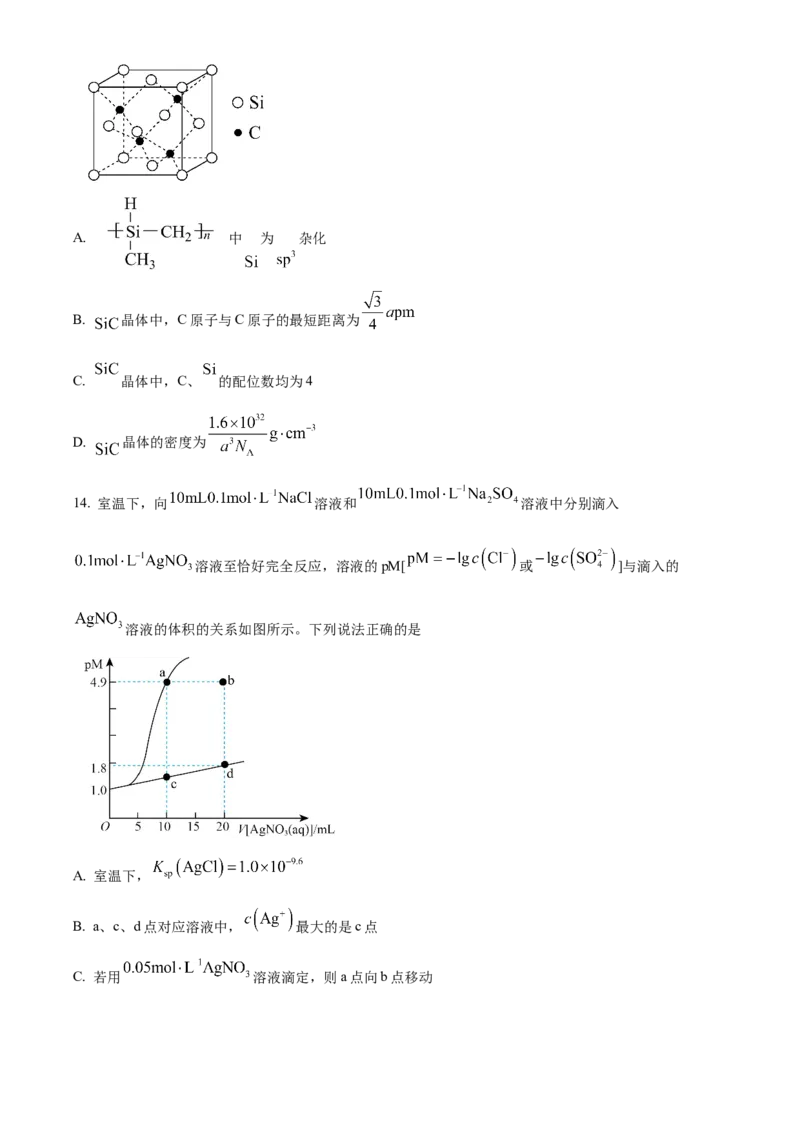
13. 碳化硅是一种半导体,一定条件下可由聚硅烷反应制得,反应过程为
。 的晶胞结构如图所示,晶胞参数为a pm。下列说法错误的是A. 中 为 杂化
B. 晶体中,C原子与C原子的最短距离为
C. 晶体中,C、 的配位数均为4
D. 晶体的密度为
14. 室温下,向 溶液和 溶液中分别滴入
溶液至恰好完全反应,溶液的pM[ 或 ]与滴入的
溶液的体积的关系如图所示。下列说法正确的是
A. 室温下,
B. a、c、d点对应溶液中, 最大的是c点
C. 若用 溶液滴定,则a点向b点移动D. 室温下,反应 的平衡常数
二、非选择题:本题共4小题,共58分。
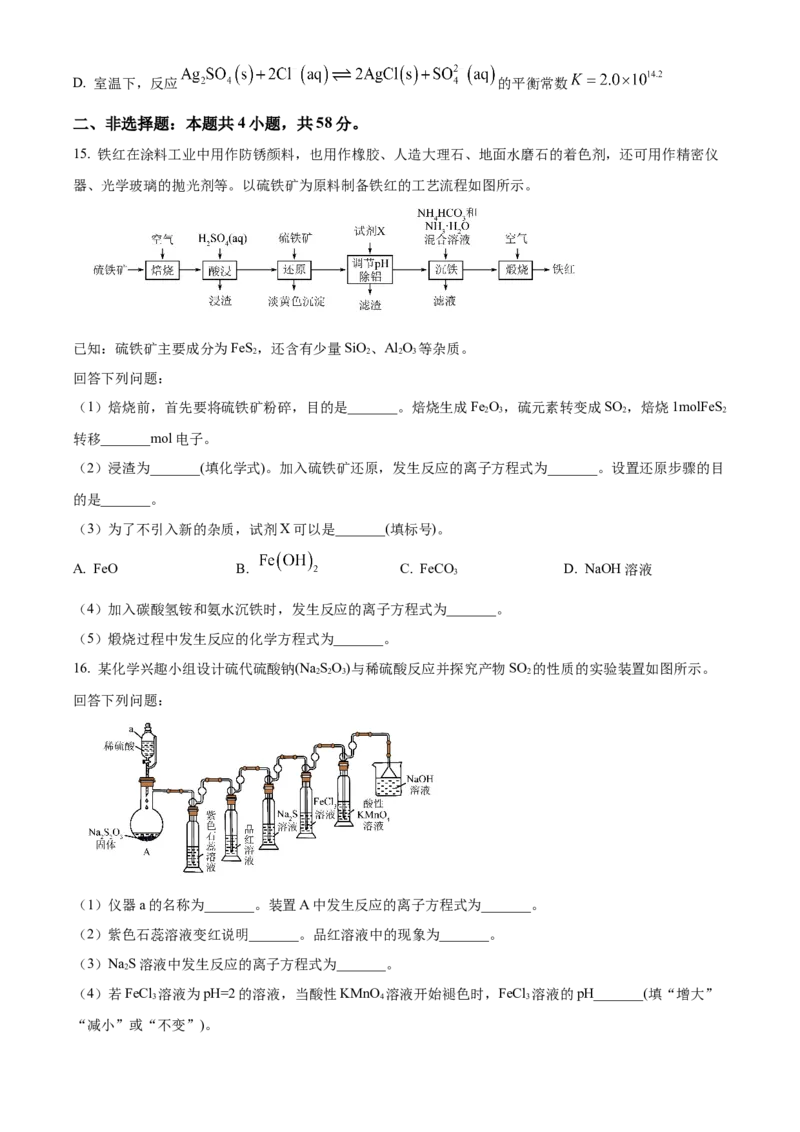
15. 铁红在涂料工业中用作防锈颜料,也用作橡胶、人造大理石、地面水磨石的着色剂,还可用作精密仪
器、光学玻璃的抛光剂等。以硫铁矿为原料制备铁红的工艺流程如图所示。
已知:硫铁矿主要成分为FeS,还含有少量SiO、Al O 等杂质。
2 2 2 3
回答下列问题:
(1)焙烧前,首先要将硫铁矿粉碎,目的是_______。焙烧生成Fe O,硫元素转变成SO ,焙烧1molFeS
2 3 2 2
转移_______mol电子。
(2)浸渣为_______(填化学式)。加入硫铁矿还原,发生反应的离子方程式为_______。设置还原步骤的目
的是_______。
(3)为了不引入新的杂质,试剂X可以是_______(填标号)。
A. FeO B. C. FeCO D. NaOH溶液
3
(4)加入碳酸氢铵和氨水沉铁时,发生反应的离子方程式为_______。
(5)煅烧过程中发生反应的化学方程式为_______。
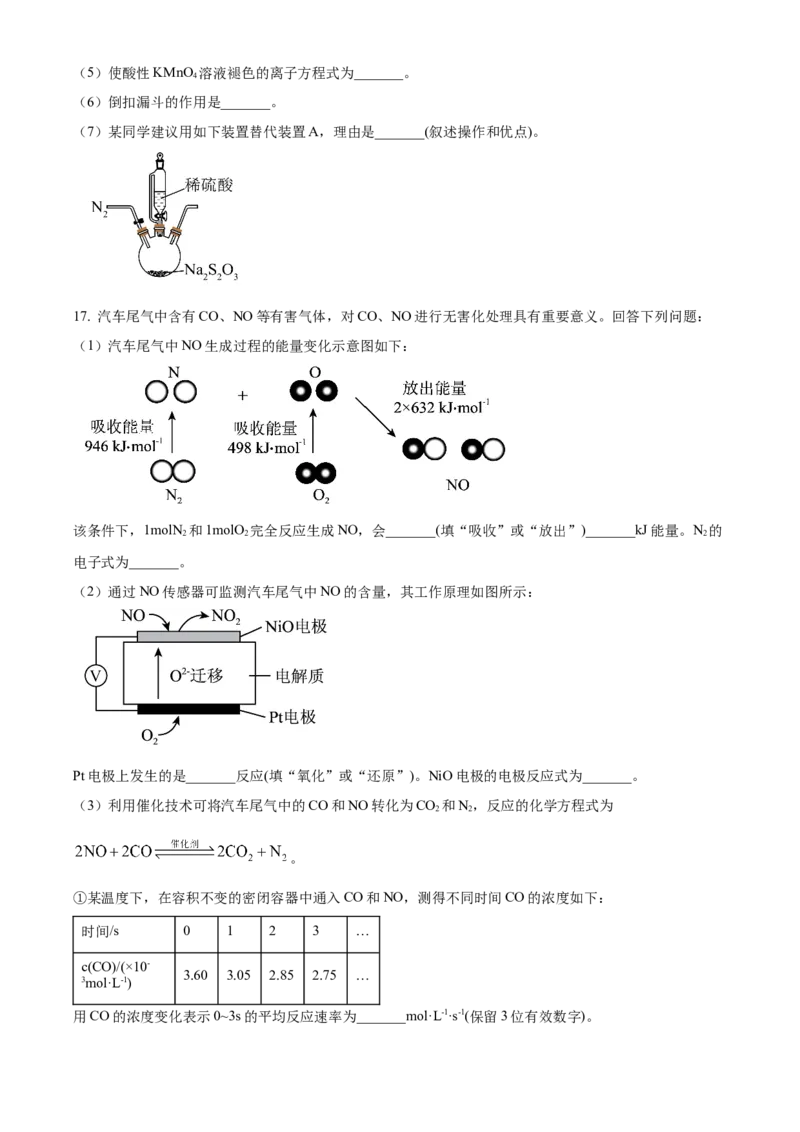
16. 某化学兴趣小组设计硫代硫酸钠(Na SO)与稀硫酸反应并探究产物SO 的性质的实验装置如图所示。
2 2 3 2
回答下列问题:
(1)仪器a的名称为_______。装置A中发生反应的离子方程式为_______。
(2)紫色石蕊溶液变红说明_______。品红溶液中的现象为_______。
(3)NaS溶液中发生反应的离子方程式为_______。
2
(4)若FeCl 溶液为pH=2的溶液,当酸性KMnO 溶液开始褪色时,FeCl 溶液的pH_______(填“增大”
3 4 3
“减小”或“不变”)。(5)使酸性KMnO 溶液褪色的离子方程式为_______。
4
(6)倒扣漏斗的作用是_______。
(7)某同学建议用如下装置替代装置A,理由是_______(叙述操作和优点)。
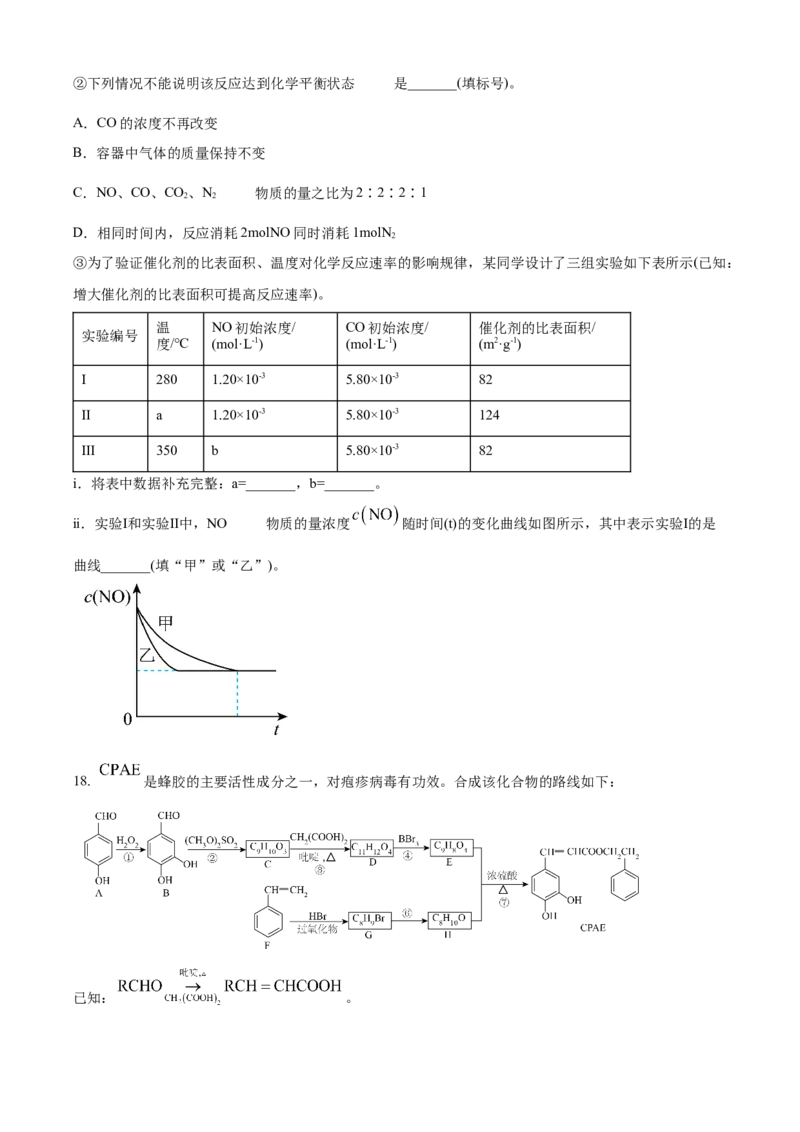
17. 汽车尾气中含有CO、NO等有害气体,对CO、NO进行无害化处理具有重要意义。回答下列问题:
(1)汽车尾气中NO生成过程的能量变化示意图如下:
该条件下,1molN 和1molO 完全反应生成NO,会_______(填“吸收”或“放出”)_______kJ能量。N 的
2 2 2
电子式为_______。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
Pt电极上发生的是_______反应(填“氧化”或“还原”)。NiO电极的电极反应式为_______。
(3)利用催化技术可将汽车尾气中的CO和NO转化为CO 和N,反应的化学方程式为
2 2
。
①某温度下,在容积不变的密闭容器中通入CO和NO,测得不同时间CO的浓度如下:
时间/s 0 1 2 3 …
c(CO)/(×10-
3.60 3.05 2.85 2.75 …
3mol·L-1)
用CO的浓度变化表示0~3s的平均反应速率为_______mol·L-1·s-1(保留3位有效数字)。的
②下列情况不能说明该反应达到化学平衡状态 是_______(填标号)。
A.CO的浓度不再改变
B.容器中气体的质量保持不变
的
C.NO、CO、CO、N 物质的量之比为2∶2∶2∶1
2 2
D.相同时间内,反应消耗2molNO同时消耗1molN
2
③为了验证催化剂的比表面积、温度对化学反应速率的影响规律,某同学设计了三组实验如下表所示(已知:
增大催化剂的比表面积可提高反应速率)。
温 NO初始浓度/ CO初始浓度/ 催化剂的比表面积/
实验编号
度/℃ (mol·L-1) (mol·L-1) (m2·g-1)
I 280 1.20×10-3 5.80×10-3 82
Ⅱ a 1.20×10-3 5.80×10-3 124
Ⅲ 350 b 5.80×10-3 82
ⅰ.将表中数据补充完整:a=_______,b=_______。
ⅱ.实验Ⅰ和实验Ⅱ中,NO 的物质的量浓度 随时间(t)的变化曲线如图所示,其中表示实验Ⅰ的是
曲线_______(填“甲”或“乙”)。
18. 是蜂胶的主要活性成分之一,对疱疹病毒有功效。合成该化合物的路线如下:
已知: 。回答下列问题:
(1)A的化学名称是_______。C中的官能团名称是_______。
(2)反应②、反应⑤的反应类型分别是_______、_______。
(3)设计反应②和反应④的目的是_______。
(4)D的结构简式为_______。
(5)反应⑦的化学方程式为_______。
(6)化合物I与C互为同分异构体,同时满足下列条件的I有_______种(不考虑立体异构)。
①含有苯环且苯环上有两个取代基
②与饱和 溶液反应产生
③与 溶液作用显紫色
其中核磁共振氢谱显示为六组峰,且峰面积比为 的同分异构体的结构简式为_______。