文档内容
五市十校 届高三第一次学业质量评价化学
T8& 2025
参考答案、提示及评分细则
【答案】
1. B
【解析】工业炼铜 化合态变为游离态 涉及氧化还原反应 项正确 铜属于不活泼金属 不能与酸反应生成氢
( ) ,A ; ,
气 不能发生析氢腐蚀 项错误 雕像基座上的瓷砖属于无机非金属材料 项正确 工人师傅的工具锤常采
, ,B ; ,C ;
用铁质而不采用铜质 铁质锤硬度比铜质锤硬度大 是主要原因之一 项正确
, , ,D .
【答案】
2. C
【解析】 的电子式 项错误
Na2O2 : ,C .
【答案】
3. D
【解析】金属钠与皮肤接触会腐蚀皮肤 严禁用手拿 项正确 含氯消毒剂具有一定的毒性 腐蚀性和刺激性 使
, ,A ; 、 ,
用时要注意个人防护 必要时佩戴防护眼镜 项正确 酸性高锰酸钾溶液具有腐蚀性 不慎沾到皮肤上 应立即
, ,B ; , ,
用大量水冲洗 项正确 分解产生水和二氧化碳 而镁能与水和二氧化碳反应 项错误
,C ;NaHCO3 , ,D .
【答案】
4. B
【解析】核糖和脱氧核糖都是含有 个碳原子的戊糖 项正确 杂化轨道只可用于形成 键 项错误
5 ,A ; σ ,B ;
虽难溶于水 但溶解的部分完全电离 属于强电解质 项正确 均为分子晶体 分子
BaSO4 , , ,C ;HF、HCl、HBr ,HF
间存在氢键 不存在分子间氢键 三种物质中沸点最高的是 的相对分子质量大于
,HCl、HBr , HF,HBr HCl,
沸点高于 三种物质沸点由高到低的顺序是 项正确
HBr HCl, HF>HBr>HCl,D .
【答案】
5. B
【解析】 葡萄糖和 葡萄糖在水溶液中能相互转化 所以无法用银氨溶液鉴别 项错误 工业上以淀粉
αGDG DG , ,A ;
水解生成的葡萄糖为原料 可用于合成氨基酸 项正确 葡萄糖属于单糖 不能发生水解反应 项错误
, ,B ; , ,C ;
葡萄糖和 葡萄糖均有饱和碳原子构成的环状结构 分子中所有碳原子不可能共平面 项错误
αGDG βGDG , ,D .
【答案】
6. C
【解析】漂白液生效的原理 项正确 保存氢氧化钠溶液不能用磨口
- -
:ClO +CO2+H2OHClO+HCO3 ,A ;
玻璃塞 项正确 铅酸蓄电池充电时 极 原电池的负极 也是充电时与外
- 2-
:2OH +SiO2SiO3 +H2O,B ; ○- ( ,
接电源负极相连的电极 反应 项错误 将 通入水中
- 2-
) :PbSO4+2e Pb+SO4 ,C ; NO2 :3NO2+H2O
项正确
2HNO3+NO,D .
【答案】
7. C
【解析】根据资料 在相应温度下 与 的反应为 实验 说明实验 后的
3+ - 3+ - 2+
, Fe I 2Fe +2I 2Fe +I2. (ⅱ) (ⅰ)
溶液中含有 实验 说明实验 后的溶液中含有 能验证相应温度下 与 的反应为可逆反
3+ 3+ -
Fe , (ⅲ) (ⅰ) I2, Fe I
应 项正确 实验 振荡过程中水层里的 进入 水层c 减小
3+
与
-
的反应向正方向移动
,A ; (ⅲ) I2 CCl4, (I2) ,Fe I ,B
项正确 溶液中存在的 对 的检验产生干扰 项错误 由于反应 溶液中
3+ 2+ 3+ 2+
; Fe Fe ,C ; 2Fe +Fe3Fe ,
c 3+ 减小 导致 3+ - 平衡逆向移动 红色变浅 项正确
(Fe ) , Fe +3SCN Fe(SCN)3 , ,D .
高三化学试题参考答案 第 页 共 页
【 1 ( 5 )】【答案】
8. D
【解析】苯不能与氢氧化钠溶液反应 苯酚能与氢氧化钠溶液反应 所以用氢氧化钠溶液洗涤后分液 重复
, , , 2~3
次 再用硫酸钠固体干燥有机层 最后除去干燥剂可以除去苯中的苯酚 项合理 向
-1
, , ,A ; 4mL0.1molL CuSO4
溶液中滴加 氨水至沉淀溶解 再加入 乙醇 过滤 可得 项合理
-1
1molL , 8mL95% , , [Cu(NH3)4]SO4H2O,B ;
硫酸和碳酸钠反应产生的二氧化碳 直接通入 溶液中 生成白色沉淀 说明酸性 碳酸大于硅酸 最高价
, Na2SiO3 , , : ,
氧化物的水化物的酸性越强 非金属性越强 项合理 用惰性电极电解硫酸铜溶液 足量 电解反应为
, ,C ; ( ), 2CuSO4
电解
欲使反应后的溶液恢复原状 应加入一定量的 项不合理
+2H2O2Cu+O2↑+2H2SO4, , CuO,D .
【答案】
9. C
【解析】电负性 项正确 分子中的每个氧原子均存在 对孤对电子 受孤对电子排斥力影
:N>C>H,A ;H2O2 2 ,
响 导致 分子中正负电荷中心不重合 故 是极性分子 项正确 氰基 中碳原子的杂化类
, H2O2 , H2O2 ,B ; (-CN)
型为 项错误 据图可知 生成 的过程中涉及反应 项正确
- + -
sp,C ; , H2O2 O2 +2H +e H2O2,D .
【答案】
10. B
【解析】由可知 极为阳极 极为阴极 极的电势比 极的高 项错误 极反应式为
- -
,X ,Y ,X Y ,A ;X HSO3 -2e +
项正确 极反应式为 电解总反应为
2- + - + + -
H2OSO4 +3H ,B ;Y N2+6e +8H 2NH4 , 3HSO3 +N2+
电解一段时间后 溶液中的 浓度增大 项错误 没有说明温度和压强
2- + + +
3H2O3SO4 +2NH4 +H , , H ,C ; ,
无法计算 项错误
,D .
【答案】
11. C
【解析】根据K K K K 可判断反应 中的反应为
a1(H2CO3)> a1(H2S)> a2(H2CO3)> a2(H2S), Ⅰ H2S+
项正确 依题意 反应 中的反应为
Na2CO3NaHS+NaHCO3,A ; , Ⅱ NaHS+RNO+H2ORNHOH+
氧化剂 与还原剂 物质的量之比为
S↓+NaOH、NaHCO3+NaOH Na2CO3+H2O, (RNO) (NaHS)
项正确 溶液中的 能与 发生双水解反应 生成大量的 沉淀 降低 的利
1∶1,B ; NaHCO3 FeCl3 , Fe(OH)3 , FeCl3
用率 而该工艺中 和碳酸钠能循环使用 项错误 依题意 该过程的总反应为
, RNO ,C ; , 2H2S+O22S+
项正确
2H2O,D .
【答案】
12. D
【解析】根据晶胞结构和原子分数坐标可判断 位于顶点和体心 个 位于面上 个 位于体内 故每
,Fe ,4 Sb ,2 Sb ,
个晶胞中有 个 和 个 该材料的化学式为 项正确 观察晶胞结构 的配位数是 项正
2 Fe 4 Sb, FeSb2,A ; ,Fe 6,B
m n a m a n
确 根据Y的分数坐标为 可判断Z的分数坐标为 - - 项正确 晶胞体积为
; (a,0,a), (a ,1,a ),C ;
a3 -30 3 晶胞质量为2×56+4×122 故该晶体的密度 600 30 -3 项错误
×10 cm , N g, a3N ×10 gcm ,D .
A A
【答案】
13. C
【解析】由K 表达式可得 2+ K 由K 表达式可得
sp[Cu(OH)2] :2pH=pCu -p sp+28, a(CH3COOH) :pH=
c c
(CH3COOH) K 后者的斜率较大 故曲线L 表示 (CH3COOH)随 的变化 项错误 将L
pc - +p a, , 1 pc - pH ,A ; 2
(CH3COO ) (CH3COO )
曲线的点 带入 2+ K 可得K -19.2 K 的数量级
(6.6,7.7) 2pH=pCu -p sp+28, sp[Cu(OH)2]=10 , sp[Cu(OH)2]
c
为 -20 项错误 将L 曲线的点 带入 (CH3COOH) K 可得K
10 ,B ; 1 (3.0,7.7) pH=pc - +p a, a(CH3COOH)=
(CH3COO )
-4.7 K c (H + ) c (CH3COO - ) c2 (H + ) -4.7c + -2.7 -1
10 , a(CH3COOH)= c = =10 , (H )=10 ,0.2molL
(CH3COOH) 0.2mol/L
高三化学试题参考答案 第 页 共 页
【 2 ( 5 )】溶液 项正确 酸碱恰好中和时 溶液中溶质为 溶液显碱性 当溶液显中
CH3COOH pH=2.7,C ; , CH3COONa, ,
性时 说明V 的体积小于醋酸溶液的体积 故溶液中c + c - -1
, [ NaOH(aq)] , (Na )= (CH3COO )<0.1molL ,
c - 项错误
p (CH3COO )>-lg0.1=1,D .
【答案】
14. D
【解析】催化剂能降低反应的活化能 提高活化分子百分数 项正确 起始投料比n n
, ,A ; (C2H2)∶ (H2)=1∶2,
若只发生反应 和 的消耗量相同 则 的转化率小于 的转化率 若只发生反应 和
ⅰ,C2H2 H2 , H2 C2H2 , ⅱ,C2H2
的消耗量为 则 的转化率等于 的转化率 当两个反应同时发生时 的转化率大于 的
H2 1∶2, H2 C2H2 , ,C2H2 H2
转化率 故m曲线表示 的转化率 项正确 由图可知 T 温度后二者的转化率几乎相等 可见主要发
, C2H2 ,B ; ,2 ,
生反应 故生成乙烷的选择性增大 的选择性减小 项正确 令n 为 n 为
ⅱ, ,C2H4 ,C ; (C2H2) 1mol、(H2) 2mol.
C2H2(g) +H2(g) C2H4(g)
变化量 a a a
/mol
C2H2(g) +2H2(g) C2H6(g)
变化量 b b b
/mol 2
a b a b 解得a b 故 的选择性 0.5mol
(+ )/1=0.75、(2 + )/2=0.5, :=0.25、=0.5, C2H4 = ×100%=
0.5mol+0.25mol
项错误
66.7%,D .
【答案】 分 每空 分
15. (14 , 2 )
乙醚或苯甲酰氯 任写 个即可
(1) ( 1 )
甘氨酸分子间形成的氢键数目比丙酸分子间形成的氢键数目多 或甘氨酸分子中氨基的也参与氢键的形
(2) (
成 合理即可
, ) H2NCH2COOH+NaOHH2NCH2COONa+H2O
中和副产物 提高产率
(3) HCl,
将马尿酸钠转化成马尿酸
(4)
过滤速度快 液体和固体分离比较完全 滤出固体容易干燥 合理即可
(5) 、 、 ( ) ④③
【解析】 乙醚 的沸点 又是烃的含氧衍生物 属于易燃液体 苯甲酰氯的熔点
(1) (C2H5OC2H5) 34.6℃, , ; -1℃,
也属于易燃液体
.
甘氨酸含有羧基 能和碱反应
(2) , .
当反应发生后 生成了 导致溶液呈酸性 加入氢氧化钠中和 促进反应向正方向进行 提高产率
(3) , HCl, , HCl, , .
抽滤的优点是 过滤和洗涤速度快 液体和固体分离比较完全 滤出固体容易干燥 抽滤完毕需进行下列
(5) : 、 、 ;
操作 从实验安全角度考虑 先打开安全瓶的活塞 拔下抽滤瓶处橡皮管 关闭水泵开关 取下布氏漏斗
, , K, , , .
【答案】 分
16. (14 )
分 共价 分
10 2 2
(1)3d4s4p(1 ) (1 )
浓 n n 分 取最后一次洗涤液
(2)GeS+10HNO3( )+(-4)H2OGeO2 H2O+10NO2↑+H2SO4(2 )
于洁净试管中 加入盐酸酸化的 溶液 若不出现白色沉淀 分 合理即可
, BaCl2 , (2 , )
86.6℃ 分
(3)Na2GeO3+6HCl2NaCl+GeCl4↑+3H2O(2 )
会使得到的盐酸浓度小于 -1 增大 n 的溶解量 最终使锗产率降低 分 合理即
(4) 5.3molL , GeO2 H2O , (2 ,
可
)
当滴入最后半滴标准溶液时 溶液由无色变为蓝色 且半分钟之内不变色 分
(5)① , , (2 )
cV
31.5 分
② w (2 )
高三化学试题参考答案 第 页 共 页
【 3 ( 5 )】【解析】 锗在周期表中的位置是第四周期第 族 基态锗原子的核外电子排布式 硅和
10 2 2
(1) ⅣA , [Ar]3d4s4p;
锗是同主族相邻元素 结构和性质类似 晶体锗为共价晶体
, , .
由题意可判断 酸浸 过程生成 n 的化学中 是还原剂 氧化产物是 n 和
(2) ,“ ” GeO2 H2O ,GeS , GeO2 H2O
是氧化剂 还原产物是 配平可得 浓 n n
H2SO4,HNO3 , NO2, GeS+10HNO3( )+(-4)H2OGeO2 H2O
n n 表面吸附的离子有 2- + 等 因此判断 n 洗涤
+10NO2↑+H2SO4(>4);GeO2 H2O SO4 、H , GeO2 H2O
干净的实验方法是 取最后一次洗涤液于洁净试管中 加入盐酸酸化的 溶液 若不出现白色沉淀 证明
: , BaCl2 , ,
n 洗涤干净
GeO2 H2O .
加入盐酸蒸馏生成 即 与 反应生成 结合原子守恒 还有 和 生成
(3) GeCl4, Na2GeO3 HCl GeCl4, , NaCl H2O ,
反应的化学方程式为 86.6℃
Na2GeO3+6HCl2NaCl+GeCl4↑+3H2O.
若水过量 则会使得到的盐酸浓度小于 -1 增大 n 的溶解量 最终使锗产率降低
(4) , 5.3molL , GeO2 H2O , .
当 消耗完后 就会和生成的 发生归中反应得到 淀粉遇 变蓝 滴定终点现象为当最后
2+ - -
(5)① Ge ,IO3 I I2, I2 ,
半滴标准溶液滴下时 溶液由无色变为蓝色 且 内不褪色
, , 30s .
根据 2+ - + 4+ - 反应以及 守恒可得n n 2+ n -
② 3Ge +IO3 +6H 4Ge +I +3H2O Ge ,(GeO2)= (Ge )=3 (IO3 )=
cV -3 -1 cV
cV -3 样品中二氧化锗的质量分数是3 ×10 mol×105gmol 31.5
3 ×10 mol, w ×100%= w %.
【答案】 分
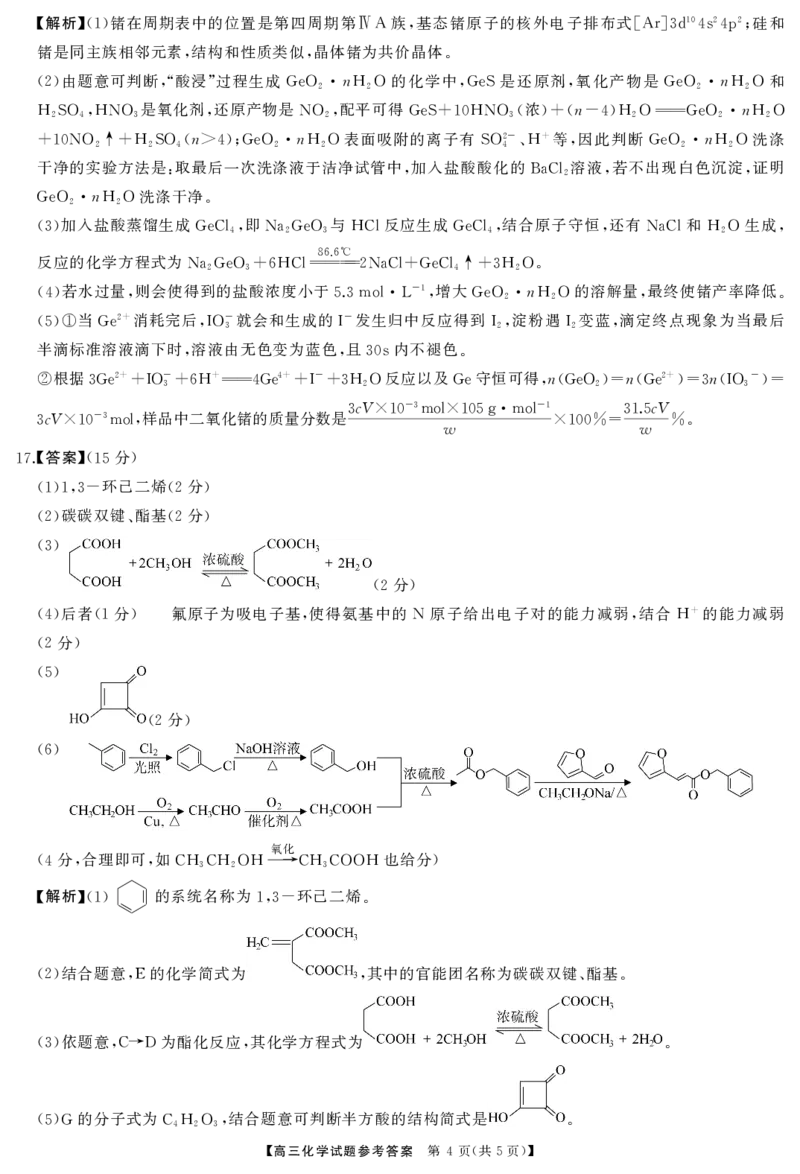
17. (15 )
环己二烯 分
(1)1,3- (2 )
碳碳双键 酯基 分
(2) 、 (2 )
(3)
分
(2 )
后者 分 氟原子为吸电子基 使得氨基中的 原子给出电子对的能力减弱 结合 的能力减弱
+
(4) (1 ) , N , H
分
(2 )
(5)
分
(2 )
(6)
氧化
分 合理即可 如 也给分
(4 , , CH3CH2OH →CH3COOH )
【解析】
(1)
高三化学试题参考答案 第 页 共 页
【 4 ( 5 )】
的系统名称为 环己二烯
1,3- .
结合题意 的化学简式为 其中的官能团名称为碳碳双键 酯基
(2) ,E , 、 .
依题意 为酯化反应 其化学方程式为
(3) ,C→D , .
的分子式为 结合题意可判断半方酸的结构简式是
(5)G C4H2O3, .结合题意和已知信息 合成 的反应物是 和 而合成 的反
(6) , ,
应物是 和 故合成路线如下
CH3COOH , :
.
【答案】 分
18. (15 )
分 或
(1)SO2+Cl2+2H2OH2SO4+2HCl(2 , SO2Cl2+2H2OH2SO4+2HCl)
分
(2)100(2 )
分 分 小于 分 该反应正反应放热 且气体分子数减小 温度越高 反
(3)①6(2 ) ②0.03(2 ) ③ (1 ) , , ,
应向正方向进行的程度越小 压强差也越小 分 合理即可
, (2 , )
分
(4)D(2 )
分
- -
(5)SO2Cl2+2e 2Cl +SO2↑(2 )
【解析】 反应 需要在无水条件下进行 其原因为
(1) SO2(g)+Cl2(g)SO2Cl2(g) , SO2+Cl2+2H2O
或
H2SO4+2HCl, SO2Cl2+2H2OH2SO4+2HCl.
根据 H 反应物的总键能 生成物的总键能可得 a -1 b -1
(2) Δ = - ,(2 +243)kJmol -(2 +255×2)kJmol =
-1a b
-67kJmol ,- =100.
已知恒温恒容情况下 容器内气体物质的量之比等于压强之比 可据此列出 三段式
(3) , , “ ”.
p
SO2(g) +Cl2(g) SO2Cl2(g) Δ
起始压强
/kPa 160 80
转化压强
/kPa 60 60 60 60
平衡压强
/kPa 100 20 60
p
内 的分压变化速率为Δ (Cl2)
-1
①0~10min Cl2 =6kPa∙min .
10min
p
K (SO2Cl2) 60kPa -1
② p=p p = =0.03kPa .
(SO2) (Cl2) 100kPa20kPa
该反应正反应放热 且气体分子数减小 反应正向进行时 容器内压强减小 压强差越小 说明反应正向进
③ , , , , ,
行程度也越小 对应的温度也越高
, .
n
对 而言 当反应物中 (SO2) 时 达到平衡状态 的体积分数最
(4) SO2(g)+Cl2(g)SO2Cl2(g) , n =1 , SO2Cl2
(Cl2)
n n
大 当反应物中 (SO2) 和 (SO2) 时 达到平衡状态 的体积分数相等 故 点符合题意
, n =0.5 n =2 , SO2Cl2 , D .
(Cl2) (Cl2)
石墨电极是电池的正极 正极上的 得电子转化为 和 其电极反应式为
- -
(5) , SO2Cl2 SO2 Cl , SO2Cl2+2e
-
2Cl +SO2↑.
高三化学试题参考答案 第 页 共 页
【 5 ( 5 )】