文档内容
滨城高中联盟 2024-2025 学年度上学期高三期中 II 考试
化学试卷参考答案
一、选择题(本大题共15小题,每小题3分,共45分。每小题只有一个正确答案)
1.【答案】B
【解析】A.“燃煤脱硫”技术是减少二氧化硫的排放,与“碳达峰、碳中和”无关,A错误
B.“神舟十八号”返回舱使用的耐高温材料包括碳化硅等属于新型陶瓷,B正确
C.研制了高效率钙钛矿太阳能电池能将太阳能转化为电能,C错误
D.光导纤维其主要成分是二氧化硅,D错误
2.【答案】D
【解析】D.三氧化硫分子中硫原子的价层电子对数为3、孤电子对数为0,价层电子对
互斥模型和分子结构都为平面三角形,D错误。
3.【答案】D
【解析】D.1mol[Co(NH ) ]Cl 中含有 σ 键的数目为24N ,配位键也是 σ 键,D错
3 6 3 A
误。
4.【答案】D
【解析】A.乙醇和水都能和金属钠反应,A错误
B.氯苯和溴苯均为非电解质和硝酸银不能直接反应,B错误
C.酸性高锰酸钾溶液均能氧化甲苯与环己烯,C错误
D.BaCl 溶液能与SO 反应生产硫酸钡沉淀,与SO 不反应,D正确
2 3 2
5.【答案】C
【解析】A.标准状况下2.24LSO 物质的量为0.1mol,通入1L0.5molL1CaClO 溶液
2 2
中,SO 不足,部分ClO-与SO 发生氧化还原反应,生成Cl-和SO2,未反应的ClO-
2 2 4
会与生产的氢离子生成HClO,Ca2++3CIO-+SO +H 0=CaS0 ↓+2HCIO+Cl-,A错误;
2 2 4
B. 电 解 产 生 的 OH - 会 与 Mg2+ 产 生 沉 淀 ,
通电
Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑B错误;
C.向FeSO 溶液中滴加NaHCO 溶液和稀氨水,产生大量白色FeCO 沉淀,同时有
4 3 3
硫酸铵和水生成,选项所给离子方程式正确,C正确;
D.滴加过量 Ba(OH) 溶液能使 Al(OH) 转化为[Al(OH) ]-,正确的离子方程式为
2 3 4
AI3++2S0 2-+2Ba2++40H-=2BaSO ↓+AI(OH) -,D错误。
4 4 4
6.【答案】B
【解析】A.活化分子间的碰撞不一定发生有效碰撞,不一定能发生化学反应,A错误
B.加入适宜的催化剂能降低反应的活化能,增大活化分子百分数,B正确
C.增大反应物浓度化学平衡正向移动,反应物平衡转化率可能减小,C错误
D.该反应 S0,G<0时可自发进行,所以该反应高温下可自发进行,该反应在
高温条件可能自发进行,D错误
7.【答案】C
【解析】A.异戊二烯与丙烯醛还可以生成 , 发生过程②的反应生成
间二甲苯,A错误;
*
B.根据M的结构简式 ,有手性碳原子B错误;
C.过程①为狄尔斯阿尔德反应属于加成反应,C正确;
D.M中所含元素第一电离能小于N的有O、C、H共3种,D错误;
高二化学试卷参考答案 第 1 页 共 7 页
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}8.【答案】D
【分析】由图可知,b电极上HCHO被氧化为HCOO-,则b电极为阳极,a电极为阴极;
电解质溶液为KOH溶液,结合反应机理
,则阳极反应涉及:
1
①HCHO+OH--e-=HCOOH+ H ,②HCOOH+OH-=HCOO-+H O,则阳极反应式为:
2 2
2
2HCHO2e4OH 2HCOOH 2H O,阴极反应式为:
2 2
2H O+2e-=H ↑+2OH-,据此解题。
2 2
【解析】A.由分析可知,b极为阳极,a极为阴极,电解时e 由b电极流出回到电源正
极,从电源负极流入a电极,A错误;
B.由分析可知OH- 通过阴离子交换膜向b电极区域移动,B错误;
C.由分析可知,阳极反应为:2HCHO2e4OH 2HCOOH 2H O,C
2 2
错误;
D.由分析可知,阳极反应式为:2HCHO2e4OH 2HCOOH 2H O,
2 2
阴极反应式为:2H O+2e-=H ↑+2OH-,则转移2mol电子时,阳极生成1molH ,阴
2 2 2
极生成1molH 2 ,共生成2molH 2 ,而传统电解水的反应式:2H 2 O 通 电 2H 2 ↑+O 2 ↑,转
移2mol电子生成1molH ,所以相同电量下H 理论产量是传统电解水的2倍,D正
2 2
确。
9.【答案】B
【解析】A.NO不与水反应,A错误;
B.利用MnO 和浓盐酸混合加热制Cl ,再将Cl 与石灰乳反应可得漂白粉,B正确;
2 2 2
C.黄铁矿在沸腾炉中燃烧产物为SO ,C错误;
2
D.配制新制的Cu(OH) 需要在NaOH溶液中滴加少量CuSO (aq),蔗糖不是还原性
2 4
糖不生成Cu O,D错误。
2
10.【答案】C
【详解】A.bc段反应转化率α(X)低于平衡时转化率α(X),说明反应未达到平衡,不是升
高温度平衡逆向移动造成的,可能是温度升高,催化剂失活,反应速率减小,A错
误;
B.0~10min,X的转化量a、c点相同,由v= Δc,得va=vc,B错误;
Δt
C.b点为400℃,反应10min时X的转化率低于平衡转化率,若使用高效催化剂,
反应速率增大,可能使b点移动到d点,C正确;
D.d点已达平衡状态,体系中,只有X是气体,温度不变,故K值不变,即
cX0.4mol/L
,D错误;
11.【答案】B
【解析】A.实验室制取少量氨气应该是氯化铵和氢氧化钙固体加热,A错误;
B.防止氯化镁水解在氯化氢气流中加热,B正确;
C.硝酸与金属反应不产生氢气,C错误;
D.探究浓度对反应速率的影响高锰酸钾的量相同,草酸浓度不同来做实验,D错误
12.答案A
【解析】A.根据图示,中间体2→过渡态2能量差值较大,中间体2→中间体3的反应,
活化能最大,反应速率最慢,是反应的决速步,A正确;
B.反应过程中涉及C—C键的断裂和C—H键的形成,涉及非极性键的断裂,极性
键的形成,故B错误;
高二化学试卷参考答案 第 2 页 共 7 页
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}C.根据图示,Ni参与反应并生成NiCH ,是反应物不是催化剂,C错误;
2
D.热化学方程式需标注反应物和生成物的状态,热化学方程式为
Ni(s)+C H (g)=NiCH (s)+CH (g) ΔH=-6.57 kJmol-1,D错误。
2 6 2 4
13.【答案】D
【解析】A.As属于p区元素,A正确;
B.图甲中,As原子位于Ga原子构成的正四面体空隙中,B正确;
apm
C.图甲中,若GaAs的键长为 等于晶胞体对角线的四分之一,则晶胞边长
4 3
为
apm
故C正确;
3
D.稀磁性半导体材料中,Mn、As的原子个数比为5:32,故D错误
14.【答案】A
【解析】A根据上表所给数据,水的状态为气态,因此不能求N H (l)的燃烧热,A正确
2 4
B.在相同状况下, 根据上表所给数据N H (l)比NH (g)生成焓大不稳定,B错误
2 4 3
C. 1molN (g)与3molH (g)的反应为可逆反应,放出热量小于91.8kJ,C错误
2 2
D.生成H O(l)放热多摩尔生成焓小H于241.8kJ/mol,D错误
2
15.【答案】C
【分析】根据充电时总反应为: x2+1 C+xLi++xPF-=Li C+xC PF 结合图可知充电时
6 x x 6
阳极:xC+PF--e-=C PF ,b电极附近聚集大量阴离子,b为阳极,a为阴极,发生
6 x 6
反应C+xLi++xe-=Li C;放电时,a为负极发生氧化反应Li C-xe-=C+xLi+,b为正极,
x x
发生还原反应C PF +e-=xC+PF-。
x 6 6
【解析】A.充电时,a为阴极,发生还原反应C+xLi++xe-=Li C,A正确;
x
B.放电时为原电池,负极的电极反应为:Li C-xe-=xLi++C,B正确;
x
C.充电时,电解池中阳离子移向阴极,Li+向阴极移动,C错误;
D.双离子电池在充放电过程中,缩短离子运动路程,有利于提高电池的能量密度,
D正确;
二、非选择题(本大题共4小题,共55分)
16.(每空2分,共14分)
(1)4
(2)30℃、5min
(3)
PbSO
、
SiO
4 2
(4)1:1
(5)ab
(6)As O 6Zn12H 2AsH 6Zn23H O
2 3 3 2
(7)85.8%
【解析】
【分析】高铟烟灰渣(主要含PbO、SiO 、FeAsO 2H O、In O )在高铟烟灰中
2 4 2 2 3
加入硫酸进行酸浸,PbO、FeAsO 2H O、In O 分别与硫酸反应转化为硫酸铅
4 2 2 3
沉淀和硫酸铁,硫酸铟,同时生成As O ,滤渣为硫酸铅和As O 、SiO ;过滤,
2 3 2 3 2
向滤液中加Na S O 将铁还原为FeS O ;然后加萃取剂H A 使In3+进入有机相,铁
2 2 3 4 6 2 2
进入水相从而除去铁;分离后在萃取液中加硫酸反萃取In3+进入水相,然后在水溶液
中加Zn置换出铟,据此分析解答。
【小问1详解】
基态铁原子的价电子排布式为3d64s2,则未成对电子数有4个;
高二化学试卷参考答案 第 3 页 共 7 页
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}【小问2详解】
由图可知5min时铟、铁的萃取率基本达到最高值,萃取温度30℃时铟、铁的萃取率
基本达到最高值,再延长萃取时间或升高萃取温度对萃取率提高不大,因此最佳条
件为30℃、5min;
【小问3详解】
由分析可知,水浸时酸溶过程中反应生成的PbSO ,以及不溶于酸的SiO 也进入浸渣中;
4 2
【小问4详解】
“还原铁”时,Fe3+被还原为亚铁离子,根据得失电子守恒及元素守恒得反应离子方程式:
2Fe3 2S O2-=2Fe2 S O2-,则氧化剂与还原剂的物质的量之比为1:1;
2 3 4 6
【小问5详解】
反萃取过程In3 3H A In HA 3H要使平衡逆向移动;
2 2 2 3
a.适当提高酸的浓度,可使平衡逆向移动,a选;
b.多次萃取有利于提高In3+的萃取率,b选;
c.大剂量溶液一次性萃取,不利于提高In3+的萃取率,c不选;故选ab;
【小问6详解】
“置换铟”时,Zn与As O 在酸性条件下发生反应生成会有少量的AsH 和锌离子,根据
2 3 3
得失电子守恒及元素守恒可得反应离子方程式
As O 6Zn12H 2AsH 6Zn2 3H O;
2 3 3 2
【小问7详解】
烟灰渣中含铟量为1.5%(质量分数),以1t该烟灰渣为原料,理论上能够制取
1000kg×1.5%=15kg铟,实际得到13kg×99%=12.87kg铟,则则该工艺中铟回收率为
12.87kg
100%85.8%。
15kg
17(14分)(每空2分)
【答案】(1) 直形冷凝管 A
(2)受热均匀;防止温度过高过氧化氢分解(或控制反应温度在一定范围内,受热均匀)
(3)NaOH溶液
(4) 溶液刚好变为浅红色,且半分钟内不褪色
38(cV-5c V )
1 1 2 2
CH3COOOH+2Fe2++2H+ CH3COOH+2Fe3++H2O V 0
【分析】由题意可知,该实验的实验目的是制备过氧乙酸,制备过程为先将稀过氧化氢
溶液浓缩浓过氧化氢溶液,再用浓过氧化氢溶液与乙酸酐反应制得过氧乙酸,并用
氧化还原滴定法测定产品中过氧乙酸含量。
【解析】(1)由实验装置图可知,仪器B为直形冷凝管;由75%过氧化氢溶液的沸点为
150.2℃可知,装置A中得到浓过氧化氢溶液、装置C中为蒸馏出来的水,故答案为:
直形冷凝管;A;
(2)75%过氧化氢溶液的沸点为150.2℃,且过氧化氢溶液高温易分解,所以制备过氧
乙酸时应选择水浴加热的方法控制反应温度,故答案为:受热均匀;防止温度过高
过氧化氢分解
(3)由方程式可知,浓硫酸作用下,过氧化氢浓溶液与乙酸酐反应生成过氧乙酸和乙酸,
所以实验生成的尾气应用氢氧化钠溶液吸收,防止污染空气,故答案:NaOH溶液;
(4)①由题给流程可知,第2步发生的反应为酸性高锰酸钾溶液与过氧化氢溶液反应生
成硫酸钾、硫酸锰、氧气和水,完全反应时,再滴入最后半滴酸性高锰酸钾溶液,
高二化学试卷参考答案 第 4 页 共 7 页
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}溶液会变为浅红色,且半分钟内不褪色,故答案为:溶液刚好变为浅红色,且半分
钟内不褪色;
②由题给流程可知,第3步发生的反应为过氧乙酸溶液与稀硫酸、硫酸亚铁溶液反应生
成硫酸铁和乙酸,反应的离子方程式为
CH3COOOH+2Fe2++2H+ CH3COOH+2Fe3++H2O,故答案为:
CH3COOOH+2Fe2++2H+ CH3COOH+2Fe3++H2O;
③由题意可知,滴定溶液中过量亚铁离子消耗V2mLc2mol/L酸性高锰酸钾溶液,由得失
1
电子数目守恒可知,过氧乙酸的物质的量为(10—3c V —5×10—3c V )mol×2 ,则过氧
1 1 2 2
1
(103cV-5103c V )mol 76g/mol
1 1 2 2 2 38(c 1 V 1 -5c 2 V 2 )
10-3VL V
乙酸含量为 0 = 0 g/L,故答案为:
38(cV-5c V )
1 1 2 2
V
0 。
18、(14分)(每空2分)
【答案】(1)CH gCs2H g H73.5kJ/mol
4 2
(2)ac
(3)减小 > K E K F K N 1.25
(4) m
1
【解析】(1)根据燃烧热分别写出热化学方程式,
1
①C(s)+O (g)=CO (g)H=-393.5kJ/mol②H (g)+ O (g)=H O(l)H=-285kJ/mol
2 2 2 2 2 2
③CH (g)+2O (g)=CO (g)+2H O(l)H=-890kJ/mol根据盖斯定律计算③-①-2②得
4 2 2 2
CH (g)C(s)+2H (g)H=(-890+393.5+2285)kJ/mol=73.5kJ/mol,故答案为
4 2
+73.5kJ/mol;
(2)向绝热、恒容密闭容器中加入一定量的CH g和NOg发生反应
4
CH g4NOg 2N gCO g2H Og ΔH1155kJ/mol;
4 2 2 2
a.反应为气体体积不变的反应,根据理想气体状态方程pV=nRT,温度变化,故压强也
是变量,根据“变量不变达平衡”,体系中混合气体的压强不变能说明反应达平衡状
态,选项a正确;
b.随着反应的进行,根据物质计量数关系,反应后体系中保持vN :vCO 2:1,无
2 2
法说明反应达平衡状态,选项b错误;
c.反应为放热反应,随着反应的进行温度发生变化,当体系的温度不变时反应达平衡,
选项c正确;
d.反应为气体体积不变的反应,气体总质量、总物质的量不变,混合气体的平均相对分
子质量始终不变,无法说明反应达平衡,选项d错误;
e.反应为气体体积不变的反应,气体总质量、总体积不变,混合气体的密度始终不变,
无法说明反应达平衡,选项e错误;
答案选ac;
(3)①正反应为放热反应,降低温度,平衡正向移动,则P 时降低温度,n(CH )减小,
1 4
增大压强,平衡正向移动,CH 的物质的量减小,则p >p ;
4 1 2
②升高温度,平衡逆向移动,平衡常数减小,相同温度平衡常数相同,则有
K K K ;
E F N
③根据数据列三段式:
高二化学试卷参考答案 第 5 页 共 7 页
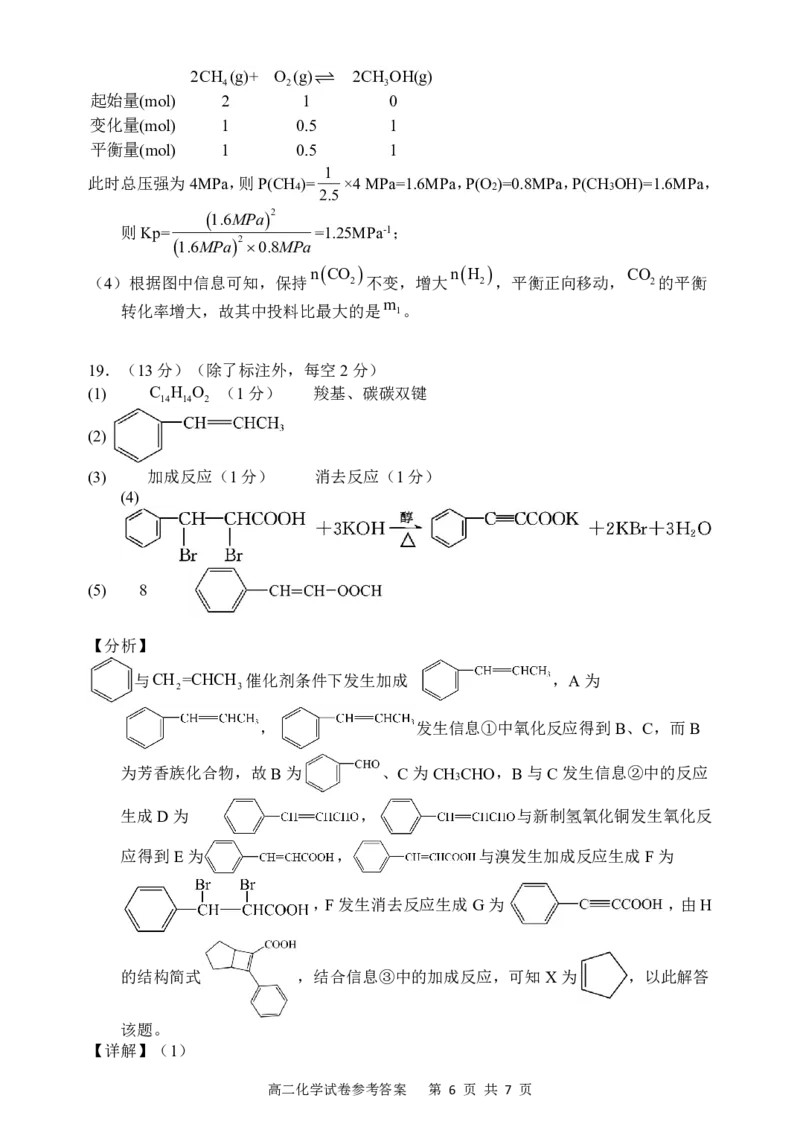
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}2CH (g)+ O (g) 2CH OH(g)
4 2 3
起始量(mol) 2 1 0
变化量(mol) 1 0.5 1
平衡量(mol) 1 0.5 1
1
此时总压强为4MPa,则P(CH )= ×4MPa=1.6MPa,P(O )=0.8MPa,P(CH OH)=1.6MPa,
4 2 3
2.5
1.6MPa2
则Kp= =1.25MPa-1;
1.6MPa20.8MPa
nCO nH
CO
(4)根据图中信息可知,保持 2 不变,增大 2 ,平衡正向移动, 2的平衡
m
转化率增大,故其中投料比最大的是 1。
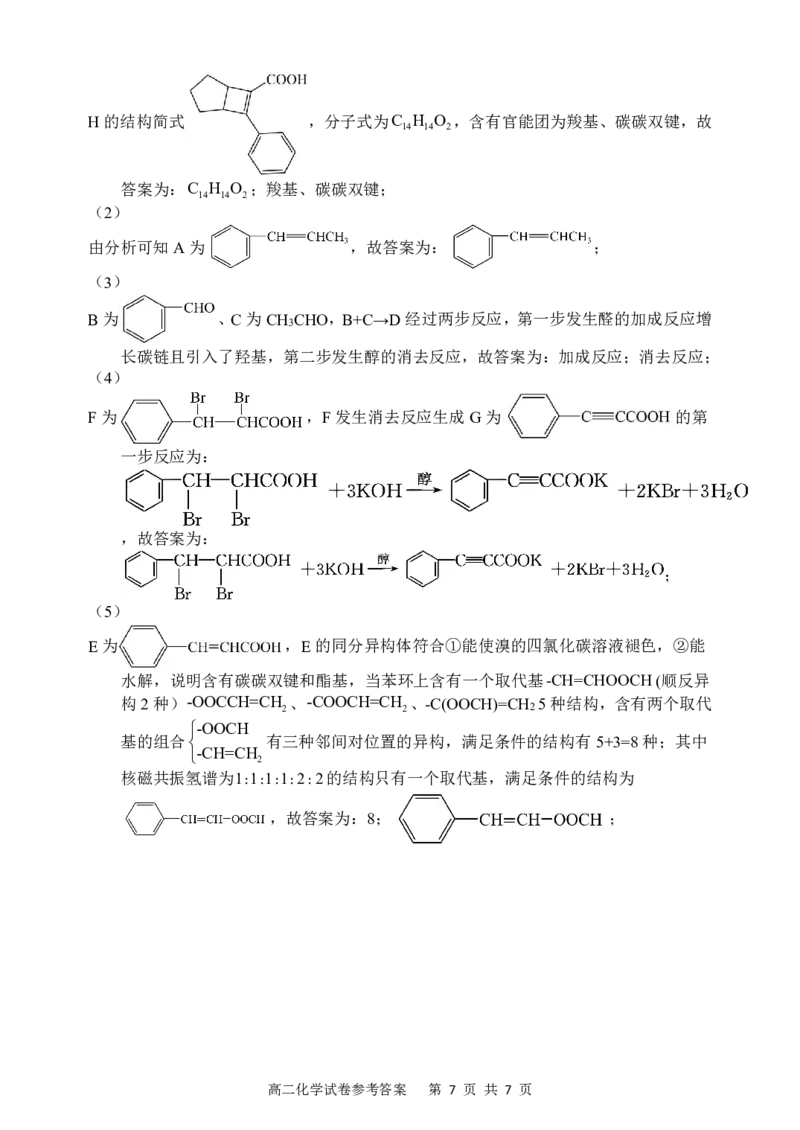
19.(13分)(除了标注外,每空2分)
(1) C H O (1分) 羧基、碳碳双键
14 14 2
(2)
(3) 加成反应(1分) 消去反应(1分)
(4)
(5) 8
【分析】
与CH =CHCH 催化剂条件下发生加成 ,A为
2 3
, 发生信息①中氧化反应得到B、C,而B
为芳香族化合物,故B为 、C为CH CHO,B与C发生信息②中的反应
3
生成D为 , 与新制氢氧化铜发生氧化反
应得到E为 , 与溴发生加成反应生成F为
,F发生消去反应生成G为 ,由H
的结构简式 ,结合信息③中的加成反应,可知X为 ,以此解答
该题。
【详解】(1)
高二化学试卷参考答案 第 6 页 共 7 页
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}H的结构简式 ,分子式为C H O ,含有官能团为羧基、碳碳双键,故
14 14 2
答案为:C H O ;羧基、碳碳双键;
14 14 2
(2)
由分析可知A为 ,故答案为: ;
(3)
B为 、C为CH CHO,B+C→D经过两步反应,第一步发生醛的加成反应增
3
长碳链且引入了羟基,第二步发生醇的消去反应,故答案为:加成反应;消去反应;
(4)
F为 ,F发生消去反应生成G为 的第
一步反应为:
,故答案为:
;
(5)
E为 ,E的同分异构体符合①能使溴的四氯化碳溶液褪色,②能
水解,说明含有碳碳双键和酯基,当苯环上含有一个取代基-CH=CHOOCH(顺反异
构2种)-OOCCH=CH 、-COOCH=CH 、-C(OOCH)=CH 5种结构,含有两个取代
2 2 2
-OOCH
基的组合 有三种邻间对位置的异构,满足条件的结构有5+3=8种;其中
-CH=CH
2
核磁共振氢谱为1:1:1:1:2:2的结构只有一个取代基,满足条件的结构为
,故答案为:8; ;
高二化学试卷参考答案 第 7 页 共 7 页
{#{QQABSYQAoggIQBIAAAhCAw2ACgMQkhECAYgOhBAAsAAAyAFABAA=}#}