文档内容
届高三 月适应性考试化学
2024 5
参考答案、提示及评分细则
【答案】
1. B
【解析】乙烯可以调节植物生长 正确 高纯硅具有半导体性能 常用来作为计算机 通信设备等的芯片 用来生
,A ; , 、 ,
产光导纤维的是二氧化硅 错误 橡胶具有高弹性 可用来制造汽车 飞机轮胎和各种密封材料 正确 硫酸钡
,B ; , 、 ,C ;
不容易被 射线透过 在医疗上可被用作消化系统 射线检查的内服药剂 正确 故选
X , X ;D , B.
【答案】
2. C
【解析】根据核外电子排布的洪特规则 基态 原子的 轨道上的两个电子应该自旋方向相同的排入两个简并
, Si 3p
轨道 错误 故选
,C , C.
【答案】
3. B
【解析】容量瓶只能用来配制溶液 不能用来储存药品 错误 蒸发皿可用来蒸发溶剂 正确 量筒只能读数到
, ,A ; ,B ;
错误 浓硫酸会与氨气反应 不能用来干燥氨气 错误 故选
0.1mL,C ; , ,D , B.
【答案】
4. D
【解析】原子半径 所以硬度大小顺序为金刚石 碳化硅 硅 正确 甲醛分子中的碳原子是 杂化
2
C<Si, > > ,A ; sp ,B
正确 基态 原子核外有 个电子 所以有 种核外电子运动状态 正确 分子是极性分子 但极性很弱 它
; F 9 , 9 ,C ;O3 , ,
在四氯化碳中的溶解度大于在水中的溶解度 错误 故选
,D , D.
【答案】
5. B
【解析】稀硝酸具有强氧化性 也能将 氧化成 错误 往 溶液滴加 溶液至溶液呈中性时
-
, I I2,A ; NH4HSO4 NaOH ,
还有铵根离子剩余 正确 惰性电极电解饱和 溶液 镁离子能与氢氧根离子反应
2+ -
,B ; MgCl2 , Mg +2H2O+2Cl
电解
错误 与 反应中 既不是氧化剂也不是还原剂 在生
18 18 18
Mg(OH)2↓+H2↑+Cl2↑,C ;Na2O2 H2 O ,H2 O ,O
成的 中 生成 中不含 错误 故选
18
NaOH , O2 O,D , B.
【答案】
6. C
【解析】分析结构式可知 为铝元素 元素有五个共价键 推知 是磷元素 元素有两个共价键 结合原子序
,X ;Z , Z ;Y ,
数依次增大的信息 推知 是氧元素 是碳元素 是氢元素 氯化铝是共价化合物 熔融时不导电 不能发生
, Y ;E ,F . , ,
电解反应 错误 依据核外电子排布相同序大径小的规律 推知离子半径是 错误 磷酸是中强酸 正
,A ; , Y>X,B ; ,C
确 在此物质中磷元素原子最外层电子数是 个 错误 故选
; 10 ,D , C.
【答案】
7. A
【解析】 和浓硫酸反应生成二氧化硫 二氧化硫能使品红溶液褪色 所以用品红溶液检验二氧化硫 浓硫
Na2SO3 , , ,
酸具有吸水性且不和二氧化硫反应 所以能干燥二氧化硫 二氧化硫的密度比空气大 所以用向上排空气法收
, , ,
集 二氧化硫有毒 应进行尾气处理 正确 一氧化氮能与氧气反应 不能用排空气法收集 错误 乙炔密度与
, , ,A ; , ,B ;
空气相差不大 不能用排空气法收集 错误 和浓盐酸常温下不反应 缺少加热装置 错误 故选
, ,C ;MnO2 , ,D , A.
【答案】
8. C
【解析】有机物 有一个酯基能发生碱性水解 一个氯原子也可以发生水解 故 最多可以消耗
M , , 1molM 2mol
错误 碳氧双键中存在的 键使成键电子之间的斥力增大 故键角 小于键角 错误 标 的为手
NaOH,A ; π , ① ②,B ; ∗
高三化学试题参考答案 第 页 共 页
【 1 ( 6 )】
{#{QQABCYSEogCAApAAARgCAwUCCEAQkBGAAIoOgAAIsAAAyRNABAA=}#}性碳原子 正确 含 键数目为 N 错误 故选
,C ;1molM σ 25 A,D , C.
【答案】
9. D
【解析】 铝箔中含有少量 不与 反应 滤渣中含 故 错误 铝箔中含有少量 不
A. Mg、Fe NaOH , Mg、Fe, A ;B. Mg、Fe
与 反应 先加 后加硫酸更节约成本 故 错误 步骤 稀硫酸过量是乙溶液显酸性的主要原因
NaOH , NaOH , B ;C. ③ ,
故 错误 向 加入 饱和溶液 析出溶解度小的 晶体 故 正确
C ;D. Al2(SO4)3 K2SO4 , KAl(SO4)212H2O , D .
【答案】
10. C
【解析】 依据题干信息 次磷酸 溶液中存在两种分子及 三种离子 可知次磷酸
- + -
A. : (H3PO2) OH 、H 、H2PO2 ,
为一元弱酸 故 错误 原电池工作时 被氧化 被还原 所以电极 为负极 为正极
- +
(H3PO2) , A ;B. H2PO2 ,Ag , a ,b .
盐桥中 移向正极区即 溶液 故 错误 负极发生氧化反应 被氧化为 负极的电极
+ -
K AgNO3 , B ;C. ,H2PO2 H3PO4,
反应式为 故 正确 盐桥中的物质不能与电解质溶液反应 与
- - +
H2PO2 +2H2O-4e H3PO4+3H , C ;D. ,KCl
溶液能反应生成 故 错误
AgNO3 AgCl, D .
【答案】
11. C
【解析】 由晶胞结构图甲可知晶胞的俯视图是图乙 故 正确 分析图甲可知 晶体中 围成的四面体
A. , A ;B. , Cu、In
空隙共 个 原子填充了其中 个 填充百分比为 故 正确 已知A点 B点原子的分数坐标分别
16 ,Te 8 , 50%, B ;C. 、
( ) ( )
为 1 1 1 则C点原子的分数坐标为 3 3 5 故 错误 AD点及D沿z轴投影的点构
(0,0,0)、 , , , , , , C ;D.、
2 2 2 4 4 8
c a2 c2
成一个直角三角形 两条直角边的长度分别为 2a 计算AD斜边长为 8 + 故 正确
, pm、 pm, pm, D .
8 4 8
【答案】
12. C
【解析】 升高温度 反应速率增大 单位时间内 丁二醇的产量提高 故 正确 氢气的浓度越大 越
A. → → 1,4- , A ;B. →
有利于提高 丁内酯的平衡转化率 根据图 可知m m m 故 正确 正反应放热 升高温度平衡逆
γ- → 1 1> 2> 3, B ;C. ,
向进行 反应物的含量增加 根据反应的化学计量关系可知 表示氢气 表示 丁内酯 表示 丁二
, , ,a ,b γ- ,c 1,4-
醇 故 错误 图 中 点时 丁内酯和 丁二醇的含量相等 设反应前氢气是 丁内酯是
, C ;D. 2 q γ- 1,4- , 2mol、γ- 1
消耗 丁内酯是x 则生成 丁二醇是x 则x x 解得x 所以 的转化率
mol, γ- mol, 1,4- mol, =1- , =0.5,
为 故 正确
50%, D .
【答案】
13. B
【解析】 和 结构虽相似 但官能团数目不同 不互为同系物 故 错误 的结构对称 只有
A.EtP5 EtP10 , , , A ;B.TTF ,
一种氢原子 核磁共振氢谱中含有 组峰 故 正确 和 间通过非共价键相互作用即分子间作用力
, 1 , B ;C.EtP5 TTF
自组装得到超分子聚合物 故 错误 若用 替换 碳环变大 不能很好的识别 得不到
SMP, C ;D. EtP10 EtP5, , TTF,
更稳定的 故 错误
SMP, D .
【答案】
14. C
【解析】 由电离常数可知 溶液中 c (HF) c (F - )则溶液中 é ê ê c (HF) ù ú ú越大 溶液中 - 浓度越大 2+
A. , c (H + ) = K a , lgëc (H + ) û , F ,Ba 、
éc ù
2+ 的浓度越小 的溶度积大于 则L 代表 c - 与 ê ê (HF)ú ú的关系 L L 分别代表
Ca ,BaF2 CaF2, 3 -lg (F ) lgëc + û 、1、2
(H )
c 2+ c 2+ 与 é ê ê c (HF) ù ú ú的关系 故 正确 c (HF) c (F - )当 é ê ê c (HF) ù ú ú 即 c (HF)
-lg(Ca )、-lg(Ba ) lgëc (H + ) û , A ;Bc. (H + ) = Ka , lgëc (H + ) û=1( c (H + )
高三化学试题参考答案 第 页 共 页
【 2 ( 6 )】
{#{QQABCYSEogCAApAAARgCAwUCCEAQkBGAAIoOgAAIsAAAyRNABAA=}#}时 溶液中c
- -3
故K
-4
故 正确 由图ab点可知 当溶液中c
-
=10) , (F )=10 mol/L, a(HF)=1×10 , B ;C. 、 , (F )=
-3
时c
2+ -4
则K
-4 -3 2 -10
同理由图bc点可知K
10 mol/L 、(Ca )=10 mol/L, sp(CaF2)=10 ×(10 )=10 . 、 sp(BaF2)
-2 -3 2 -8 当 2+ 沉淀完全时c 2+ -5 c - -2.5 此时c 2+
=10 ×(10 )=10 . Ca (Ca )=10 mol/L,(F )=10 mol/L, (Ba )=
即 已经沉淀了很大一部分 所以不能分步沉淀进行分离 故 错误 在 的浊液
-3 2+
10 mol/L, Ba , , C ;D. CaF2、BaF2
中 由于 2+ 和 2+ 不水解 根据质子守恒可得出c c + c - 也可根据物料守恒和电荷守恒
, Ba Ca , (HF)+ (H )= (OH )(
联合得出 故 正确
), D .
【答案】 分 除特殊标注外 每空 分
15. (15 , , 2 )
分 防暴沸 兼起搅拌作用 答 防暴沸 就可给 分
(1)①b(1 ) ② , ( “ ” 2 )
邻羟基苯甲酸分子易形成分子内的氢键 对羟基苯甲酸分子中更易形成分子间的氢键 故邻羟基苯甲酸的沸
③ , ,
点低于对羟基苯甲酸
.
油浴加热 分
(2) (1 )
冷水或冰水 分 用冷水或冰水洗涤可以减少因溶解造成的损失
(3) (1 ) .
水杨酸与 反应不计入得分
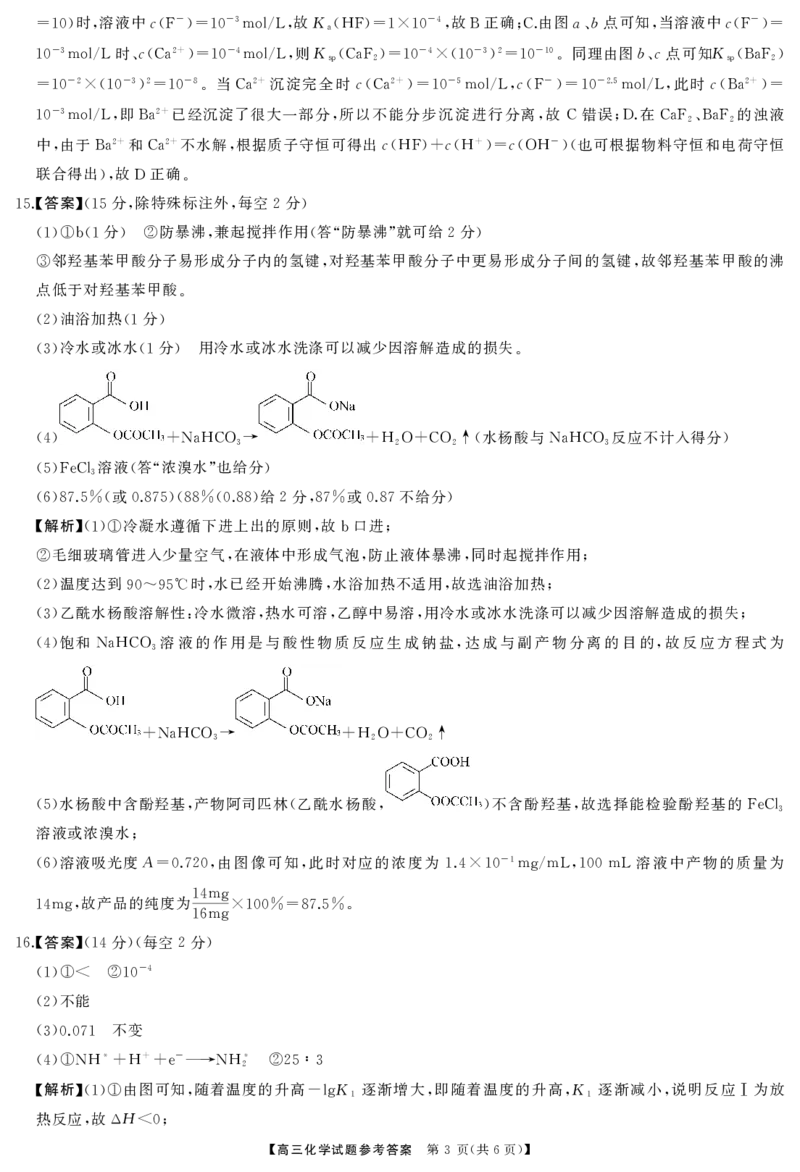
(4) +NaHCO3→ +H2O+CO2↑( NaHCO3 )
溶液 答 浓溴水 也给分
(5)FeCl3 ( “ ” )
或 给 分 或 不给分
(6)87.5%( 0.875)(88%(0.88) 2 ,87% 0.87 )
【解析】 冷凝水遵循下进上出的原则 故 口进
(1)① , b ;
毛细玻璃管进入少量空气 在液体中形成气泡 防止液体暴沸 同时起搅拌作用
② , , , ;
温度达到 时 水已经开始沸腾 水浴加热不适用 故选油浴加热
(2) 90~95℃ , , , ;
乙酰水杨酸溶解性 冷水微溶 热水可溶 乙醇中易溶 用冷水或冰水洗涤可以减少因溶解造成的损失
(3) : , , , ;
饱和 溶液的作用是与酸性物质反应生成钠盐 达成与副产物分离的目的 故反应方程式为
(4) NaHCO3 , ,
+NaHCO3→ +H2O+CO2↑
水杨酸中含酚羟基 产物阿司匹林 乙酰水杨酸 不含酚羟基 故选择能检验酚羟基的
(5) , ( , ) , FeCl3
溶液或浓溴水
;
溶液吸光度A 由图像可知 此时对应的浓度为
-1
溶液中产物的质量为
(6) =0.720, , 1.4×10 mg/mL,100mL
故产品的纯度为14mg
14mg, ×100%=87.5%.
16mg
【答案】 分 每空 分
16. (14 )( 2 )
-4
(1)①< ②10
不能
(2)
不变
(3)0.071
∗ + - ∗
(4)①NH +H +e →NH2 ②25∶3
【解析】 由图可知 随着温度的升高 K 逐渐增大 即随着温度的升高 K 逐渐减小 说明反应 为放
(1)① , -lg 1 , , 1 , Ⅰ
热反应 故 H
, Δ <0;
高三化学试题参考答案 第 页 共 页
【 3 ( 6 )】
{#{QQABCYSEogCAApAAARgCAwUCCEAQkBGAAIoOgAAIsAAAyRNABAA=}#}c2 c c2 c
由图可知 时 K K 则K (NOCl)(I2) -1.1 K (NO)(Cl2)
② ,430K ,-lg 1=1.1、-lg 2=2.9, 1=c2 c2 =10 、 2= c2 =
(ICl) (NO) (NOCl)
c c
-2.9 反应 的K (I2)(Cl2) KK -1.1 -2.9 -4
10 , 2ICl(g)I2(g)+Cl2(g) = c2 = 1 2=10 ×10 =10 ;
(ICl)
G H T S -1 -1 -1 反应 在常温常压
(2)Δ =Δ - Δ =+112.7kJmol -298×(+0.150)kJmol =68kJmol >0, ①
下不能自发进行
;
(3) CH4(g)+2NO(g)+O2(g)CO2(g)+N2(g)+2H2O(g)
起始
/mol 1 3.2 45.8 0 0 0
转化
/mol 0.8 1.6 0.8 0.8 0.8 1.6
平衡
/mol 0.2 1.6 45.0 0.8 0.8 1.6
2
由于反应前后气体分子数相等 K 1.6×0.8×0.8
, x= 2 =0.071
0.2×1.6×45
将生成的 从体系中分离出去 温度没有改变 达到新的平衡时 平衡常数K 不变
H2O(g) , , , x .
结合反应机理 和 可知反应 的机理为
∗ + - ∗
由图知 当电解电压为U 时
(4)① Ⅰ V, Ⅳ NH +H +e →NH2 ;② , 1 ,
Q
的法拉第效率分别为 根据FE x知 电解生成 和 转移电子物质的量之比为
H2、NH3 60%、18%, %=Q总 , H2 NH3
生成 的电极反应式分别为
+ - - +
60%∶18%=10∶3, H2、NH3 2H +2e H2↑、NO+5e +5H NH3+H2O,
则电解生成的 和 的物质的量之比为10 3
H2 NH3 ∶ =25∶3.
2 5
【答案】 分
17. (14 )
各 分
2 4
(1)4s4p In(OH)3( 1 )
分
+ 2+
(2)Cu2O+H2O2+4H 2Cu +3H2O(2 )
分 分
-6
(3)4.7(2 ) 2.0×10 (2 )
稀盐酸 氯化钡溶液 分
(4) 、 (2 )
高温
分 优点是产品纯度高 质量好 化学反应速度快 生产效率高 缺点是高
(5)GaCl3+NH3GaN+3HCl(2 ) , ; , ;
温反应对生产设备 生产成本和技术要求都比较高 分 言之有理即可
、 (2 , )
【解析】 硫为第 族元素 硒 与硫为同族元素 位于第四周期 故 的价层电子排布式为 铟
2 4
(1) ⅥA , (Se) , , Se 4s4p;
位于元素周期表第 族 则其最高价氧化物的水化物为
(In) ⅢA , In(OH)3;
酸浸氧化 为酸性条件下 与烧渣中 发生氧化还原反应 其反应的离子方程式为
(2)“ ” H2O2 Cu2O , :Cu2O+H2O2
+ 2+
+4H =2Cu +3H2O;
3 -33
3+ 恰好完全沉淀时c - 1.0×10 -9.3c + -4.7 为 由反应方程式
(3)In (OH )= -5 ≈1.0×10 ,(H )=1.0×10 ,pH 4.7;
1.0×10
c -
([Ga(OH)4]) c 3+ c4 - c +
可 知 得 K c ([Ga(OH)4] - )× c (NH4 + ) c (Ga 3+ )× c4 (OH - ) × (Ga )× (OH )× (NH4 )
, = c = c =
(NH3H2O) (NH3H2O)
34 c 3+ c3 - c + c -
1.0×10 × (Ga )× (OH )× (NH4 )× (OH ) 34 K K 代入
c =1.0×10 × sp[Ga(OH)3]× b(NH3H2O),
(NH3H2O)
数据可知K
-6
=2.0×10 ;
检验滤渣中 是否洗净的操作为 取少量最后一次洗涤液于试管中 先滴入稀盐酸 再滴入氯化钡溶液
2-
(4) SO4 : , , ,
如果不变浑浊 则证明已洗净 所以所需试剂为稀盐酸和氯化钡溶液
, , ;
高温
高温气相沉积 过程中是氨气和 反应 其方程式为
(5)“ ” GaCl3 , :GaCl3+NH3GaN+3HCl.
高三化学试题参考答案 第 页 共 页
【 4 ( 6 )】
{#{QQABCYSEogCAApAAARgCAwUCCEAQkBGAAIoOgAAIsAAAyRNABAA=}#}基于工业流程的信息介绍可分析得此方法的优点是产品纯度高 质量好 化学反应速度快 生产效率高 缺点是
, ; , ;
高温反应对生产设备 生产成本和技术要求都比较高
、 .
【答案】 分
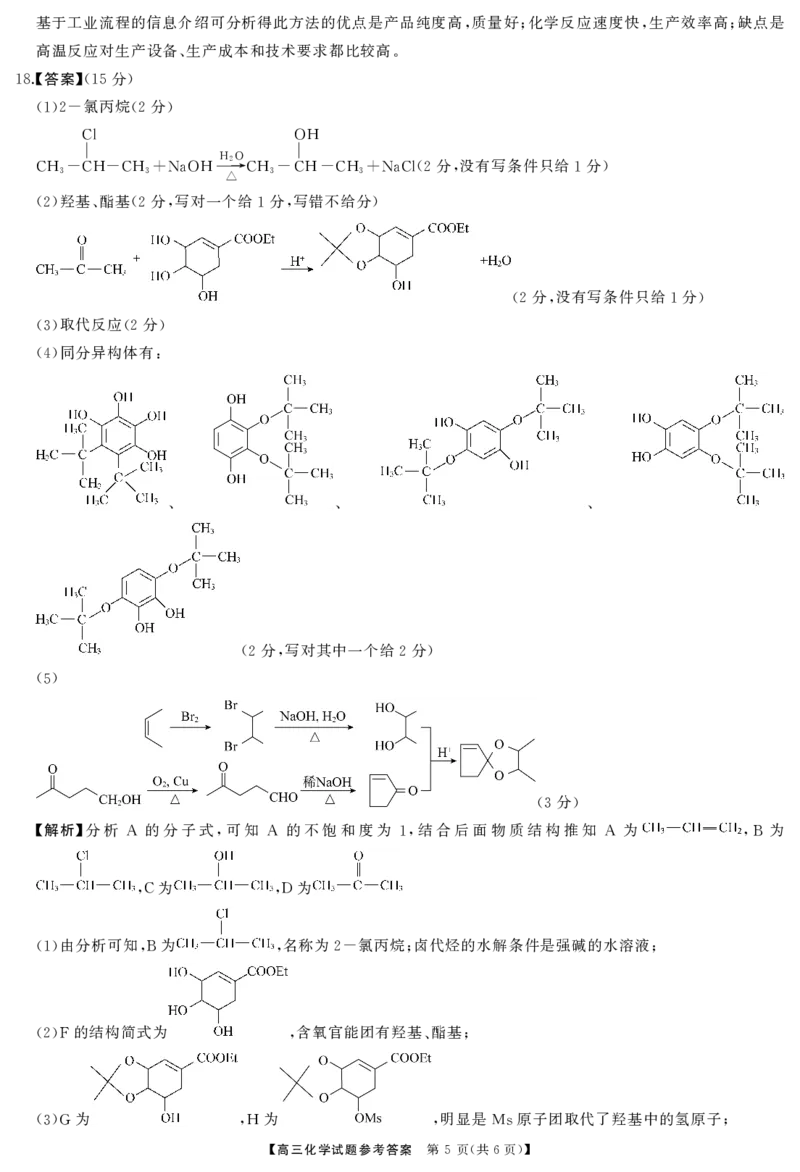
18. (15 )
氯丙烷 分
(1)2- (2 )
Cl OH
H2O 分 没有写条件只给 分
CH3-CH-CH3+NaOH →CH3-CH-CH3+NaCl(2 , 1 )
△
羟基 酯基 分 写对一个给 分 写错不给分
(2) 、 (2 , 1 , )
分 没有写条件只给 分
(2 , 1 )
取代反应 分
(3) (2 )
同分异构体有
(4) :
、 、 、
分 写对其中一个给 分
(2 , 2 )
(5)
分
(3 )
【解析】分析 的分子式 可知 的不饱和度为 结合后面物质结构推知 为 为
A , A 1, A ,B
为 为
,C ,D
由分析可知 为 名称为 氯丙烷 卤代烃的水解条件是强碱的水溶液
(1) ,B , 2- ; ;
的结构简式为 含氧官能团有羟基 酯基
(2)F , 、 ;
为 为 明显是 原子团取代了羟基中的氢原子
(3)G ,H , Ms ;
高三化学试题参考答案 第 页 共 页
【 5 ( 6 )】
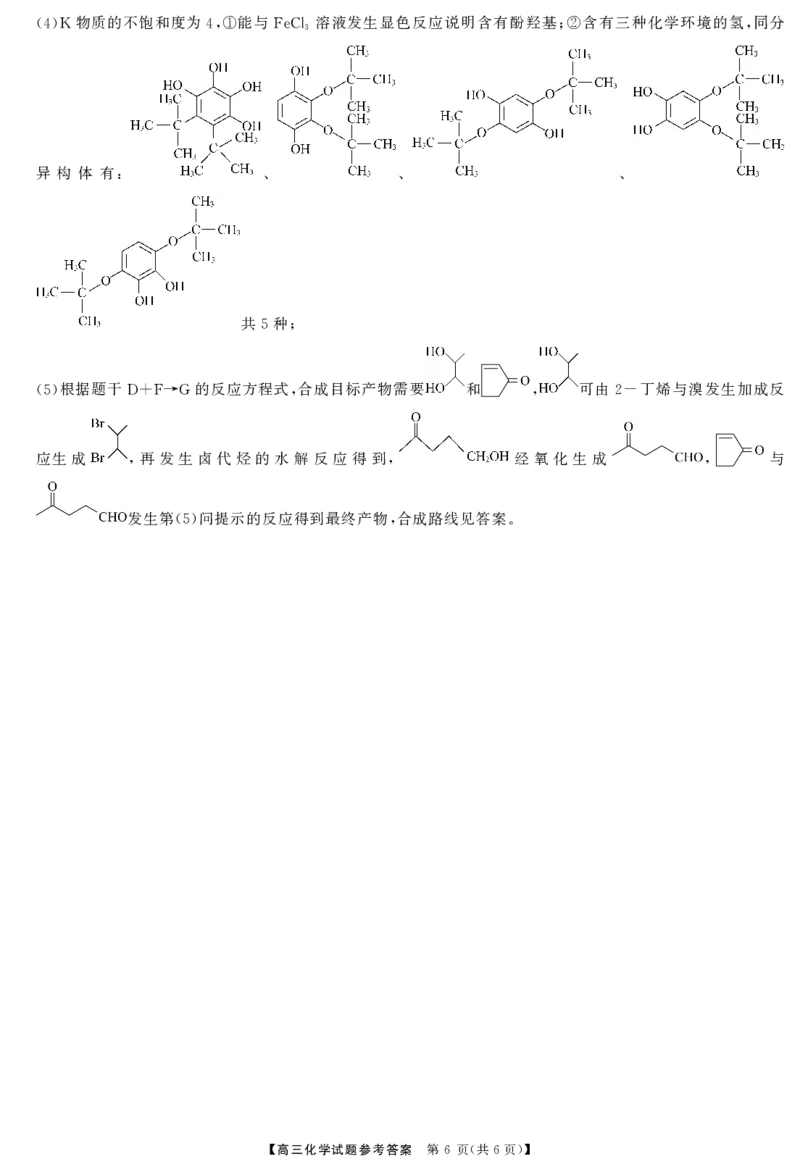
{#{QQABCYSEogCAApAAARgCAwUCCEAQkBGAAIoOgAAIsAAAyRNABAA=}#}物质的不饱和度为 能与 溶液发生显色反应说明含有酚羟基 含有三种化学环境的氢 同分
(4)K 4,① FeCl3 ;② ,
异 构 体 有
: 、 、 、
共 种
5 ;
根据题干 的反应方程式 合成目标产物需要 和 可由 丁烯与溴发生加成反
(5) D+F→G , , 2-
应生成 再 发 生 卤 代 烃 的 水 解 反 应 得 到 经 氧 化 生 成 与
, , ,
发生第 问提示的反应得到最终产物 合成路线见答案
(5) , .
高三化学试题参考答案 第 页 共 页
【 6 ( 6 )】
{#{QQABCYSEogCAApAAARgCAwUCCEAQkBGAAIoOgAAIsAAAyRNABAA=}#}