文档内容
2022 年北京卷部分试题
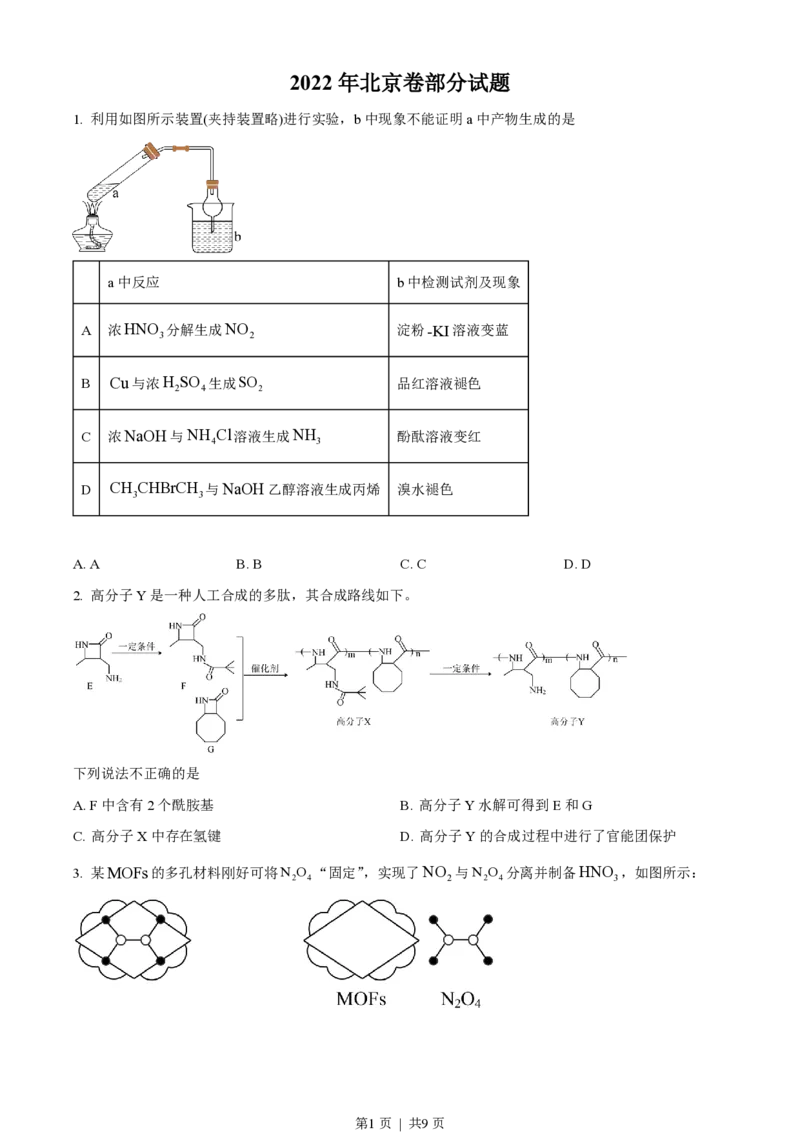
1. 利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是
a中反应 b中检测试剂及现象
A 浓HNO 分解生成NO 淀粉-KI溶液变蓝
3 2
B Cu与浓H SO 生成SO 品红溶液褪色
2 4 2
C 浓NaOH与NH Cl溶液生成NH 酚酞溶液变红
4 3
D CH CHBrCH 与NaOH乙醇溶液生成丙烯 溴水褪色
3 3
A. A B. B C. C D. D
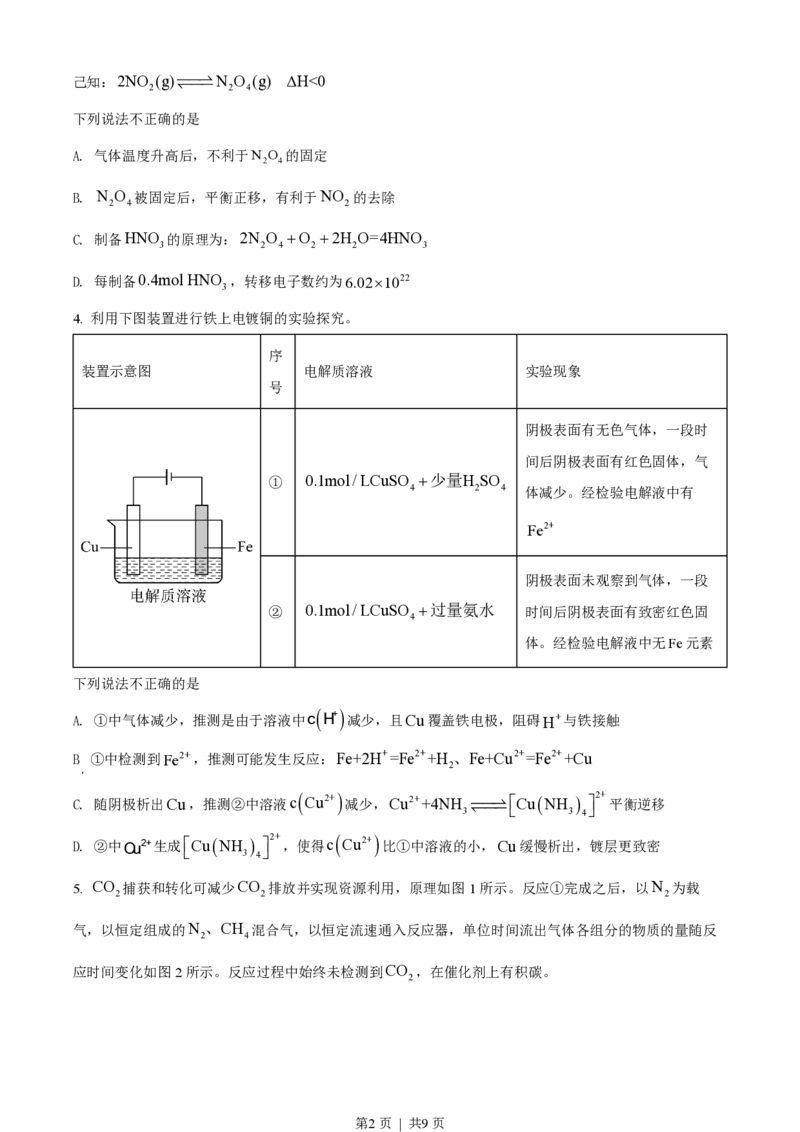
2. 高分子Y是一种人工合成的多肽,其合成路线如下。
下列说法不正确的是
A. F中含有2个酰胺基 B. 高分子Y水解可得到E和G
C. 高分子X中存在氢键 D. 高分子Y的合成过程中进行了官能团保护
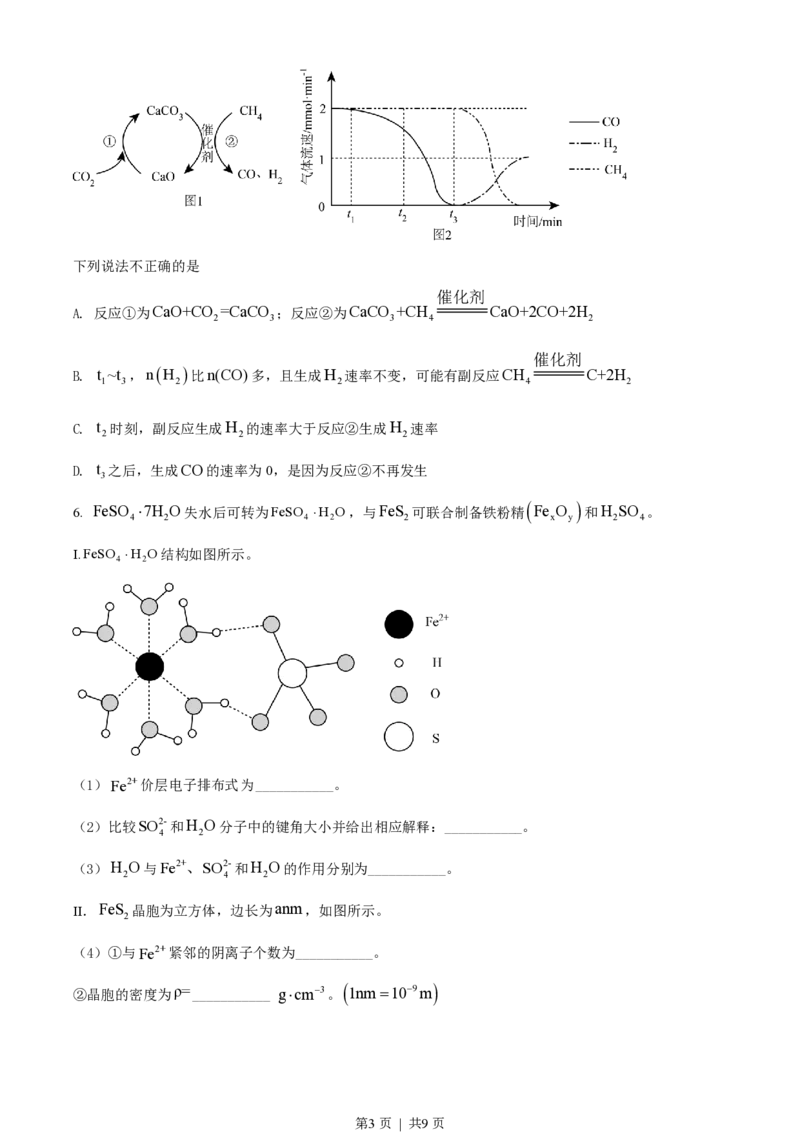
3. 某MOFs的多孔材料刚好可将N O “固定”,实现了NO 与N O 分离并制备HNO ,如图所示:
2 4 2 2 4 3
第1页 | 共9页己知:2NO (g)ˆˆ†N O (g) ΔH<0
2 ‡ˆˆ 2 4
下列说法不正确的是
A. 气体温度升高后,不利于N O 的固定
2 4
B. N O 被固定后,平衡正移,有利于NO 的去除
2 4 2
C. 制备HNO 的原理为:2N O +O +2H O=4HNO
3 2 4 2 2 3
D. 每制备0.4mol HNO ,转移电子数约为6.02´1022
3
4. 利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时
间后阴极表面有红色固体,气
① 0.1mol/LCuSO +少量H SO
4 2 4 体减少。经检验电解液中有
Fe2+
阴极表面未观察到气体,一段
② 0.1mol/LCuSO +过量氨水 时间后阴极表面有致密红色固
4
体。经检验电解液中无Fe元素
下列说法不正确的是
A. ①中气体减少,推测是由于溶液中c
H+
减少,且Cu覆盖铁电极,阻碍H+与铁接触
B ①中检测到Fe2+,推测可能发生反应:Fe+2H+=Fe2++H 、Fe+Cu2+=Fe2++Cu
. 2
C. 随阴极析出Cu,推测②中溶液c Cu2+ 减少,Cu2++4NH 3‡ ˆˆ ˆ † ˆ é ë CuNH 3 4 ù û 2+ 平衡逆移
D. ②中Cu2+生成éCuNH ù 2+ ,使得c Cu2+ 比①中溶液的小,Cu缓慢析出,镀层更致密
ë 3 4 û
5. CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完成之后,以N 为载
2 2 2
气,以恒定组成的N 、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反
2 4
应时间变化如图2所示。反应过程中始终未检测到CO ,在催化剂上有积碳。
2
第2页 | 共9页下列说法不正确的是
催化剂
A. 反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+2CO+2H
2 3 3 4 2
催化剂
B. t ~t ,nH 比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C. t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D. t 之后,生成CO的速率为0,是因为反应②不再发生
3
6. FeSO ×7H O失水后可转为FeSO ×H O,与FeS 可联合制备铁粉精 Fe O 和H SO 。
4 2 4 2 2 x y 2 4
I.FeSO ×H O结构如图所示。
4 2
(1)Fe2+价层电子排布式为___________。
(2)比较SO2-和H O分子中的键角大小并给出相应解释:___________。
4 2
(3)H O与Fe2+、SO2-和H O的作用分别为___________。
2 4 2
II.FeS 晶胞为立方体,边长为anm,如图所示。
2
(4)①与Fe2+紧邻的阴离子个数为___________。
②晶胞的密度为ρ=___________ g×cm-3。 1nm=10-9m
第3页 | 共9页
(5)以FeS 为燃料,配合FeSO ×H O可以制备铁粉精 Fe O 和H SO 。结合图示解释可充分实现
2 4 2 x y 2 4
能源和资源有效利用的原因为___________。
7. 煤中硫的存在形态分为有机硫和无机硫(CaSO 、硫化物及微量单质硫等)。库仑滴定法是常用的快捷检
4
测煤中全硫含量的方法。其主要过程如下图所示。
已知:在催化剂作用下,煤在管式炉中燃烧,出口气体主要含O 、CO 、H O、N 、SO 。
2 2 2 2 2
(1)煤样需研磨成细小粉末,其目的是___________。
(2)高温下,煤中CaSO 完全转化为SO ,该反应的化学方程式为___________。
4 2
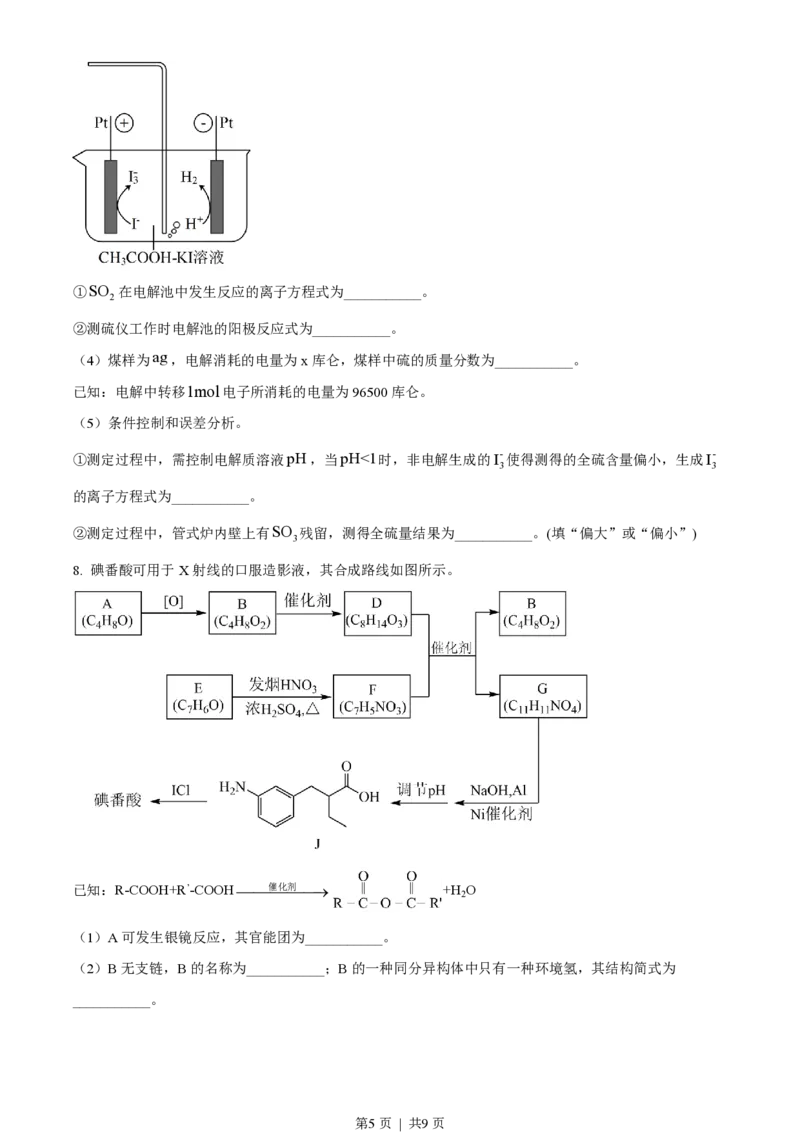
(3)通过干燥装置后,待测气体进入库仑测硫仪进行测定。
c
I-
3
已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。待
c
I-
c
I-
测气体进入电解池后,SO 溶解并将I-还原,测硫仪便立即自动进行电解到 3 又回到原定值,测定结
2 3 c I-
束,通过测定电解消耗的电量可以求得煤中含硫量。
第4页 | 共9页①SO 在电解池中发生反应的离子方程式为___________。
2
②测硫仪工作时电解池的阳极反应式为___________。
(4)煤样为ag,电解消耗的电量为x库仑,煤样中硫的质量分数为___________。
已知:电解中转移1mol电子所消耗的电量为96500库仑。
(5)条件控制和误差分析。
①测定过程中,需控制电解质溶液pH,当pH<1时,非电解生成的I-使得测得的全硫含量偏小,生成I-
3 3
的离子方程式为___________。
②测定过程中,管式炉内壁上有SO 残留,测得全硫量结果为___________。(填“偏大”或“偏小”)
3
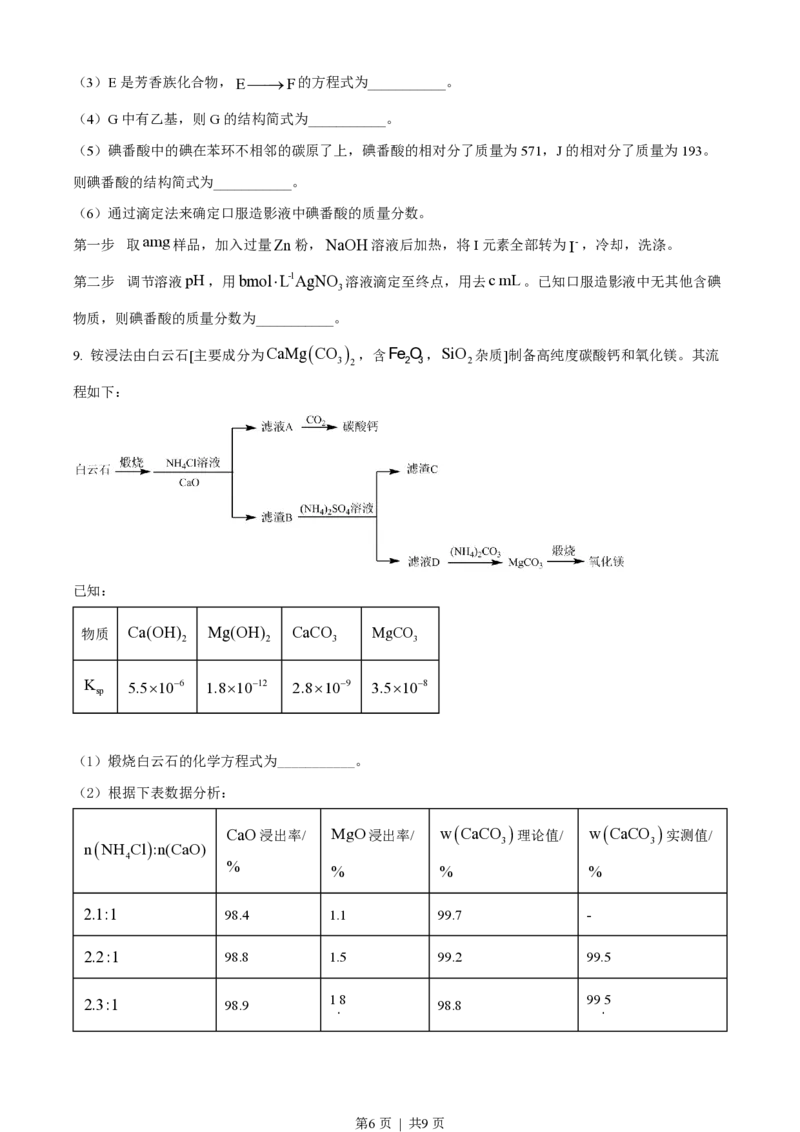
8. 碘番酸可用于X射线的口服造影液,其合成路线如图所示。
已知:R-COOH+R’-COOH¾¾催¾化剂¾¾® +H O
2
(1)A可发生银镜反应,其官能团为___________。
(2)B无支链,B的名称为___________;B的一种同分异构体中只有一种环境氢,其结构简式为
___________。
第5页 | 共9页(3)E是芳香族化合物,E¾¾®F的方程式为___________。
(4)G中有乙基,则G的结构简式为___________。
(5)碘番酸中的碘在苯环不相邻的碳原了上,碘番酸的相对分了质量为571,J的相对分了质量为193。
则碘番酸的结构简式为___________。
(6)通过滴定法来确定口服造影液中碘番酸的质量分数。
第一步 取amg样品,加入过量Zn 粉,NaOH溶液后加热,将I元素全部转为I-,冷却,洗涤。
第二步 调节溶液pH,用bmol×L-1AgNO 溶液滴定至终点,用去cmL。已知口服造影液中无其他含碘
3
物质,则碘番酸的质量分数为___________。
9. 铵浸法由白云石[主要成分为CaMgCO ,含Fe O,SiO 杂质]制备高纯度碳酸钙和氧化镁。其流
3 2 2 3 2
程如下:
已知:
物质 Ca(OH) Mg(OH) CaCO MgCO
2 2 3 3
K 5.5´10-6 1.8´10-12 2.8´10-9 3.5´10-8
sp
(1)煅烧白云石的化学方程式为___________。
(2)根据下表数据分析:
CaO浸出率/ MgO浸出率/ wCaCO 理论值/ wCaCO 实测值/
nNH Cl:n(CaO) 3 3
4
%
% % %
2.1:1 98.4 1.1 99.7 -
2.2:1 98.8 1.5 99.2 99.5
18 995
2.3:1 98.9 . 98.8 .
第6页 | 共9页2.4:1 99.1 6.0 95.6 97.6
已知:i.对浸出率给出定义
ii.对wCaCO
给出定义
3
①“沉钙”反应的化学方程式为___________。
②CaO浸出率远高于MgO浸出率的原因为___________。
③不宜选用的“nNH Cl:n(CaO)”数值为___________。
4
④wCaCO
实测值大于理论值的原因为___________。
3
⑤蒸馏时,随馏出液体积增大,MgO浸出率可出68.7%增加至98.9%,结合化学反应原理解释MgO浸
出率提高的原因为___________。
(3)滤渣C为___________。
(4)可循环利用的物质为___________。
10. 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i.Mn2+在一定条件下被Cl 或ClO-氧化成MnO (棕黑色)、MnO2-(绿色)、MnO-(紫色)。
2 2 4 4
ii.浓碱条件下,MnO-可被OH-还原为MnO2-。
4 4
iii.Cl 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
2
实验装置如图(夹持装置略)
C中实验现象
序
物质a
号
通入Cl 前 通入Cl 后
2 2
第7页 | 共9页I 水 得到无色溶液 产生棕黑色沉淀,且放置后不发生变化
产生白色沉淀,在空气中缓慢变成棕 棕黑色沉淀增多,放置后溶液变为紫
II 5%NaOH溶液
黑色沉淀 色,仍有沉淀
40%NaOH 溶 产生白色沉淀,在空气中缓慢变成棕 棕黑色沉淀增多,放置后溶液变为紫
III
液 黑色沉淀 色,仍有沉淀
(1)B中试剂是___________。
(2)通入Cl 前,II、III中沉淀由白色变为黑色的化学方程式为___________。
2
(3)对比实验I、II通入Cl 后的实验现象,对于二价锰化合物还原性的认识是___________。
2
(4)根据资料ii,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl 导致溶液的碱性减弱。
2
原因二:可能是氧化剂过量,氧化剂将MnO2-氧化为MnO-。
4 4
①化学方程式表示可能导致溶液碱性减弱的原因___________,但通过实验测定溶液的碱性变化很小。
②取III中放置后的1 mL悬浊液,加入4 mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。
溶液紫色变为绿色的离子方程式为___________,溶液绿色缓慢加深,原因是MnO 被___________(填“化
2
学式”)氧化,可证明III的悬浊液中氧化剂过量;
③取II中放置后的1 mL悬浊液,加入4 mL水,溶液紫色缓慢加深,发生的反应是___________。
④从反应速率的角度,分析实验III未得到绿色溶液的可能原因___________。
第8页 | 共9页第9页 | 共9页