文档内容
【中小学教辅资源店 微信:mlxt2022】
2022 年上海市中考真题精品解析(word 版)
化学部分
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Ca-40
五、选择题(本大题共17题,共20分)
21~34每题只有1个正确选项,每题1分,共14分。
21.室温时某中性溶液的pH为( )
A. 1 B.3 C.7 D.10
22.磷肥为植物生长提供的主要营养元素是( )
A.N B.P C.K D.Na
23.银元素以游离态存在的物质是( )
A.Ag B.AgCl C. AgO D.AgNO
2 3
24.会造成酸雨的物质是( )
A.SO B.H C.CH D.N
2 2 4 2
25.下列物质的组成中含有原子团的是( )
A.Zn B.ZnO C.ZnCl D.ZnSO
2 4
26.在水的净化过程中,可用作吸附剂的是( )
A.氯气 B.氯化钠 C.活性炭 D.硫酸铜
27.加入水中能形成溶液的是( )
A.氧化铜 B.铁粉 C.氢氧化铁 D.硝酸钾
28.互为同素异形体的一组物质是( )
A.氧气和臭氧 B.冰和干冰 C.生石灰和熟石灰 D.纯碱和烧碱
29.Mg(OH) 作止酸剂的主要原理是Mg(OH)+2HCl=MgCl+2HO该反应属于( )
2 2 2
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
30.干垃圾焚烧可用于发电,焚烧前一般需粉碎处理。粉碎的目的是( )
A.缓解温室效应 B.使可燃物分子变小
C.使其充分燃烧 D.减少参加反应的氧气量
31.关于1mol氨(NH)的说法,正确的是( )
3
A.含有1mol氢原子 B.质量为17g
C.氮、氢元素质量比为1:3 D.氨的摩尔质量为17
32.在CO+CuO Cu+CO,反应中,CO表现出( )
2
A.稳定性 B.还原性 C.可燃性 D.助燃性
CO+CuO Cu+CO33.关于电解水实验中生成的氢气和氧气,说法正确的是( )
2
A.都是无色气体 B.体积比为8:1
C.物质的量之比为1:1 D.密度均大于空气
34.关于二氧化碳的说法,正确的是( )
A.二氧化碳分子由碳原子和氧分子构成【中小学教辅资源店 微信:mlxt2022】
B.能使紫色石蕊试液变蓝
C.常用块状大理石和稀硫酸反应制得
D.可用于制作碳酸饮料
35~37每题有1~2个正确选项,每题2分,共6分。有2个正确选项的,选对1个得1分,多选
或错选得0分。
35.5%的葡萄糖溶液可用于补充人体所需能量,“5%”表示( )
A.葡萄糖的质量分数 B.每100g溶液中含5g葡萄糖
C.葡萄糖的溶解度为5g/100g水 D.葡萄糖与水的质量比为5:100
36.甲烷和水蒸气制氢气的化学方程式为CH+HO CO+3H,有关说法正确的是( )
4 2 2
A.反应过程中碳元素的总质量保持不变
B.参加反应的CH 和HO的质量比为1:1
4 2
C.若生成3mol H 则有1mol CH 参加反应
2 4
D.反应物的摩尔质量之和等于生成物的摩尔质量之和
37.下图表示甲、乙、丙三类物质的相互关系,甲包含全部乙、部分丙及其他物质。下表中符合
图示关系的是( )
选项 甲 乙 丙
A 含金属元素的盐 钠盐 硝酸盐
B 纯净物 单质 化合物
C 氧化物 酸性氧化物 碱性氧化物
D 含氢元素的化合物 酸 盐
六、简答题(本大题共4题,共30分)
38.硫酸盐的结晶水合物通常称为“矾”,我国多部古籍都有记载。
(1)东汉《神农本草经》记载,胆矾能“化铁为铜”。胆矾的化学式为 CuSO·5HO,胆矾受热
4 2
失去结晶水的过程属于_________(选填“物理”或“化学”)变化;将铁片浸入硫酸铜溶液可
实现“化铁为铜”,反应的化学方程是___________________________,说明铁的金属活动性比
铜_______(选填“强”或“弱”)。
(2)唐代《千金翼方》记载,明矾可入药用。明矾的化学式为KAl(SO)·12HO,其中含有
4 2 2
_______种金属元素;KSO 中K元素的化合价是______________。
2 4
(3)明代《天工开物》记载,绿矾可用黄铁矿为原料制得。绿矾的化学式为FeSO·7HO。
4 2
FeSO·7HO属于__________(选填“纯净物“或”混合物); 1mol FeSO 中约含有_______个S
4 2 4
原子。
39.催化剂可显著提高反应效率,二氧化锰是常见的催化剂。
(1)实验室用HO 溶液制取氧气,常用MnO 作催化剂反应的化学方程式是________________;
2 2 2
用排水法收集氧气,是因为氧气_______(选填“易”或“不易”)溶于水;将带火星的木条伸
入盛有氧气的集气瓶中,现象是__________________________________________。
(2)FeCl 对HO 分解也有催化作用。为比较MnO 和FeCl 对HO 分解快慢的不同影响,用下图
3 2 2 2 3 2 2【中小学教辅资源店 微信:mlxt2022】
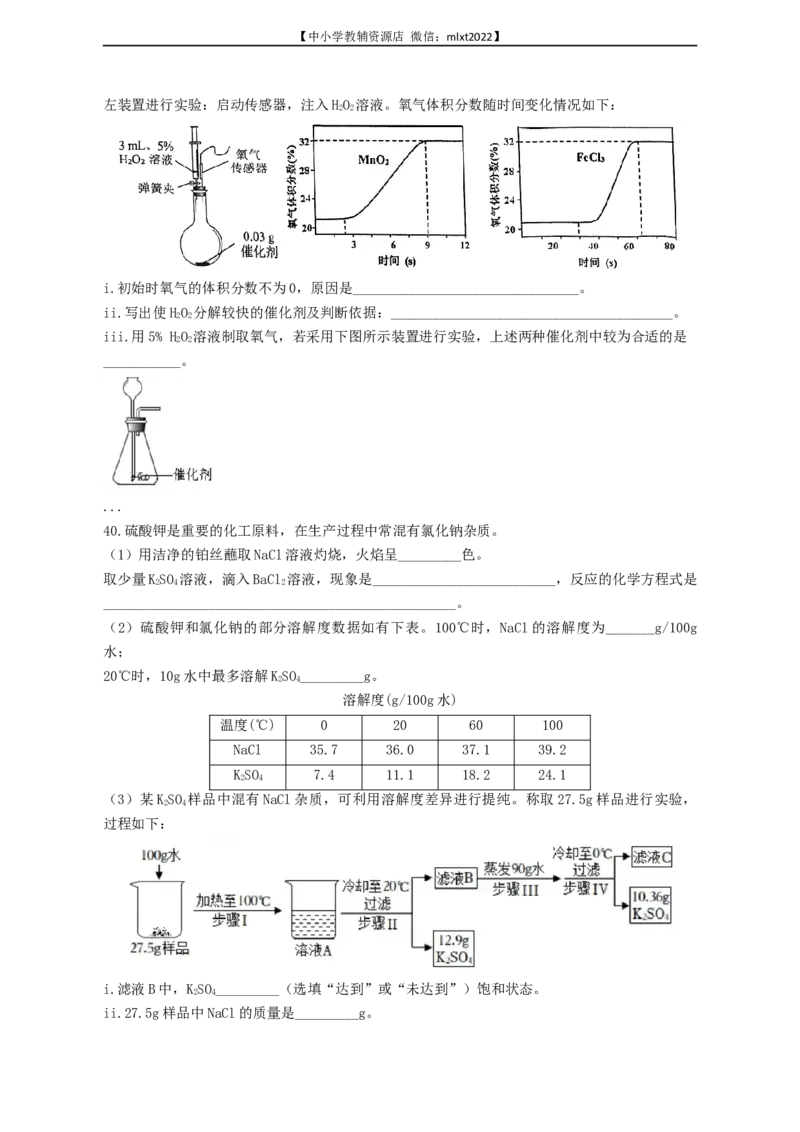
左装置进行实验:启动传感器,注入HO 溶液。氧气体积分数随时间变化情况如下:
2 2
i.初始时氧气的体积分数不为0,原因是________________________________。
ii.写出使HO 分解较快的催化剂及判断依据:________________________________________。
2 2
iii.用5% HO 溶液制取氧气,若采用下图所示装置进行实验,上述两种催化剂中较为合适的是
2 2
___________。
...
40.硫酸钾是重要的化工原料,在生产过程中常混有氯化钠杂质。
(1)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈_________色。
取少量KSO 溶液,滴入BaCl 溶液,现象是__________________________,反应的化学方程式是
2 4 2
__________________________________________________。
(2)硫酸钾和氯化钠的部分溶解度数据如有下表。100℃时,NaCl的溶解度为_______g/100g
水;
20℃时,10g水中最多溶解KSO_________g。
2 4
溶解度(g/100g水)
温度(℃) 0 20 60 100
NaCl 35.7 36.0 37.1 39.2
KSO 7.4 11.1 18.2 24.1
2 4
(3)某KSO 样品中混有NaCl杂质,可利用溶解度差异进行提纯。称取27.5g样品进行实验,
2 4
过程如下:
i.滤液B中,KSO_________(选填“达到”或“未达到”)饱和状态。
2 4
ii.27.5g样品中NaCl的质量是_________g。【中小学教辅资源店 微信:mlxt2022】
iii. 分 析 上 述 实 验 , 说 明 设 计 步 骤 II 对 后 续 操 作 的 作 用 :
________________________________。
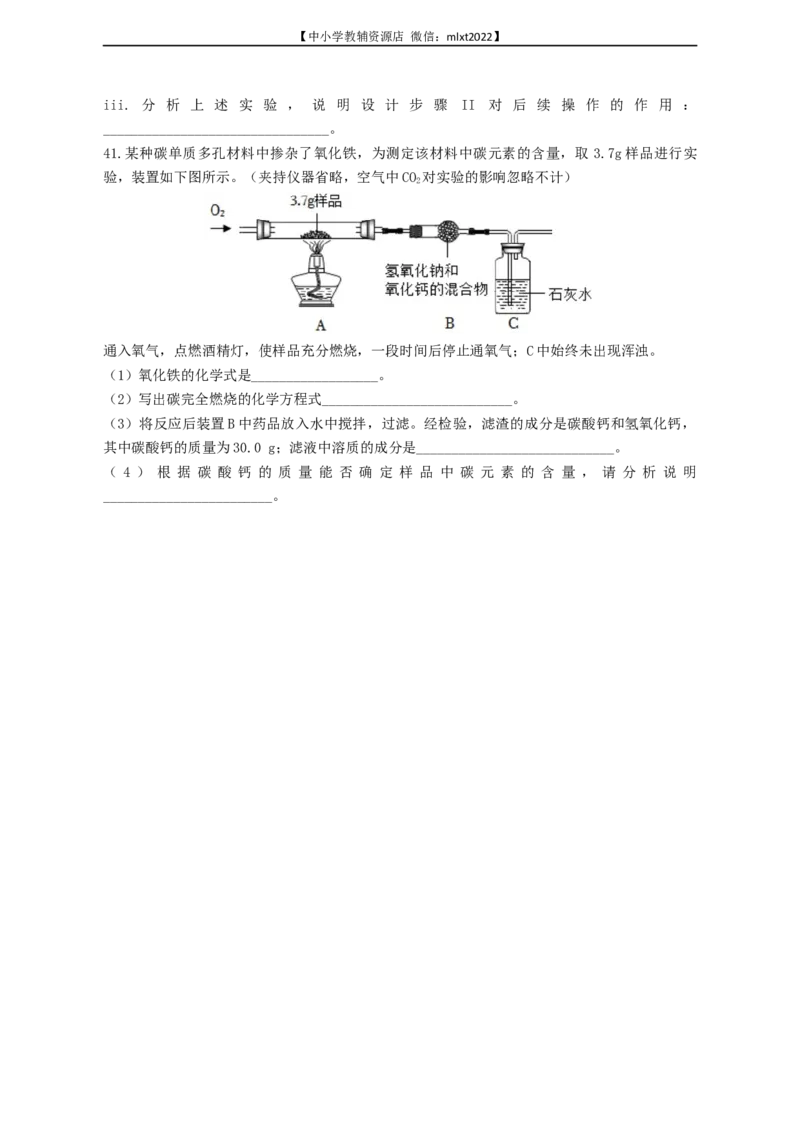
41.某种碳单质多孔材料中掺杂了氧化铁,为测定该材料中碳元素的含量,取 3.7g样品进行实
验,装置如下图所示。(夹持仪器省略,空气中CO 对实验的影响忽略不计)
2
通入氧气,点燃酒精灯,使样品充分燃烧,一段时间后停止通氧气;C中始终未出现浑浊。
(1)氧化铁的化学式是__________________。
(2)写出碳完全燃烧的化学方程式___________________________。
(3)将反应后装置B中药品放入水中搅拌,过滤。经检验,滤渣的成分是碳酸钙和氢氧化钙,
其中碳酸钙的质量为30.0 g;滤液中溶质的成分是____________________________。
( 4 ) 根 据 碳 酸 钙 的 质 量 能 否 确 定 样 品 中 碳 元 素 的 含 量 , 请 分 析 说 明
________________________。【中小学教辅资源店 微信:mlxt2022】