文档内容
2019年河南省普通高中招生考试化学
注意事项:
1、本试卷共4页,四个大题,25个小题。满分50分,考试时间50分钟。
2、本试卷上不要答题,请安答题卡上注意事项的要求直接把答案填写在答题卡上。答
在试卷上的答案无效。
3、可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
Cl-35.5 K-39 Mn-55 Fe-56 Cu-64 Zn-65 Ag-108 Ba-137
4、本试卷由冰橙醉整理于2019年6月26日。
一、选择题(本体包括14个小题,每小题1分,共14分。每小题只有一个选项符合题
意)
1、下列过程属于物理变化的是( )
A、粮食酿酒 B、陶瓷烧制 C、石油分馏 D、煤的干馏
2、河南地处中原,物产丰富。下列食材或食品中复函蛋白质的是( )
A、黄河鲤鱼 B、新郑大枣 C、叶县岩盐 D、原阳大米
3、空气中含量较多且化学性质不活泼的气体是( )
A、O B、CO C、N D、Ne
2 2 2
4、2019年北京世园会主题为“绿色生活,美丽家园”。下列做法值得提倡的是(
)
A、排放未达标的工业废水 B、露天焚烧树叶、秸秆
C、选用一次性筷子、塑料袋 D、将垃圾分类回收并利用
5、下列各组物质中,都由分子构成的一组是( )
A、铁、汞 B、氨、干冰 C、水、金刚石 D、硫酸铜、氯化钠
6、稀土元素镝(Dy)常用于制造硬盘驱动器。下列有关说法中不正确的是( )
A、镝属于非金属元素 B、镝原子的质子数为66
66 Dy
镝
C、镝的相对原子质量为162.5 D、稀土资源需要合理利用和保护
162.5
7、分类、归纳等是化学学习常用的方法。下列分类、归纳中正确的是( )
A、氧化物:SO、CH O B、复合肥料:KNO、CO(NH)
2 6 12 6 3 2 2
C、人体必需微量元素:Ca、Sc D、有机物:CHOH、CHCOOH
2 5 3
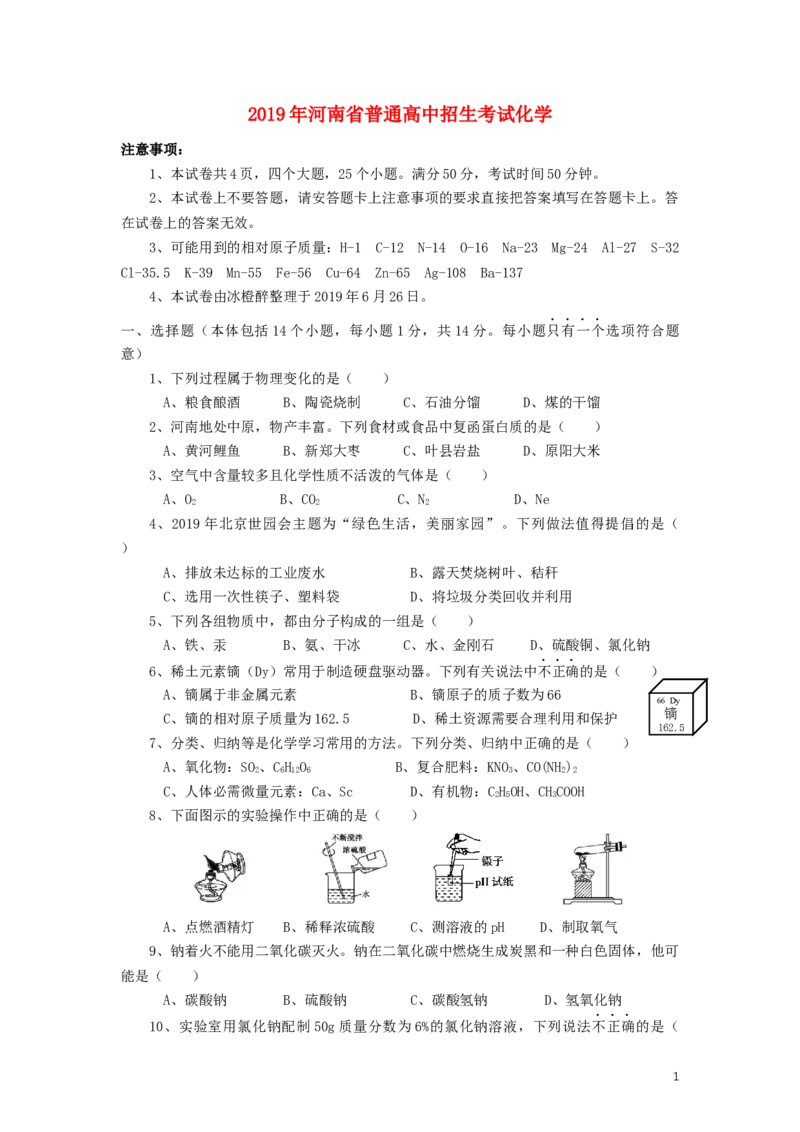
8、下面图示的实验操作中正确的是( )
A、点燃酒精灯 B、稀释浓硫酸 C、测溶液的pH D、制取氧气
9、钠着火不能用二氧化碳灭火。钠在二氧化碳中燃烧生成炭黑和一种白色固体,他可
能是( )
A、碳酸钠 B、硫酸钠 C、碳酸氢钠 D、氢氧化钠
10、实验室用氯化钠配制50g质量分数为6%的氯化钠溶液,下列说法不正确的是(
1)
A、所需氯化钠的质量为3g B、氯化钠放在托盘天平的左盘称量
C、俯视量筒读数会使所配溶液偏稀 D、所需玻璃仪器有烧杯、玻璃棒、量筒等
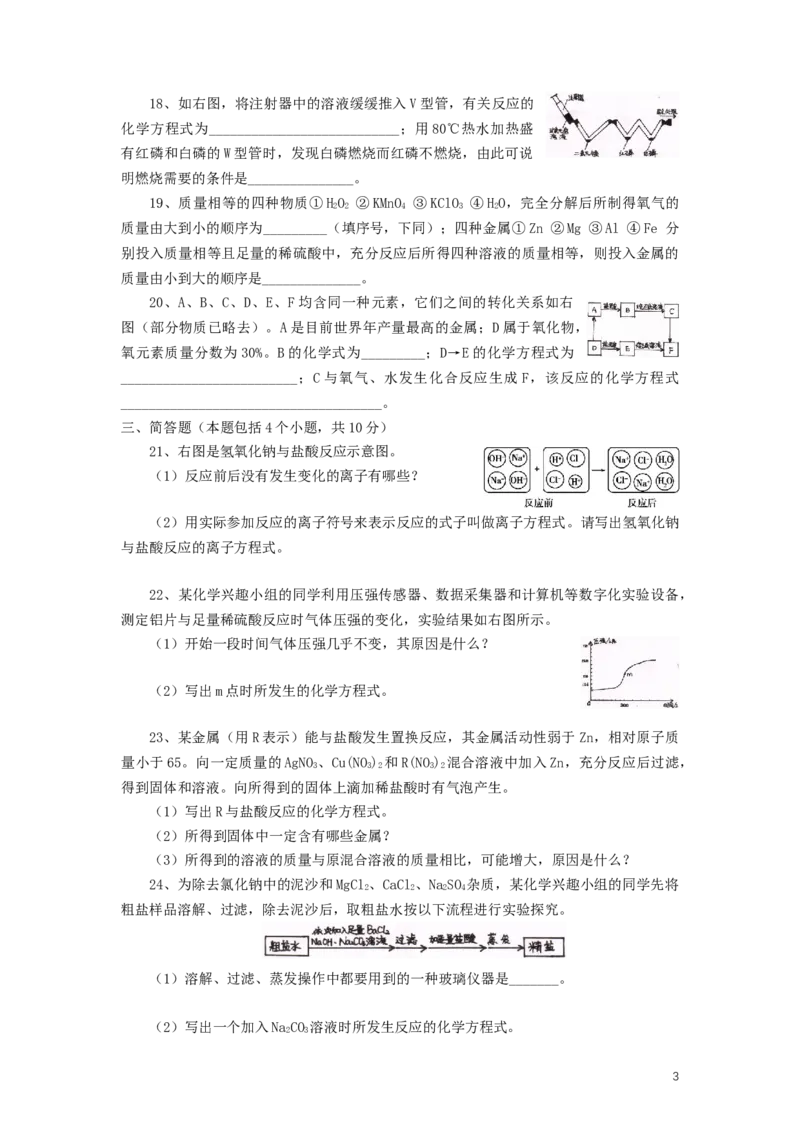
11、右图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
A、开始时应先预热玻璃管,后通入一氧化碳
尾气
B、实验中玻璃管里粉末由黑色逐渐变为红棕色 →
C、参加反应的氧化铁和一氧化碳质量比为40:7
D、将尾气点燃或收集,可防止一氧化碳污染空气
12、下列区分物质的方法或试剂不正确的是( )
A、用灼烧法区分腈纶线、羊毛线 B、用肥皂水区分硬水、软水
C、用熟石灰区分氯化铵、硫酸铵 D、用水区分硝酸铵、氢氧化钠
13、下列图像分别与选项中的操作相对应,其中合理的是( )
A B C
D
A、向pH为13 的氢氧化钠溶液中加水
B、向一定质量二氧化锰固体中加一定质量过氧化氢溶液
C、温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
D、想一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液
14、向某氯化钡溶液中加入一定质量的硫酸溶液,二者恰好完全反应,过滤,所得溶
液的质量与原氯化钡溶液的质量相等。则所加硫酸溶液中溶质质量分数的计算式为
( )
98 98 49 49
A、 ×100% B、 ×100% C、 ×100% D、 ×100%
208 233 233 73
二、填空题(本题包括6个小题,每空1分,共16分)
15、2019年被联合国大会确定为“国际化学元素周期表年”。发现了元素周期律并编
制出元素周期表的化学家是________;形成化合物种类最多的元素是_____;地壳中含量居
前两位的元素所形成的化合物的化学式为_________。
16、右图是甲、乙固体的溶解度曲线。甲、乙溶解度相等时的温度为
_____℃;将a℃时等质量甲、乙饱和溶液升温到a℃,溶质的质量为甲
1 2
_____乙(填“大于”“小于”或“等于”);a℃时,65g甲的饱和溶液
2
稀释到20%,需加水______g。
17、天然气(主要成分为CH)完全燃烧的化学方程式为________________________;
4
某种燃气灶的燃料由水煤气(CO和H 的混合气体)改为天然气后,炉灶的进风口应_____
2
(填“改大”“改小”或“不变”);氢气作为新能源的优点是________(答出一条即
可)。
218、如右图,将注射器中的溶液缓缓推入V型管,有关反应的
化学方程式为___________________________;用80℃热水加热盛
有红磷和白磷的W型管时,发现白磷燃烧而红磷不燃烧,由此可说
明燃烧需要的条件是_______________。
19、质量相等的四种物质①HO ②KMnO ③KClO ④HO,完全分解后所制得氧气的
2 2 4 3 2
质量由大到小的顺序为_________(填序号,下同);四种金属①Zn ②Mg ③Al ④Fe 分
别投入质量相等且足量的稀硫酸中,充分反应后所得四种溶液的质量相等,则投入金属的
质量由小到大的顺序是______________。
20、A、B、C、D、E、F均含同一种元素,它们之间的转化关系如右
图(部分物质已略去)。A是目前世界年产量最高的金属;D属于氧化物,
氧元素质量分数为30%。B的化学式为_________;D→E的化学方程式为
_________________________;C与氧气、水发生化合反应生成 F,该反应的化学方程式
_____________________________________。
三、简答题(本题包括4个小题,共10分)
21、右图是氢氧化钠与盐酸反应示意图。
(1)反应前后没有发生变化的离子有哪些?
(2)用实际参加反应的离子符号来表示反应的式子叫做离子方程式。请写出氢氧化钠
与盐酸反应的离子方程式。
22、某化学兴趣小组的同学利用压强传感器、数据采集器和计算机等数字化实验设备,
测定铝片与足量稀硫酸反应时气体压强的变化,实验结果如右图所示。
(1)开始一段时间气体压强几乎不变,其原因是什么?
(2)写出m点时所发生的化学方程式。
23、某金属(用R表示)能与盐酸发生置换反应,其金属活动性弱于 Zn,相对原子质
量小于65。向一定质量的AgNO 、Cu(NO) 和R(NO) 混合溶液中加入Zn,充分反应后过滤,
3 3 2 3 2
得到固体和溶液。向所得到的固体上滴加稀盐酸时有气泡产生。
(1)写出R与盐酸反应的化学方程式。
(2)所得到固体中一定含有哪些金属?
(3)所得到的溶液的质量与原混合溶液的质量相比,可能增大,原因是什么?
24、为除去氯化钠中的泥沙和MgCl、CaCl、NaSO 杂质,某化学兴趣小组的同学先将
2 2 2 4
粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。
(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是_______。
(2)写出一个加入NaCO 溶液时所发生反应的化学方程式。
2 3
3(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含哪些杂质?
(BaSO 不溶于水,也不溶于酸)
4
四、综合应用题(10分)
25、已知:2NaO+2CO=2NaCO+O↑;2NaO+2HO=4NaOH+O↑。为了证明过氧化钠
2 2 2 2 3 2 2 2 2 2
(NaO )固体可在呼吸面具和潜水艇中做供氧剂,某化学兴趣小组的同学利用下图所示实
2 2
验装置进行探究活动(铁架台等已略去)
(1)A装置中所发生反应的化学方程式为______________________。
(2)请将右图方框中A装置的长颈漏斗和玻璃导管补画完整。
(3)D 装置的作用是___________;E 装置中可能发生的有关反映的化学方程式为
________________________________________。
(4)为了达到实验目的,以上装置导管接口正确的连接顺序为a接______、_____接
_____、______接______、_____接b。
(5)氧气可采用B装置收集并用带火星的木条检验,这是利用了氧气的哪些性质?
(6)实验结束后,取C装置中固体溶于水,无气泡产生。请设计实验,检验C装置中固
体的成分。(简要写出实验步骤、现象和结论)
(7)某潜水艇上有100人,如果每人每分钟消耗氧气为0.001kg,加入所需要的氧气全
部由NaO 与CO 反应来提供,则该潜水艇一天所需要NaO 的质量是多少?
2 2 2 2 2
42019年河南省普通高中招生考试
化学参考答案
一、选择题(每小题1分,共14分)
1、C 2、A 3、C 4、D 5、B 6、A 7、D 8、B 9、A 10、C
11、D 12、C 13、D 14、B
二、填空题(每空1分,共16分)
15、门捷列夫;C或碳;SiO
2
16、a;等于;10
1
17、CH+2O 点燃 CO+2HO 改大; 产物是水无污染
4 2 2 2
18、2HO MnO2 2HO+O↑;温度达到可燃物的最低温度(着火点)
2 2 2 2
19、②③①④;①④②③
20、FeCl;FeO+6HCl=2FeCl+3HO;4Fe(OH)+2HO+O=4Fe(OH)
2 2 3 3 2 2 2 2 2
三、简答题(共10分)
21、(1)Na+、Cl-(1分) (2)OH-+H+=HO(1分)
2
22、(1)铝片表面有一层致密的氧化铝薄膜,稀硫酸与氧化铝反应时不生成气体。
(1分)
(2)3HSO+2Al=Al(SO)+3HO(1分)
2 4 2 4 3 2
23、(1)R+2HCl=RCl+H↑(1分)
2 2
(2)Cu、Ag、R(1分)
(3)锌与AgNO 溶液反应,溶液的质量减小;与Cu(NO) 、R(NO) 反应,溶液的质量均
3 3 2 3 2
增大;当增大的质量大于减小的质量时,溶液的质量增大。(1分)
24、(1)玻璃棒(1分)
(2)NaCO+CaCl=CaCO↓+2NaCl(1分)或NaCO+BaCl=BaCO↓+2NaCl
2 3 2 3 2 3 2 3
(3)所得精盐产品中含有BaCl、CaCl、MgCl 杂质(1分)
2 2 2
四、综合应用题(共10分)
25、(1)CaCO+2HCl=CaCl+HO+CO↑(1分)
3 2 2 2
(2)如图所示 (1分)
(3)吸收A装置中挥发出的HCl气体(1分)Ca(OH)+CO= CaCO↓+ HO(1分)
2 2 3 2
(4)a接e、f接c、d接h、g接b(1分)
(5)氧气不易溶于水,能助燃(1分)
(6)取少量固体溶于水中,加入足量的氯化钙或氯化钡溶液,有白色沉淀生成,
说明固体中含有碳酸钠;静置,取上层清液,滴加无色酚酞溶液,若溶液变红,说
明固体成分是碳酸钠、氢氧化钠;若溶液未变红,说明固体成分是碳酸钠。(1分)
(7)解:该潜水艇一天所需要NaO 的质量为x。
2 2
一天消耗O 的质量为:100×24×60×0.001kg=144kg。(1分)
2
2NaO+2CO=2NaCO+O
2 2 2 2 3 2
2×78 32
x 144kg
2×78 x 2×78×144kg
= 解得:x= = 702kg(1分)
32 144kg 32
答:所需NaO 的质量为702kg。
2 2
56