文档内容
湖北省黄冈市2018年中考化学真题试题
可能用到的相对原子质量: H-1 C-12 O-16 C1-35.5 Ca-40
一、选择题(每小题只有一个选项符合题意。每小题2分,共16分)
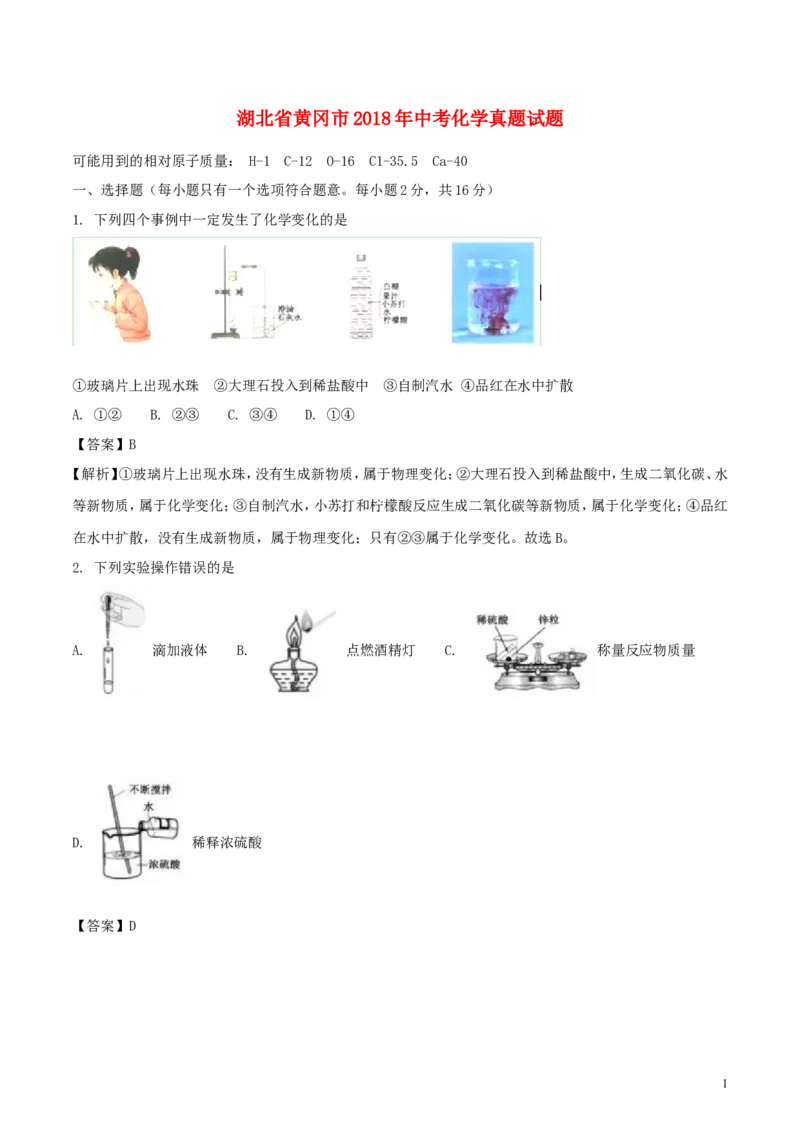
1. 下列四个事例中一定发生了化学变化的是
①玻璃片上出现水珠 ②大理石投入到稀盐酸中 ③自制汽水 ④品红在水中扩散
A. ①② B. ②③ C. ③④ D. ①④
【答案】B
【解析】①玻璃片上出现水珠,没有生成新物质,属于物理变化;②大理石投入到稀盐酸中,生成二氧化碳、水
等新物质,属于化学变化;③自制汽水,小苏打和柠檬酸反应生成二氧化碳等新物质,属于化学变化;④品红
在水中扩散,没有生成新物质,属于物理变化;只有②③属于化学变化。故选B。
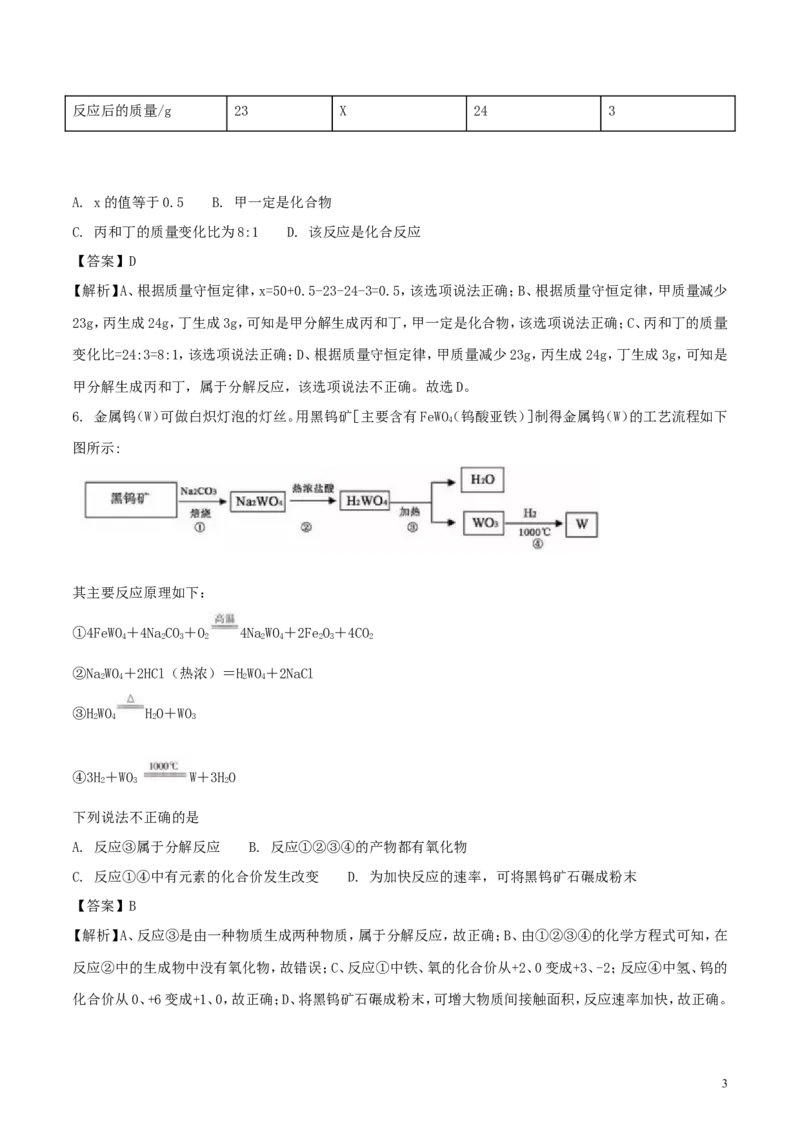
2. 下列实验操作错误的是
A. 滴加液体 B. 点燃酒精灯 C. 称量反应物质量
D. 稀释浓硫酸
【答案】D
13. 下列说法:①二氧化硫和臭氧都是空气污染物;②洁净的空气和水都是纯净物;③因为水体有自净能力,
所以生活污水可任意排放;④降低可燃物的着火点是灭火的途径之一;⑤烧碱和熟石灰的溶液都显碱性;⑥
复合肥中一定要含有氮、磷、钾三种元素;⑦如果将化合物按有机化合物和无机化合物两大类划分,则葡萄糖
和尿素应属于有机化合物。其中正确的是
A. ①⑤⑦ B. ①②④⑥ C. ④⑤⑦ D. ①②⑤⑥
【答案】A
【解析】①二氧化硫和臭氧都是空气污染物,故正确;②水是由一种分子构成的,属于纯净物,故错误;③生活
污水可任意排放,会导致水体受到污染,故错误;④可燃物的着火点是物质的性质,不能降低,故错误;⑤烧
碱和熟石灰都属于碱,溶液都显碱性,故正确;⑥复合肥中一定要含有氮、磷、钾三种元素中任两种元素,故
错误;⑦如果将化合物按有机化合物和无机化合物两大类划分,则葡萄糖和尿素应属于有机化合物,故正确;
只有①⑤⑦正确。故选A。
4. 小雨同学依据描述书写的化学符号:①3个锌原子;3Z;②两个氢分子:2H;③两个氢氧根离子:2OH-;④
N 2
原子结构示意图 对应的粒子:Mg2+;⑤氯化亚铁的化学式:FeCl;⑥-2价的氧元素:O2-。其中正确的有
2
A. ②③⑤ B. ①⑤⑥ C. ②③④ D. ①③⑤
【答案】A
【解析】正确的有:②两个氢分子:2H;③两个氢氧根离子:2OH-;⑤氯化亚铁的化学式:FeCl;错误的有:①3
2 2
个锌原子应为:3Zn;④原子结构示意图 对应的粒子应为:Mg;⑥-2价的氧元素应为: 。故选A。
点睛:化学符号周围的数字表示不同的意义:符号前面的数字,表示原子、分子或离子的个数;右上角的数字
表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合
价。
5. 一定条件下,甲、乙混合后发生化学反应,测得反应前后各物质的质量变化如下表所示。下列说法中,不正
确的是
物质 甲 乙 丙 丁
反应前的质量/g 50 0.5 0 0
2反应后的质量/g 23 X 24 3
A. x的值等于0.5 B. 甲一定是化合物
C. 丙和丁的质量变化比为8:1 D. 该反应是化合反应
【答案】D
【解析】A、根据质量守恒定律,x=50+0.5-23-24-3=0.5,该选项说法正确;B、根据质量守恒定律,甲质量减少
23g,丙生成24g,丁生成3g,可知是甲分解生成丙和丁,甲一定是化合物,该选项说法正确;C、丙和丁的质量
变化比=24:3=8:1,该选项说法正确;D、根据质量守恒定律,甲质量减少23g,丙生成24g,丁生成3g,可知是
甲分解生成丙和丁,属于分解反应,该选项说法不正确。故选D。
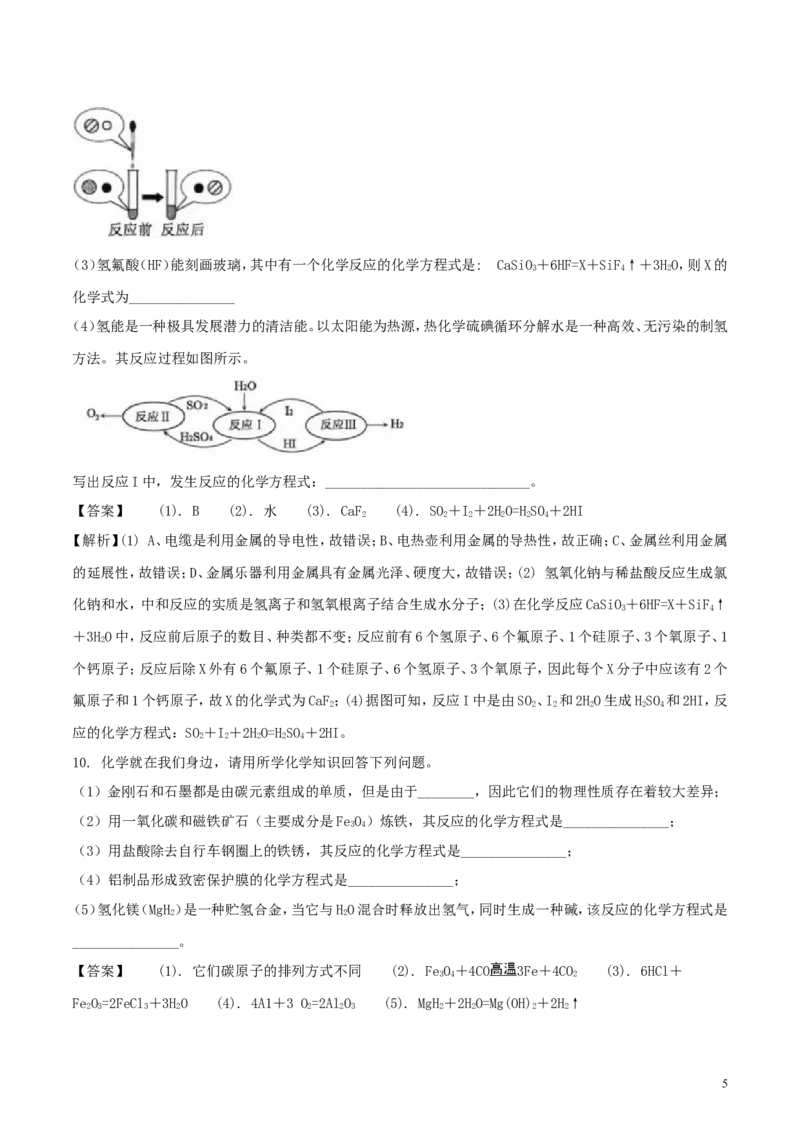
6. 金属钨(W)可做白炽灯泡的灯丝。用黑钨矿[主要含有FeWO(钨酸亚铁)]制得金属钨(W)的工艺流程如下
4
图所示:
其主要反应原理如下:
①4FeWO+4NaCO+O 4NaWO+2FeO+4CO
4 2 3 2 2 4 2 3 2
②NaWO+2HCl(热浓)=HWO+2NaCl
2 4 2 4
③HWO HO+WO
2 4 2 3
④3H+WO W+3HO
2 3 2
下列说法不正确的是
A. 反应③属于分解反应 B. 反应①②③④的产物都有氧化物
C. 反应①④中有元素的化合价发生改变 D. 为加快反应的速率,可将黑钨矿石碾成粉末
【答案】B
【解析】A、反应③是由一种物质生成两种物质,属于分解反应,故正确;B、由①②③④的化学方程式可知,在
反应②中的生成物中没有氧化物,故错误;C、反应①中铁、氧的化合价从+2、0变成+3、-2;反应④中氢、钨的
化合价从0、+6变成+1、0,故正确;D、将黑钨矿石碾成粉末,可增大物质间接触面积,反应速率加快,故正确。
3故选B。
7. 下列关于物质的组成、结构、性质及变化规律的总结,正确的是
A. C、CO、CO 组成中都含有碳元素,故参与反应时均具有碳的还原性
2
B. HCl和NaOH反应生成了盐和水,故有盐和水生成的反应都是复分解反应
C. 酸溶液都含有H+,故酸都有相似的化学性质
D. 浓HSO、NaOH都具有吸水性,故它们都能用来干燥二氧化碳气体
2 4
【答案】C
【解析】A、C、CO具有还原性而CO 没有,故选项错误;B、HCl和NaOH反应生成了盐和水,是复分解反应,而CO
2 2
和NaOH反应也生成了盐和水,但两者没有相互交换成分,不是复分解反应,故选项错误;C、酸具有相似的化
学性质,是因为酸溶液都含有H+,故选项正确;D、浓HSO、NaOH都具有吸水性,浓硫酸可以干燥二氧化碳气
2 4
体,氢氧化钠不可以,因为二氧化碳与氢氧化钠反应生成碳酸钠和水,故选项错误。故选C。
8. 一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO 和HO,且总质量为20.8g,其
2 2
中HO的质量为10.8g,则CO 的质量为
2 2
A. 5.6g B. 8.8g C. 4.4g D. 4.8g
【答案】C
【解析】解:甲烷中碳和氢元素的质量之比是12:4=3:1,所以生成物中碳元素和氢元素的质量比也为3:1,
10.8gHO中氢元素的质量=10.8g× =1.2g,则CO和CO 中总的碳元素的质量=1.2g×3=3.6g,设生成的CO
2 2
的质量是x,CO 的质量为y,则x+y=20.8g−10.8g, x+ y=3.6g,解得x=5.6g,y=4.4g。故选C。
2
二、填空简答题(本题包括3小题,共13分)
9. 化学基础与常识
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);
A电缆 B.电热壶 C.金属丝 D.金属乐器
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“○”
“ ”“●”“ ”表示不同离子)。则“○”与“ ”反应生成了_________(填物质名称)。
4(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是: CaSiO+6HF=X+SiF↑+3HO,则X的
3 4 2
化学式为_______________
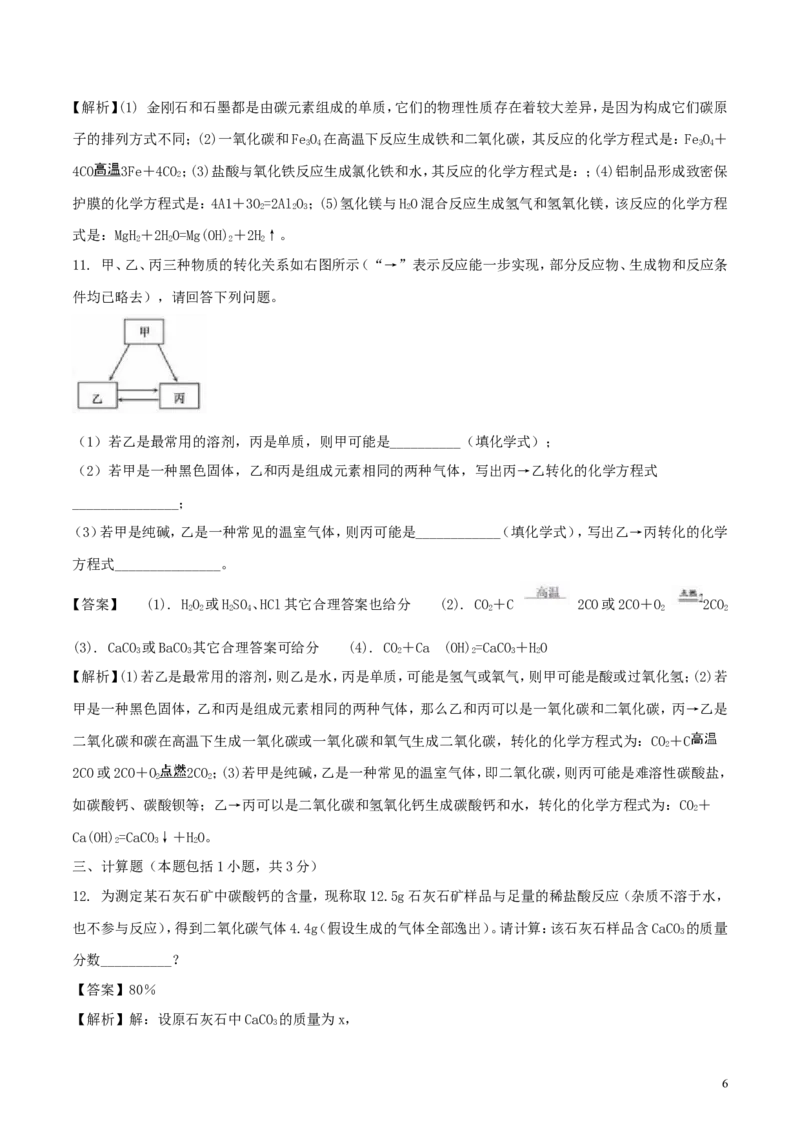
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢
方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式:_____________________________。
【答案】 (1). B (2). 水 (3). CaF (4). SO+I+2HO=HSO+2HI
2 2 2 2 2 4
【解析】(1) A、电缆是利用金属的导电性,故错误;B、电热壶利用金属的导热性,故正确;C、金属丝利用金属
的延展性,故错误;D、金属乐器利用金属具有金属光泽、硬度大,故错误;(2) 氢氧化钠与稀盐酸反应生成氯
化钠和水,中和反应的实质是氢离子和氢氧根离子结合生成水分子;(3)在化学反应CaSiO+6HF=X+SiF↑
3 4
+3HO中,反应前后原子的数目、种类都不变;反应前有6个氢原子、6个氟原子、1个硅原子、3个氧原子、1
2
个钙原子;反应后除X外有6个氟原子、1个硅原子、6个氢原子、3个氧原子,因此每个X分子中应该有2个
氟原子和1个钙原子,故X的化学式为CaF;(4)据图可知,反应I中是由SO、I 和2HO生成HSO 和2HI,反
2 2 2 2 2 4
应的化学方程式:SO+I+2HO=HSO+2HI。
2 2 2 2 4
10. 化学就在我们身边,请用所学化学知识回答下列问题。
(1)金刚石和石墨都是由碳元素组成的单质,但是由于________,因此它们的物理性质存在着较大差异;
(2)用一氧化碳和磁铁矿石(主要成分是FeO)炼铁,其反应的化学方程式是_______________;
3 4
(3)用盐酸除去自行车钢圈上的铁锈,其反应的化学方程式是_______________;
(4)铝制品形成致密保护膜的化学方程式是_______________;
(5)氢化镁(MgH)是一种贮氢合金,当它与HO混合时释放出氢气,同时生成一种碱,该反应的化学方程式是
2 2
_______________。
【答案】 (1). 它们碳原子的排列方式不同 (2). FeO+4CO 3Fe+4CO (3). 6HCl+
3 4 2
FeO=2FeCl+3HO (4). 4A1+3 O=2AlO (5). MgH+2HO=Mg(OH)+2H↑
2 3 3 2 2 2 3 2 2 2 2
5【解析】(1) 金刚石和石墨都是由碳元素组成的单质,它们的物理性质存在着较大差异,是因为构成它们碳原
子的排列方式不同;(2)一氧化碳和FeO 在高温下反应生成铁和二氧化碳,其反应的化学方程式是:FeO+
3 4 3 4
4CO 3Fe+4CO;(3)盐酸与氧化铁反应生成氯化铁和水,其反应的化学方程式是:;(4)铝制品形成致密保
2
护膜的化学方程式是:4A1+3O=2AlO;(5)氢化镁与HO混合反应生成氢气和氢氧化镁,该反应的化学方程
2 2 3 2
式是:MgH+2HO=Mg(OH)+2H↑。
2 2 2 2
11. 甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应能一步实现,部分反应物、生成物和反应条
件均已略去),请回答下列问题。
(1)若乙是最常用的溶剂,丙是单质,则甲可能是__________(填化学式);
(2)若甲是一种黑色固体,乙和丙是组成元素相同的两种气体,写出丙→乙转化的化学方程式
_______________;
(3)若甲是纯碱,乙是一种常见的温室气体,则丙可能是____________(填化学式),写出乙→丙转化的化学
方程式_______________。
【答案】 (1). HO 或HSO、HCl其它合理答案也给分 (2). CO+C 2CO或2CO+O 2CO
2 2 2 4 2 2 2
(3). CaCO 或BaCO 其它合理答案可给分 (4). CO+Ca (OH)=CaCO+HO
3 3 2 2 3 2
【解析】(1)若乙是最常用的溶剂,则乙是水,丙是单质,可能是氢气或氧气,则甲可能是酸或过氧化氢;(2)若
甲是一种黑色固体,乙和丙是组成元素相同的两种气体,那么乙和丙可以是一氧化碳和二氧化碳,丙→乙是
二氧化碳和碳在高温下生成一氧化碳或一氧化碳和氧气生成二氧化碳,转化的化学方程式为:CO+C
2
2CO或2CO+O 2CO;(3)若甲是纯碱,乙是一种常见的温室气体,即二氧化碳,则丙可能是难溶性碳酸盐,
2 2
如碳酸钙、碳酸钡等;乙→丙可以是二氧化碳和氢氧化钙生成碳酸钙和水,转化的化学方程式为:CO+
2
Ca(OH)=CaCO↓+HO。
2 3 2
三、计算题(本题包括1小题,共3分)
12. 为测定某石灰石矿中碳酸钙的含量,现称取12.5g石灰石矿样品与足量的稀盐酸反应(杂质不溶于水,
也不参与反应),得到二氧化碳气体4.4g(假设生成的气体全部逸出)。请计算:该石灰石样品含CaCO 的质量
3
分数__________?
【答案】80%
【解析】解:设原石灰石中CaCO 的质量为x,
3
6CaCO+2HCl═CaCl+HO+CO↑
3 2 2 2
100 44
x 4.4g
x=10g
石灰石中CaCO 的质量分数为: ×100%=80%。
3
四、探究与实验题(本题包括2小题,共8分)
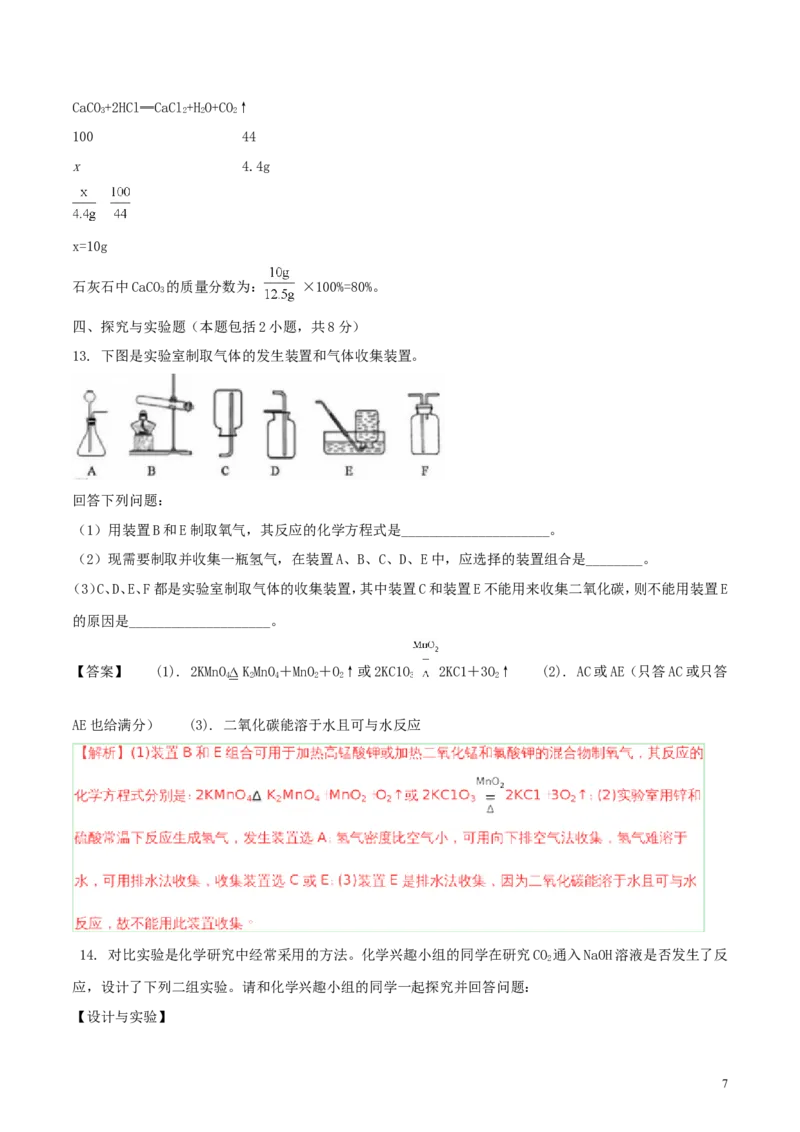
13. 下图是实验室制取气体的发生装置和气体收集装置。
回答下列问题:
(1)用装置B和E制取氧气,其反应的化学方程式是_____________________。
(2)现需要制取并收集一瓶氢气,在装置A、B、C、D、E中,应选择的装置组合是________。
(3)C、D、E、F都是实验室制取气体的收集装置,其中装置C和装置E不能用来收集二氧化碳,则不能用装置E
的原因是____________________。
【答案】 (1). 2KMnO KMnO+MnO+O↑或2KC1O 2KC1+3O↑ (2). AC或AE(只答AC或只答
4 2 4 2 2 3 2
AE也给满分) (3). 二氧化碳能溶于水且可与水反应
14. 对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究CO 通入NaOH溶液是否发生了反
2
应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
【设计与实验】
7实验 实验
实验步骤一 实验步骤二 实验步骤一 实验步骤二
序号 序号
实验I 实验II
【探究与结论】
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是____________________。(2)实验Ⅱ中步骤二看到
有白色沉淀析出,则发生反应的化学方程式是__________。
(3)在实验Ⅱ的步骤一中CO 和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是
2
____________________。
【拓展延伸】现有下列信息:
资料卡片一
20℃NaOH、NaCO 在水中的溶解度
2 3
物质 溶解度(S)/g
NaOH 109
NaCO 21.8
2 3
资料卡片二
20℃NaOH、NaCO 在乙醇中的溶解度
2 3
物质 溶解度(S)/g
NaOH 17.3
NaCO <0.01
2 3
请你和化学兴趣小组的同学一起利用以上料信息再设计实验Ⅲ,证明CO 确实与NaOH发生了化学反应。
2
实验Ⅲ的操作为:_____________________________。
看到的现象是_________________________________。
【答案】 (1). 有气泡冒出 (2). CaCl+NaCO=CaCO↓+2NaCl (3). CO 与NaOH溶液反应生成
2 2 3 3 2
易溶于水的NaCO (4). 将二氧化碳通入盛有一定体积的饱和NaOH乙醇溶液试管中 (5). 有白色沉
2 3
淀产生
【解析】(1)盐酸和碳酸钠反应会生成二氧化碳和水、氯化钠,所以实验I中步骤一的溶液中加入稀盐酸,观察
8到气泡产生现象;(2)实验Ⅱ步骤二中加入的氯化钙溶液和碳酸钠反应生成碳酸钙沉淀和氯化钠,反应的化
学方程式是:CaCl+NaCO=CaCO↓+2NaCl;(3)CO 与NaOH溶液反应生成易溶于水的NaCO,此反应没有明
2 2 3 3 2 2 3
显现象;【拓展延伸】有资料卡片中的信息可知,氢氧化钠既溶于水,也溶入酒精,而碳酸钠能溶于水,不溶于
酒精中,可设计如下实验:将二氧化碳通入盛有一定体积的饱和NaOH乙醇溶液试管中,观察到有白色沉淀产
生,证明二氧化碳与氢氧化钠发生了反应。
9