文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.6 溶液
【基础作业】
1.食堂里的下列饮品属于溶液的是 ( )
A.可乐 B.西瓜汁
C.冰水 D.绿豆汤
2.(生活情境)厨房里的下列物质放入水中,能形成溶液的是 ( )
A.面粉 B.白糖
C.植物油D.辣椒面
3.溶液用途广泛,与人们的生活息息相关。下列说法正确的是( )
A.溶液是由溶质和溶剂组成的
B.溶液都是无色透明的液体
C.溶液是具有均一性、稳定性的纯净物
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
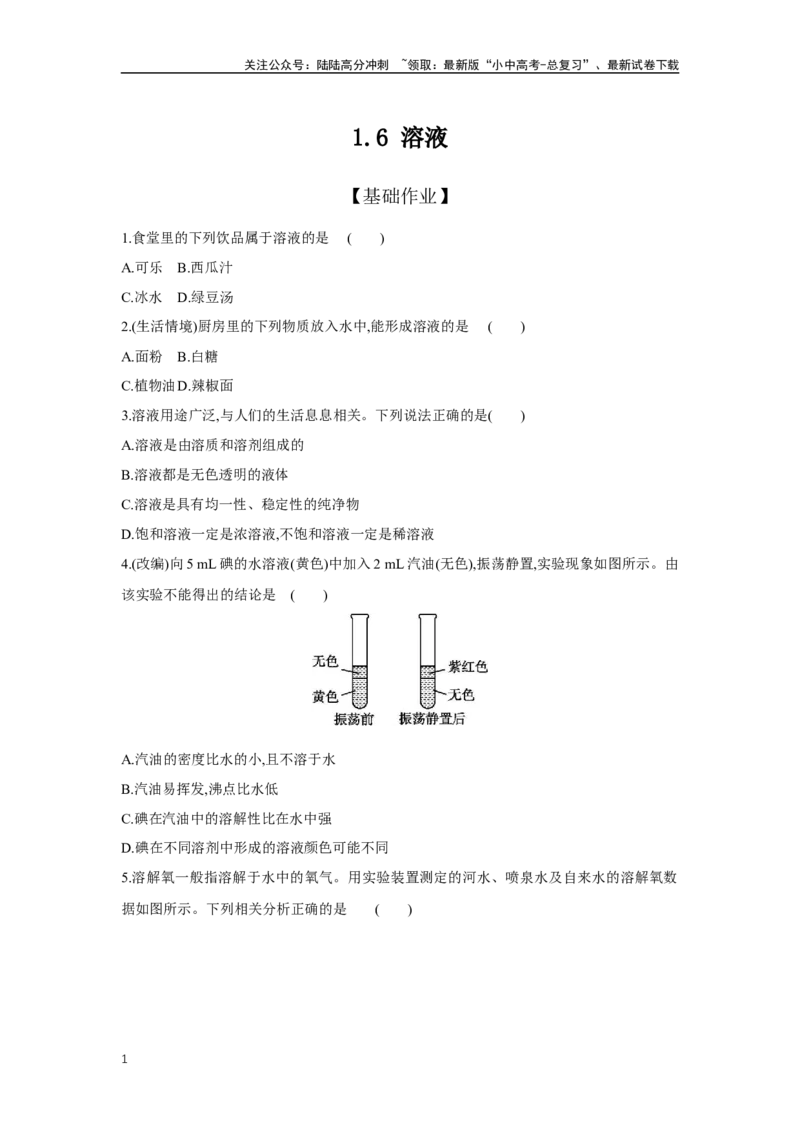
4.(改编)向5 mL碘的水溶液(黄色)中加入2 mL汽油(无色),振荡静置,实验现象如图所示。由
该实验不能得出的结论是 ( )
A.汽油的密度比水的小,且不溶于水
B.汽油易挥发,沸点比水低
C.碘在汽油中的溶解性比在水中强
D.碘在不同溶剂中形成的溶液颜色可能不同
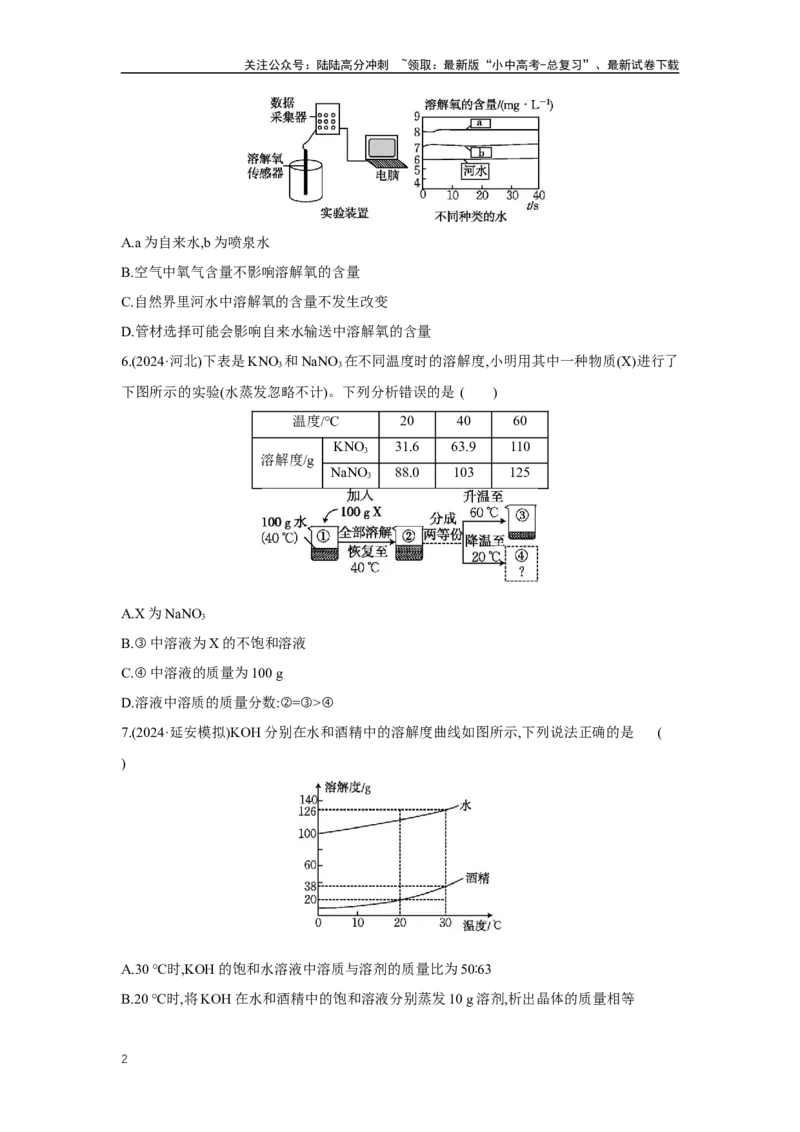
5.溶解氧一般指溶解于水中的氧气。用实验装置测定的河水、喷泉水及自来水的溶解氧数
据如图所示。下列相关分析正确的是 ( )
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.a为自来水,b为喷泉水
B.空气中氧气含量不影响溶解氧的含量
C.自然界里河水中溶解氧的含量不发生改变
D.管材选择可能会影响自来水输送中溶解氧的含量
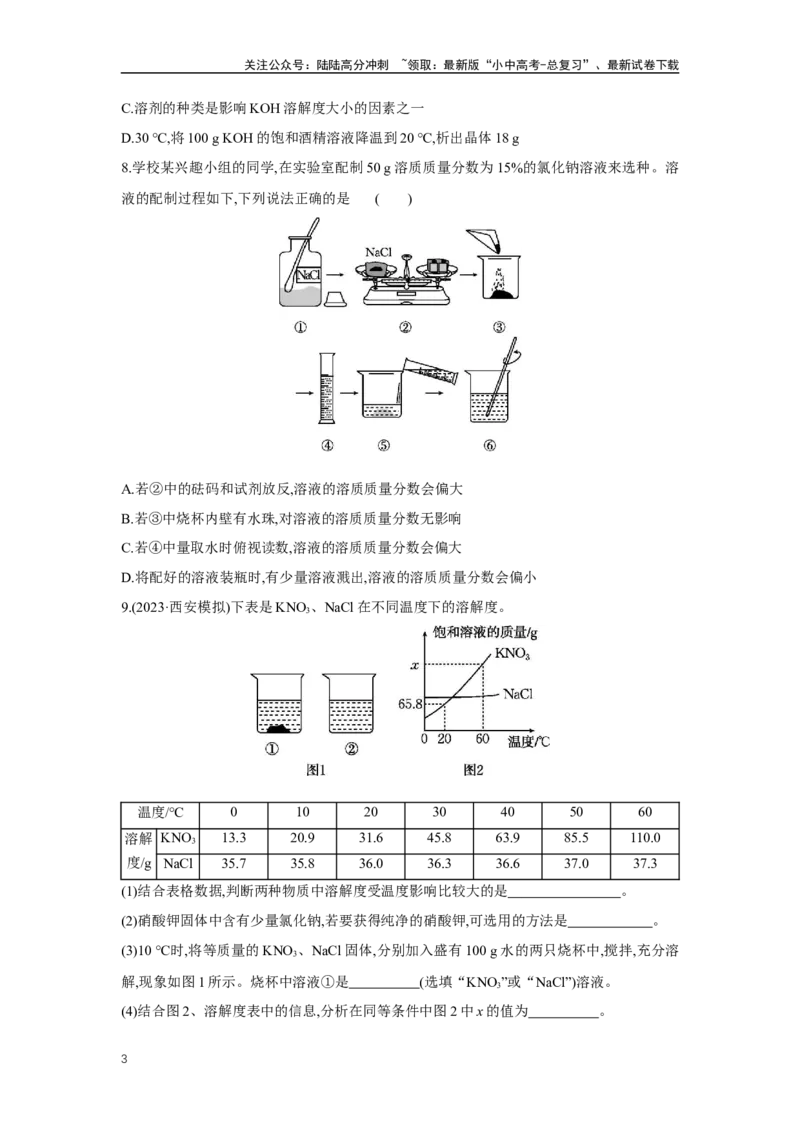
6.(2024·河北)下表是KNO 和NaNO 在不同温度时的溶解度,小明用其中一种物质(X)进行了
3 3
下图所示的实验(水蒸发忽略不计)。下列分析错误的是 ( )
温度/℃ 20 40 60
KNO 31.6 63.9 110
3
溶解度/g
NaNO 88.0 103 125
3
A.X为NaNO
3
B.③中溶液为X的不饱和溶液
C.④中溶液的质量为100 g
D.溶液中溶质的质量分数:②=③>④
7.(2024·延安模拟)KOH分别在水和酒精中的溶解度曲线如图所示,下列说法正确的是 (
)
A.30 ℃时,KOH的饱和水溶液中溶质与溶剂的质量比为50∶63
B.20 ℃时,将KOH在水和酒精中的饱和溶液分别蒸发10 g溶剂,析出晶体的质量相等
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.溶剂的种类是影响KOH溶解度大小的因素之一
D.30 ℃,将100 g KOH的饱和酒精溶液降温到20 ℃,析出晶体18 g
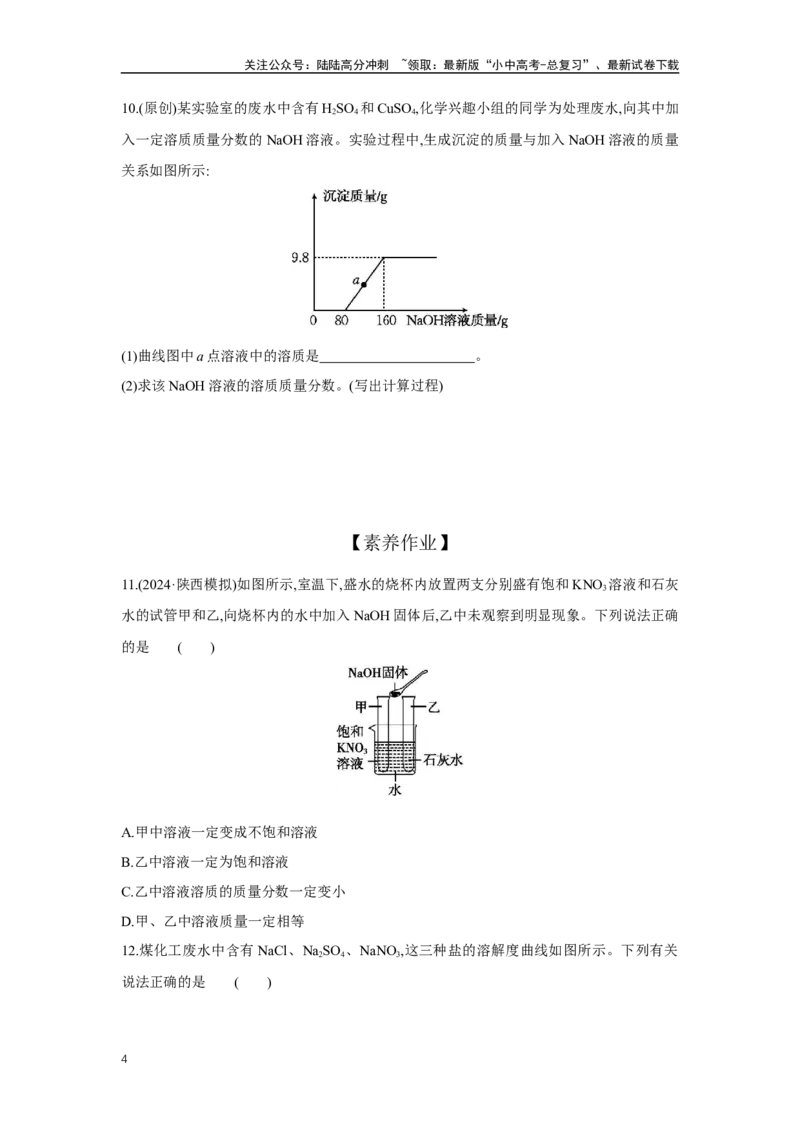
8.学校某兴趣小组的同学,在实验室配制50 g溶质质量分数为15%的氯化钠溶液来选种。溶
液的配制过程如下,下列说法正确的是 ( )
A.若②中的砝码和试剂放反,溶液的溶质质量分数会偏大
B.若③中烧杯内壁有水珠,对溶液的溶质质量分数无影响
C.若④中量取水时俯视读数,溶液的溶质质量分数会偏大
D.将配好的溶液装瓶时,有少量溶液溅出,溶液的溶质质量分数会偏小
9.(2023·西安模拟)下表是KNO、NaCl在不同温度下的溶解度。
3
温度/℃ 0 10 20 30 40 50 60
溶解 KNO 13.3 20.9 31.6 45.8 63.9 85.5 110.0
3
度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
(1)结合表格数据,判断两种物质中溶解度受温度影响比较大的是 。
(2)硝酸钾固体中含有少量氯化钠,若要获得纯净的硝酸钾,可选用的方法是 。
(3)10 ℃时,将等质量的KNO 、NaCl固体,分别加入盛有100 g水的两只烧杯中,搅拌,充分溶
3
解,现象如图1所示。烧杯中溶液①是 (选填“KNO”或“NaCl”)溶液。
3
(4)结合图2、溶解度表中的信息,分析在同等条件中图2中x的值为 。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
10.(原创)某实验室的废水中含有HSO 和CuSO ,化学兴趣小组的同学为处理废水,向其中加
2 4 4
入一定溶质质量分数的NaOH溶液。实验过程中,生成沉淀的质量与加入NaOH溶液的质量
关系如图所示:
(1)曲线图中a点溶液中的溶质是 。
(2)求该NaOH溶液的溶质质量分数。(写出计算过程)
【素养作业】
11.(2024·陕西模拟)如图所示,室温下,盛水的烧杯内放置两支分别盛有饱和KNO 溶液和石灰
3
水的试管甲和乙,向烧杯内的水中加入NaOH固体后,乙中未观察到明显现象。下列说法正确
的是 ( )
A.甲中溶液一定变成不饱和溶液
B.乙中溶液一定为饱和溶液
C.乙中溶液溶质的质量分数一定变小
D.甲、乙中溶液质量一定相等
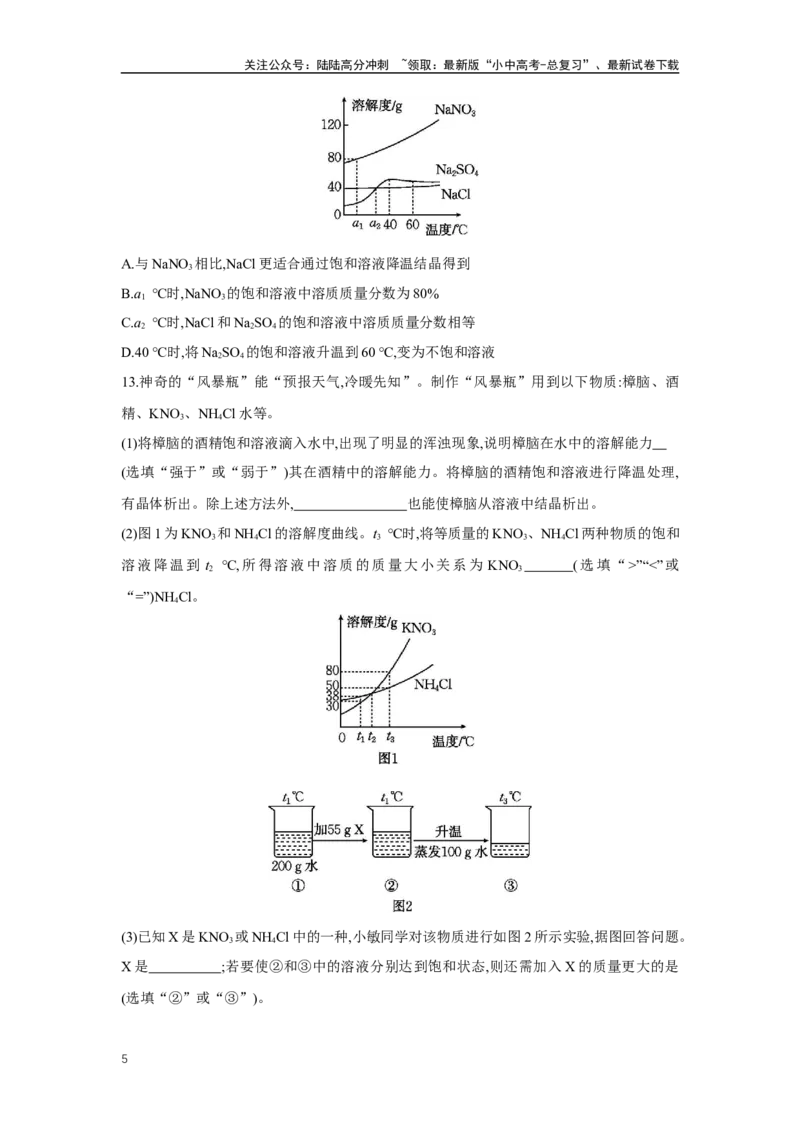
12.煤化工废水中含有NaCl、NaSO 、NaNO ,这三种盐的溶解度曲线如图所示。下列有关
2 4 3
说法正确的是 ( )
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.与NaNO 相比,NaCl更适合通过饱和溶液降温结晶得到
3
B.a ℃时,NaNO 的饱和溶液中溶质质量分数为80%
1 3
C.a ℃时,NaCl和NaSO 的饱和溶液中溶质质量分数相等
2 2 4
D.40 ℃时,将NaSO 的饱和溶液升温到60 ℃,变为不饱和溶液
2 4
13.神奇的“风暴瓶”能“预报天气,冷暖先知”。制作“风暴瓶”用到以下物质:樟脑、酒
精、KNO、NH Cl水等。
3 4
(1)将樟脑的酒精饱和溶液滴入水中,出现了明显的浑浊现象,说明樟脑在水中的溶解能力
(选填“强于”或“弱于”)其在酒精中的溶解能力。将樟脑的酒精饱和溶液进行降温处理,
有晶体析出。除上述方法外, 也能使樟脑从溶液中结晶析出。
(2)图1为KNO 和NH Cl的溶解度曲线。t ℃时,将等质量的KNO、NH Cl两种物质的饱和
3 4 3 3 4
溶液降温到 t ℃,所得溶液中溶质的质量大小关系为 KNO (选填“>”“<”或
2 3
“=”)NHCl。
4
(3)已知X是KNO 或NH Cl中的一种,小敏同学对该物质进行如图2所示实验,据图回答问题。
3 4
X是 ;若要使②和③中的溶液分别达到饱和状态,则还需加入X的质量更大的是
(选填“②”或“③”)。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
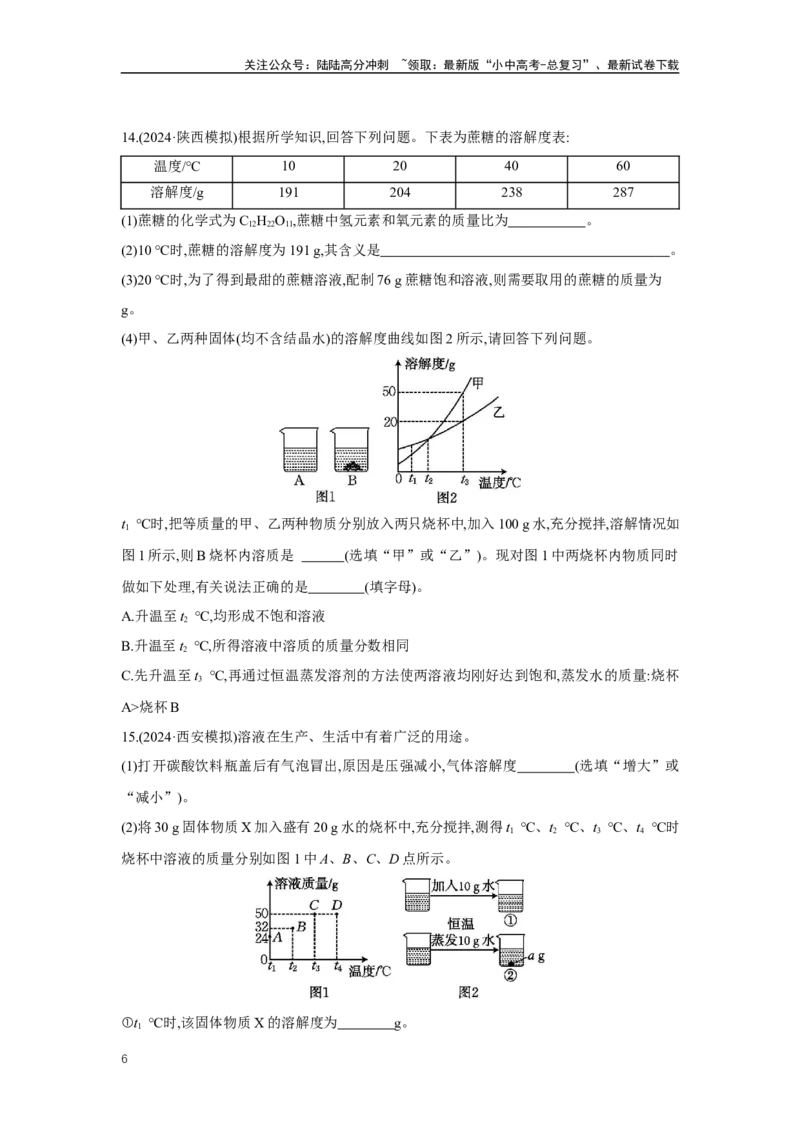
14.(2024·陕西模拟)根据所学知识,回答下列问题。下表为蔗糖的溶解度表:
温度/℃ 10 20 40 60
溶解度/g 191 204 238 287
(1)蔗糖的化学式为C H O ,蔗糖中氢元素和氧元素的质量比为 。
12 22 11
(2)10 ℃时,蔗糖的溶解度为191 g,其含义是 。
(3)20 ℃时,为了得到最甜的蔗糖溶液,配制76 g蔗糖饱和溶液,则需要取用的蔗糖的质量为
g。
(4)甲、乙两种固体(均不含结晶水)的溶解度曲线如图2所示,请回答下列问题。
t ℃时,把等质量的甲、乙两种物质分别放入两只烧杯中,加入100 g水,充分搅拌,溶解情况如
1
图1所示,则B烧杯内溶质是 (选填“甲”或“乙”)。现对图1中两烧杯内物质同时
做如下处理,有关说法正确的是 (填字母)。
A.升温至t ℃,均形成不饱和溶液
2
B.升温至t ℃,所得溶液中溶质的质量分数相同
2
C.先升温至t ℃,再通过恒温蒸发溶剂的方法使两溶液均刚好达到饱和,蒸发水的质量:烧杯
3
A>烧杯B
15.(2024·西安模拟)溶液在生产、生活中有着广泛的用途。
(1)打开碳酸饮料瓶盖后有气泡冒出,原因是压强减小,气体溶解度 (选填“增大”或
“减小”)。
(2)将30 g固体物质X加入盛有20 g水的烧杯中,充分搅拌,测得t ℃、t ℃、t ℃、t ℃时
1 2 3 4
烧杯中溶液的质量分别如图1中A、B、C、D点所示。
①t ℃时,该固体物质X的溶解度为 g。
1
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
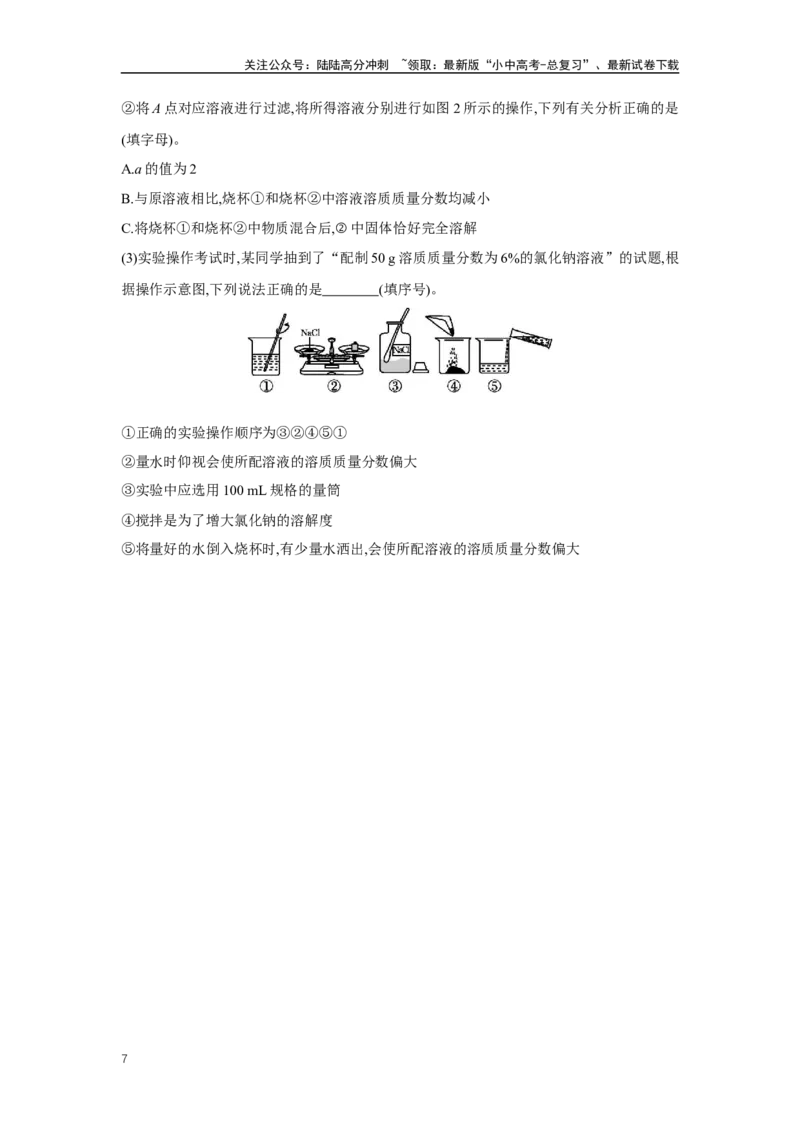
②将A点对应溶液进行过滤,将所得溶液分别进行如图2所示的操作,下列有关分析正确的是
(填字母)。
A.a的值为2
B.与原溶液相比,烧杯①和烧杯②中溶液溶质质量分数均减小
C.将烧杯①和烧杯②中物质混合后,②中固体恰好完全溶解
(3)实验操作考试时,某同学抽到了“配制50 g溶质质量分数为6%的氯化钠溶液”的试题,根
据操作示意图,下列说法正确的是 (填序号)。
①正确的实验操作顺序为③②④⑤①
②量水时仰视会使所配溶液的溶质质量分数偏大
③实验中应选用100 mL规格的量筒
④搅拌是为了增大氯化钠的溶解度
⑤将量好的水倒入烧杯时,有少量水洒出,会使所配溶液的溶质质量分数偏大
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答案
1.A 2.B 3.A 4.B
5.D 【解析】A.a为喷泉水,b为自来水,而不是a为自来水,b为喷泉水,故A分析错误;B.空
气中氧气含量会影响溶解氧的含量,故B分析错误;C.水中的饱和氧气含量取决于温度,则自
然界里河水中溶解氧的含量会发生改变,故C分析错误;D.管材选择可能会影响自来水输送
中溶解氧的含量,故D分析正确。
6.C 【解析】A.40 ℃时,硝酸钾的溶解度为63.9 g,硝酸钠的溶解度为103 g,向40 ℃时的
100 g水中加入 100 g X,全部溶解,温度恢复至 40 ℃时,烧杯中没有固体析出,则X为
NaNO ,正确。B.②中溶液平均分成两等份,其中一份温度升高至60 ℃时,60 ℃时,硝酸钠的
3
溶解度为125 g,温度升高,硝酸钠的溶解度增大,则③中溶液为X的不饱和溶液,正确。C.②
中溶液平均分成两等份,其中一份溶液中溶质的质量为50 g,溶剂的质量为50 g,降温至20
℃,20 ℃时,硝酸钠的溶解度为88.0 g,该温度下50 g水中最多能溶解44 g硝酸钠,④中溶液
的质量为50 g+44 g=94 g,正确。D.溶液具有均一性,其中一份温度升高至60 ℃时,溶液的组
成没有发生改变,则溶质质量分数②=③;另一份降温至20 ℃,有晶体析出,溶液中溶质的质量
分数减小,则溶液中溶质的质量分数②=③>④,正确。
7.C 【解析】A.30 ℃时,氢氧化钾的溶解度是126 g,KOH的饱和水溶液中溶质与溶剂的质
量比为126 g∶100 g=63∶50,错误;B.20 ℃时,将KOH在水和酒精中(溶解度不相等)的饱和溶液
分别蒸发10 g溶剂,析出晶体的质量不一定相等,错误;C.溶剂的种类是影响KOH溶解度大小
的因素之一,正确;D.30 ℃时,将100 g KOH的饱和酒精溶液降温到20 ℃,析出的晶体的质量
是18 g×100 g÷138 g≈13 g,错误。
8.C 【解析】A.若②中的砝码和试剂放反,则所取的氯化钠质量偏小,溶液的溶质质量分数
偏小,故A说法错误;B.若③中烧杯内壁有水珠,则溶剂水的质量偏大,溶液的溶质质量分数偏
小,故B说法错误;C.若④中量取水时俯视读数,则溶剂水的质量偏小,溶液的溶质质量分数会
偏大,故C说法正确;D.溶液具有均一性,将配好的溶液装瓶时,有少量溶液溅出,溶液的溶质质
量分数不变,故D说法错误。
9.(1)硝酸钾 (2)降温结晶 (3)KNO (4)105
3
【解析】(1)由表中数据可知,溶解度受温度影响比较大的是硝酸钾。
(2)硝酸钾、氯化钠的溶解度均随温度的升高而增加,硝酸钾的溶解度受温度影响较大,氯化
钠的溶解度受温度影响较小,故硝酸钾固体中含有少量氯化钠,若获得纯净的硝酸钾,可选用
的方法是降温结晶。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)10 ℃时,氯化钠的溶解度大于硝酸钾的溶解度,该温度下,将等质量的KNO、NaCl固体,分
3
别加入盛有100 g水的两只烧杯中,搅拌,充分溶解,①中固体部分溶解,②中固体全部溶解,则
烧杯中溶液①是KNO 溶液。
3
(4)20 ℃时,硝酸钾的溶解度为31.6 g,该温度下,65.8 g硝酸钾饱和溶液中溶质质量为65.8
31.6g
g× ×100%=15.8 g,则溶剂质量为65.8 g-15.8 g=50 g,升温至60 ℃时,硝酸钾的
31.6g+100g
溶解度为110 g,则该温度下,50 g水中能溶解55 g硝酸钾固体形成饱和溶液,则图2中x的值
为55+50=105。
10.(1)Na SO 、CuSO
2 4 4
(2)解:由图可知,加入160 g-80 g=80 g氢氧化钠溶液时,硫酸铜和氢氧化钠恰好完全反应生
成9.8 g沉淀。
设该NaOH溶液的溶质质量分数为x。
CuSO +2NaOH Cu(OH) ↓+Na SO
4 2 2 4
80 98
80 g×x 9.8 g
80 80g×x
=
98 9.8g
x=10%
答:该NaOH溶液的溶质质量分数为10%。
【解析】(1)向含有HSO 和CuSO 的废水中加入一定溶质质量分数的NaOH溶液,氢氧化钠
2 4 4
先和硫酸反应生成硫酸钠和水,再和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,由图可知,a点之
后沉淀质量继续增加,则曲线图中 a 点溶液中的溶质是生成的 NaSO 和未完全反应的
2 4
CuSO 。
4
11.A 【解析】A.氢氧化钠固体溶于水放出热量,温度升高,硝酸钾的溶解度随着温度的升高
而增大,因此甲中溶液一定变成不饱和溶液,正确; B.氢氧化钙的溶解度随着温度的升高而减
小,实验中,乙中未观察到明显现象,因此乙中的溶液可能是氢氧化钙的不饱和溶液,也可能是
氢氧化钙的饱和溶液,错误; C.氢氧化钙的溶解度随着温度的升高而减小,实验中,乙中未观察
到明显现象,因此乙中溶液溶质的质量分数一定没有改变,错误; D.题干没有提到两种溶液的
质量关系,因此无法判断甲、乙中溶液质量是否相等,错误。
12.C 【解析】A.与NaNO 相比,NaCl的溶解度受温度变化影响较小,所以更适合通过饱和
3
溶液蒸发结晶得到,故A错误;B.a ℃时,NaNO 的溶解度是80 g,所以饱和溶液中溶质的质量
1 3
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
80g
分数为 ×100%≠80%,故B错误;C.a ℃时,NaCl和NaSO 的溶解度相等,所以饱和溶液
180g 2 2 4
的溶质质量分数相等,故C正确;D.40 ℃时,Na SO 的饱和溶液升温到60 ℃,溶解度减小,仍为
2 4
饱和溶液,故D错误。
13.(1)弱于 恒温蒸发溶剂 (2)< (3)硝酸钾 ③
【解析】(1)将樟脑的酒精饱和溶液滴入水中,出现了明显的浑浊,说明樟脑在水中的溶解能
力弱于其在酒精中的溶解能力。樟脑的酒精饱和溶液降温也实现了晶体析出。除上述方法
外,恒温蒸发溶剂也能使樟脑从溶液中结晶析出。
(2)图1为KNO 和NH Cl的溶解度曲线。t ℃时,硝酸钾的溶解度大于氯化铵的溶解度,则等
3 4 3
质量的KNO 、NH Cl两种物质的饱和溶液中,溶质质量关系为硝酸钾>氯化铵,溶剂质量关
3 4
系为硝酸钾<氯化铵;t ℃时,将等质量的KNO 、NH Cl两种物质的饱和溶液降温到t ℃,都
3 3 4 2
有晶体析出,但溶剂质量不变,此时二者的溶解度相等,而溶剂质量关系为硝酸钾<氯化铵,溶剂
质量越大,能溶解的溶质质量也越大,则所得溶液中的溶质质量大小关系为KNO