文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 02 金属与酸、盐溶液反应分析
【题型一】等量金属和足量酸反应
[例题1] (2024•榆树市校级一模)小圳同学在探究金属与酸的反应时做了如图1实验,
分别将形状、质量相同的Mg、Al、Zn、Fe和Cu打磨后放入烧瓶中,再注入足量体积和浓度
均相同的稀硫酸,利用压强传感器采集数据,得到图2所示的气压变化情况。下列有关说法错
误 的 是 ( )
A.五种金属中Mg的金属活动性最强
B.Zn与稀硫酸反应产生H 速率比Fe快
2
C.反应结束后消耗稀硫酸最少的金属是Al
D.由图2可知金属Cu不能与稀硫酸反应
【解答】解:A、由图示可知,镁反应用时最短到达反应终点,则五种金属中Mg的金属活动性
最强,故选项说法正确。
B、由图示可知,锌反应速率适中,压强变化比较平稳,铁与稀硫酸反应的速率较慢,则 Zn与
稀硫酸反应产生H 速率比Fe快,故选项说法正确。
2
C、由图示可知,铝和稀硫酸反应产生的气压最大,说明最终生成的氢气质量最多,则反应结束
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
后消耗稀硫酸最多的金属是Al;铁和稀硫酸反应产生的气压最小,说明最终生成的氢气质量最
少,反应结束后消耗稀硫酸最少的金属是铁,故选项说法错误。
D、由图示可知,铜和稀硫酸接触,压强没有明显变化,铜不能与稀硫酸反应,故选项说法正确。
故选:C。
[例题2] (2023•兴庆区校级一模)等质量的三种金属分别与足量的、浓度相同的盐酸反
应,产生氢气的质量与反应时间的关系如图所示,下列有关说法正确的是(金属不是K、Na、
Ca,且与盐酸反应形成化合物中化合价均为+2价)( )
A.三种金属的活动性顺序是a>b>c
B.三种金属产生H 的质量a>c>b
2
C.三种金属最终消耗盐酸的质量相等
D.三种金属的相对原子质量大小关系是c>b>a
【解答】解:A、等质量的a、b、c三种金属,a最先完成反应,其次为c,而b最后反应完全,
依据金属活动性顺序的意义可判断三种金属的活动性大小为:a>c>b,故A不正确;
B、由图象可知,完全反应后生成氢气的质量关系是:a>b>c,故B不正确;
C、反应所放出氢气质量全部来自于盐酸,由于所放出氢气的质量不同,三种金属最终消耗盐酸
的质量不相等,故C不正确;
金属化合价
D、根据一定量金属完全反应产生氢气质量= ×金属的质量,因此金属
金属的相对原子质量
的质量及化合价均相同,所以金属的相对原子质量与反应放出氢气的多少成反应比,则三种金
属的相对原子质量是:c>b>a,故D正确。
故选:D。
[例题3] (2023•西峡县一模)等质量的镁、锌、铁分别跟足量的稀硫酸在室温下起反应,
图测中能够正确反映产生氢气质量m与反应时间t关系的图象为( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. B.
C. D.
【解答】解:在金属活动性顺序中,镁>锌>铁,与硫酸反应时镁的速率最快,在坐标中斜线
最陡,铁的反应速率最慢,在坐标中斜线最平缓,观察图象,排除 BC,等质量的镁,锌,铁,
分别跟足量的稀硫酸在室温下起反应,则镁生成的氢气最多,锌生成的氢气最少,观察图象,
排除D,
故选:A。
1.等量金属与足量酸反应,金属完全反应,生成氢气的质量由金属的质量决定,计算公式:金属的化
合价氢气的质量=参加反应的金属质量x金属的化合价➗金属的相对原子质量
2.金属的化合价相同时(铝的化合价等效成+2 价,相对原子质量等效为18),相对原子质量越小,产
生氢气的质量越大,如金属 Al、Mg、Fe、Zn生成H,的质量由多至少的顺序为:AI>Mg>Fe>Zn.
2
3.等质量的金属Mg、Al、Zn、Fe与足量的稀盐酸反应制取的H ,产生H 的量由多到少的是 Al>
2 2
Mg>Fe>Zn 。
画出图像1:(X-时间,Y-H 的质量) 图像2:(X-HCl的质量,Y- H 的质量)
2 2
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【题型二】足量金属和等量酸反应
[例题4] (2016•宿迁校级一模)向一定质量的稀盐酸中加入镁粉至过量,下列图象合理
的是( )
A. B.
C. D.
【解答】解:A、反应前没有氯化镁,氯化镁质量为零,镁与盐酸反应生成氯化镁,随着反应的
进行,氯化镁的质量不断增加,反应结束,氯化镁的质量不再改变,改成横线,故A错;
B、反应前氢气质量为零,镁与盐酸反应不断生成氯化镁和氢气,氢气质量不断增加,当反应完
毕氢气质量不再改变,改成横线,故B正确;
C、金属与酸反应放出热量,溶液的温度应该升高,故C错;
D、镁与盐酸反应生成氯化镁和氢气,进入溶液的是镁,跑出来的是氢气,所以溶液质量增加,
反应结束后,溶液质量不再改变,故D错。
故选:B。
[例题5] (2023•天河区校级三模)分别往等量的稀盐酸中加入过量的镁粉和锌粒,下列
图示与实验结果相符的是( )
A. B.
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C. D.
【解答】解:在金属活动性顺序表中,镁排在锌的前面,镁的活动性大于锌,镁与稀盐酸反应
速率快,反应完全所需的时间短,金属与酸反应生成的氢气质量等于酸中氢元素的质量,由于
金属过量,酸等量,所以反应完全生成氢气的质量是相等的。
故选:D。
1.足量金属与等量的酸反应,酸完全反应,生成氢气的质量由酸的质量决定,最终产生氢气的质量
相等。
2.生成等质量的 H,参加反应的金属 Al、Mg、Fe、Zn 的质量比为 18:24:56:65。
2
【题型三】金属与盐溶液反应后滤液、滤渣成分分析
[例题6] (2023•东港区校级三模)某金属加工厂生产过程中的废液含有少量的硝酸银和
硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向
滤液中加入少量的稀盐酸,无沉淀产生,则下列有关说法正确的是( )
A.滤出的固体中一定含有银,可能含有铜,一定不含铁
B.滤出的固体中一定含有银,可能含有铜和铁
C.滤液中一定含有硝酸亚铁,可能含有硝酸银
D.滤液中一定含有硝酸亚铁,可能含有硝酸银和硝酸铜
【解答】解:铁的金属活动性比银、铜强,向含有硝酸银和硝酸铜溶液中加入一定量的铁粉,
铁先与AgNO 反应生成硝酸亚铁和银,AgNO 反应完,若还有铁粉,铁才能与Cu(NO ) 反
3 3 3 2
应生成硝酸亚铁和铜。反应停止后过滤,向滤液中加入少量的稀盐酸,无沉淀产生,说明滤液
中不含硝酸银。
A、滤出的固体中一定含有银,可能含有铜,也可能含有铁,因为铁粉可能是过量的,故选项说
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
法错误。
B、滤出的固体中一定含有银,可能含有铜和铁,故选项说法正确。
C、滤液中一定含有硝酸亚铁,不可能含有硝酸银,故选项说法错误。
D、滤液中一定含有硝酸亚铁,不可能含有硝酸银,可能含有硝酸铜,故选项说法错误。
故选:B。
[例题7] (2023•咸宁模拟)将锌粉持续加入到100g含有AgNO 和Cu(NO )两种溶质
3 3
的混合溶液中,充分反应。生成固体质量随加入锌的质量变化的关系如图所示,下列说法正确
的是( )
A.在a点时,溶液质量最小
B.在b点时,固体成分为Ag和Cu
C.当加入锌粉质量为9.75g充分反应后,生成固体质量为24.8g
D.在c点时,溶液中溶质的质量分数为37.8%
【解答】解:A、根据以上分析可知,锌与硝酸银反应固体质量增加,溶液质量减小,锌与硝酸
铜反应,固体质量减小,溶液质量增大,但锌与硝酸银反应溶液减小大于锌与硝酸铜反应溶液
增加的质量,故b的溶液质量最小,而不是a点,故A错误;
B、b点是锌与硝酸银恰好完全反应生成硝酸锌和银,则在b点时,固体成分为Ag,而不是Ag
和Cu,故B错误;
C、当加入锌粉质量为9.75g时,6.5g与硝酸银反应生成21.6g银,与硝酸铜反应的锌的质量为
9.75g﹣6.5g=3.25g,3.25g锌与硝酸铜反应生成铜 3.2g,则得到的固体总质量为 21.6g+3.2g=
24.8g,故C正确;
65
D、参加反应的锌的总质量为 13.0g,生成硝酸锌的质量为 13.0g÷ =
65+(14+16×3)×2
37.8g,原溶液的质量为100g,加入了13.0g锌,析出固体28g,则溶液质量为100g+13.0g﹣28g
37.8g
=85g,则在c点时,溶液中溶质的质量分数为 ×100%≈44.5%,而不是37.8%,故D错
85g
误;
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选:C。
1.根据金属活动性顺序写出先后发生反应的化学方程式。多种金属+一种盐溶液反应:最活泼的金属
先反应;一种金属+多种盐溶液反应:最不活泼的金属先被置换出来。
2.根据加入金属的量分析滤液、滤渣成分。
3.常考隐含条件:
(1)向滤渣中加入酸有气泡产生,说明滤渣中含有金属活动性位于氢前面的金属。
(2)溶液的特殊颜色:蓝色→含有Cu2+、浅绿色→含有Fe2+
1. (2024•平城区一模)将一定量的铁粉加入到盛有一定量硝酸银和硝酸铜的混合溶液
中,充分反应后过滤,将所得滤渣放入稀盐酸中,无气泡产生,下列说法错误的是( )
A.滤液中最多含有三种溶质
B.滤液中一定含有Fe(NO ) ,一定没有AgNO ,可能含有Cu(NO )
3 2 3 3 2
C.滤渣里一定含有Ag,一定没有Fe
D.如果滤液呈蓝色,则滤液中可能含有AgNO
3
【解答】解:在金属活动性顺序中,铁>氢>铜>银,铁能与硝酸银反应生成硝酸亚铁和银,
能与硝酸铜反应生成硝酸亚铁和铜,所以溶液中一定含有硝酸亚铁,铜能与硝酸银反应生成硝
酸铜和银。在滤渣中加入稀盐酸,没有气体产生,说明铁全部参加反应,硝酸银和硝酸铜是否
含有无法确定。由以上分析可知:
A、滤液中一定有硝酸亚铁,可能含有硝酸铜、硝酸银,滤液中最多含有三种溶质,故说法正确;
B、滤液中一定有硝酸亚铁,可能含有硝酸铜、硝酸银,故说法错误;
C、在滤渣中加入稀盐酸,没有气体产生,说明铁全部参加反应,滤渣中一定有银,铜不能确定,
故说法正确;
D、如果滤液呈蓝色,只能说明滤液中含有硫酸铜,无法判断是否含有AgNO ,故说法正确。
3
故选:B。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2. (多选)(2024•济南模拟)将ag镁粉和银粉的混合物加到ZnSO 和CuSO 的混合溶
4 4
液中,充分反应后过滤,得到无色滤液和部分滤渣。下列有关说法中,合理的是( )
A.滤渣的质量一定大于ag
B.滤液中一定不含Cu2+和Ag+
C.若滤液中的金属阳离子只有Mg2+,则滤渣中一定含有Ag、Cu、Zn金属单质
D.若滤渣中含有Ag、Cu、Zn金属单质,则滤液中的金属阳离子只有Mg2+
【解答】解:A、由Mg+CuSO =MgSO +Cu可知,每24份质量的镁置换出64份质量的铜,固
4 4
体质量增加;由Mg+ZnSO =MgSO +Zn可知,每24份质量的镁置换出65份质量的锌,固体质
4 4
量增加,则滤渣的质量一定大于ag,故选项说法正确。
B、充分反应后过滤,得到无色滤液,则硫酸铜已经完全反应,银没有参与反应,则滤液中一定
不含铜离子和银离子,故选项说法正确。
C、若滤液中的金属阳离子只有Mg2+,则硫酸锌、硫酸铜已经完全反应,银没有参与反应,故
滤渣中一定含银、铜、锌,可能含镁,故选项说法正确。
D、若滤渣中含有Ag、Cu、Zn金属单质,硫酸铜已经完全反应,银没有参与反应,硫酸锌可能
完全反应,也可能部分反应,故滤液中的金属阳离子一定含镁离子,可能含锌离子,故选项说
法错误。
故选:ABC。
3. (2023•仙桃校级一模)向装有一定量硝酸铜和硝酸银混合溶液的试管中,缓慢加入
细铁粉,充分反应。下列关于试管中物质的变化关系图错误的是( )
A. B.
C. D.
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:A、向装有一定量硝酸铜和硝酸银混合溶液的试管中,缓慢加入细铁粉,铁粉先和
硝酸银反应生成银和硝酸亚铁,一开始试管中只有银一种金属;硝酸银反应完后,铁粉再和硝
酸铜反应生成铜和硝酸亚铁,此时试管中有银和铜两种金属;当硝酸铜也反应完之后,继续加
入铁粉,没有物质反应,此时试管中有银、铜、铁三种金属;故选项图像正确。
B、一开始没有加入铁粉时,溶质只有硝酸银和硝酸铜两种,开始加入铁粉后,铁粉和硝酸银反
应生成银和硝酸亚铁,溶质有硝酸银、硝酸铜和生成的硝酸亚铁三种,随着硝酸银反应完,溶
质有硝酸铜和硝酸亚铁两种,硝酸铜也反应完后,溶质只有硝酸亚铁,故选项图像正确。
C、铁、铜、银三种金属的相对原子质量由大到小的顺序是:银>铜>铁,一开始铁置换硝酸银
中的银时,溶液总质量减小的快,硝酸银反应完后,铁置换硝酸铜中的铜时,溶液总质量减小
的慢,完全反应后,溶液总质量不变,故选项图像正确。
D、铁、铜、银三种金属的相对原子质量由大到小的顺序是:银>铜>铁,一开始铁置换硝酸银
中的银时,固体总质量增加的快,硝酸银反应完后,铁置换硝酸铜中的铜时,固体总质量增加
的慢,完全反应后,随着铁粉的不断加入,固体总质量不断增大,故选项图像错误。
故选:D。
4. (2023•高要区二模)向400.0gCuSO 的溶液中先逐渐加入一定量的锌粉,再逐渐加
4
入铁粉,测得剩余固体质量与加入金属的质量关系如图所示。下列说法正确的是( )
A.a点对应的溶液为无色
B.n=13,m=19.2
C.c点对应的固体中加稀盐酸,有气泡产生
D.原溶液中CuSO 的溶质质量分数为16.0%
4
【解答】解:A、向硫酸铜中加一定量的锌粉,锌和硫酸铜反应生成硫酸锌和铜,再加入铁粉,
铁和硫酸锌不反应,铁和硫酸铜反应生成硫酸亚铁和铜,图中出现 3个转折点,0﹣a段表示锌
和硫酸铜反应,a点表示锌刚好消耗,a﹣b表示铁和硫酸铜反应,b点表示硫酸铜刚好消耗,则
a点含有硫酸铜,对应的溶液为蓝色,故选项说法错误。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B、0﹣a段表示锌和硫酸铜反应生成硫酸锌和铜,a点时,剩余固体为反应生成的铜,此时铜的
质量为12.8g,
设加入锌的质量为x,
Zn+CuSO =ZnSO +Cu
4 4
65 64
x 12.8g
65 x
=
64 12.8g
x=13g
则n=13
a﹣b表示铁和硫酸铜反应生成硫酸亚铁和铜,b点表示硫酸铜刚好反应完,此时消耗铁的质量为:
29.8g﹣13g=16.8g,
设铁和硫酸铜反应生成的铜的质量为y,
Fe+CuSO =FeSO +Cu
4 4
56 64
16.8g y
56 16.8g
=
64 y
y=19.2g
则m=12.8+19.2=32,故选项说法错误。
C、c点对应的固体中有铁和铜,加稀盐酸,铁和盐酸反应生成氯化亚铁和氢气,有气泡产生,
故选项说法正确。
64
D、生成的铜的质量为32g,铜元素来自硫酸铜,则硫酸铜的质量为32g÷( )=
64+32+16×4
80g
80g,则原溶液中CuSO 的溶质质量分数为 ×100%=20%,故选项说法错误。
4
400.0g
故选:C。
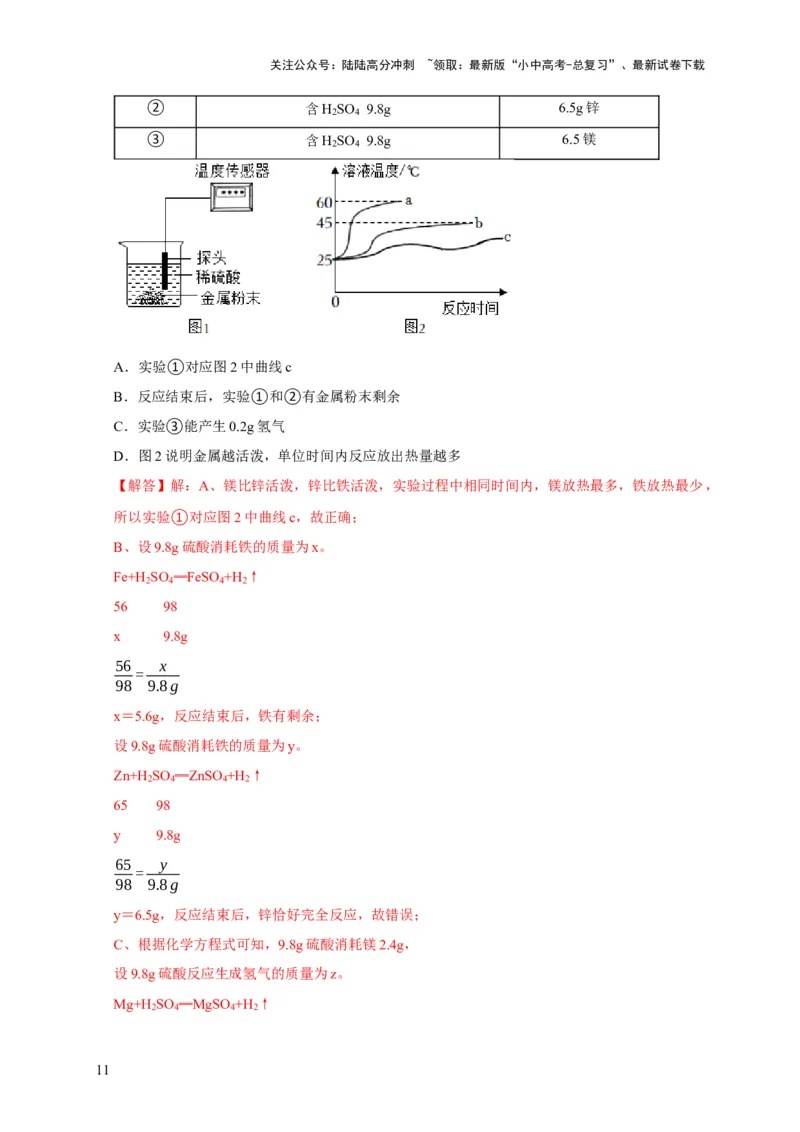
5. (2023•南平模拟)某实验小组在相同条件下探究金属与酸反应的放热情况,实验装
置如图 1,实验所用药品如下表。溶液温度随反应时间变化如图 2。下列分析错误的是
( )
实验编组 等质量稀硫酸 金属粉末质量
① 含H SO 9.8g 6.5g铁
2 4
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
② 含H SO 9.8g 6.5g锌
2 4
③ 含H SO 9.8g 6.5镁
2 4
A.实验①对应图2中曲线c
B.反应结束后,实验①和②有金属粉末剩余
C.实验③能产生0.2g氢气
D.图2说明金属越活泼,单位时间内反应放出热量越多
【解答】解:A、镁比锌活泼,锌比铁活泼,实验过程中相同时间内,镁放热最多,铁放热最少,
所以实验①对应图2中曲线c,故正确;
B、设9.8g硫酸消耗铁的质量为x。
Fe+H SO ═FeSO +H ↑
2 4 4 2
56 98
x 9.8g
56 x
=
98 9.8g
x=5.6g,反应结束后,铁有剩余;
设9.8g硫酸消耗铁的质量为y。
Zn+H SO ═ZnSO +H ↑
2 4 4 2
65 98
y 9.8g
65 y
=
98 9.8g
y=6.5g,反应结束后,锌恰好完全反应,故错误;
C、根据化学方程式可知,9.8g硫酸消耗镁2.4g,
设9.8g硫酸反应生成氢气的质量为z。
Mg+H SO ═MgSO +H ↑
2 4 4 2
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
98 2
9.8g z
98 9.8g
=
2 z
z=0.2g,故正确;
D、由图可以看出,金属越活泼,单位时间内反应放出热量越多,故正确。
故选:B。
6. (2023•郁南县校级二模)向硝酸银和硝酸铜的混合溶液中加入一定量的镁粉,充分
反应后再加入一定量的稀盐酸,有气体产生,将混合液过滤,则下列说法中正确的是( )
A.滤出的固体中一定含银,可能含铜
B.滤液呈蓝色
C.滤出的固体中一定含银、铜和镁
D.滤液中一定含有硝酸镁,一定没有硝酸铜和硝酸银
【解答】解:A、由分析可知,滤出的固体中一定含铜、银,可能含镁,该选项说法错误,故该
选项不符合题意;
B、由分析可知,硝酸银、硝酸铜已经完全反应,滤液中一定含硝酸镁和氯化镁,可能含盐酸,
故滤液呈无色,该选项说法错误,故该选项不符合题意;
C、由分析可知,滤出的固体中一定含银和铜,可能含镁,该选项说法错误,故该选项不符合题
意;
D、由分析可知,滤液中一定含硝酸镁,一定不含硝酸铜和硝酸银,该选项说法正确,故该选项
符合题意;
故选:D。
7. (2023•孝感模拟)某溶液中含有Cu(NO ) 和AgNO ,现向其中加入一定量的锌
3 2 3
粉进行处理,并绘制出参加反应的锌与溶液中溶质种类的关系如图所示。下列说法中不正确的
是( )
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.当溶质种类为1种时,金属单质种类不可能为1种
B.c~d间(不含两点)发生反应的化学方程式为Zn+Cu(NO ) =Cu+Zn(NO )
3 2 3 2
C.从m 变化到m 时,溶液中硝酸铜的质量分数变大
1 2
D.若m =6.5g,m =13.0g,则d点滤渣质量不大于28g
2 4
【解答】解:A、根据图示,当溶质种类为1种时,此时溶质为Zn(NO ) ,说明锌已将硝酸
3 2
铜和硝酸银中的铜和银完全置换出来,金属单质至少有2种,故选项正确;
B、c~d间(不含两点)有2种溶质,分别是Zn(NO ) ,Cu(NO ) ,说明锌和硝酸银已反
3 2 3 2
应完,锌开始与硝酸铜反应,化学方程式为Zn+Cu(NO ) =Zn(NO ) +Cu,故选项正确;
3 2 3 2
C、从m 变化到m ,溶液种有3种溶质,分别是Zn(NO ) ,AgNO ,Cu(NO ) ,说明此
1 2 3 2 3 3 2
时发生的是锌和硝酸银的反应
Zn+2AgNO =Zn(NO ) +2Ag
3 3 2
65 216
由反应时的质量比可知,每65份质量的锌可置换出216份质量的银,析出金属质量增加,则溶
液总质量减少,该反应过程硫酸铜质量不变,根据以下公式:溶液中硫酸铜的质量分数
硫酸铜质量
= ×100%,得出溶液中硝酸铜的质量分数增大,故选项正确;
溶液总质量
D、m 位于ab段,此时发生的是锌和硝酸银的反应假设m 恰好和硝酸银反应,此时生成的银质
2 2
量为x
Zn+2AgNO =Zn(NO ) +2Ag
3 3 2
65 216
6.5g x
65 6.5g
=
216 x
x=21.6g,说明此时生成的滤渣含量小于21.6g,m 位于e点,此时锌已将硝酸铜和硝酸银中的
4
铜和银完全置换出来,此时和硝酸铜反应的锌质量最大为 m ﹣m =13.0g﹣6.5g=6.5g,假设
4 2
6.5g为参与反应的锌质量,设生成的铜质量为y
Zn+Cu(NO ) =Zn(NO ) +Cu
3 2 3 2
65 64
6.5g y
65 6.5g
=
64 y
y=6.4g说明此时生成的铜含量小于6.4g,则d点滤渣质量应该小于216g+64g=28g,故选项D
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
错误;
故选:D。
8. (2023•滑县校级一模)某锌的样品中含有Fe、Mg、Al、Cu等金属杂质中的2种,
6.5g该样品与足量的稀硫酸反应,可得到0.2g氢气,对该样品中含有金属杂质的组成有如下猜
测:①Mg和Al;②Mg和Fe;③Mg和Cu;④Al和Fe;⑤Al和Cu;⑥Fe和Cu。其
中合理的个数为( )
A.3个 B.4个 C.5个 D.6个
【解答】解:铜和稀硫酸不反应,锌、镁、铝、铁四种金属均能与稀硫酸生成氢气。
Zn+H SO ═ZnSO +H ↑
2 4 4 2
65 2
Mg+H SO ═MgSO +H ↑
2 4 4 2
24 2
Fe+H SO ═FeSO +H ↑
2 4 4 2
56 2
2Al+3H SO ═Al (SO ) +3H ↑
2 4 2 4 3 2
54 6
18 2
由以上质量关系可知,6.5g锌完全反应生成0.2g氢气,6.5g镁、铝、铁完全反应生成氢气质量
均大于0.2g,故杂质不可能同时含有镁、铝、铁中的两种,杂质一定是铜和镁、铝、铁中的一
种。
若是①Mg和Al;②Mg和Fe;④Al和Fe,会导致生成的氢气质量大于0.2g,以上均不合理。
猜想③Mg和Cu;⑤Al和Cu;⑥Fe和Cu,合理,则合理个数为3个。
故选:A。
9. (2023•宝鸡模拟)向5.6g铁粉中先逐滴加入一定量的Cu(NO ) 溶液,充分反应
3 2
后再逐滴加入AgNO 溶液,剩余固体质量与所加溶液总质量的关系如图所示,下列说法正确
3
的是( )
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.所加溶液质量为M g时,生成Cu的质量为m g
1 1
B.a~b段和b~c段溶液中的溶质均为Fe(NO )
3 2
C.c点对应的剩余固体中含有Fe、Cu
D.e点溶液中只含AgNO
3
【解答】解:A、所加溶液质量为M g时,m g为生成铜的质量与剩余铁的质量总和,所以生成
1 1
铜的质量不等于m g,故A错误;
1
B、a~b段,铁和硝酸铜反应生成硝酸亚铁和铜,b~c段,铁和硝酸银反应生成硝酸亚铁和银,
所以a~b段和b~c段溶液中的溶质均为Fe (NO ) ,故B正确;
3 2
C、a~b段,是铁和硝酸铜的反应,b点铁有剩余,b点固体为铁和铜,b~c段,是铁和硝酸银
的反应,且铁被完全反应,则c点含有Cu、Ag,故C错误;
D、e点溶液中溶质是过量的硝酸银、反应生成的硝酸亚铁和硝酸铜,故D错误。
故选:B。
10. (2023•任丘市模拟)分别向两份100g浓度为9.8%的稀硫酸中加入足量且等量的锌粉、
铁粉。绘制如图所示的横坐标为时间 t或横坐标为金属质量 m的图像,其中不正确的是
( )
A. B.
C. D.
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:A、由于金属过量,设生成的氢气的质量为x,则
H SO ~ H
2 4 2¿x¿
98 ¿ ¿
98 100g×9.8%
= ‘
2 x
解得x=0.2g,即两种物质均产生0.2g氢气,且由于锌比铁活泼,则锌比铁反应较快,故正确;
B、金属活动性锌>铁,锌反应比铁快,故正确;
Zn + H SO = ZnSO + H ↑
C 、 由 于 2 4 4 2 、
65 ¿98 ¿ ¿ ¿ ¿ ¿
Fe + H SO = FeSO + H ↑
2 4 4 2 ,则消耗的锌的质量比铁多,且生成氢气为0.2g,
56 ¿98 ¿ ¿ ¿ ¿ ¿
故正确;
D、由C中分析可知,相同质量的硫酸,消耗的锌的质量比铁多,故错误。
故选:D。
11. (2023•禹城市二模)向等质量的四种金属X、Y、Z、M分别加入等浓度等体积的足
量稀盐酸;再将Y投入MNO 溶液中充分反应。得到如图两个关系图,据此得出四种金属的
3
活动性强弱顺序正确的是( )
A.Z>X>M>Y B.X>Z>Y>M C.X>Z>M>Y D.Y>M>Z>X
【解答】解:由图象可知,等质量的X、Z能和稀盐酸反应,并且X和稀盐酸反应时间短,说明
X比Z活泼;Y、M不能和稀盐酸反应,说明Y、M不如X、Z活泼。Y能和MNO 反应,说明
3
Y比M活泼,因此四种金属的活动性顺序为:X>Z>Y>M。
故选:B。
12. (2023•随县模拟)金属材料广泛应用于生活和生产中。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)不法分子常用假“金元宝”(铜锌合金)蒙骗人们,下列鉴别真假元宝办法中错误的是
。
A.加盐酸B.测密度C.用火烧D.看颜色
(2)某化学兴趣小组同学在实验室将一定质量的锌粉放入盛有硝酸银、硝酸铜和硝酸镁的混合
溶液中,充分反应后过滤,得到滤渣和滤液,滤液呈无色。
①滤渣中可能含有的金属是 。
②滤液中一定含有的阳离子是 。
(3)往盛有4.0g久置的铝片的烧杯中滴加稀盐酸,让其充分反应,放出氢气的质量与所滴加稀
盐酸的质量关系如图所示。
请回答下列问题并计算:
① 刚 开 始 滴 加 稀 盐 酸 时 , 没 有 氢 气 放 出 的 原 因 是
。
②该铝片中铝的质量分数为 。
【解答】解:(1)A、放入盐酸中,铜锌合金中的锌与盐酸反应生成氢气,但金不会与盐酸反
应,所以有气体放出者为假,可以区别真伪,故正确;
B、测定密度,铜锌合金密度小于黄金,测定密度时会发现二者密度不同,密度小者为假,可以
区别真伪,故正确;
C、铜锌合金中的铜和氧气会生成黑色的氧化铜,而金不会与氧气反应,现象不同,可以区别真
伪,故正确;
D、观察颜色,由于二者的颜色基本一致,所以难于比较真假,故错误。
故选:D。
(2)①将一定质量的锌粉放入盛有硝酸银、硝酸铜和硝酸镁的混合溶液中,锌和硝酸镁不反应,
锌先和硝酸银反应生成银和硝酸锌,等硝酸银完全反应后,锌再和硝酸铜反应生成铜和硝酸锌,
充分反应后过滤,滤液呈无色,说明硝酸铜完全反应,滤渣中一定含有银和铜,可能含有锌;
②综上分析,滤液中一定含有硝酸镁和硝酸锌,含有的阳离子是Zn2+、Mg2+;
(3)①刚开始滴加稀盐酸时,没有氢气放出的原因是:铝片表面有一层致密的氧化铝薄膜,稀
盐酸先和氧化铝反应生成氯化铝和水;
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②由图示可知,充分反应后,产生氢气的质量是0.4g。
设参加反应的铝的质量为x。
2Al+6HCl═2AlCl +3H ↑
3 2
54 6
x 0.4g
54 x
= 解得:x=3.6g
6 0.4g
3.6g
该铝片中铝的质量分数为 ×100%=90%。
4.0g
答:该铝片中铝的质量分数为90%。
故答案为:(1)D;
(2)①锌;
②Zn2+、Mg2+;
(3)①铝片表面有一层致密的氧化铝薄膜,稀盐酸先和氧化铝反应生成氯化铝和水;
②90%。
13. (2023•保康县二模)金属及金属材料具有广泛的应用。
Ⅰ.纽扣电池是生活中常用的电源。纽扣电池的金属外壳可以加工得很薄,说明金属具有
性。
Ⅱ.运用手持技术探究金属与酸的反应。向250mL的烧瓶内注入25mL某浓度的稀硫酸(足量),
分别剪取相同长度和宽度、质量的镁、铝、锌、铁、铜金属片,打磨后投入烧瓶中,迅速塞紧
带有压强传感器的橡皮塞(见图1),点击采集,得到如图2所示的变化曲线。
(1)曲线b对应的金属是铁,反应的化学方程式为 。
(2)下列说法不正确的是 (填字母)。
A.曲线a对应的金属是铜。
B.曲线d对应的反应速率适中适合实验室制取气体。
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.曲线e在0~100s段几乎没有上升,可能是该金属活动性比较弱。
D.曲线c在18s左右达到最高点后又略下降的原因是反应结束,温度降低,压强下降。
E.如延长横坐标时间,曲线c、d、e最终将交于一点。
【解答】解:Ⅰ、金属的延展性是金属能压成薄片和拉成细丝,纽扣电池的金属外壳可以加工
得很薄,说明金属具有延展性;
Ⅱ、(1)曲线 b 对应的金属是铁,铁与盐酸反应生成氯化亚铁和氢气,化学方程式为:
Fe+2HCl=FeCl +H ↑;
2 2
(2)A、金属铜在金属活动顺序表中,排在氢的后面,不与盐酸反应,则曲线a对应的金属是
铜,故A正确;
B、分析曲线图可知,曲线d为锌,反应速率适中,适合实验室制取氢气,故B正确;
C、分析曲线图可知,曲线e为铝,铝在常温下,表面易生成氧化铝,氧化铝与盐酸反应没有气
体生成,则在0~100s段几乎没有上升,可能是铝表面的氧化铝打磨不彻底,故C错误;
D、镁、铝、锌、铁、铜金属活性顺序为镁>铝>锌>铁>铜,分析曲线图可知,曲线 c为镁,
镁与盐酸反应现象是迅速产生大量气泡,并放热,曲线c在18s左右达到最高点后又略微下降的
原因是镁与稀盐酸反应放热,18s左右反应结束,温度恢复为室温,压强略下降,故D正确;
E、分析曲线图可知,c为镁,d为锌,e为铝,分别剪取相同长度和宽度的镁、铝、锌金属片,
不知道镁、锌、铝的质量,无法判断生成氢气的质量,则如延长横坐标时间,曲线 c、d、e最终
不一定能交一点,故E错误。
故选:CE。
故答案为:Ⅰ、延展;
Ⅱ、(1)Fe+2HCl=FeCl +H ↑;
2 2
(2)CE。
14. (2023•新乡三模)将铁粉放入含有Al(NO ) 、Cu(NO ) 、AgNO 三种溶质的溶
3 3 3 2 3
液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
( 1 ) 若 向 滤 渣 上 滴 加 稀 盐 酸 没 有 气 泡 产 生 , 请 分 析 滤 渣 的 成 分 :
。
(2)对滤液中溶质的成分作出以下猜想:①Al(NO ) 、Fe(NO ) ;②Al(NO ) 、Fe
3 3 3 2 3 3
(NO ) 、AgNO ;③Al(NO ) 、Fe(NO ) 、Cu(NO ) ;④Al(NO ) 、Fe(NO )
3 2 3 3 3 3 2 3 2 3 3 3
、Cu(NO ) 、AgNO 。其中不合理的猜想是 (填序号),请简述理由
2 3 2 3
。
【解答】解:(1)若向滤渣上滴加稀盐酸没有气泡产生,说明滤渣中没有排在氢前面的金属,
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
即滤渣中不含有铁,则滤渣中一定含有银,可能含有铜,一定不含有铁;
(2)根据金属活动性顺序:铝>铁>氢>铜>银,铁不能与硝酸铝反应,铁会先与硝酸银反应
生成硝酸亚铁和银,待硝酸银反应完全,铁才会与硝酸铜反应生成硝酸亚铁和铜,当溶液中含
有硝酸银时,溶液中一定含有硝酸铜,故猜想②不合理;
①当硝酸银和硝酸铜反应完全,滤液中为硝酸铝和硝酸亚铁;
③当硝酸银反应完全、硝酸铜部分参加反应或没有参加反应,滤液中为硝酸铝、硝酸亚铁和硝
酸铜;
④当硝酸银部分参加反应,滤液中为硝酸铝、硝酸亚铁、硝酸铜和硝酸银。
故答案为:
(1)滤渣中一定含有银,可能含有铜,一定不含有铁
(2)②;根据金属活动性顺序:铝>铁>氢>铜>银,铁不能与硝酸铝反应,铁会先与硝酸银
反应生成硝酸亚铁和银,待硝酸银反应完全,铁才会与硝酸铜反应生成硝酸亚铁和铜,当溶液
中含有硝酸银时,溶液中一定含有硝酸铜,所以猜想②不合理。
15. (2023•红河州一模)金属材料与我们的生活息息相关。
(1)选择铸造纪念章的材料(紫铜胎镀金或银)不需要考虑的因素是 (填标号)。
A.金属的导电性
B.金属的耐腐蚀性
C.金属的价格
(2)采用相互刻画的方法,可以比较黄铜片和铜片的 不同。
(3)镁铜合金可用于储氢。在氩气的氛围中,将一定比例的金属镁和铜熔炼得到镁铜合金。熔
炼时须通入氩气,其目的是 。
(4)氧化铁粉末与铝粉在高温条件下发生置换反应,并放出大量的热,这一反应可用于焊接钢
轨 、 制 备 金 属 纳 米 复 合 材 料 等 , 该 反 应 的 化 学 方 程 式 为
高温 ,氧化铁中铁元素的化合价为 价。
e O ¯ 2Fe+Al O
2 3 ❑ 2 3
(5)向一定质量AgNO 和Cu(NO ) 的混合溶液中加入Zn,溶液质量与加入Zn的质量关系
3 3 2
如图所示,下列说法正确的是 (填标号)。
A.a~b段的溶液为蓝色
B.c点溶液中溶质为Zn(NO )
3 2
C.取b~c段溶液,滴加稀盐酸,有白色沉淀
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.取d点的固体,加入稀盐酸,有气泡产生
【解答】解:(1)选择铸造纪念章的材料(紫铜胎镀金或银)需要考虑金属的耐腐蚀性、硬度、
价格等,不需要考虑金属的导电性。
(2)黄铜片是铜的合金,合金的硬度大于成分金属,用相互刻画的方法可以比较黄铜片和铜片
的硬度。即采用相互刻画的方法,可以比较黄铜片和铜片的硬度不同。
(3)氩气化学性质稳定,为防止Mg、Cu被氧化,镁铜合金熔炼时须通入氩气。
(4)氧化铁粉末与铝粉在高温条件下发生置换反应生成铁和氧化铝,化学方程式
高温 ;
2Al+Fe O ¯ 2Fe+Al O
2 3 ❑ 2 3
氧化铁中氧元素化合价是﹣2价,根据化合价规则可求出氧化铁中铁元素的化合价为+3价。
(5)在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO 和Cu(NO ) 的混合溶液中加
3 3 2
入Zn,与两种溶质依次发生反应
Zn+2AgNO ═Zn(NO ) +2Ag,Zn+Cu(NO ) ═Zn(NO ) +Cu,
3 3 2 3 2 3 2
65 216 65
64
析出银的过程是溶液质量减少的过程;析出铜的过程是溶液质量增加的过程。
在b点时,硝酸银全部参加反应,溶液中含有硝酸铜和生成的硝酸锌;d点时锌过量,得到的固
体有银、铜和锌。
A、a~b段是锌与硝酸银反应的过程,硝酸铜没有反应,硝酸铜溶液是蓝色的,所以 a~b段的
溶液为蓝色。A正确,该选项符合题意;
B、在b点时,硝酸银全部参加反应,生成硝酸锌,c点时硝酸铜全部参加反应,生成硝酸锌。
所以c点溶液中溶质为Zn(NO ) 。B正确,该选项符合题意;
3 2
C、在b点时,硝酸银全部参加反应,b~c段是锌与硝酸铜反应的过程,b~c段溶液中没有硝酸
银,滴加稀盐酸,不会有白色沉淀产生。C不正确,该选项不符合题意;
21关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、d点的固体是银、铜和锌,加入稀盐酸,锌与稀盐酸反应生成氢气,所以取d点的固体,加
入稀盐酸,有气泡产生。D正确,该选项符合题意;
综上所述:选择ABD。
22