文档内容
2006 年全国普通高等学校招生统一考试
上海化学试卷
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对
后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原于质量: H—1 C—12 N—14 0—16 Mg—24 S.32 C1—35.5 Fe—56
一.选择题(本题共10分),每小题2分,只有一个正确选项,答案涂写在答题纸上。
1.石油是一种重要能源,人类正面临着石油短缺、油价上涨的困惑。以下解决能源问题
的方法不当的是
A.用木材作燃料 B。用液氢替代汽油 C.开发风能 D.开发地热
2.以下化学用语正确的是
A.乙烯的结构简式CH CH B.乙酸的分子式C H O
2 2 2 4 2
··
C.明矾的化学式KAlSO ·12H O D.氯化钠的电子式Na · C·
4 2 · ·
··
l
3.科学家发现C 后,近年又合成了许多球形分子(富勒烯),如C 、C 、C 、C 等它
60 50 70 120 540
们互称为
A.同系物 B.同分异构体 C.同素异形体 D.同位素
4.下列不符合当今化学研究方向的是
A.发现新物质 B.合成新材料
C.研究化学反应的微观过程 D.研究化学反应中原子守恒关系
5.下列有机物命名正确的是
A、2-乙基丙烷C H - CH -
3
CH
3
CH CH
2 3
B.CH CH CH CH OH 1-丁醇
3 2 2 2
C、 CH — —CH
3 3
间二甲苯
CH
3
CH - C =
D. 3 2—甲基—2—丙烯
CH
2
二、选择题(本题36分)每小题3分、只有一个正确选项,答案涂写在答题纸上。
6.下列含有非极性键的共价化合物是
A.HCl B.Na O C.C H D.CH
2 2 2 2 4
7.下列反应中生成物总能量高于反应物总能量的是A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
8.某非金属单质A和氧气发生化合反应生成B。B为气体,其体积是反应掉氧气体积的两
倍(同温同压)。以下对B分子组成的推测一定正确的是
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
9.二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘
醇的结构简式是HO—CH CH —O—CH CH —OH。下列有关二甘醇的叙述正确的是
2 2 2 2
A.不能发生消去反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D.符合通式C H O
n 2n 3
10.已知某溶液中存在较多的H+、SO 2-、NO -,则溶液中还可能大量存在的离子组是
4 3
A.A13+、CH COO—、C1— B.Na+、NH +、C1—
3 4
C.Mg2+、C1—、Fe2+ D. Mg2+、Ba2+、Br—
11.已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内
装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确
的是
① ② ③ ④
A 黄绿色 橙色 蓝色 白色
B 无色 橙色 紫色 白色
C 黄绿色 橙色 蓝色 无色
D 黄绿色 无色 紫色 白色
12.N 代表阿伏加德罗常数,下列说法正确的是
A
A.9gD O中含有的电子数为5N
2 A
B.1molMgCl 中含有的离子数为2N
2 A
C.1molCH 分子中共价键总数为4N
4 A
D.7.1g C1 与足量NaOH溶液反应转移的电子数为0.2N
2 A
13.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
14.下列物质能通过化合反应直接制得的是
①FeCl ②H SO ③NH NO ④HCl
2 2 4 4 3
A.只有①②③ B.只有②③
C. 只有①③④ D.全部15.在标准状况下,向100mL氢硫酸溶液中通人二氧化硫气体,
溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为
A.0.5mol/L B.0.05mol/L
C.1mol/L D.0.1mol/L
16.将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正
确的是
A.反应速率:两者相同
B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
17.根据相关化学原理,下列判断正确的是
A.若X是原子晶体,Y是分子晶体,则熔点:X A
2 2 2 2
C.若R2—和M+的电子层结构相同,则原子序数:R>M
D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA________
甲、乙的最高价氧化物水化物的酸性强弱为:________>________ (用化学式表示)。
(4)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的__________,请
写出元素在元素周期表中的位置与元素原子结构的关系:
_______________________________________________________________________________
23.(B)下表中的实线表示元素周期表的部分边界。①-⑤分别表示元素周期表中对应位置
的元素。(1)请在上表中用实线补全元素周期表边界。
(2)元素⑤的原子核外p电子数比s电子总数多_______个。
元素③氢化物的电子式为_______。
(3)元素④—般在化合物中显_____价,但与_____形成化合物时,所显示的价态则恰好相反。
(4)在元素①的单质、元素②的单质和元素①②形成的合金这三种物质中,熔点最低的是
_____。
a.元素①的单质 b.元素②的单质 c.元素①②形成的合金 d.无法判断
24.(1)请将5种物质:N O、FeSO 、Fe(NO ) 、HNO 和Fe (SO ) 分别填入下面对
2 4 3 3 3 2 4 3
应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H O
2
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
__________+ __________→
25.(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________,
K值大小与温度的关系是:温度升高,K值______________
(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H O,在850℃时发生如下反应:
2
CO(g)十H O(g) CO (g)十H (g)十Q(Q>0)
2 2 2
CO和H O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)
2
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。①表中3min—4min之间反应处于_________状态;
C 数值_________0.08 mol/L (填大于、小于或等于)。
1
②反应在4min—5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min—6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
考生注意:26题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计
分。A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
26(A)某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体 M的成分,设计
了如右图装置。倾斜A使稀硫酸(足量)与固体M
充分反应,待反应停止后,B装置增重,C装置
中溶液无变化,反应后进入量气管气体的体积为
VmL(已折算成标准状况)
由上述实验事实可知:
( 1 ) ① 固 体 M 中 一 定 有 的 物 质 是
____________(填化学式)
理由是_________________________________________________________________________
②其中一种物质的质量可以确定为___________g(用代数式表示)。
(2)B装置的名称是________。
写出B装置中反应的离子方程式_______________________________________。
(3)C装置的作用是_________________________,如果实验中没有B装置,则C装置中产生
的现象是____________________________________________________________________。
(4)稀硫酸和固体M反应后溶液中还残留淡黄色固体,该固体是_____________,要分离出该
固体,在实验操作中,除烧杯外还需要用到的玻璃仪器是_____________。
(5)通过进一步实验,测得固体M中各种成分的质量之和小于反应前铁粉和硫粉的质量
之和,产生这种现象的原因可能是_____________
a.M中有未反应的铁和硫 b.测定气体体积时水准管的水面高于量气管的水面
c.A中留有反应生成的气体 d.气体进入D装置前未用浓硫酸干燥
26 (B)
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热
至反应完全,在试管C内得到环己烯粗品。①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________。
②试管C置于冰水浴中的目的是________________________________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环
己烯在_________层(填上或下),分液后用_________ (填入编 号)
洗涤。
a.KMnO 溶液 b.稀H SO
4 2 4
c.Na CO 溶液
2 3
②再将环己烯按右图装置蒸馏,冷却水
从_________口进入。蒸馏时要加入生石灰,
目的是__________________。
③收集产品时,控制的温度应在_________左右,实验制得 的
环己烯精品质量低于理论产量,可能的原因是( )
a.蒸馏时从70℃开始收集产品 b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
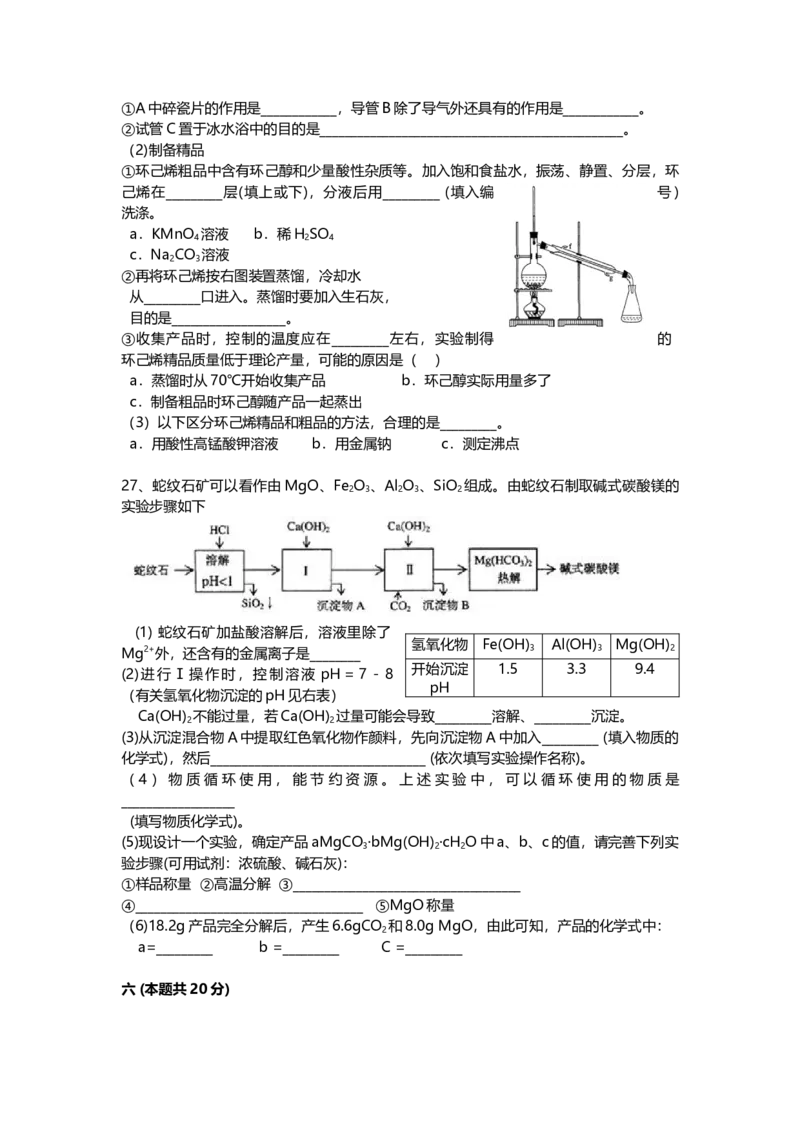
27、蛇纹石矿可以看作由MgO、Fe O 、Al O 、SiO 组成。由蛇纹石制取碱式碳酸镁的
2 3 2 3 2
实验步骤如下
(1) 蛇纹石矿加盐酸溶解后,溶液里除了
氢氧化物 Fe(OH) Al(OH) Mg(OH)
Mg2+外,还含有的金属离子是________ 3 3 2
开始沉淀 1.5 3.3 9.4
(2)进行Ⅰ操作时,控制溶液 pH=7-8
pH
(有关氢氧化物沉淀的pH见右表)
Ca(OH) 不能过量,若Ca(OH) 过量可能会导致_________溶解、_________沉淀。
2 2
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_________ (填入物质的
化学式),然后__________________________________ (依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是
__________________
(填写物质化学式)。
(5)现设计一个实验,确定产品aMgCO ·bMg(OH) ·cH O中a、b、c的值,请完善下列实
3 2 2
验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解 ③____________________________________
④____________________________________ ⑤MgO称量
(6)18.2g产品完全分解后,产生6.6gCO 和8.0g MgO,由此可知,产品的化学式中:
2
a=_________ b =_________ C =_________
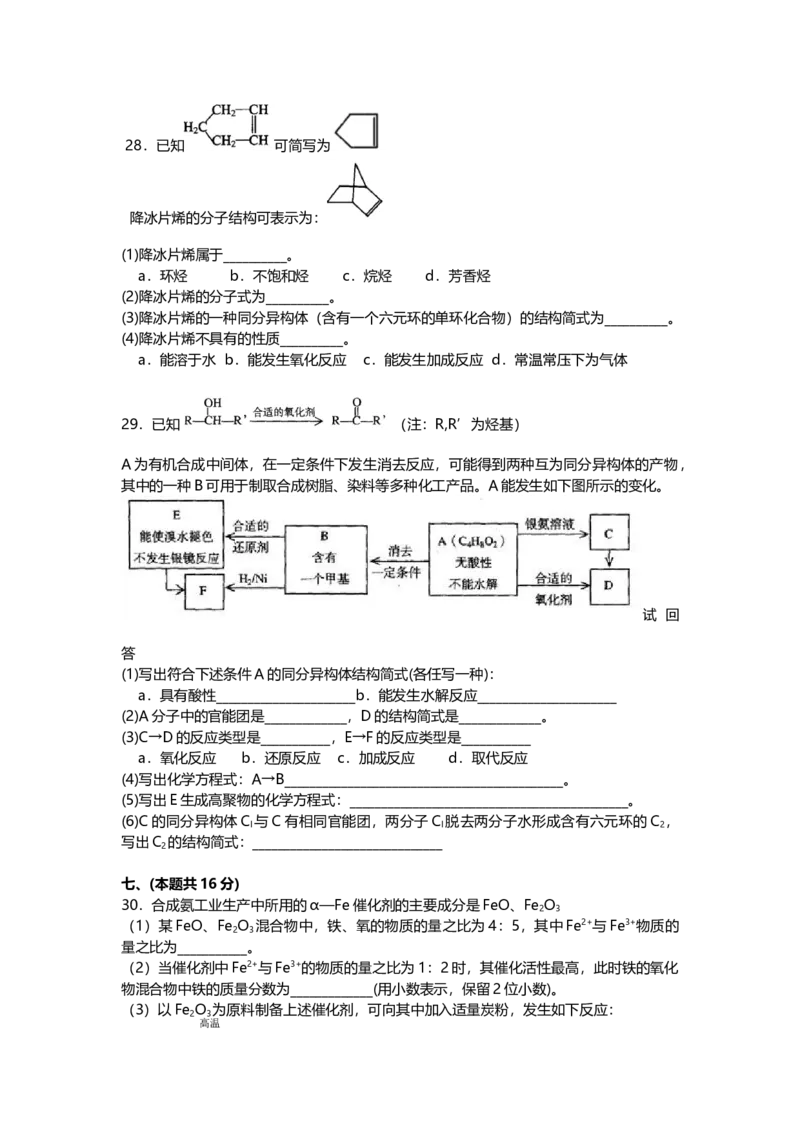
六 (本题共20分)28.已知 可简写为
降冰片烯的分子结构可表示为:
(1)降冰片烯属于__________。
a.环烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)降冰片烯的分子式为__________。
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为__________。
(4)降冰片烯不具有的性质__________。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
29.已知 (注:R,R’为烃基)
A为有机合成中间体,在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,
其中的一种B可用于制取合成树脂、染料等多种化工产品。A能发生如下图所示的变化。
试 回
答
(1)写出符合下述条件A的同分异构体结构简式(各任写一种):
a.具有酸性______________________b.能发生水解反应______________________
(2)A分子中的官能团是_____________,D的结构简式是_____________。
(3)C→D的反应类型是___________,E→F的反应类型是___________
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
(4)写出化学方程式:A→B____________________________________________。
(5)写出E生成高聚物的化学方程式:____________________________________________。
(6)C的同分异构体C 与C有相同官能团,两分子C 脱去两分子水形成含有六元环的C ,
l l 2
写出C 的结构简式:______________________________
2
七、(本题共16分)
30.合成氨工业生产中所用的α—Fe催化剂的主要成分是FeO、Fe O
2 3
(1)某FeO、Fe O 混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的
2 3
量之比为___________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,此时铁的氧化
物混合物中铁的质量分数为_____________(用小数表示,保留2位小数)。
(3)以Fe O 为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
2 3
高温2 Fe O 十C → 4FeO十CO ↑。为制得这种活性最高的催化剂,应向480g Fe O 粉末中
2 3 2 2 3
加入炭粉的质量为_________g。
一定条件下
31.已知: 4NH 十5O → 4NO+6H O
3 2 2
4NO十3O 十2H O→4HNO
2 2 3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算
(1)amolNO完全转化为HNO 需要氧气_______ mol
3
(2)为使NH 恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为________(保留2
3
位小数)。
(3)20.0moL 的NH 用空气氧化,产生混合物的组成为:NO18.0mol、O 12.0 mol、
3 2
N 150.0 mol和一定量的硝酸,以及其它成分。(高温下NO和O 不反应)
2 2
计算氨转化为NO和HNO 的转化率。
3
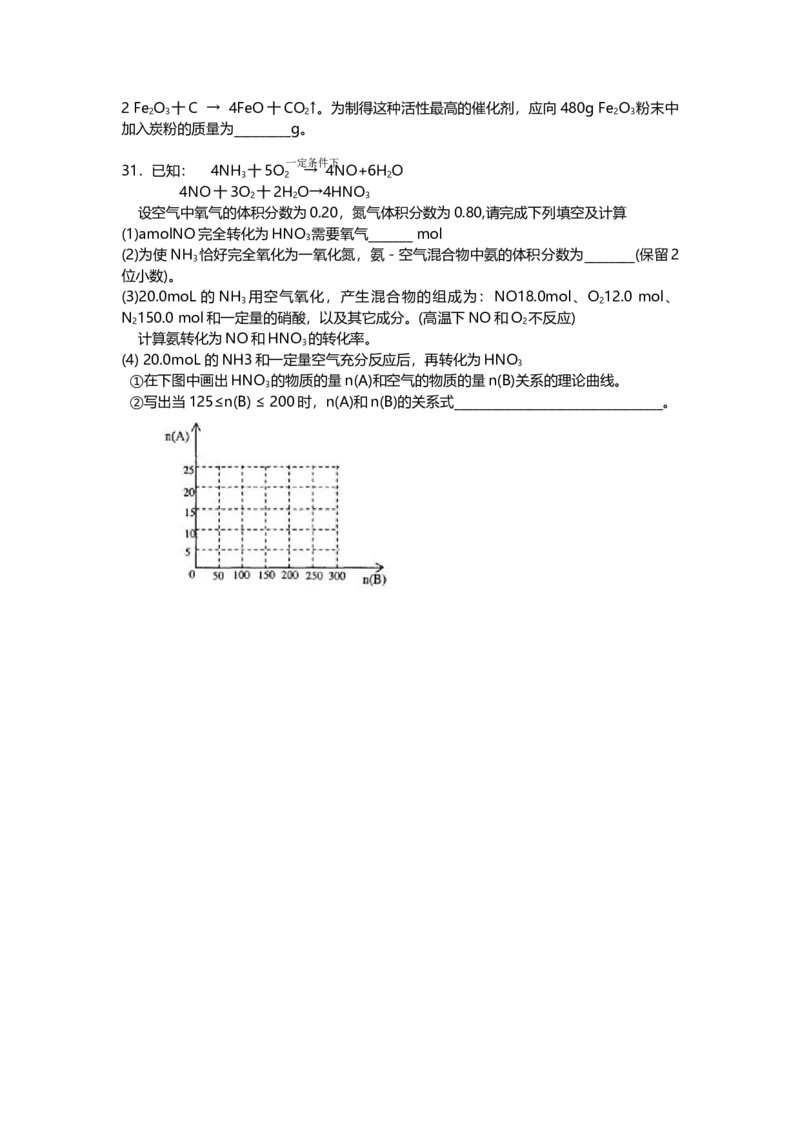
(4) 20.0moL 的NH3和一定量空气充分反应后,再转化为HNO
3
①在下图中画出HNO 的物质的量n(A)和空气的物质的量n(B)关系的理论曲线。
3
②写出当125≤n(B) ≤ 200时,n(A)和n(B)的关系式_________________________________。2006 年全国普通高等学校招生统一考试
上海化学试卷参考答案
一、选择题(本题10分),每小题2分,只有一个正确选项
(1)A (2)B (3)C (4)D (5)B
二、选择题(本题36分),每小题3分,只有一个正确选项.
(6)C (7)A (8)A (9)B (10)B (11)A (12)C (13)C (14)D
(15)D (16)B (17)D
三、选择题(本题共20分),每小题4分,每小题有一个或两个正确选项.只有一个正
确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题不给分.
(18)B (19)AC (20)BD (21)BC (22)B
四、(本题共24分)
23(A).(本题共8分)
(1)
(2分)
(2) 16 S
硫
32
3S23P4
(3)3S23P1 Al>S
(4)周期性变化 元素的周期数即为原子结构最外电子层数;元素的主族序数
即为原子结构的最外层电子数。
23(B)(2)1个 H:N:H (3)-2 氟 (4)C
24.(本题共8分)
(1) FeSO +HNO →Fe(NO ) +Fe (SO ) +N O+H O
4 3 3 3 2 4 3 2 2
(2) FeSO +5N (3)得到 4 (4)3FeSO +30HNO →
4 4 3
25.(本题共8分)
(1) 可逆反应的进行程度越大 可能增大也可能减小
(2) 0.03
(3) ① 平衡 > ②d a
五、(本题共24分)
26(A)(本题共12分)
(1)①FeS、Fe B装置增重、量气管有气体。② V/11200
(2)洗气瓶 2OH-+H S → 2H O+S2--
2 2
(3)证明 H S 已被完全吸收 黑色沉淀
2
(4)硫 漏斗、玻璃棒 (5) b、C
26(B)(1)①防暴沸 冷凝 ②防止环己烯挥发
(2)①上层 C ②g 冷却水与气体形成逆流 ③83oC b (3)C
27.(本题共12分)
(1)Fe3+ Al3+ (2)Al(OH) 、Mg(OH) (3)NaOH 过滤、洗涤、灼烧 (4)CO
3 2 2
(5)③测出CO 的质量 ④测出水蒸汽的质量 (6)3、1、3
2
六、(本题共20分)
28.(本题共9分)
(1)b (2)C H (3) -CH (4)a、d
7 10 3
29.(本题共11分)
(1)a、CH CH CH COOH b、CH CH COOCH
3 2 2 3 2 3
(2)羟基、醛基 CH COCH COOH
3 2
(3)a; b、c (4)CH CHOHCH CHO → CH CH=CHCHO+H O
3 2 3 2
(5) nCH CH=CHCH OH → [-CH-CH]
3 2 n
(6)CH CH CH
3 2
七、(本题共16分)
30.(本题共6分)
((1)2:1 (2)0.71 (3)3.6克
31.(本题共10分)
(1)0.75a mol (2)0.14(3)氨转化为NO的转化率为90%;氨转化为HNO 的转化
3率为6%
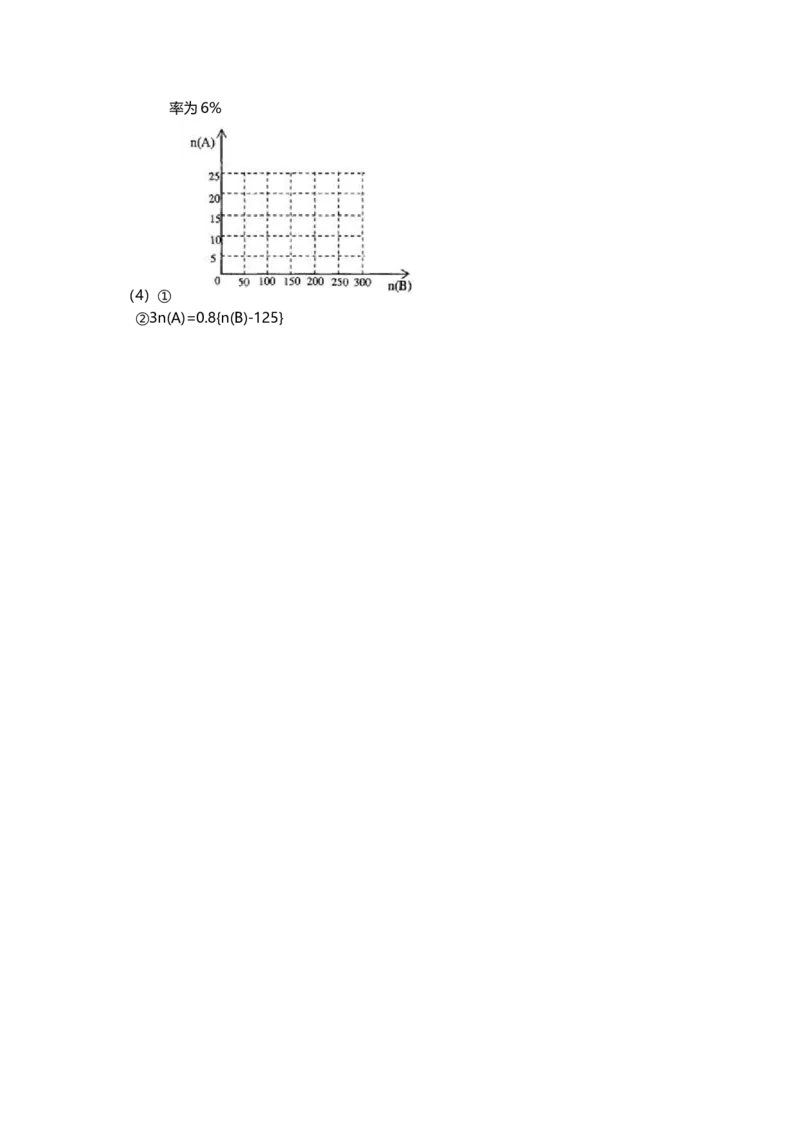
(4)①
②3n(A)=0.8{n(B)-125}