文档内容
2008年全国统一高考化学试卷(全国卷Ⅱ)
一、选择题(共8小题,每小题5分,满分40分)
1.(5分)2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列
有关丙烷的叙述中不正确的是( )
A.分子中碳原子不在一条直线上
B.光照下能够发生取代反应
C.比丁烷更易液化
D.是石油分馏的一种产品
2.(5分)实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1
~4.4、石蕊:5.0~8.0、酚酞:8.2~10.0用0.1000mol•L﹣1NaOH溶液滴定未
知浓度的CH COOH溶液,反应恰好完全时,下列叙述正确的是( )
3
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
3.(5分)对于ⅣA族元素,下列叙述中不正确的是( )
A.SiO 和CO 中,Si和O、C和O之间都是共价键
2 2
B.Si、C、Ge的最外层电子数都是4,次外层电子数都是8
C.SiO 和CO 中都是酸性氧化物,在一定条件下都能和氧化钙反应
2 2
D.该族元素的主要化合价是+4和+2
4.(5分)物质的量浓度相同的NaOH和HCl溶液以3:2体积比相混合,所
得溶液的pH=12.则原溶液的物质的量浓度为( )
A.0.01 mol•L﹣1 B.0.017 mol•L﹣1
C.0.05 mol•L﹣1 D.0.50 mol•L﹣1
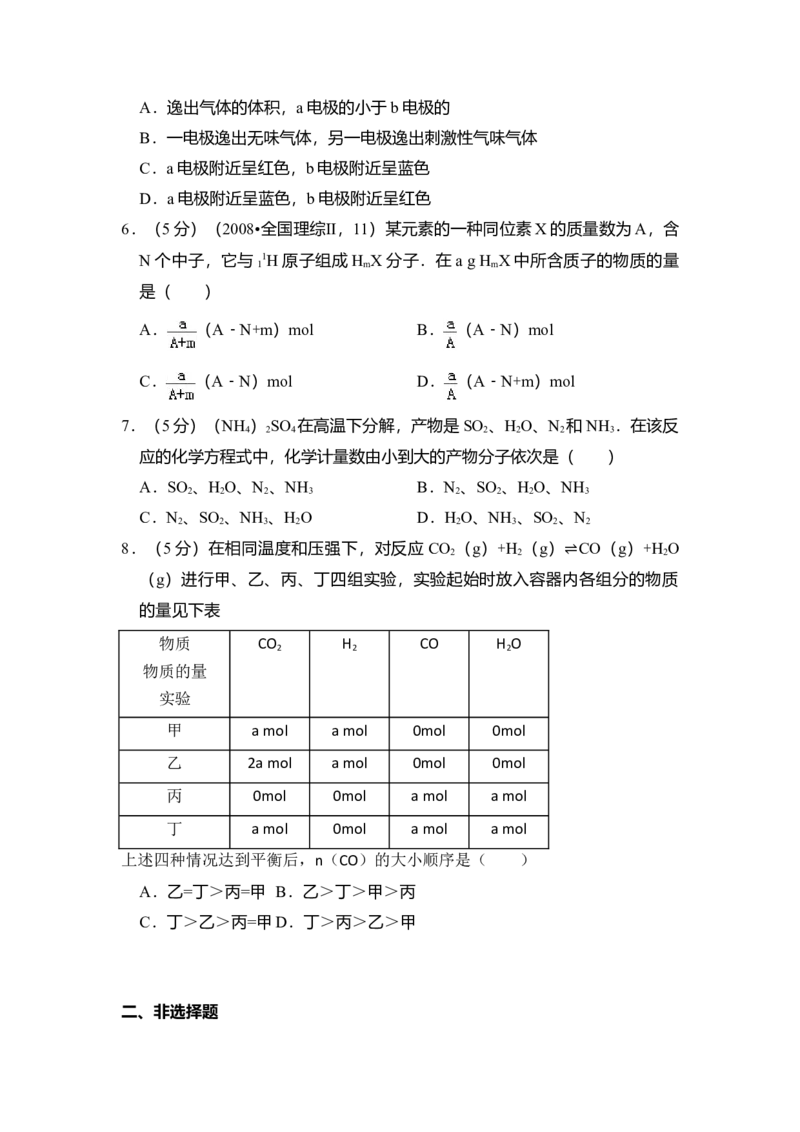
5.(5分)如图为直流电源电解稀Na SO 水溶液的装置.通电后在石墨电极a
2 4
和b附近分别滴加几滴石蕊溶液.下列实验现象中正确的是( )A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
6.(5分)(2008•全国理综Ⅱ,11)某元素的一种同位素X的质量数为A,含
N个中子,它与 1H原子组成H X分子.在a g H X中所含质子的物质的量
1 m m
是( )
A. (A﹣N+m)mol B. (A﹣N)mol
C. (A﹣N)mol D. (A﹣N+m)mol
7.(5分)(NH ) SO 在高温下分解,产物是SO 、H O、N 和NH .在该反
4 2 4 2 2 2 3
应的化学方程式中,化学计量数由小到大的产物分子依次是( )
A.SO 、H O、N 、NH B.N 、SO 、H O、NH
2 2 2 3 2 2 2 3
C.N 、SO 、NH 、H O D.H O、NH 、SO 、N
2 2 3 2 2 3 2 2
8.(5分)在相同温度和压强下,对反应 CO (g)+H (g) CO(g)+H O
2 2 2
(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质
⇌
的量见下表
物质 CO H CO H O
2 2 2
物质的量
实验
甲 a mol a mol 0mol 0mol
乙 2a mol a mol 0mol 0mol
丙 0mol 0mol a mol a mol
丁 a mol 0mol a mol a mol
上述四种情况达到平衡后,n(CO)的大小顺序是( )
A.乙=丁>丙=甲 B.乙>丁>甲>丙
C.丁>乙>丙=甲D.丁>丙>乙>甲
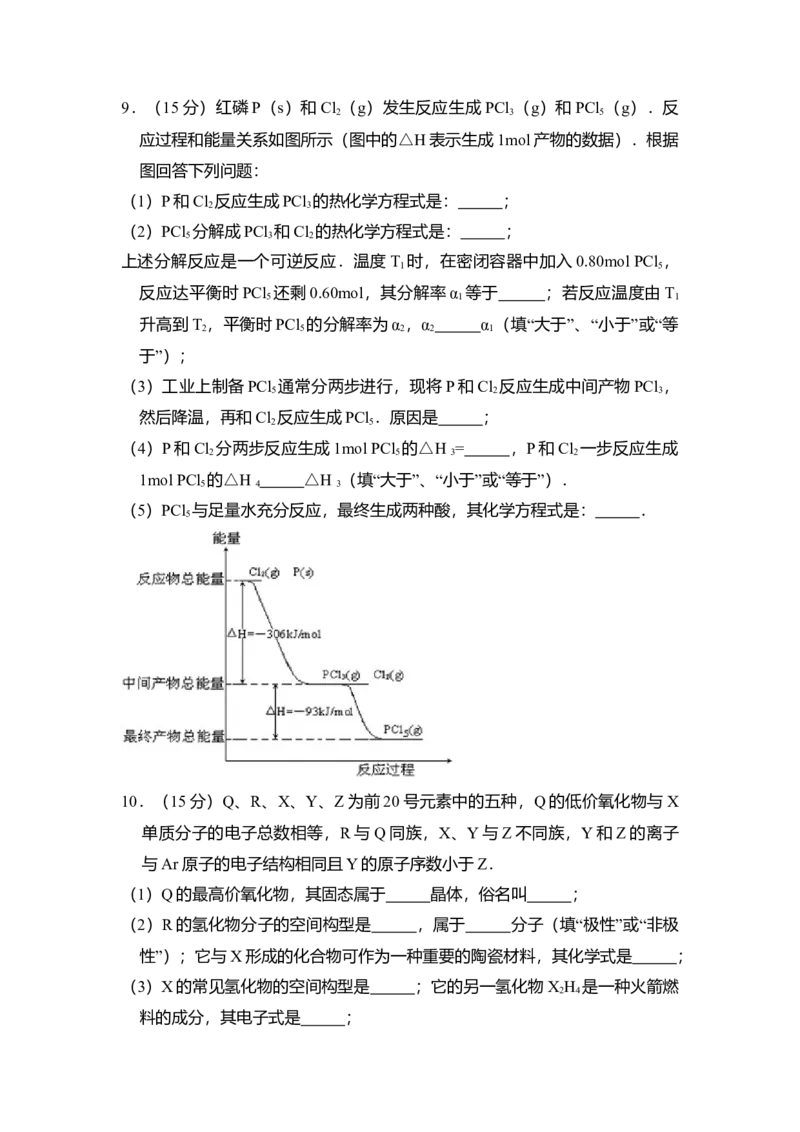
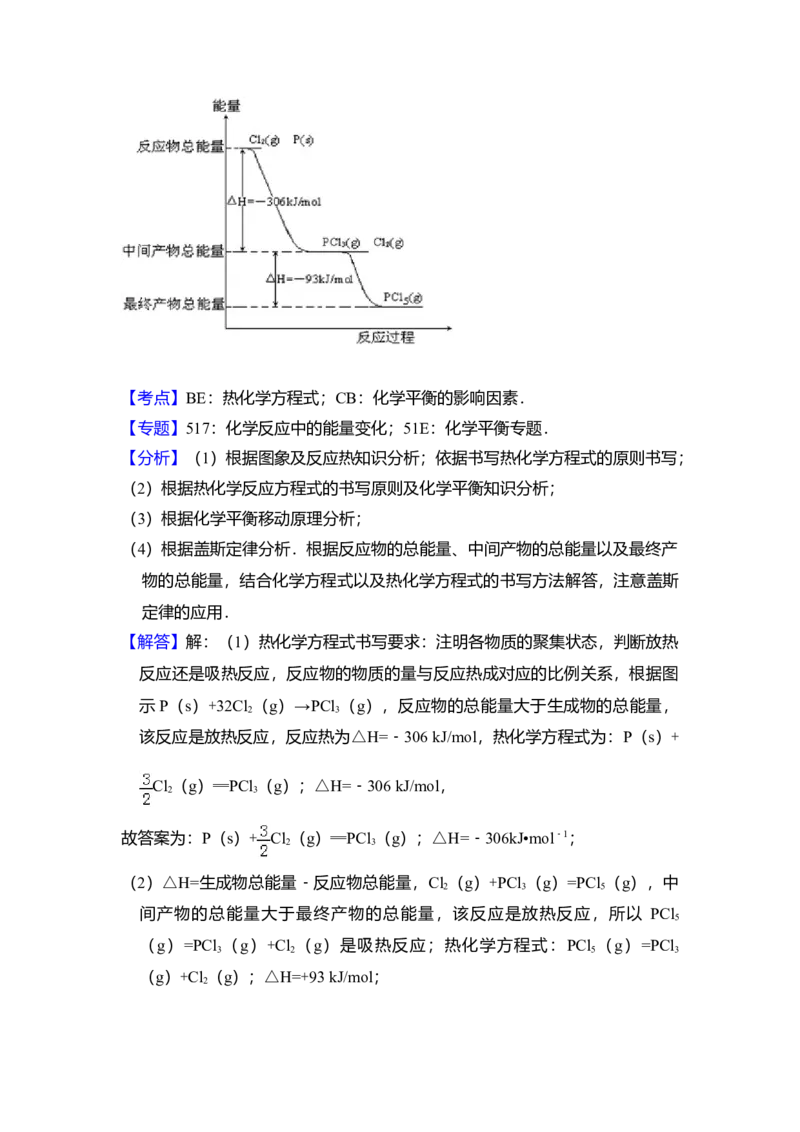
二、非选择题9.(15分)红磷P(s)和Cl (g)发生反应生成PCl (g)和PCl (g).反
2 3 5
应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据
图回答下列问题:
(1)P和Cl 反应生成PCl 的热化学方程式是: ;
2 3
(2)PCl 分解成PCl 和Cl 的热化学方程式是: ;
5 3 2
上述分解反应是一个可逆反应.温度 T 时,在密闭容器中加入0.80mol PCl ,
1 5
反应达平衡时PCl 还剩0.60mol,其分解率α 等于 ;若反应温度由T
5 1 1
升高到T ,平衡时PCl 的分解率为α ,α α (填“大于”、“小于”或“等
2 5 2 2 1
于”);
(3)工业上制备PCl 通常分两步进行,现将P和Cl 反应生成中间产物PCl ,
5 2 3
然后降温,再和Cl 反应生成PCl .原因是 ;
2 5
(4)P和Cl 分两步反应生成1mol PCl 的△H = ,P和Cl 一步反应生成
2 5 3 2
1mol PCl 的△H △H (填“大于”、“小于”或“等于”).
5 4 3
(5)PCl 与足量水充分反应,最终生成两种酸,其化学方程式是: .
5
10.(15分)Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X
单质分子的电子总数相等,R与Q同族,X、Y与Z不同族,Y和Z的离子
与Ar原子的电子结构相同且Y的原子序数小于Z.
(1)Q的最高价氧化物,其固态属于 晶体,俗名叫 ;
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极
性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是 ;
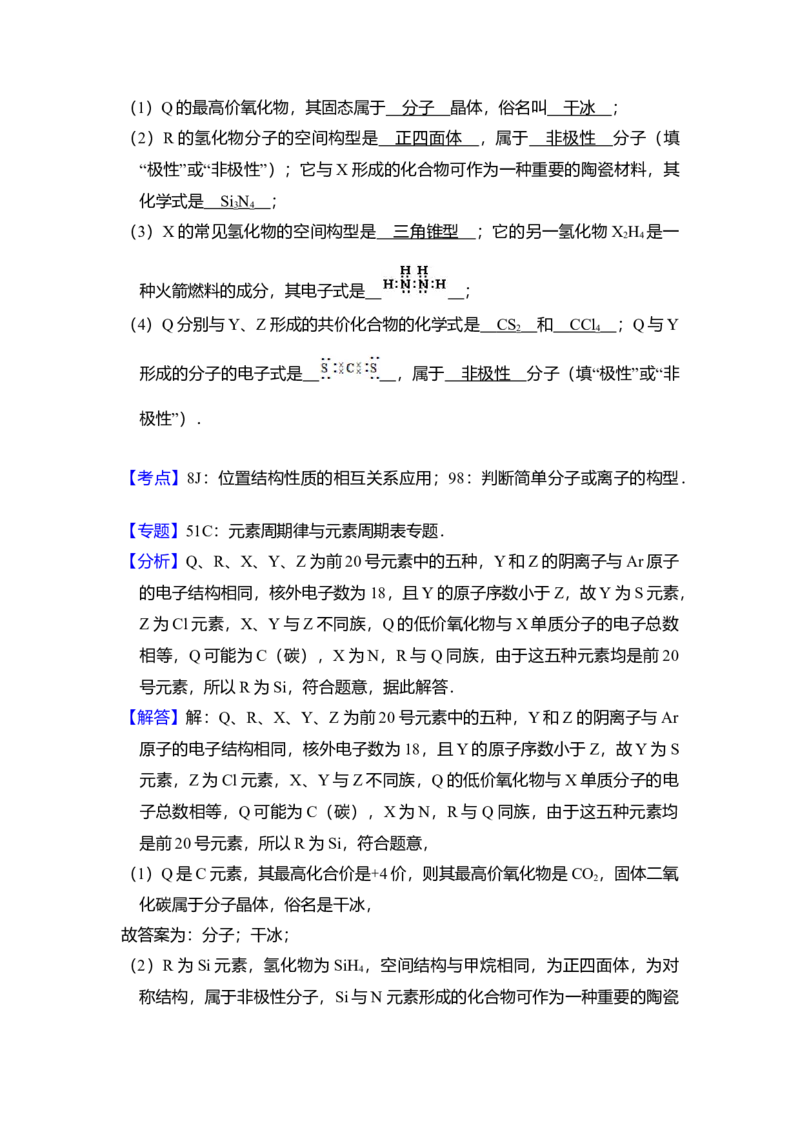
(3)X的常见氢化物的空间构型是 ;它的另一氢化物X H 是一种火箭燃
2 4
料的成分,其电子式是 ;(4)Q分别与Y、Z形成的共价化合物的化学式是 和 ;Q与Y形
成的分子的电子式是 ,属于 分子(填“极性”或“非极性”).
11.(13分)某钠盐溶液可能含有阴离子NO ﹣、CO 2﹣、SO 2﹣、SO 2﹣、Cl﹣、
3 3 3 4
Br﹣、I﹣.为了鉴别这些离子,分别取少量溶液进行以下实验:
①所得溶液呈碱性;
②加HCl后,生成无色无味的气体.该气体能使饱和石灰水变浑浊.
③加CCl ,滴加少量氯水,振荡后,CCl 层未变色.
4 4
④加BaCl 溶液产生白色沉淀,分离,在沉淀中加入足量的盐酸,沉淀不能完
2
全溶解.
⑤加HNO 酸化后,再加过量的AgNO ,溶液中析出白色沉淀.
3 3
(1)分析上述5个实验,写出每一实验鉴定离子的结论与理由.
实验① .
实验② .
实验③ .
实验④ .
实验⑤ .
(2)上述5个实验不能确定是否的离子是 .
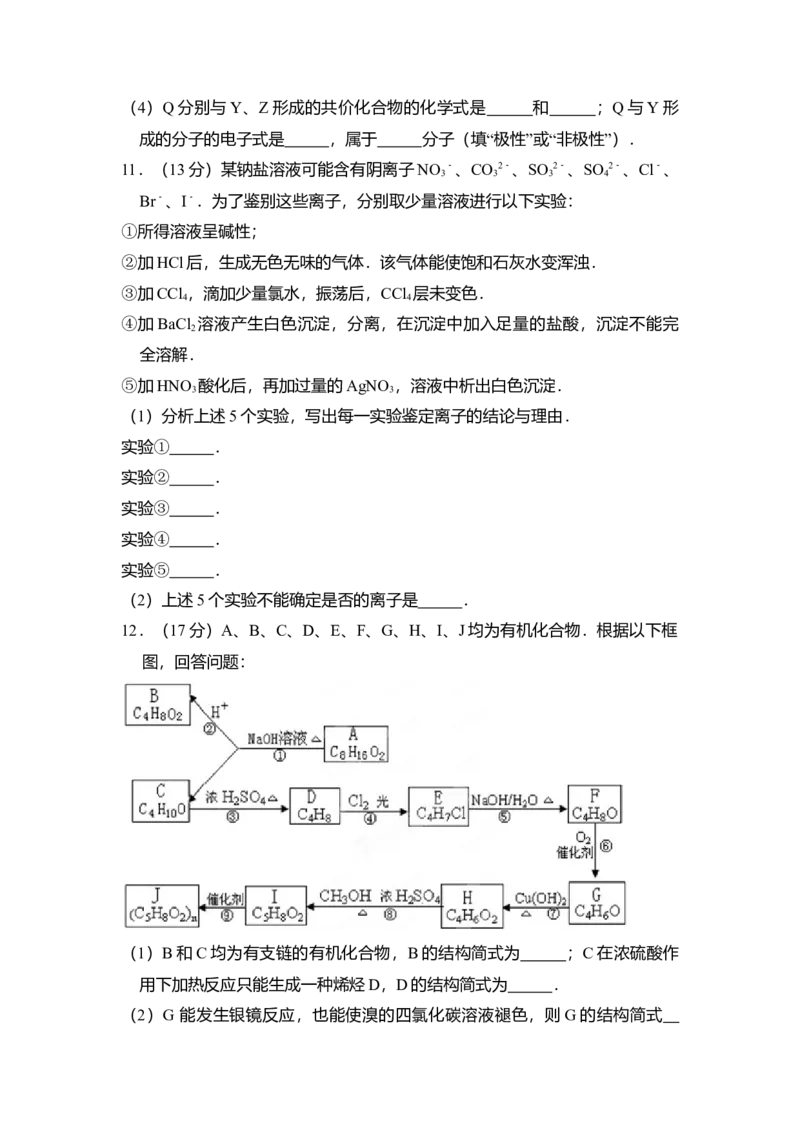
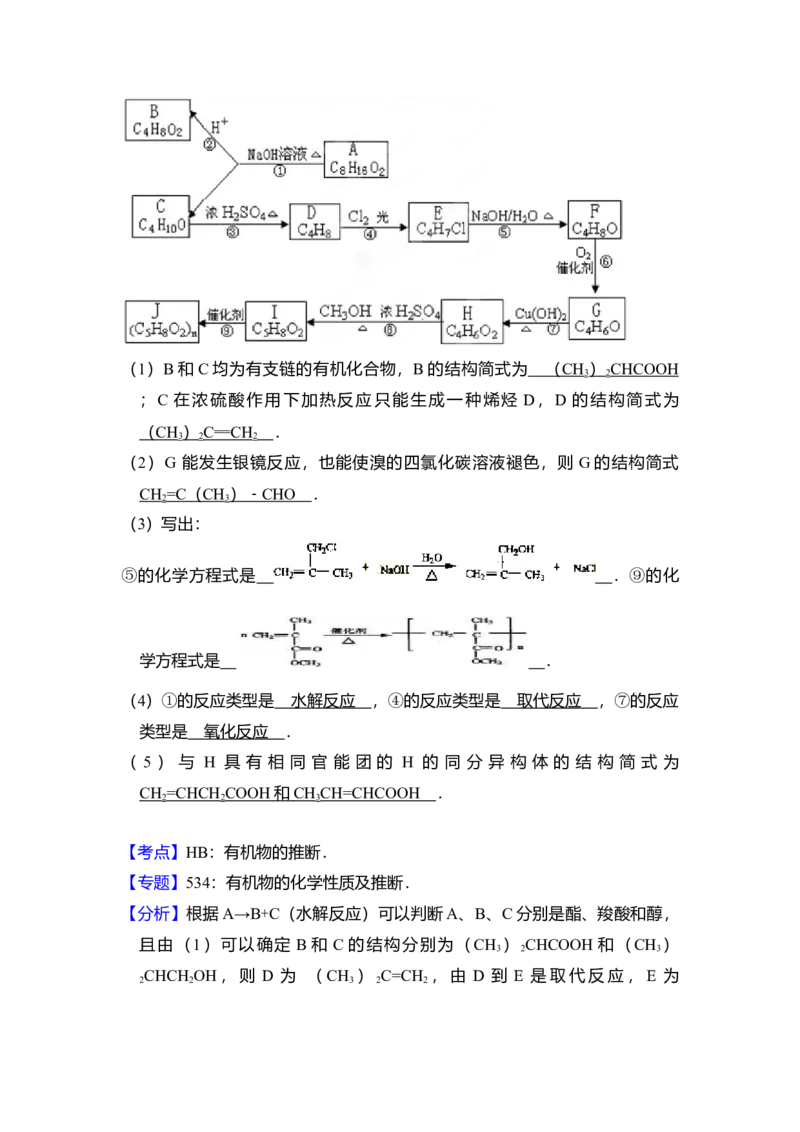
12.(17分)A、B、C、D、E、F、G、H、I、J均为有机化合物.根据以下框
图,回答问题:
(1)B和C均为有支链的有机化合物,B的结构简式为 ;C在浓硫酸作
用下加热反应只能生成一种烯烃D,D的结构简式为 .
(2)G 能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式.
(3)写出:
⑤的化学方程式是 .⑨的化学方程式是 .
(4)①的反应类型是 ,④的反应类型是 ,⑦的反应类型是 .
(5)与H具有相同官能团的H的同分异构体的结构简式为 .2008 年全国统一高考化学试卷(全国卷Ⅱ)
参考答案与试题解析
一、选择题(共8小题,每小题5分,满分40分)
1.(5分)2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列
有关丙烷的叙述中不正确的是( )
A.分子中碳原子不在一条直线上
B.光照下能够发生取代反应
C.比丁烷更易液化
D.是石油分馏的一种产品
【考点】I3:烷烃及其命名.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
【分析】A、烷烃分子中有多个碳原子应呈锯齿形,丙烷呈角形;
B、丙烷等烷烃在光照的条件下可以和氯气发生取代反应;
C、烷烃中碳个数越多沸点越高;
D、属于石油分馏的产物,是液化石油气的成分之一.
【解答】解:A、烷烃分子中有多个碳原子应呈锯齿形,丙烷呈角形,碳原子
不在一条直线上,故A正确;
B、丙烷等烷烃在光照的条件下可以和氯气发生取代反应,故B正确;
C、烷烃中碳个数越多沸点越高,丙烷分子中碳原子数小于丁烷,故丁烷沸点
高,更易液化,故C错误;
D、丙烷属于石油分馏的产物,是液化石油气的成分之一,故D正确。
故选:C。
【点评】本题主要考查烷的结构与性质等,难度较小,注意基础知识的积累掌
握.
2.(5分)实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1
~4.4、石蕊:5.0~8.0、酚酞:8.2~10.0用0.1000mol•L﹣1NaOH溶液滴定未知浓度的CH COOH溶液,反应恰好完全时,下列叙述正确的是( )
3
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
【考点】R3:中和滴定.
菁优网版权所有
【专题】542:化学实验基本操作.
【分析】根据盐类的水解考虑溶液的酸碱性,然后根据指示剂的变色范围与酸
碱中和后的越接近越好,且变色明显(终点变为红色),溶液颜色的变化由
浅到深容易观察,而由深变浅则不易观察.
【解答】解:A、NaOH 溶液滴和 CH COOH 溶液反应恰好完全时,生成了
3
CH COONa,CH COONa水解溶液呈碱性,应选择碱性范围内变色的指示剂,
3 3
即酚酞,故A错误;
B、NaOH 溶液滴和 CH COOH 溶液反应恰好完全时,生成了 CH COONa,
3 3
CH COONa水解溶液呈碱性,应选择碱性范围内变色的指示剂,即酚酞,故
3
B错误;
C、NaOH 溶液滴和 CH COOH 溶液反应恰好完全时,生成了 CH COONa,
3 3
CH COONa水解溶液呈碱性,应选择碱性范围内变色的指示剂,即酚酞,故
3
C错误;
D、NaOH 溶液滴和 CH COOH 溶液反应恰好完全时,生成了 CH COONa,
3 3
CH COONa水解溶液呈碱性,应选择碱性范围内变色的指示剂,即酚酞,故
3
D正确;
故选:D。
【点评】本题主要考查了指示剂的选择方法,只要掌握方法即可完成本题,注
意滴定终点与反应终点尽量接近.
3.(5分)对于ⅣA族元素,下列叙述中不正确的是( )
A.SiO 和CO 中,Si和O、C和O之间都是共价键
2 2
B.Si、C、Ge的最外层电子数都是4,次外层电子数都是8C.SiO 和CO 中都是酸性氧化物,在一定条件下都能和氧化钙反应
2 2
D.该族元素的主要化合价是+4和+2
【考点】74:同一主族内元素性质递变规律与原子结构的关系;FG:碳族元素
简介;FH:硅和二氧化硅.
菁优网版权所有
【专题】525:碳族元素.
【分析】A、根据非金属元素间形成的是共价键;
B、根据各原子的结构示意图可判断;
C、根据酸性氧化物的通性,
D、根据碳族元素的最外层电子数判断,
【解答】解:A、共价化合物中非金属元素之间以共价键结合,故A正确;
B、最外层都是4没错,但是C次外层不是8,故B错误;
C、酸性氧化物和碱性氧化物一定条件可以反应,故C正确;
D、碳族元素的最外层电子数为 4,所以最高正价为+4价,当然也能形成+2价,
故D正确;
故选:B。
【点评】同一主族,从上到下,元素的最外层电子数相同,性质相似,具有递
变性.
4.(5分)物质的量浓度相同的NaOH和HCl溶液以3:2体积比相混合,所
得溶液的pH=12.则原溶液的物质的量浓度为( )
A.0.01 mol•L﹣1 B.0.017 mol•L﹣1
C.0.05 mol•L﹣1 D.0.50 mol•L﹣1
【考点】5C:物质的量浓度的相关计算.
菁优网版权所有
【专题】51G:电离平衡与溶液的pH专题.
【分析】酸碱混合后,pH=12,则碱过量,剩余的c(OH﹣)=0.01mol/L,以此
来计算.
【解答】解:设NaOH和HCl的物质的量浓度均为x,NaOH和HCl溶液以3:
2体积比相混合,体积分别为3V、2V,
酸碱混合后,pH=12,则碱过量,剩余的c(OH﹣)=0.01mol/L,则 =0.01mol/L,
解得x=0.05mol/L,
故选:C。
【点评】本题考查酸碱混合的计算,明确混合后pH=12为碱过量是解答本题的
关键,并注意pH与浓度的换算来解答,题目难度不大.
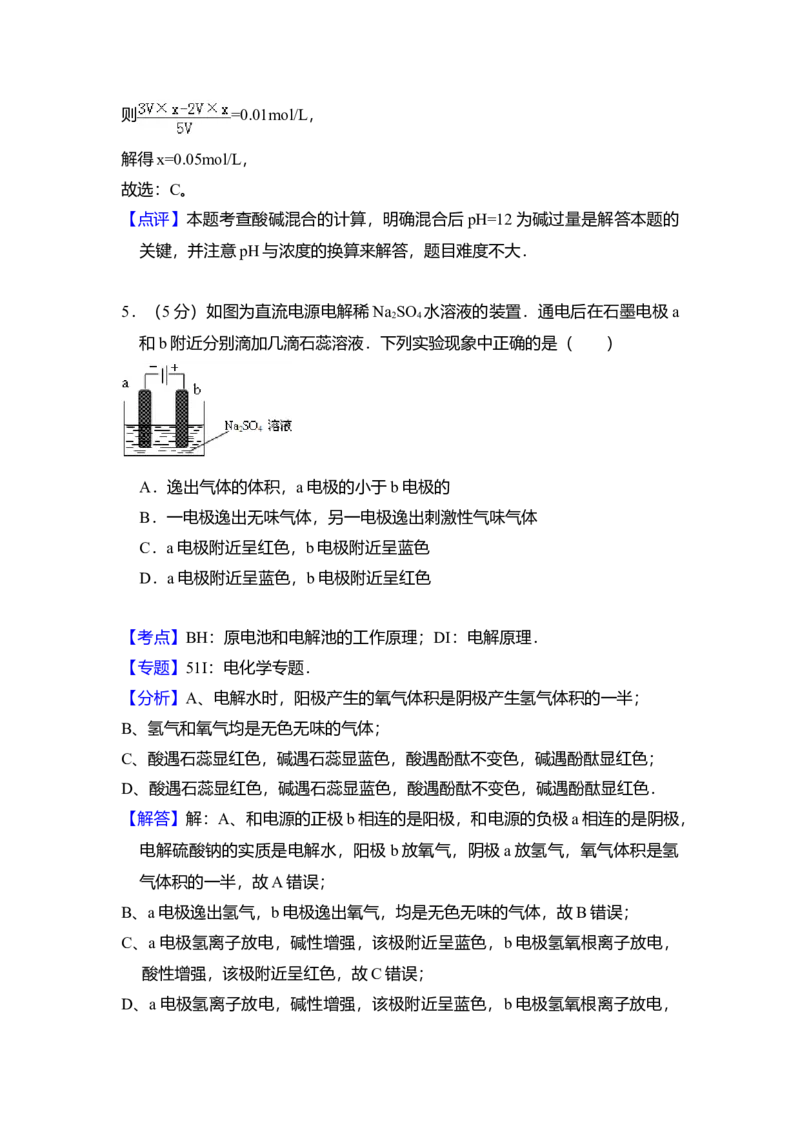
5.(5分)如图为直流电源电解稀Na SO 水溶液的装置.通电后在石墨电极a
2 4
和b附近分别滴加几滴石蕊溶液.下列实验现象中正确的是( )
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
【考点】BH:原电池和电解池的工作原理;DI:电解原理.
菁优网版权所有
【专题】51I:电化学专题.
【分析】A、电解水时,阳极产生的氧气体积是阴极产生氢气体积的一半;
B、氢气和氧气均是无色无味的气体;
C、酸遇石蕊显红色,碱遇石蕊显蓝色,酸遇酚酞不变色,碱遇酚酞显红色;
D、酸遇石蕊显红色,碱遇石蕊显蓝色,酸遇酚酞不变色,碱遇酚酞显红色.
【解答】解:A、和电源的正极b相连的是阳极,和电源的负极a相连的是阴极,
电解硫酸钠的实质是电解水,阳极b放氧气,阴极a放氢气,氧气体积是氢
气体积的一半,故A错误;
B、a电极逸出氢气,b电极逸出氧气,均是无色无味的气体,故B错误;
C、a电极氢离子放电,碱性增强,该极附近呈蓝色,b电极氢氧根离子放电,
酸性增强,该极附近呈红色,故C错误;
D、a电极氢离子放电,碱性增强,该极附近呈蓝色,b电极氢氧根离子放电,酸性增强,该极附近呈红色,故D正确。
故选:D。
【点评】本题考查学生电解池的工作原理,要求学生熟记教材知识,并会灵活
运用.
6.(5分)(2008•全国理综Ⅱ,11)某元素的一种同位素X的质量数为A,含
N个中子,它与 1H原子组成H X分子.在a g H X中所含质子的物质的量
1 m m
是( )
A. (A﹣N+m)mol B. (A﹣N)mol
C. (A﹣N)mol D. (A﹣N+m)mol
【考点】33:同位素及其应用;54:物质的量的相关计算;85:质量数与质子
数、中子数之间的相互关系.
菁优网版权所有
【专题】16:压轴题;51B:原子组成与结构专题.
【分析】根据公式:分子中质子的物质的量=分子的物质的量×一个分子中含有
的质子数= ×一个分子中含有的质子数来计算.
【解答】解:同位素X的质量数为A,中子数为N,因此其质子数为A﹣N.故
H X分子中的质子数为m+A﹣N,又由于H X中H为 1H,故agH X分子中
m m 1 m
所含质子的物质的量为:
×(A+m﹣N)mol。
故选:A。
【点评】本题考查学生教材中的基本公式和质量数、质子数、中子数之间的关
系知识,可以根据所学知识进行回答,较简单.
7.(5分)(NH ) SO 在高温下分解,产物是SO 、H O、N 和NH .在该反
4 2 4 2 2 2 3
应的化学方程式中,化学计量数由小到大的产物分子依次是( )
A.SO 、H O、N 、NH B.N 、SO 、H O、NH
2 2 2 3 2 2 2 3C.N 、SO 、NH 、H O D.H O、NH 、SO 、N
2 2 3 2 2 3 2 2
【考点】B1:氧化还原反应.
菁优网版权所有
【专题】515:氧化还原反应专题.
【分析】方法一:(NH ) SO ═NH +N +SO +H O,反应中:N:﹣3→0,化
4 2 4 3 2 2 2
合价变化总数为6,S:+6→+4,化合价变化数为2,根据化合价升高和降低
的总数相等,所以应在SO 前配3,N 前配1,根据原子守恒(NH ) SO 前
2 2 4 2 4
面配3,NH 前面配4,H O前面配6,最后计算反应前后的O原子个数相等.
3 2
方法二:利用待定系数法,令(NH ) SO 系数为1,根据原子守恒,依次配平
4 2 4
SO 前配1,H O前面配2,NH 前面配 ,N 前配 ,然后各物质系数同时
2 2 3 2
扩大3倍.
【解答】解:方法一:对于(NH ) SO →NH +N +SO +H O,反应中:N:﹣
4 2 4 3 2 2 2
3→0,化合价变化总数为6,S:+6→+4,化合价变化数为2,根据化合价升
高和降低的总数相等,最小公倍数为 6,所以应在SO 前配3,N 前配1,根
2 2
据硫原子守恒(NH ) SO 前面配3,根据氮原子守恒NH 前面配4,根据氢
4 2 4 3
原子守恒H O前面配6,最后计算反应前后的O原子个数相等。配平后的化
2
学方程式为:3(NH ) SO 4NH ↑+N ↑+3SO ↑+6H O。
4 2 4 3 2 2 2
方法二:利用待定系数法,令(NH ) SO 系数为1,根据硫原子原子守恒SO
4 2 4 2
前配1,根据氧原子守恒H O前面配2,根据氢原子守恒NH 前面配 ,根据
2 3
氮原子守恒N 前配 ,然后各物质系数同时扩大3倍,3(NH ) SO
2 4 2 4
4NH ↑+N ↑+3SO ↑+6H O。
3 2 2 2
故选:C。
【点评】此题实际上是考查化学方程式的配平,难度中等,根据化合价升降、
原子守恒配平方程式是关键,分解反应中利用待定系数法结合原子守恒配平
比较简单.掌握常见的配平方法.8.(5分)在相同温度和压强下,对反应 CO (g)+H (g) CO(g)+H O
2 2 2
(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质
⇌
的量见下表
物质 CO H CO H O
2 2 2
物质的量
实验
甲 a mol a mol 0mol 0mol
乙 2a mol a mol 0mol 0mol
丙 0mol 0mol a mol a mol
丁 a mol 0mol a mol a mol
上述四种情况达到平衡后,n(CO)的大小顺序是( )
A.乙=丁>丙=甲 B.乙>丁>甲>丙C.丁>乙>丙=甲D.丁>丙>乙>
甲
【考点】CB:化学平衡的影响因素.
菁优网版权所有
【专题】51E:化学平衡专题.
【分析】在相同温度和压强下的可逆反应,反应后气体体积不变,按方程式的
化学计量关系转化为方程式同一边的物质进行分析.
【解答】解:假设丙、丁中的CO、H O(g)全部转化为CO 、H ,再与甲、
2 2 2
乙比较:
CO (g)+H (g) CO(g)+H O(g)
2 2 2
丙开始时 0mol 0mol anol anol
⇌
丙假设全转化 anol anol 0mol 0mol
丁开始时 amol 0mol amol amol
丁假设全转化 2amol amol 0mol 0mol
通过比较,甲、丙的数值一样,乙、丁的数值一样,且乙、丁的数值大于甲、
丙的数值。
故选:A。
【点评】本题考查了化学平衡的分析应用,采用极端假设法是解决本题的关键,
本题还涉及等效平衡,等效平衡是一种解决问题的模型,对复杂的对比问题若设置出等效平衡模型,然后改变条件平衡移动,问题就迎刃而解,题目难
度中等.
二、非选择题
9.(15分)红磷P(s)和Cl (g)发生反应生成PCl (g)和PCl (g).反
2 3 5
应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据
图回答下列问题:
(1)P 和 Cl 反应生成 PCl 的热化学方程式是: P ( s ) + Cl ( g ) ═ PCl
2 3 2 3
( g ); △ H=﹣306kJ•mol ﹣1 ;
(2)PCl 分解成 PCl 和 Cl 的热化学方程式是: PCl ( g ) =PCl ( g ) + Cl
5 3 2 5 3 2
( g ); △ H= + 93 kJ/mol ;
上述分解反应是一个可逆反应.温度 T 时,在密闭容器中加入0.80mol PCl ,
1 5
反应达平衡时PCl 还剩0.60mol,其分解率α 等于 25% ;若反应温度由
5 1
T 升高到T ,平衡时PCl 的分解率为α ,α 大于 α (填“大于”、“小于”
1 2 5 2 2 1
或“等于”);
(3)工业上制备PCl 通常分两步进行,现将P和Cl 反应生成中间产物PCl ,
5 2 3
然后降温,再和Cl 反应生成PCl .原因是 两步反应均为放热反应,降低
2 5
温度有利于提高产率,防止产物分解 ;
(4)P和Cl 分两步反应生成1mol PCl 的△H = ﹣ 399kJ•mol ﹣1 ,P和Cl 一
2 5 3 2
步反应生成1mol PCl 的△H 等于 △H (填“大于”、“小于”或“等于”).
5 4 3
(5)PCl 与足量水充分反应,最终生成两种酸,其化学方程式是:
5
PCl + 4H O=H PO + 5HC l .
5 2 3 4【考点】BE:热化学方程式;CB:化学平衡的影响因素.
菁优网版权所有
【专题】517:化学反应中的能量变化;51E:化学平衡专题.
【分析】(1)根据图象及反应热知识分析;依据书写热化学方程式的原则书写;
(2)根据热化学反应方程式的书写原则及化学平衡知识分析;
(3)根据化学平衡移动原理分析;
(4)根据盖斯定律分析.根据反应物的总能量、中间产物的总能量以及最终产
物的总能量,结合化学方程式以及热化学方程式的书写方法解答,注意盖斯
定律的应用.
【解答】解:(1)热化学方程式书写要求:注明各物质的聚集状态,判断放热
反应还是吸热反应,反应物的物质的量与反应热成对应的比例关系,根据图
示P(s)+32Cl (g)→PCl (g),反应物的总能量大于生成物的总能量,
2 3
该反应是放热反应,反应热为△H=﹣306 kJ/mol,热化学方程式为:P(s)+
Cl (g)═PCl (g);△H=﹣306 kJ/mol,
2 3
故答案为:P(s)+ Cl (g)═PCl (g);△H=﹣306kJ•mol﹣1;
2 3
(2)△H=生成物总能量﹣反应物总能量,Cl (g)+PCl (g)=PCl (g),中
2 3 5
间产物的总能量大于最终产物的总能量,该反应是放热反应,所以 PCl
5
(g)=PCl (g)+Cl (g)是吸热反应;热化学方程式:PCl (g)=PCl
3 2 5 3
(g)+Cl (g);△H=+93 kJ/mol;
2PCl 分解率α = ×100%=25%.PCl (g)=PCl (g)+Cl (g)是
5 1 5 3 2
吸热反应;升高温度向吸热反应方向移动,正反应(分解反应是吸热反应)
是吸热反应,升高温度向正反应方向移动,转化率增大,α >α ;
2 1
故答案为:PCl (g)═PCl (g)+Cl (g);△H=+93kJ•mol﹣1;25%; 大于;
5 3 2
(3)Cl (g)+PCl (g)=PCl (g),是放热反应,降温平衡向放热反应方向
2 3 5
移动,降温有利于PCl (g)的生成,
5
故答案为:两步反应均为放热反应,降低温度有利于提高产率,防止产物分解;
(4)根据盖斯定律,P和Cl 分两步反应和一步反应生成 PCl 的△H应该是相
2 5
等的,P和Cl 分两步反应生成1 molPCl 的热化学方程式:
2 5
P(s)+32Cl (g)=PCl (g);△H =﹣306 kJ/mol,
2 3 1
Cl (g)+PCl (g)=PCl (g);△H =﹣93 kJ/mol;
2 3 5 2
P 和 Cl 一步反应生成 1molPCl 的△H =﹣306 kJ/mol+(﹣93 kJ/mol)=﹣399
2 5 3
kJ/mol,
由图象可知,P 和 Cl 分两步反应生成 1molPCl 的△H =﹣306kJ/mol﹣
2 5 3
(+93kJ/mol)=399kJ/mol,根据盖斯定律可知,反应无论一步完成还是分多
步完成,生成相同的产物,反应热相等,则 P和Cl 一步反应生成1molPCl
2 5
的反应热等于P和Cl 分两步反应生成1molPCl 的反应热;
2 5
故答案为:﹣399kJ•mol﹣1;等于;
(5)PCl 与足量水充分反应,最终生成两种酸磷酸和盐酸,依据原子守恒写出
5
化学方程式为:PCl +4H O=H PO +5HCl;
5 2 3 4
故答案为:PCl +4H O=H PO +5HCl;
5 2 3 4
【点评】本题考查热化学方程式的书写、化学平衡计算、外界条件对化学平衡
移动的影响及反应热的计算等知识.解题中需注意:热化学方程式中没有标
注各物质的聚集状态,各物质的物质的量与反应热没有呈现对应的比例关系,
不能正确判断放热反应和吸热反应.
10.(15分)Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X
单质分子的电子总数相等,R与Q同族,X、Y与Z不同族,Y和Z的离子
与Ar原子的电子结构相同且Y的原子序数小于Z.(1)Q的最高价氧化物,其固态属于 分子 晶体,俗名叫 干冰 ;
(2)R的氢化物分子的空间构型是 正四面体 ,属于 非极性 分子(填
“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其
化学式是 Si N ;
3 4
(3)X的常见氢化物的空间构型是 三角锥型 ;它的另一氢化物X H 是一
2 4
种火箭燃料的成分,其电子式是 ;
(4)Q分别与Y、Z形成的共价化合物的化学式是 CS 和 CCl ;Q与Y
2 4
形成的分子的电子式是 ,属于 非极性 分子(填“极性”或“非
极性”).
【考点】8J:位置结构性质的相互关系应用;98:判断简单分子或离子的构型.
菁优网版权所有
【专题】51C:元素周期律与元素周期表专题.
【分析】Q、R、X、Y、Z 为前20号元素中的五种,Y和Z 的阴离子与Ar原子
的电子结构相同,核外电子数为 18,且Y的原子序数小于Z,故Y为S元素,
Z为Cl元素,X、Y与Z不同族,Q的低价氧化物与X单质分子的电子总数
相等,Q可能为C(碳),X为N,R与 Q同族,由于这五种元素均是前20
号元素,所以R为Si,符合题意,据此解答.
【解答】解:Q、R、X、Y、Z 为前20号元素中的五种,Y和Z 的阴离子与Ar
原子的电子结构相同,核外电子数为18,且Y的原子序数小于Z,故Y为S
元素,Z为Cl元素,X、Y与Z不同族,Q的低价氧化物与X单质分子的电
子总数相等,Q可能为C(碳),X为N,R与 Q同族,由于这五种元素均
是前20号元素,所以R为Si,符合题意,
(1)Q是C元素,其最高化合价是+4价,则其最高价氧化物是CO ,固体二氧
2
化碳属于分子晶体,俗名是干冰,
故答案为:分子;干冰;
(2)R为Si元素,氢化物为SiH ,空间结构与甲烷相同,为正四面体,为对
4
称结构,属于非极性分子,Si与N元素形成的化合物可作为一种重要的陶瓷材料,其化学式是Si N ,
3 4
故答案为:正四面体;非极性;Si N ;
3 4
(3)X为氮元素,常见氢化物为 NH ,空间结构为三角锥型,N H 的电子式
3 2 4
为 ,故答案为:三角锥型; ;
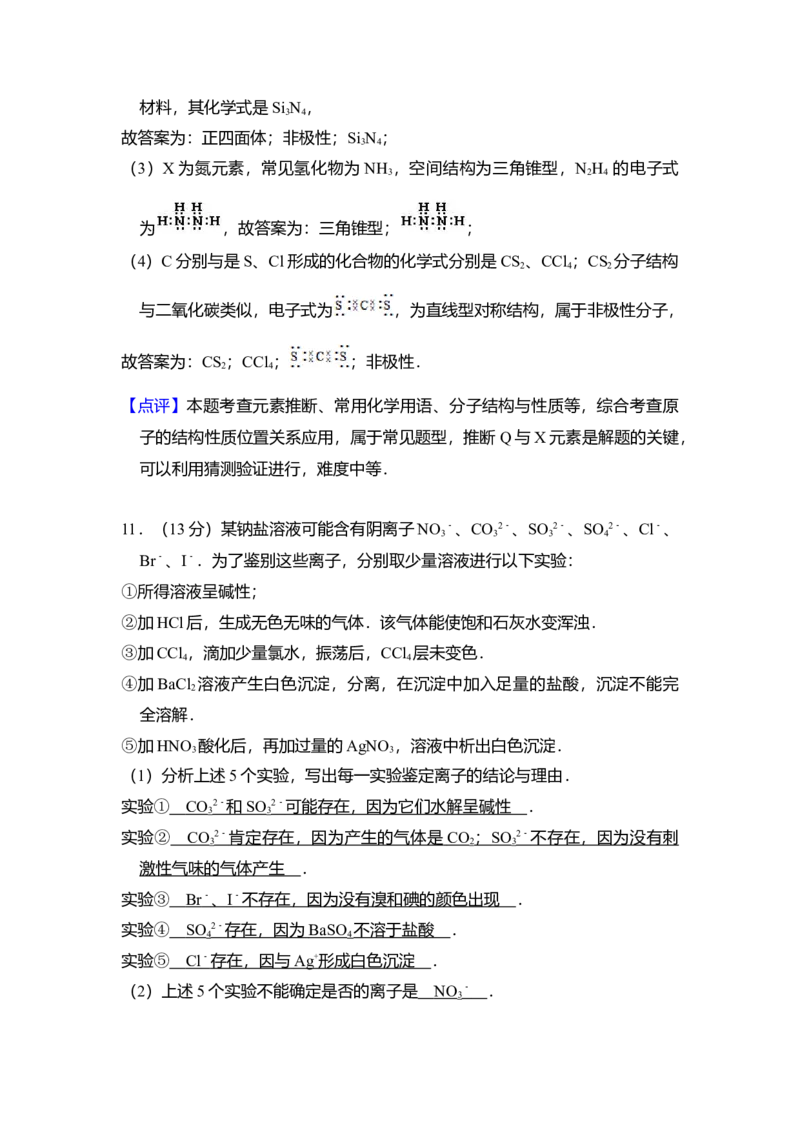
(4)C分别与是S、Cl形成的化合物的化学式分别是CS 、CCl ;CS 分子结构
2 4 2
与二氧化碳类似,电子式为 ,为直线型对称结构,属于非极性分子,
故答案为:CS ;CCl ; ;非极性.
2 4
【点评】本题考查元素推断、常用化学用语、分子结构与性质等,综合考查原
子的结构性质位置关系应用,属于常见题型,推断 Q与X元素是解题的关键,
可以利用猜测验证进行,难度中等.
11.(13分)某钠盐溶液可能含有阴离子NO ﹣、CO 2﹣、SO 2﹣、SO 2﹣、Cl﹣、
3 3 3 4
Br﹣、I﹣.为了鉴别这些离子,分别取少量溶液进行以下实验:
①所得溶液呈碱性;
②加HCl后,生成无色无味的气体.该气体能使饱和石灰水变浑浊.
③加CCl ,滴加少量氯水,振荡后,CCl 层未变色.
4 4
④加BaCl 溶液产生白色沉淀,分离,在沉淀中加入足量的盐酸,沉淀不能完
2
全溶解.
⑤加HNO 酸化后,再加过量的AgNO ,溶液中析出白色沉淀.
3 3
(1)分析上述5个实验,写出每一实验鉴定离子的结论与理由.
实验① CO 2﹣ 和 SO 2﹣ 可能存在,因为它们水解呈碱性 .
3 3
实验② CO 2﹣ 肯定存在,因为产生的气体是 CO ; SO 2﹣ 不存在,因为没有刺
3 2 3
激性气味的气体产生 .
实验③ Br ﹣ 、 I ﹣ 不存在,因为没有溴和碘的颜色出现 .
实验④ SO 2﹣ 存在,因为 BaSO 不溶于盐酸 .
4 4
实验⑤ Cl ﹣ 存在,因与 Ag + 形成白色沉淀 .
(2)上述5个实验不能确定是否的离子是 NO ﹣ .
3【考点】PH:常见阴离子的检验.
菁优网版权所有
【专题】516:离子反应专题.
【分析】①CO 2﹣和SO 2﹣它们水解呈碱性;
3 3
②CO 2﹣和盐酸反应产生的气体是 CO ;SO 2﹣和盐酸反应生成的是刺激性气味
3 2 3
的气体二氧化硫;
③Br﹣、I﹣不存在,因为没有溴和碘的颜色出现.(2分)
④SO 2﹣存在,因为BaSO 不溶于盐酸.(2分)
4 4
⑤Cl﹣存在,因与Ag+形成白色沉淀
【解答】解:(1)①在所给的各种离子中,只有 CO 2﹣和SO 2﹣水解呈碱性,
3 3
它们可能存在,故答案为:CO 2﹣和SO 2﹣可能存在,因为它们水解呈碱性;
3 3
②CO 2﹣可以和盐酸反应,产生的气体是CO ;但是SO 2﹣和盐酸反应生成的是
3 2 3
有刺激性气味的气体二氧化硫,故答案为:CO 2﹣肯定存在,因为产生的气
3
体是CO ;SO 2﹣不存在,因为没有刺激性气味的气体产生;
2 3
③Br﹣、I﹣能被氯气氧化为溴和碘的单质,它们均是易溶于四氯化碳的一种有
颜色的物质,故答案为:Br﹣、I﹣不存在,因为没有溴和碘的颜色出现;
④SO 2﹣和BaCl 溶液反应生成BaSO 不溶于盐酸,故答案为:SO 2﹣存在,因
4 2 4 4
为BaSO 不溶于盐酸;
4
⑤Cl﹣与Ag+形成白色沉淀不溶于稀硝酸,所以加 HNO 酸化后,再加过量的
3
AgNO ,溶液中析出白色沉淀一定是氯化银,而碘化银、溴化银都有颜色,
3
则一定不存在Br﹣、I﹣,
故答案为:Cl﹣存在,因与Ag+形成白色沉淀.
(2)根据实验的结果可以知道NO ﹣不能确定是否含有,故答案为:NO ﹣.
3 3
【点评】本题考查学生常见离子的检验知识,可以根据所学知识进行回答,难
度不大.
12.(17分)A、B、C、D、E、F、G、H、I、J均为有机化合物.根据以下框
图,回答问题:(1)B和C均为有支链的有机化合物,B的结构简式为 ( CH ) CHCOOH
3 2
;C 在浓硫酸作用下加热反应只能生成一种烯烃 D,D 的结构简式为
( CH ) C ═ CH .
3 2 2
(2)G 能发生银镜反应,也能使溴的四氯化碳溶液褪色,则 G 的结构简式
CH =C ( CH )﹣ CHO .
2 3
(3)写出:
⑤的化学方程式是 .⑨的化
学方程式是 .
(4)①的反应类型是 水解反应 ,④的反应类型是 取代反应 ,⑦的反应
类型是 氧化反应 .
( 5 ) 与 H 具 有 相 同 官 能 团 的 H 的 同 分 异 构 体 的 结 构 简 式 为
CH =CHCH COOH 和 CH CH=CHCOOH .
2 2 3
【考点】HB:有机物的推断.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
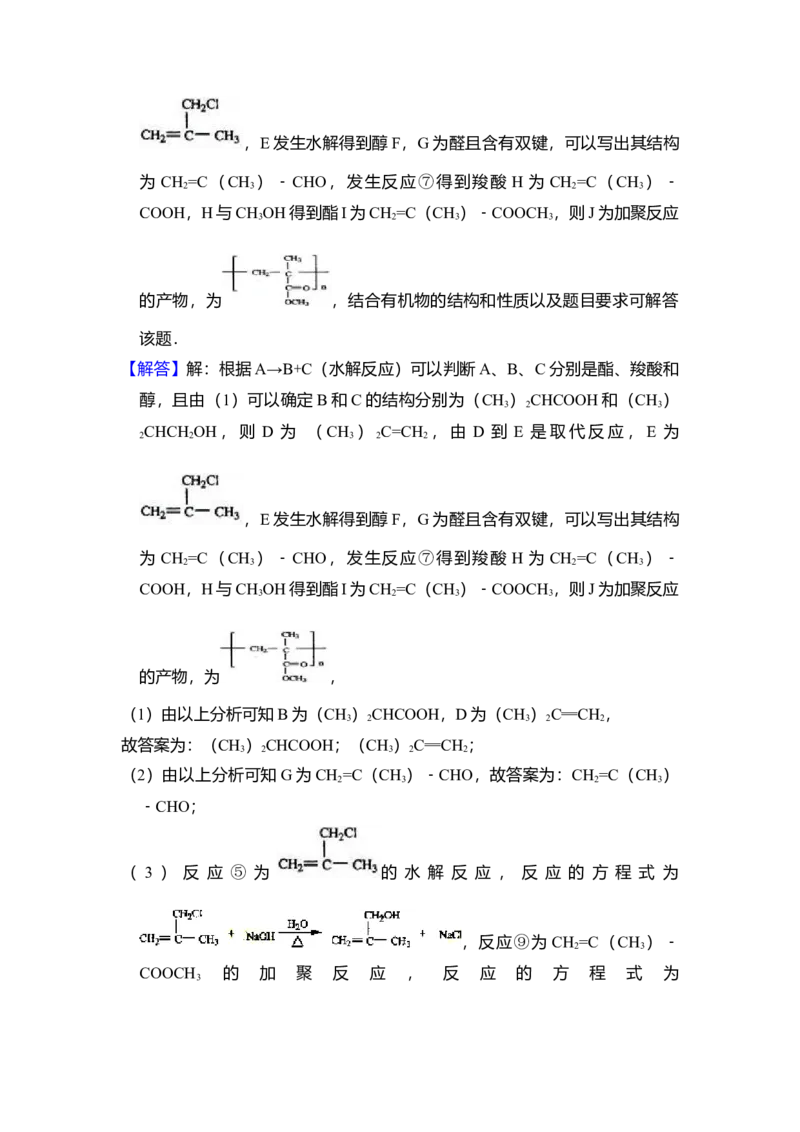
【分析】根据A→B+C(水解反应)可以判断A、B、C分别是酯、羧酸和醇,
且由(1)可以确定 B 和 C 的结构分别为(CH ) CHCOOH 和(CH )
3 2 3
CHCH OH,则 D 为 (CH ) C=CH ,由 D 到 E 是取代反应,E 为
2 2 3 2 2,E发生水解得到醇F,G为醛且含有双键,可以写出其结构
为 CH =C(CH )﹣CHO,发生反应⑦得到羧酸 H 为 CH =C(CH )﹣
2 3 2 3
COOH,H与CH OH得到酯I为CH =C(CH )﹣COOCH ,则J为加聚反应
3 2 3 3
的产物,为 ,结合有机物的结构和性质以及题目要求可解答
该题.
【解答】解:根据A→B+C(水解反应)可以判断A、B、C分别是酯、羧酸和
醇,且由(1)可以确定B和C的结构分别为(CH ) CHCOOH和(CH )
3 2 3
CHCH OH,则 D 为 (CH ) C=CH ,由 D 到 E 是取代反应,E 为
2 2 3 2 2
,E发生水解得到醇F,G为醛且含有双键,可以写出其结构
为 CH =C(CH )﹣CHO,发生反应⑦得到羧酸 H 为 CH =C(CH )﹣
2 3 2 3
COOH,H与CH OH得到酯I为CH =C(CH )﹣COOCH ,则J为加聚反应
3 2 3 3
的产物,为 ,
(1)由以上分析可知B为(CH ) CHCOOH,D为(CH ) C═CH ,
3 2 3 2 2
故答案为:(CH ) CHCOOH;(CH ) C═CH ;
3 2 3 2 2
(2)由以上分析可知G为CH =C(CH )﹣CHO,故答案为:CH =C(CH )
2 3 2 3
﹣CHO;
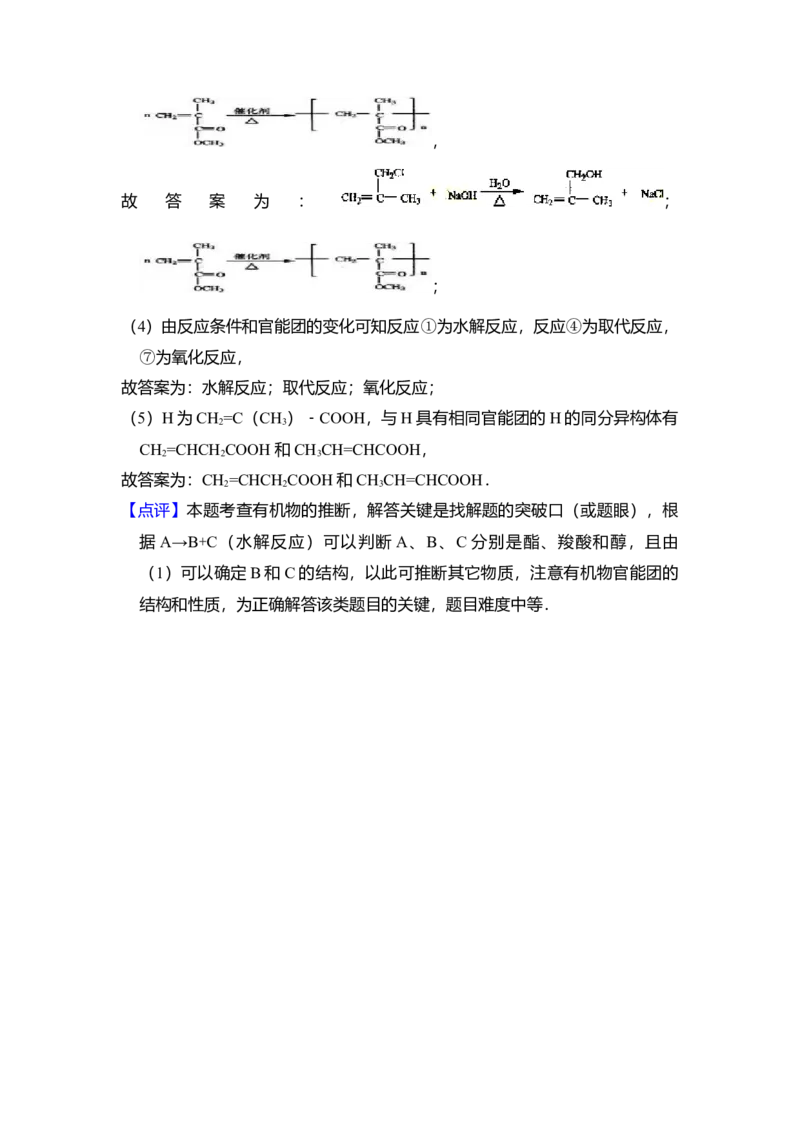
( 3 ) 反 应 ⑤ 为 的 水 解 反 应 , 反 应 的 方 程 式 为
,反应⑨为 CH =C(CH )﹣
2 3
COOCH 的 加 聚 反 应 , 反 应 的 方 程 式 为
3,
故 答 案 为 : ;
;
(4)由反应条件和官能团的变化可知反应①为水解反应,反应④为取代反应,
⑦为氧化反应,
故答案为:水解反应;取代反应;氧化反应;
(5)H为CH =C(CH )﹣COOH,与H具有相同官能团的H的同分异构体有
2 3
CH =CHCH COOH 和CH CH=CHCOOH,
2 2 3
故答案为:CH =CHCH COOH 和CH CH=CHCOOH.
2 2 3
【点评】本题考查有机物的推断,解答关键是找解题的突破口(或题眼),根
据 A→B+C(水解反应)可以判断 A、B、C 分别是酯、羧酸和醇,且由
(1)可以确定B和C的结构,以此可推断其它物质,注意有机物官能团的
结构和性质,为正确解答该类题目的关键,题目难度中等.