文档内容
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Ca-40
一、选择题(本题共10分,每小题2分,每题只有一个正确选项)
1.中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于293Lv的叙述错误的是( )
116
A.原子序数116 B.中子数177
C.核外电子数116 D.相对原子质量293
2.下列物质见光不会分解的是( )
A.HClO B.NH Cl C.HNO D.AgNO
4 3 3
第1页 | 共30页3.某晶体中含有极性键,关于该晶体的说法错误的是( )
A.不可能有很高的熔沸点 B.不可能是单质
C.可能是有机物 D.可能是离子晶体
第2页 | 共30页4.不能作为判断硫、氯两种元素非金属性强弱的依据是( )
[来源:学+科+网]
A.单质氧化性的强弱 B.单质沸点的高低
C.单质与氢气化合的难易 D.最高价氧化物对应的水化物酸性的强弱
第3页 | 共30页5.二氧化硫能使溴水褪色,说明二氧化硫具有( )
A.还原性 B.氧化性 C.漂白性 D.酸性
二、选择题(本题共36分,每小题3分,每题只有一个正确选项)
6.将Na、Na O、NaOH、Na S、Na SO 分别加热熔化,需要克服相同类型作用力的物质有( )
2 2 2 4
A.2种 B.3种 C.4种 D.5种
第4页 | 共30页7.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )
A.NaOH B.KMnO C.KSCN D.苯酚
4
8.已知H O 在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
2 2
A.加入催化剂,减小了反应的热效应
[来源:学.科.网]
B.加入催化剂,可提高H O 的平衡转化率
2 2
第5页 | 共30页C.H O 分解的热化学方程式:H O → H O + O + Q
2 2 2 2 2 2
D.反应物的总能量高于生成物的总能量
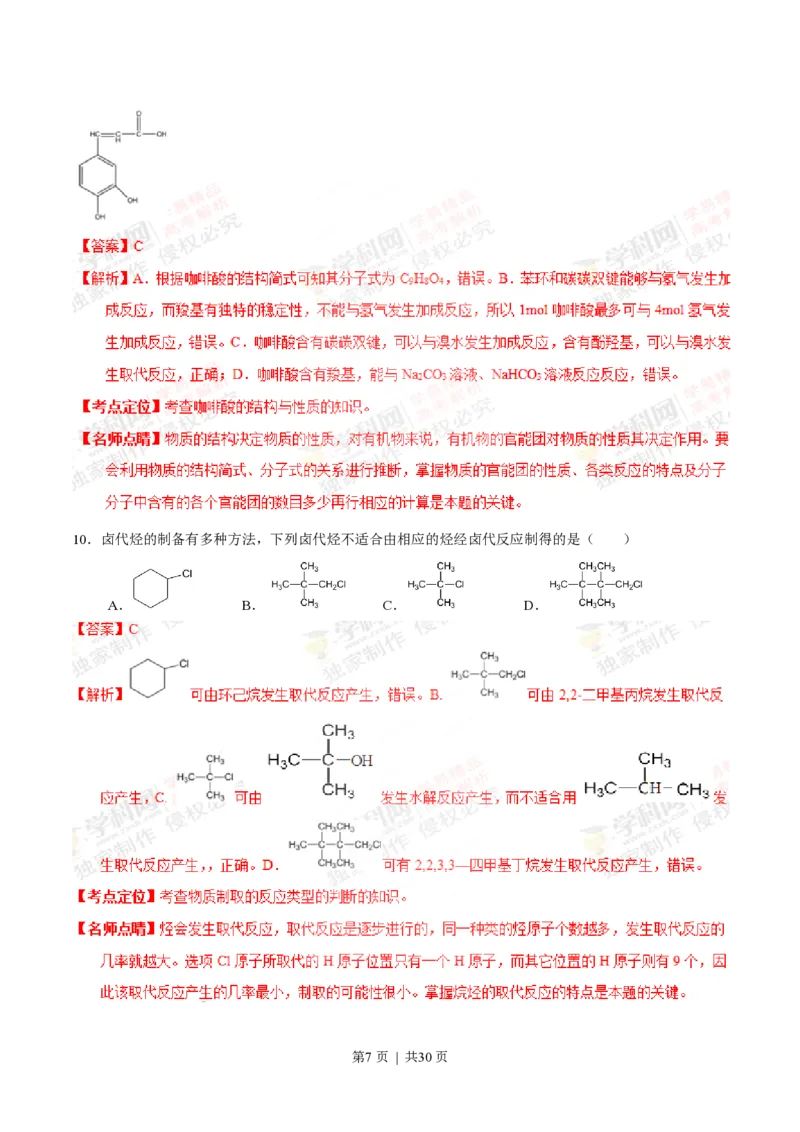
9.已知咖啡酸的结构如右图所示。关于咖啡酸的描述正确的是( )
A.分子式为C H O
9 5 4
B.1mol咖啡酸最多可与5mol氢气发生加成反应
C.与溴水既能发生取代反应,又能发生加成反应
D.能与Na CO 溶液反应,但不能与NaHCO 溶液反应
2 3 3
第6页 | 共30页10.卤代烃的制备有多种方法,下列卤代烃不适合由相应的烃经卤代反应制得的是( )
A. B. C. D.
[来源:学。科。网Z。X。X。K]
第7页 | 共30页11.下列有关物质性质的比较,错误的是( )
A.溶解度:小苏打 < 苏打 B.密度:溴乙烷 > 水
C.硬度:晶体硅 < 金刚石 D.碳碳键键长:乙烯 > 苯
12.与氢硫酸反应有沉淀生成的电解质是( )
A.硫酸铜 B.氢氧化钠 C.硫酸亚铁 D.二氧化硫
第8页 | 共30页13.实验室回收废水中苯酚的过程如右图所示。下列分析错误的是( )
A.操作I中苯作萃取剂
B.苯酚钠在苯中的溶解度比在水中的大
C.通过操作II苯可循环使用
D.三步操作均需要分液漏斗
14.研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )
A.d为石墨,铁片腐蚀加快
B.d为石墨,石墨上电极反应为:O + 2H O + 4e → 4OH–
2 2
第9页 | 共30页C.d为锌块,铁片不易被腐蚀
D.d为锌块,铁片上电极反应为:2H+ + 2e → H ↑
2
15.一般情况下,前者无法决定后者的是( )
A.原子核外电子排布——元素在周期表中的位置
B.弱电解质的相对强弱——电离常数的大小
C.分子间作用力的大小——分子稳定性的高低
D.物质内部储存的能量——化学反应的热效应
第10页 | 共30页16.短周期元素甲、乙、丙、丁的原子序数依次增大,甲和丁的原子核外均有两个未成对电子,乙、丙、
丁最高价氧化物对应的水化物两两之间能相互反应。下列说法错误的是( )
A.元素丙的单质可用于冶炼金属 B.甲与丁形成的分子中由非极性分子
C.简单离子半径:丁 > 乙 > 丙 D.甲与乙形成的化合物均有氧化性
第11页 | 共30页17.某无色溶液含有下列离子中的若干种:H+、NH +、Fe3+、Ba2+、Al3+、CO 2–、Cl–、OH–、NO –。向该
4 3 3
溶液中加入铝粉,只放出H ,则溶液中能大量存在的离子最多有( )
2
A.3种 B.4种 C.5种 D.6种
三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给
分;有两个正确选项的,选对一个给2分,选错一个,该小题不给分)
18.下列反应中的氨与反应4NH + 5O → 4NO + 6H O中的氨作用相同的是( )
3 2 2
A.2Na + 2NH → 2NaNH + H ↑ B.2NH + 3CuO → 3Cu + N +3H O
3 2 2 3 2 2
C.4NH + 6NO → 5N + 6H O D.3SiH + 4NH → Si N + 12H
3 2 2 4 3 3 4 2
第12页 | 共30页[来源:Z*xx*k.Com]
19.离子方程式2Ca2+ + 3HCO – + 3OH– → 2CaCO ↓ + CO 2– + 3H O可以表示( )
3 3 3 2
A.Ca(HCO ) 与NaOH溶液反应 B.NaHCO 与澄清石灰水反应
3 2 3
C.Ca(HCO ) 与澄清石灰水反应 D.NH HCO 与澄清石灰水反应
3 2 4 3
第13页 | 共30页二者的性质书写离子方程式,并判断离子方程式的正误。
20.对于合成氨反应,达到平衡后,以下分析正确的是( )
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大
D.加入催化剂,对逆反应的反应速率影响更大
21.工业上将Na CO 和Na S以1:2的物质的量之比配成溶液,再通入SO ,可制取Na S O ,同时放出
2 3 2 2 2 2 3
CO 。在该反应中( )
2
A.硫元素既被氧化又被还原
B.氧化剂与还原剂的物质的量之比为1:2
C.每生成1molNa S O ,转移4mol电子
2 2 3
D.相同条件下,每吸收10m3SO 就会放出2.5m3CO
2 2
【答案】A
第14页 | 共30页22.将O 和NH 的混合气体448mL通过加热的三氧化二铬,充分反应后,再通过足量的水,最终收集到
2 3
44.8mL气体。原混合气体中O 的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)
2
( )
A.231.5mL B.268.8mL C.287.5mL D.313.6mL
四、(本题共12分)
白云石的主要成份是CaCO ·MgCO ,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广
3 3
第15页 | 共30页泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离。碳化反应是
放热反应,化学方程式如下:Ca(OH) + Mg(OH) + 3CO ⇌ CaCO + Mg(HCO ) + H O
2 2 2 3 3 2 2
完成下列填空
23.Ca(OH) 的碱性比Mg(OH) 的碱性 (选填“强”或“弱”)
2 2
Ca(OH) 的溶解度比Mg(OH) 的溶解度 (选填“大”或“小”)
2 2
24.碳化温度保持在50~60℃。温度偏高不利于碳化反应,原因是 、
。温度偏低也不利于碳化反应,原因是 。
25.已知某次碳化时溶液中钙离子浓度随时间的变化如右图所示,在10 min到13 min之内钙离子的反
应速率为 。15 min之后钙离子浓度增大,原因是 (用化学方程
式表示)。
26.Mg原子核外电子排布式为 ;Ca原子最外层电子的能量 Mg原子最外层电子的能
量。(选填“低于”、“高于”或“等于”)
第16页 | 共30页五、(本题共12分)氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系
列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
27.写出电解饱和食盐水的离子方程式。
28.离子交换膜的作用为: 、 。
29.精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中 位置流出。(选填“a”、
“b”、“c”或“d”)
30.KClO 可以和草酸(H C O )、硫酸反应生成高效的消毒杀菌剂ClO ,还生成CO 和KHSO 等物
3 2 2 4 2 2 4
质。
写出该反应的化学方程式 。
31.室温下,0.1 mol/L NaClO溶液的pH 0.1 mol/L Na SO 溶液的pH。(选填“大于”、“小于”
2 3
或“等于”)。浓度均为0.1 mol/L 的Na SO 和Na CO 的混合溶液中,SO 2–、CO 2–、HSO –、
2 3 2 3 3 3 3
第17页 | 共30页HCO – 浓度从大到小的顺序为 。
3
已知: H SO K =1.54×10-2 K =1.02×10-7
2 3 i1 i2
HClO K =2.95×10-8
i1
H CO K =4.3×10-7 K =5.6×10-11
2 3 i1 i2
第18页 | 共30页六、(本题共12分)
过氧化钙(CaO )是一种白色、无毒、难溶于水的固体,能杀菌消毒,广泛用于果蔬保鲜、空气净化、
2
污水处理等方面。工业生产过程如下:
①在NH Cl溶液中加入Ca(OH) ;
4 2
②不断搅拌的同时加入30% H O ,反应生成CaO ·8H O沉淀;
2 2 2 2
③经过陈化、过滤,水洗得到CaO ·8H O,再脱水干燥得到CaO 。
2 2 2
完成下列填空
32.第①步反应的化学方程式为 。第②步反应的化学方程式为 。
33.可循环使用的物质是 。
工业上常采用Ca(OH) 过量而不是H O 过量的方式来生产,这是因为 。
2 2 2
34.检验CaO ·8H O是否洗净的方法是 。
2 2
35.CaO ·8H O加热脱水的过程中,需不断通入不含二氧化碳的氧气,目的是 、 。
2 2
36.已知CaO 在350℃迅速分解生成CaO和O 。下图是实验室测定产品中CaO 含量的装置(夹持装
2 2 2
置省略)。
第19页 | 共30页若所取产品质量是m g,测得气体体积为V mL(已换算成标准状况),则产品中CaO 的质量分数
2
为 (用字母表示)。
过氧化钙的含量也可用重量法测定,需要测定的物理量有 。
第20页 | 共30页七、(本题共12分)
甲醛是深受关注的有机化合物。甲醛含量的测定有多种方法,例如:在调至中性的亚硫酸钠溶液中加
入甲醛水溶液,经充分反应后,产生的氢氧化钠的物质的量与甲醛的物质的量相等,然后用已知浓度的硫
酸滴定氢氧化钠。
完成下列填空:
37.将4.00 mL甲醛水溶液加入到经调至中性的亚硫酸钠溶液中,充分反应后,用浓度为1.100 mol/L
的硫酸滴定,至终点时耗用硫酸20.00 mL。
甲醛水溶液的浓度为 mol/L。
38.上述滴定中,若滴定管规格为50mL,甲醛水溶液取样不能超过 mL。
39.工业甲醛含量测定的另一种方法:在甲醛水溶液中加入过氧化氢,将甲醛氧化为甲酸,然后用已
知浓度的氢氧化钠溶液滴定。
HCHO + H O → HCOOH + H O NaOH + HCOOH → HCOONa + H O
2 2 2 2
已知H O 能氧化甲酸生成二氧化碳和水。
2 2
如果H O 用量不足,会导致甲醛含量的测定结果 (选填“偏高”、“偏低”或“不受影响”),
2 2
因为 ;如果H O 过量,会导致甲醛含量的测定结果 (选填“偏高”、
2 2
“偏低”或“不受影响”),因为 。
第21页 | 共30页40.甲醛和新制氢氧化铜的反应显示了甲醛的还原性,发生反应的化学方程式通常表示如下:
HCHO + 2Cu(OH) HCOOH + Cu O↓ + 2H O
2 2 2
若向足量新制氢氧化铜中加入少量甲醛,充分反应,甲醛的氧化产物不是甲酸或甲酸盐,设计一
个简单实验验证这一判断。
①主要仪器:试管 酒精灯
②可供选用的试剂:硫酸铜溶液、甲醛、甲酸、氢氧化钠溶液
第22页 | 共30页八、(本题共10分)
对溴苯乙烯与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。
完成下列填空:
41.写出该共聚物的结构简式
42.实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体 。
写出该两步反应所需的试剂及条件。
43.将 与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl 溶液不显色。
3
A的结构简式为 。
由上述反应可推知 。
由A生成对溴苯乙烯的反应条件为 。
44.丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于
同一平面。
写出B的结构简式。
设计一条由2,3-二甲基-1-丁烯制备B的合成路线。
(合成路线常用的表示方式为: )
【答案】41. 。
第23页 | 共30页第24页 | 共30页九、(本题共12分)
第25页 | 共30页局部麻醉药普鲁卡因E(结构简式为 )的三条合成路线如下图所示(部
分反应试剂和条件已省略):
完成下列填空:
45.比A多一个碳原子,且一溴代物只有3种的A的同系物的名称是 。
[来源:学科网ZXXK]
46.写出反应试剂和反应条件。反应① ;③
47.设计反应②的目的是 。
48.B的结构简式为 ;C的名称是 。
49.写出一种满足下列条件的D的同分异构体的结构简式。
①芳香族化合物 ②能发生水解反应 ③有3种不同环境的氢原子
1 mol该物质与NaOH溶液共热最多消耗 mol NaOH。
50.普鲁卡因的三条合成路线中,第一条合成路线与第二条、第三条相比不太理想,理由是
。
第26页 | 共30页第27页 | 共30页十、(本题共14分)
氨碱法制纯碱包括石灰石分解、粗盐水精制、氨盐水碳酸化等基本步骤。
完成下列计算:
51.CaCO 质量分数为0.90的石灰石100 kg完成分解产生CO L(标准状况)。
3 2
石灰窑中,该石灰石100 kg与焦炭混合焙烧,产生CO 29120 L(标准状况),
2
如果石灰石中碳酸钙完全分解,且焦炭完全燃烧,不产生CO,则焦炭的物质的量为 mol。
52.已知粗盐水含MgCl 6.80 mol/m3,含CaCl 3.00mol/m3。
2 2
向粗盐水中加入Ca(OH) 除镁离子:MgCl + Ca(OH) → Mg(OH) ↓ + CaCl
2 2 2 2 2
然后加入Na CO 除钙离子。
2 3
处理上述粗盐水10 m3,至少需要加Na CO g。
2 3
如果用碳酸化尾气(含NH 体积分数为0.100、CO 体积分数0.040)代替碳酸钠,发生如下反应:
3 2
Ca2+ + 2NH + CO + H O → CaCO ↓ + 2NH +
3 2 2 3 4
处理上述10 m3粗盐水至少需要通入多少L(标准状况)碳酸化尾气?列式计算。
第28页 | 共30页53.某氨盐水含氯化钠1521 kg,通入二氧化碳后析出碳酸氢钠晶体,过滤后溶液中含氯化铵1070 kg。
列式计算:
(1)过滤后溶液中氯化钠的质量。
(2)析出的碳酸氢钠晶体的质量。
第29页 | 共30页第30页 | 共30页