文档内容
2009年天津市高考化学试卷
一、选择题(共6小题,每小题3分,满分18分)
1.(3分)化学与生活密切相关,下列有关说法正确的是( )
A.维生素C具有还原性,在人体内起抗氧化作用
B.糖类、蛋白质、油脂都属于天然高分子化合物
C.煤经气化和液化两个物理变化过程,可变为清洁能源
D.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
2.(3分)25℃时,浓度均为0.2mol/L的NaHCO 和Na CO 溶液中,下列判断不正确的
3 2 3
是( )
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.c(OH﹣)前者大于后者
D.分别加入NaOH固体,恢复到原温度,c(CO 2﹣)均增大
3
3.(3分)下列实验设计和结论相符的是( )
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO ) 溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有
3 2
SO 2﹣
4
D.在含FeCl 杂质的FeCl 溶液中通足量Cl 后,充分加热,除去过量的Cl ,即可得到
2 3 2 2
较纯净的FeCl 溶液
3
4.(3分)下列叙述正确的是( )
A.0.1 mol/LC H ONa溶液中:c(Na+)>c(C H O﹣)>c(H+)>c(OH﹣)
6 5 6 5
B.Na CO 溶液加水稀释后,恢复至原温度,pH和K 均减小
2 3 w
C.pH=5的CH COOH溶液和pH=5的NH Cl溶液中,c(H+)不相等
3 4
D.在Na S溶液中加入AgCl固体,溶液中c(S2﹣)下降
2
5.(3分)人体血液内的血红蛋白(Hb)易与O 结合生成HbO ,因此具有输氧能力,
2 2
CO吸入肺中发生反应:CO+HbO O +HbCO,37℃时,该反应的平衡常数 K=220.
2 2
HbCO的浓度达到HbO 浓度的0.02⇌倍,会使人智力受损。据此,下列结论错误的是(
2
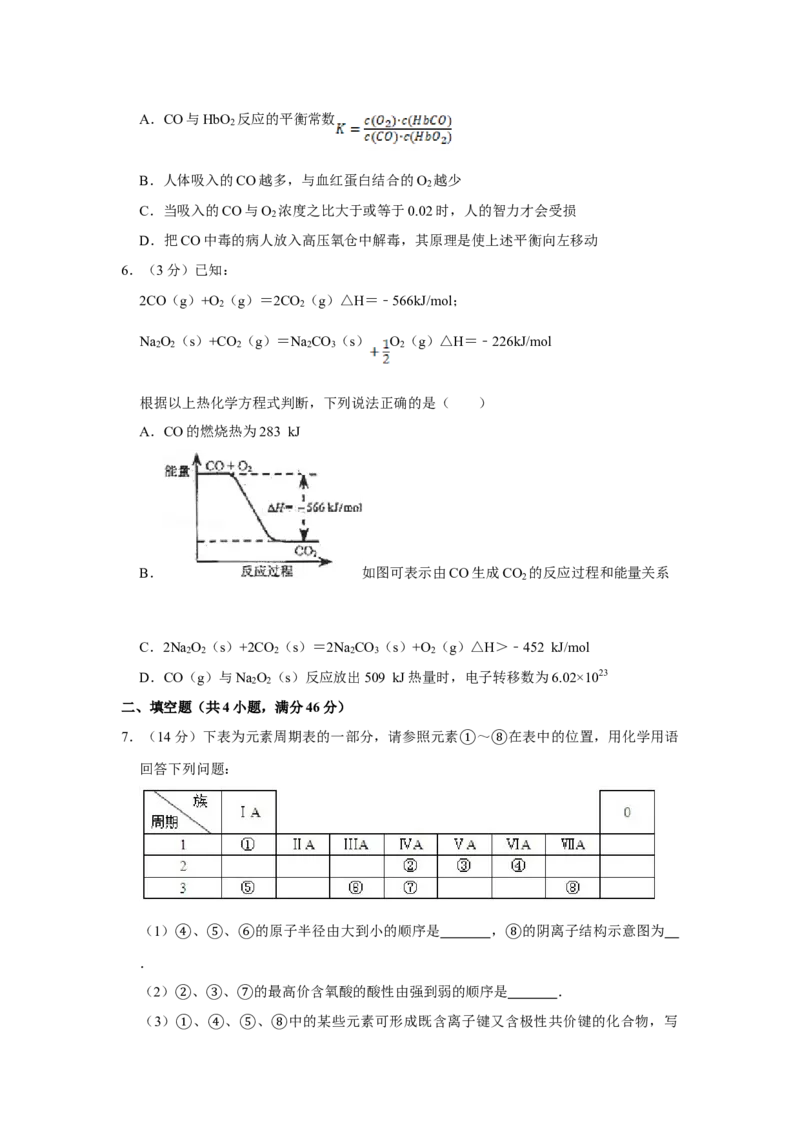
)A.CO与HbO 反应的平衡常数
2
B.人体吸入的CO越多,与血红蛋白结合的O 越少
2
C.当吸入的CO与O 浓度之比大于或等于0.02时,人的智力才会受损
2
D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
6.(3分)已知:
2CO(g)+O (g)=2CO (g)△H=﹣566kJ/mol;
2 2
Na O (s)+CO (g)=Na CO (s) O (g)△H=﹣226kJ/mol
2 2 2 2 3 2
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
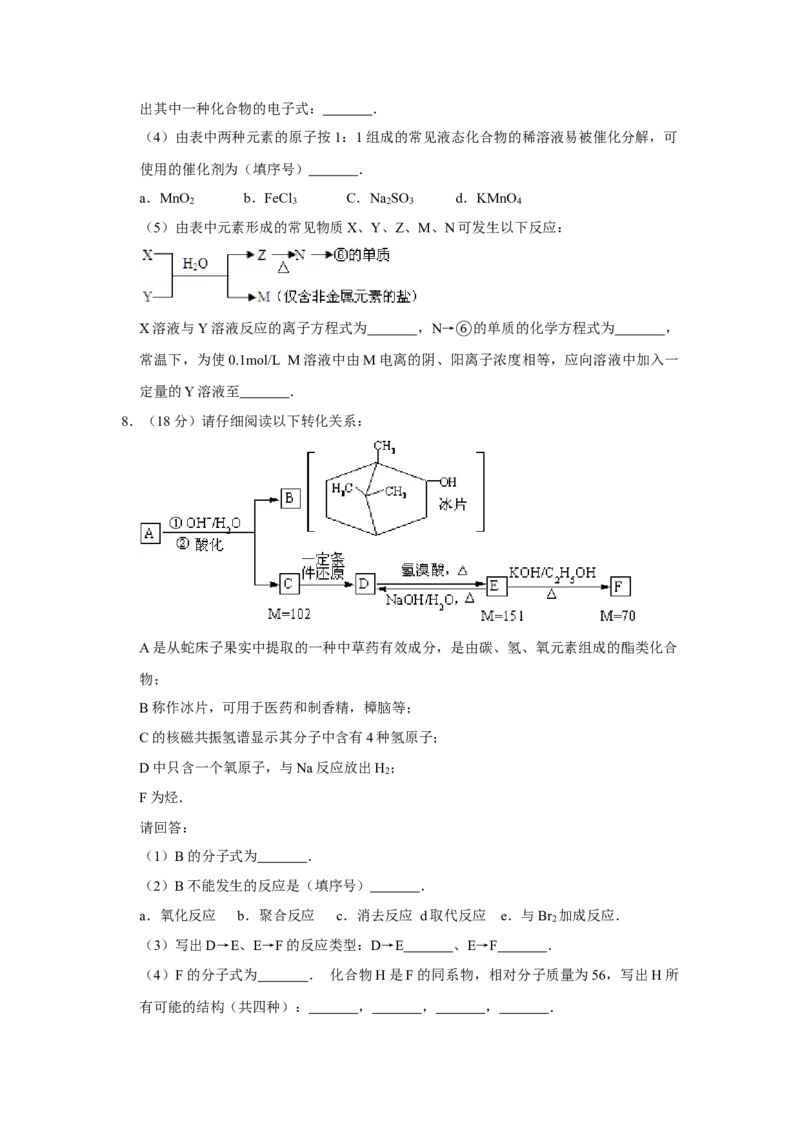
B. 如图可表示由CO生成CO 的反应过程和能量关系
2
C.2Na O (s)+2CO (s)=2Na CO (s)+O (g)△H>﹣452 kJ/mol
2 2 2 2 3 2
D.CO(g)与Na O (s)反应放出509 kJ热量时,电子转移数为6.02×1023
2 2
二、填空题(共4小题,满分46分)
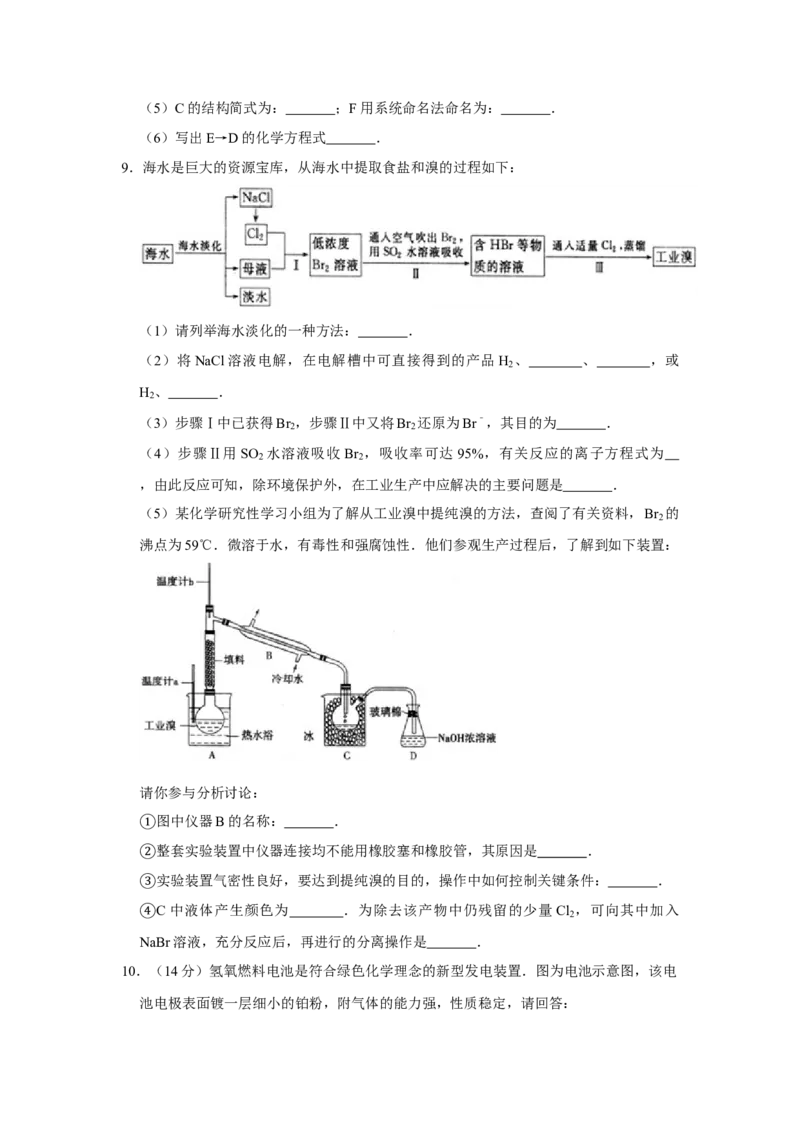
7.(14分)下表为元素周期表的一部分,请参照元素 ~ 在表中的位置,用化学用语
回答下列问题: ① ⑧
(1) 、 、 的原子半径由大到小的顺序是 , 的阴离子结构示意图为
. ④ ⑤ ⑥ ⑧
(2) 、 、 的最高价含氧酸的酸性由强到弱的顺序是 .
(3)②、③、⑦、 中的某些元素可形成既含离子键又含极性共价键的化合物,写
① ④ ⑤ ⑧出其中一种化合物的电子式: .
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可
使用的催化剂为(填序号) .
a.MnO b.FeCl C.Na SO d.KMnO
2 3 2 3 4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为 ,N→ 的单质的化学方程式为 ,
常温下,为使0.1mol/L M溶液中由M电离的阴、阳⑥离子浓度相等,应向溶液中加入一
定量的Y溶液至 .
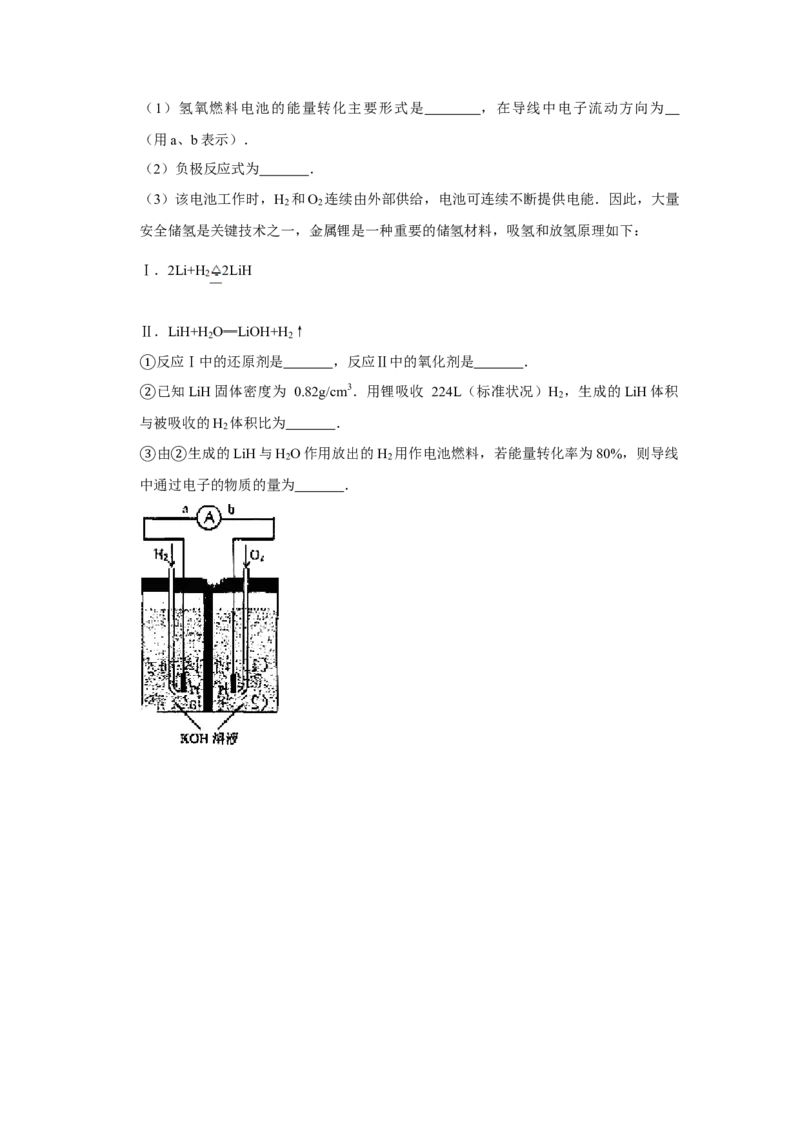
8.(18分)请仔细阅读以下转化关系:
A是从蛇床子果实中提取的一种中草药有效成分,是由碳、氢、氧元素组成的酯类化合
物;
B称作冰片,可用于医药和制香精,樟脑等;
C的核磁共振氢谱显示其分子中含有4种氢原子;
D中只含一个氧原子,与Na反应放出H ;
2
F为烃.
请回答:
(1)B的分子式为 .
(2)B不能发生的反应是(填序号) .
a.氧化反应 b.聚合反应 c.消去反应 d取代反应 e.与Br 加成反应.
2
(3)写出D→E、E→F的反应类型:D→E 、E→F .
(4)F的分子式为 . 化合物H是F的同系物,相对分子质量为56,写出H所
有可能的结构(共四种): , , , .(5)C的结构简式为: ;F用系统命名法命名为: .
(6)写出E→D的化学方程式 .
9.海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
(1)请列举海水淡化的一种方法: .
(2)将NaCl溶液电解,在电解槽中可直接得到的产品H 、 、 ,或
2
H 、 .
2
(3)步骤Ⅰ中已获得Br ,步骤Ⅱ中又将Br 还原为Br﹣,其目的为 .
2 2
(4)步骤Ⅱ用SO 水溶液吸收Br ,吸收率可达95%,有关反应的离子方程式为
2 2
,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 .
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br 的
2
沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,了解到如下装置:
请你参与分析讨论:
图中仪器B的名称: .
①整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 .
②实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: .
③C中液体产生颜色为 .为除去该产物中仍残留的少量Cl
2
,可向其中加入
④NaBr溶液,充分反应后,再进行的分离操作是 .
10.(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置.图为电池示意图,该电
池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答:(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示).
(2)负极反应式为 .
(3)该电池工作时,H 和O 连续由外部供给,电池可连续不断提供电能.因此,大量
2 2
安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H 2LiH
2
Ⅱ.LiH+H O═LiOH+H ↑
2 2
反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 .
①已知LiH固体密度为 0.82g/cm3.用锂吸收 224L(标准状况)H
2
,生成的LiH体积
②与被吸收的H 体积比为 .
2
由 生成的LiH与H O作用放出的H 用作电池燃料,若能量转化率为80%,则导线
2 2
③中通过②电子的物质的量为 .