文档内容
2009 年普通高校招生统一考试福建卷(理综-化学)
相对原子质量:H 1 C 12 N 14 O 16 Mg 24 Zn 65
6. 下列类型的反应,一定发生电子转移的是w.w.w.k.s.5.u.c.o.m
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
答案C【解析】置换反应中肯定有单质参加,一定属于氧化还原反应,即一定有电子转移,C
项正确。
7. 能实现下列物质间直接转化的元素是
A. 硅 B. 硫 C. 铜 D. 铁
答案B
【解析】S与O 生成SO ,再与HO生成HSO ,可以与NaOH生成NaSO ,B项正确。A项,
2 2 2 2 3 2 3
SiO 不与水反应,错;C项中CuO,D项中FeO 均不与HO反应,故错。
2 3 4 2
8. 设N 为阿伏伽德罗常数,下列叙述正确的是
A
A. 24g镁的原子量最外层电子数为N B. 1L0.1mol·L-1乙酸溶液中H+数为0.1N
A A
C. 1mol甲烷分子所含质子数为10N D. 标准状况下,22.4L乙醇的分子数为N
A A
答案C
【解析】A项,镁的最外层电子数为2,故错;B项,乙酸为弱电解质,部分电离,故H+小于
0.1NA,错;C项,CH 的质子数为10,正确;D项,乙醇标状下不是气体,错。
4
9. 下列关于常见有机物的说法不正确的是w.w.w.k.s.5.u.c.o.m
A. 乙烯和苯都能与溴水反应 B. 乙酸和油脂都能与氢氧化钠溶液反应
C. 糖类和蛋白质都是人体重要的营养物质 D. 乙烯和甲烷可用酸性高锰酸钾溶液鉴别
答案A
【解析】苯不与溴水反应,只能液溴反应,A项错。乙酸与NaOH发生酸碱中和,油脂在碱性
条件能水解,B项正确;C项,糖类,油脂和蛋白质是重要营养的物质,正确;D项,乙烯可
以使高锰酸钾褪色,而甲烷不可以,正确。
10. 在一定条件下,NaCO 溶液存在水解平衡: 。下列说
2 3
法正确的是
A. 稀释溶液,水解平衡常数增大 B. 通入CO ,平衡朝正反应方向移动
2
C. 升高温度, 减小 D. 加入NaOH固体,溶液PH减小
答案B
【解析】平衡常数仅与温度有关,故稀释时是不变的,A项错;CO 通入水中,相当于生成
2
HCO,可以与OH-反应,而促进平衡正向移动,B项正确;升温,促进水解,平衡正向移动,
2 3
故表达式的结果是增大的,C项错;D项,加入NaOH,碱性肯定增强,pH增大,故错。
11. 控制适合的条件,将反应 设计
成如右图所示的原电池。下列判断不正确的是
A. 反应开始时,乙中石墨电极上发生氧化反应
B. 反应开始时,甲中石墨电极上Fe3+被还原C. 电流计读数为零时,反应达到化学平衡状态
D. 电流计读数为零后,在甲中溶入FeCl 固定,乙中石墨电极为负极
2
答案D
【解析】乙中I-失去电子放电,故为氧化反应,A项正确;由总反应方程式知,Fe3+被还原
成Fe2+,B项正确;当电流计为零时,即说明没有电子发生转移,可证明反应达平衡,C项正
确。加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,而作为负极,D项错。
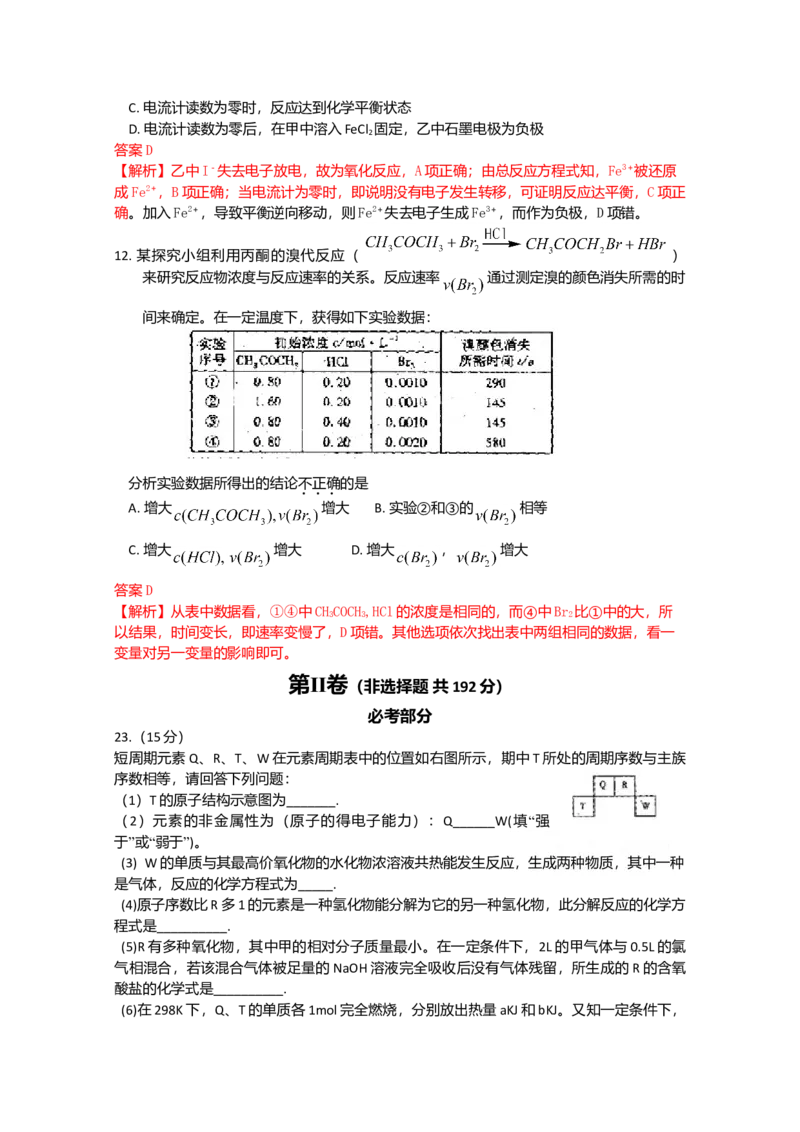
12. 某探究小组利用丙酮的溴代反应( )
来研究反应物浓度与反应速率的关系。反应速率 通过测定溴的颜色消失所需的时
间来确定。在一定温度下,获得如下实验数据:
分析实验数据所得出的结论不正确的是
A. 增大 增大 B. 实验②和③的 相等
C. 增大 增大 D. 增大 , 增大
答案D
【解析】从表中数据看,①④中CHCOCH,HCl的浓度是相同的,而④中Br 比①中的大,所
3 3 2
以结果,时间变长,即速率变慢了,D项错。其他选项依次找出表中两组相同的数据,看一
变量对另一变量的影响即可。
第Ⅱ卷(非选择题
共192分)
必考部分
23.(15分)w.w.w.k.s.5.u.c.o.m
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中T所处的周期序数与主族
序数相等,请回答下列问题:
(1)T的原子结构示意图为_______.
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强
于”或“弱于”)。
(3) W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种
是气体,反应的化学方程式为_____.
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方
程式是__________.
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯
气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧
酸盐的化学式是__________.
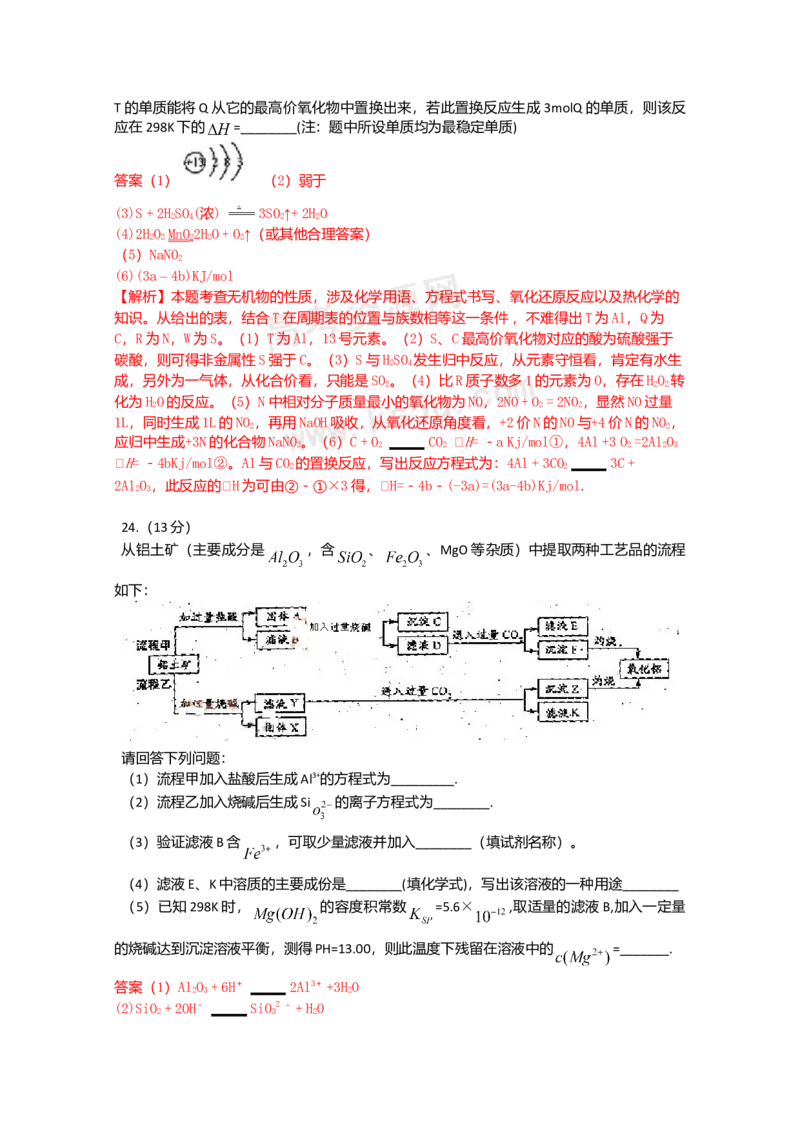
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反
应在298K下的 =________(注:题中所设单质均为最稳定单质)
答案(1) (2)弱于
(3)S + 2HSO(浓) 3SO↑+ 2HO
2 4 2 2
(4)2HO MnO2HO + O↑(或其他合理答案)
2 2 2 2 2
(5)NaNO
2
(6)(3a – 4b)KJ/mol
【解析】本题考查无机物的性质,涉及化学用语、方程式书写、氧化还原反应以及热化学的
知识。从给出的表,结合T在周期表的位置与族数相等这一条件 ,不难得出T为Al,Q为
C,R为N,W为S。(1)T为Al,13号元素。(2)S、C最高价氧化物对应的酸为硫酸强于
碳酸,则可得非金属性S强于C。(3)S与HSO 发生归中反应,从元素守恒看,肯定有水生
2 4
成,另外为一气体,从化合价看,只能是SO。(4)比R质子数多1的元素为O,存在HO 转
2 2 2
化为HO的反应。(5)N中相对分子质量最小的氧化物为NO,2NO + O = 2NO,显然NO过量
2 2 2
1L,同时生成1L的NO,再用NaOH吸收,从氧化还原角度看,+2价N的NO与+4价N的NO,
2 2
应归中生成+3N的化合物NaNO。(6)C + O CO H= -a Kj/mol①,4Al +3 O =2AlO
2 2 2 2 2 3
H= -4bKj/mol②。Al与CO 的置换反应,写出反应方程式为:4Al + 3CO 3C +
2 2
2AlO,此反应的H为可由②-①×3得,H=-4b-(-3a)=(3a-4b)Kj/mol.
2 3
24.(13分)
从铝土矿(主要成分是 ,含 、 、MgO等杂质)中提取两种工艺品的流程
如下:
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的方程式为_________.
(2)流程乙加入烧碱后生成Si 的离子方程式为________.
(3)验证滤液B含 ,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成份是________(填化学式),写出该溶液的一种用途________
(5)已知298K时, 的容度积常数 =5.6× ,取适量的滤液B,加入一定量
的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的 =_______.
答案(1)AlO + 6H+ 2Al3+ +3HO
2 3 2
(2)SiO + 2OH- SiO2 - + HO
2 3 2(3)硫氰化钾(或硫氰酸钾、苯酚溶液等合理答案)
(4)NaHCO;制纯碱或做发酵粉等合理答案
3
(5)5.6×10-10mol/L
【解析】本题考查铝土矿中氧化铝提取的工艺流程。(1)与HCl反应生成Al3+,应为铝土矿
中AlO。(2)SiO 可以溶于NaOH中生成NaSiO。(3)检验Fe3+的特征反应很多,如与
2 3 2 2 3
KSCN显血红色,与苯酚显紫色,与OH-显红褐色沉淀等。(4)生成E、K时,CO 均是过量的,
2
故应生成NaHCO。(5) , =5.6×10-12/(0.1)2=5.6×10-
3
10。
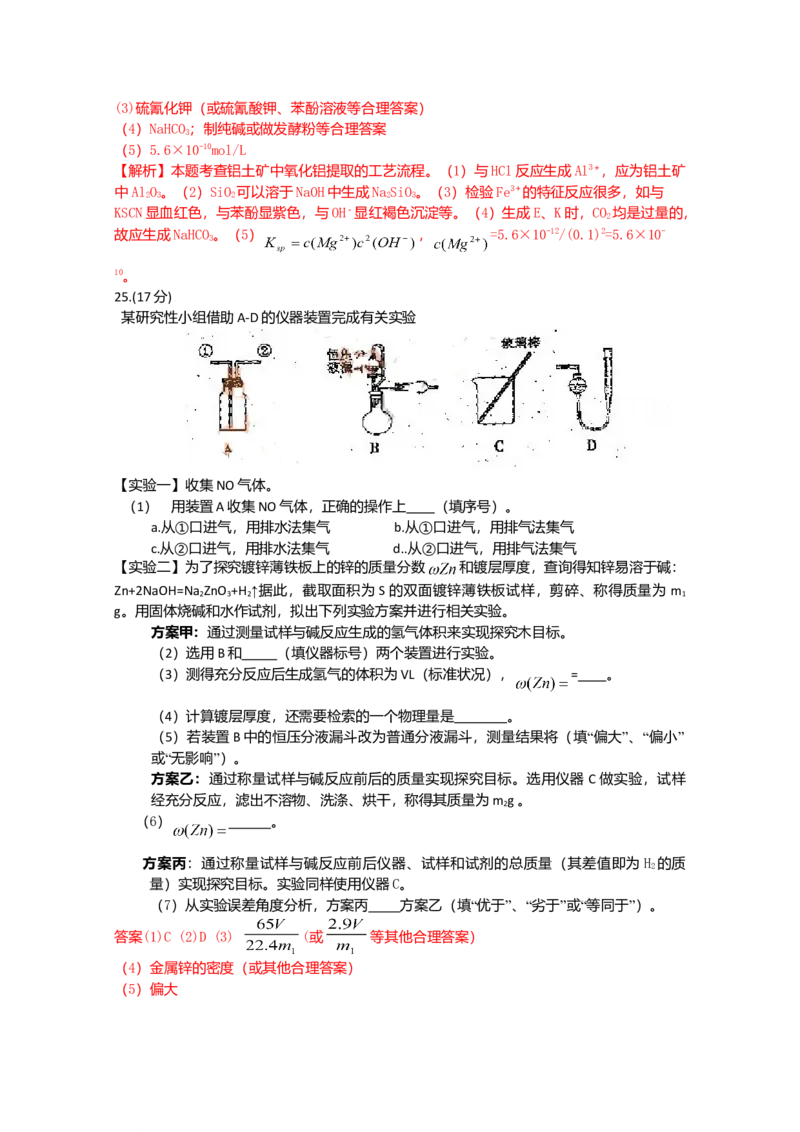
25.(17分)w.w.w.k.s.5.u.c.o.m
某研究性小组借助A-D的仪器装置完成有关实验
【实验一】收集NO气体。
(1) 用装置A收集NO气体,正确的操作上 (填序号)。
a.从①口进气,用排水法集气 b.从①口进气,用排气法集气
c.从②口进气,用排水法集气 d..从②口进气,用排气法集气
【实验二】为了探究镀锌薄铁板上的锌的质量分数 和镀层厚度,查询得知锌易溶于碱:
Zn+2NaOH=Na ZnO +H ↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为 m
2 3 2 1
g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标。
(2)选用B和 (填仪器标号)两个装置进行实验。
(3)测得充分反应后生成氢气的体积为VL(标准状况), = 。
(4)计算镀层厚度,还需要检索的一个物理量是 。
(5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”
或“无影响”)。
方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器 C做实验,试样
经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m g 。
2
(6) 。
方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H 的质
2
量)实现探究目标。实验同样使用仪器C。
(7)从实验误差角度分析,方案丙 方案乙(填“优于”、“劣于”或“等同于”)。
答案(1)C (2)D (3) (或 等其他合理答案)
(4)金属锌的密度(或其他合理答案)
(5)偏大(6) (或其他合理答案)
(7)劣于
【解析】本题考查实验的探究,涉及NO气体的收集,混合物中金属含量的计算等。(1)NO
遇空气立即被氧化,故不能用排空气法收集,只能用排水法收集。排水时应用短进长出。
(2)方案甲:Zn和Fe中只有Zn可以与NaOH产生气体,通过排水收集气体,依据反应方程
式即可算出Zn的质量分数。所以需要的装置有测H 的体积的D装置。(3)Zn与H 之间量为
2 2
1:1,则n(Zn)=V/22.4 mol,w (Zn)=m(Zn)/m = 。(4)有了Zn的质量,如果有密
1
度,则可以求出Zn的体积,再由Zn的截面积,即可求出Zn的高度(厚度)。(5)恒压式
分液漏斗产生的气体有部分残留在分液漏斗上方,故排气时收集少了,所以用普通漏斗时收
集的H 多一些,则计算出的Zn的量偏大。(6)减少的质量即为Zn的质量。(7)丙方案根
2
据H 的质量差值,显然误差大,因为产生的H 质量很小,计算偏差大。
2 2
30.[化学——物质结构与性质](13分)
Q、R、X、Y、Z五种元素的原子序数依次递增。已知: ①Z的原子序数为29,其余的均为短
周期主族元素; ②Y原子价电子(外围电子)排布msnmpn ③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:w.w.w.k.s.5.u.c.o.m
(1)Z2+ 的核外电子排布式是 。
(2)在[Z(NH ) ]2+离子中,Z2+的空间轨道受NH 分子提供的 形成配位键。
3 4 3
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲>乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4) Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 。
答案(1)1s22s22p63s23p63d9 (2)孤对电子(孤电子对)
(3)b (4)Si < C SiH。因为SiH 的相对分子质
4 4 4 4 4
量比CH 大,故分子间作用力大,沸点高。(4)C、N和Si中,C、Si位于同一主族,则上面
4
的非金属性强,故第一电离能大,而N由于具有半充满状态,故第一电离能比相邻元素大,
所以N>C>Si。(5)C、H形成的相对分子质量的物质为CH,结构式为H-C≡C-H,单键是σ
2 2
键,叁键中有两个是σ键一个π键,所以σ键与π键数之比为3:2。(6)电负性最大的
非元素是O,最小的非金属元素是Si,两者构成的SiO,属于原子晶体。
2
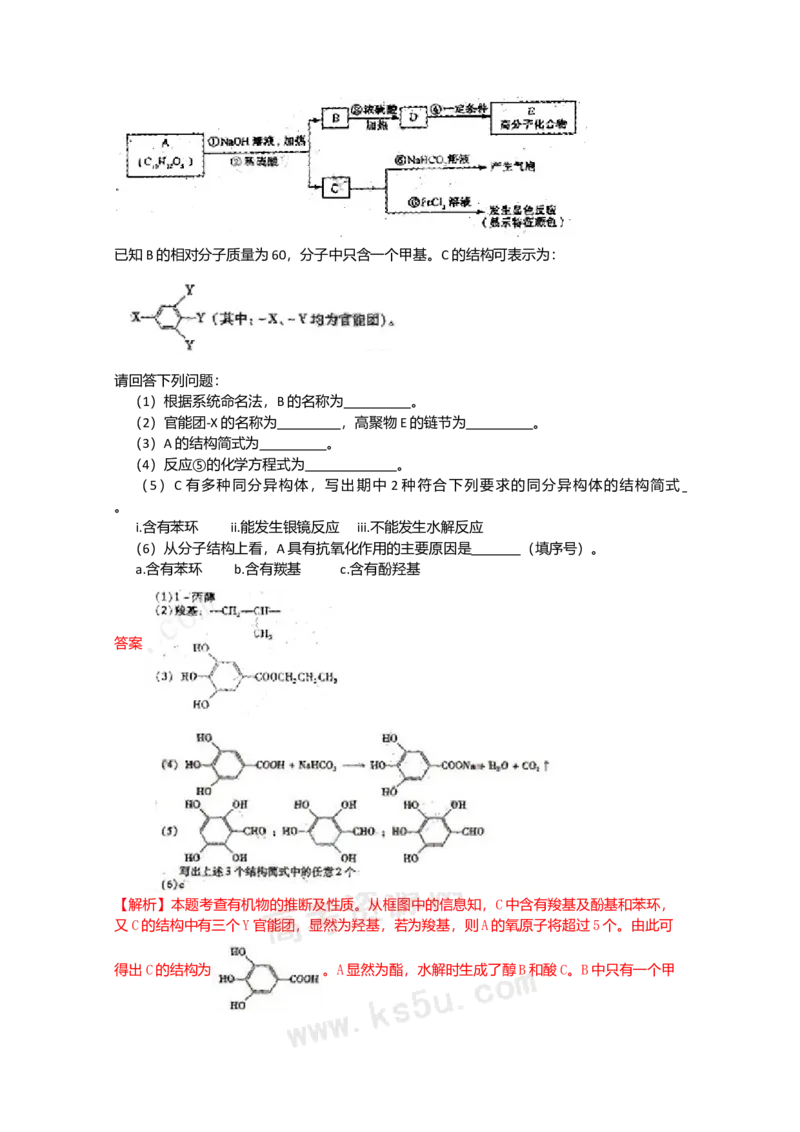
31. [化学——有机化学基础](13分)
有机物A是最常用的食用油氧化剂,分子式为C H O 可发生如下转化:
10 12 5,已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
请回答下列问题:
(1)根据系统命名法,B的名称为 。
(2)官能团-X的名称为 ,高聚物E的链节为 。
(3)A的结构简式为 。
(4)反应⑤的化学方程式为 。
(5)C 有多种同分异构体,写出期中 2 种符合下列要求的同分异构体的结构简式
。
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是 (填序号)。
a.含有苯环 b.含有羰基 c.含有酚羟基
答案
【解析】本题考查有机物的推断及性质。从框图中的信息知,C中含有羧基及酚基和苯环,
又C的结构中有三个Y官能团,显然为羟基,若为羧基,则A的氧原子将超过5个。由此可
得出C的结构为 。A显然为酯,水解时生成了醇B和酸C。B中只有一个甲基,相对分子质量为60,60-15-17=28,则为两上亚甲基,所以B的结构式为
CHCHCHOH,即1-丙醇。它在浓硫酸作用下,发生消去反应,可生成CHCH=CH,双键打开则
3 2 2 3 2
形成聚合物,其键节为 。由B与C的结构,不难写出酯A的结构简式为:
。C与NaHCO 反应时,只是羧基参与反应,由于酚羟基的酸性弱,
3
不可能使NaHCO 放出CO 气体。(5)C的同分异构体中,能发生银镜反应,则一定要有醛基,
3 2
不能发生水解,则不能是甲酸形成的酯类。显然,可以将羧基换成醛基和羟基在苯环作位置
变换即可。(6)抗氧化即为有还原性基团的存在,而酚羟基易被O 氧化,所以选C项。
2理科综合能力测试化学试题参考答案
第Ⅰ卷,共18小题,每小题6分,共108分。
一、选择题
6.C 7.B 8.C 9.A 10.B 11.D 12.D
23.(15分)
(1) (2)弱于
u 工