文档内容
2010年高考全国新课标(宁夏、吉林、黑龙江)理综化学试卷
一、选择题
1.(2010全国新课标)下列各项表达中正确的是( )
A.Na O 的电子式为
2 2
B.106g的乙醇和丙醇混合液完全燃烧生成的CO 为112L(标准状况)
2
C.在氮原子中,质子数为7而中子数不一定为7
D.Cl-的结构示意图为
2.(2010新课标)分子式为C H Cl 的同分异构体共有(不考虑立体异构)
3 6 2
( )
A.3种 B.4种 C.5种 D.6种
3.(2010全国新课标)下列各组中的反应,属于同一反应类型的是( )
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷消去制环己烯;由丙烯加溴制1,2-二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
4.(2010全国新课标)把500mL有BaCl 和KCl的混合溶液分成5等份,取
2
一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
( )
A.0.1(b-2a)mol/L B.10( 2a-b)mol/L
C.10(b-a)mol/L D.10(b-2a)mol/L
5.(2010全国新课标)己知:HCN(aq)与NaOH(aq)反应的∆H=-12.1kJ/mol;
HCl(aq)与NaOH(aq)反应的∆H=-55.6kJ/mol。则HCN 在水溶液中电离的∆H 等
于( )
A.-67.7 kJ/mol B.-43.5 kJ/mol C.+43.5 kJ/mol D.+67.7kJ/mol
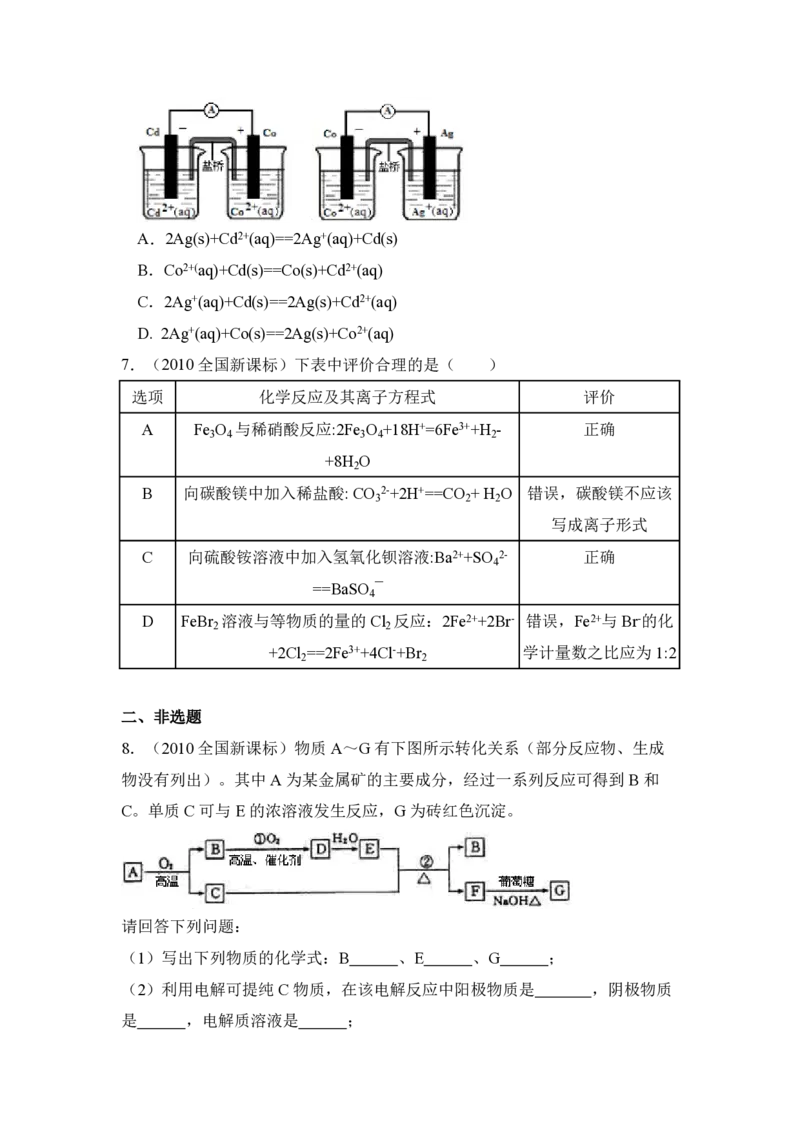
6.(2010全国新课标)根据下图,可判断出下列离子方程式中错误的是
( )A.2Ag(s)+Cd2+(aq)==2Ag+(aq)+Cd(s)
B.Co2+(aq)+Cd(s)==Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s)==2Ag(s)+Cd2+(aq)
D. 2Ag+(aq)+Co(s)==2Ag(s)+Co2+(aq)
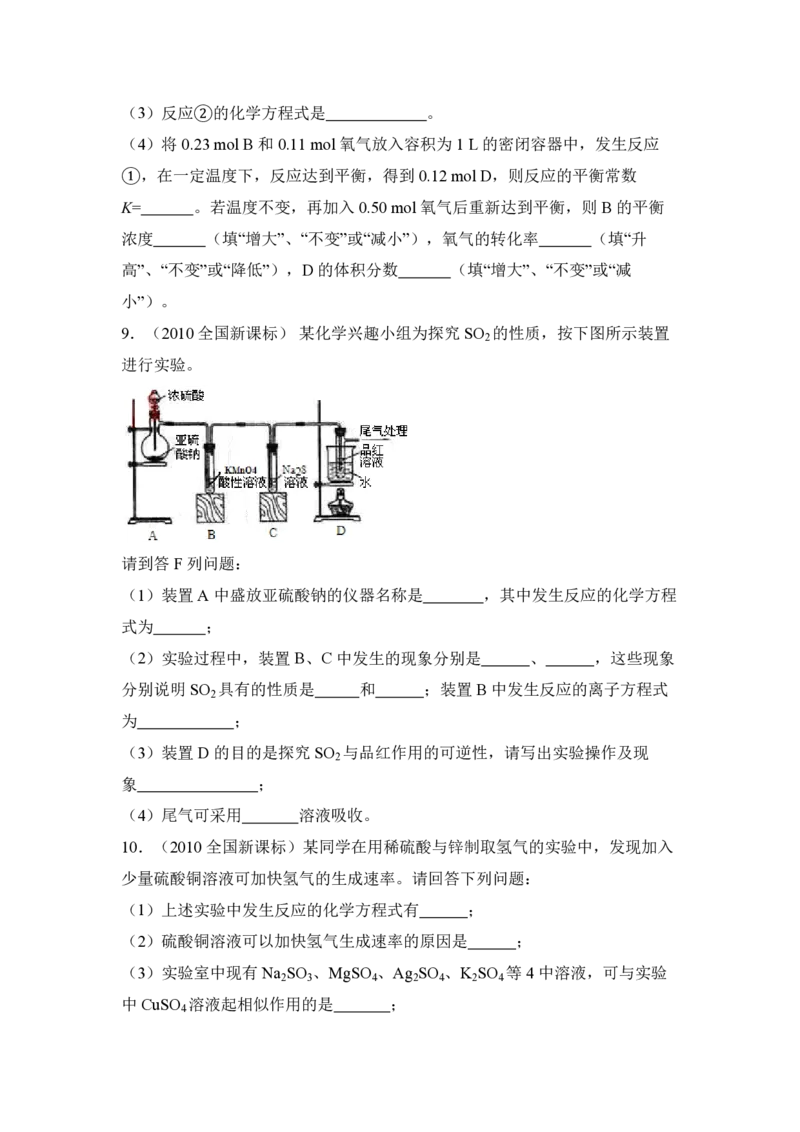
7.(2010全国新课标)下表中评价合理的是( )
选项 化学反应及其离子方程式 评价
A Fe O 与稀硝酸反应:2Fe O +18H+=6Fe3++H - 正确
3 4 3 4 2
+8H O
2
B 向碳酸镁中加入稀盐酸: CO 2-+2H+==CO + H O 错误,碳酸镁不应该
3 2 2
写成离子形式
C 向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO 2- 正确
4
==BaSO ¯
4
D FeBr 溶液与等物质的量的 Cl 反应:2Fe2++2Br- 错误,Fe2+与 Br-的化
2 2
+2Cl ==2Fe3++4Cl-+Br 学计量数之比应为 1:2
2 2
二、非选题
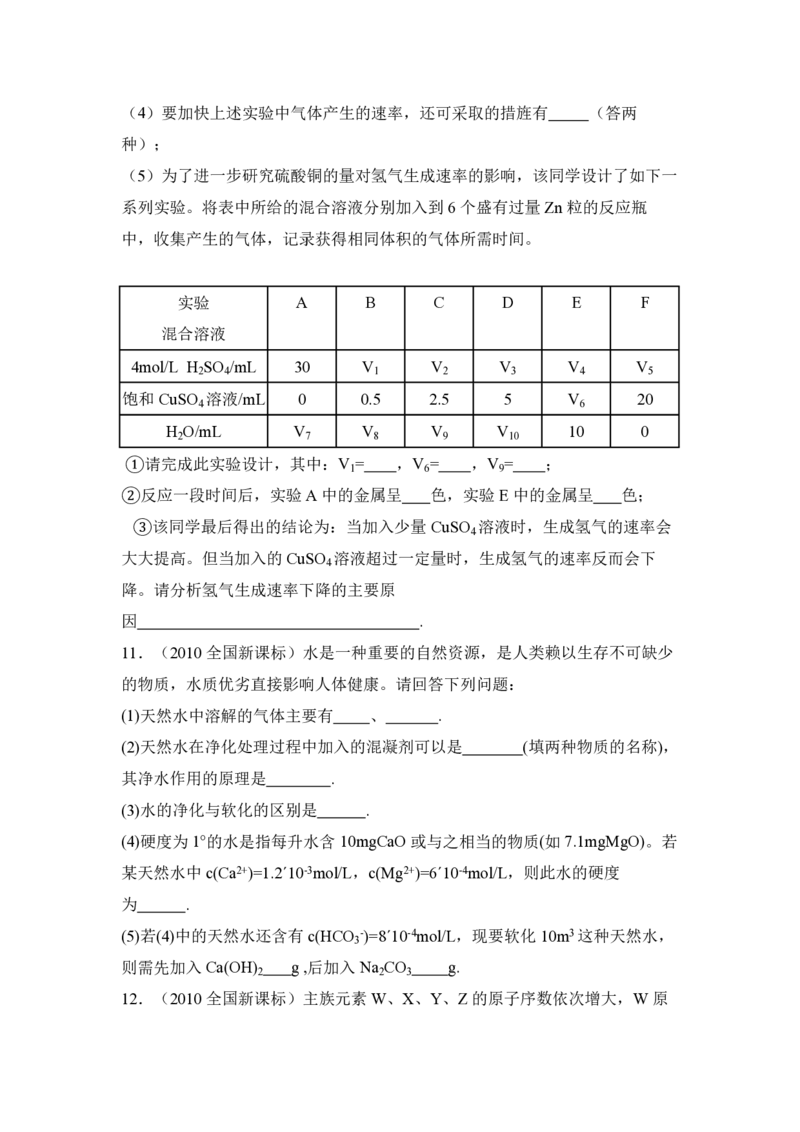
8.(2010全国新课标)物质A~G 有下图所示转化关系(部分反应物、生成
物没有列出)。其中A 为某金属矿的主要成分,经过一系列反应可得到B 和
C。单质 C可与 E的浓溶液发生反应,G 为砖红色沉淀。
请回答下列问题:
(1)写出下列物质的化学式:B 、E 、G ;
(2)利用电解可提纯C物质,在该电解反应中阳极物质是 ,阴极物质
是 ,电解质溶液是 ;(3)反应②的化学方程式是 。
(4)将0.23 mol B和0.11 mol氧气放入容积为1 L的密闭容器中,发生反应
①,在一定温度下,反应达到平衡,得到 0.12 mol D,则反应的平衡常数
K= 。若温度不变,再加入 0.50 mol氧气后重新达到平衡,则B的平衡
浓度 (填“增大”、“不变”或“减小”),氧气的转化率 (填“升
高”、“不变”或“降低”),D 的体积分数 (填“增大”、“不变”或“减
小”)。
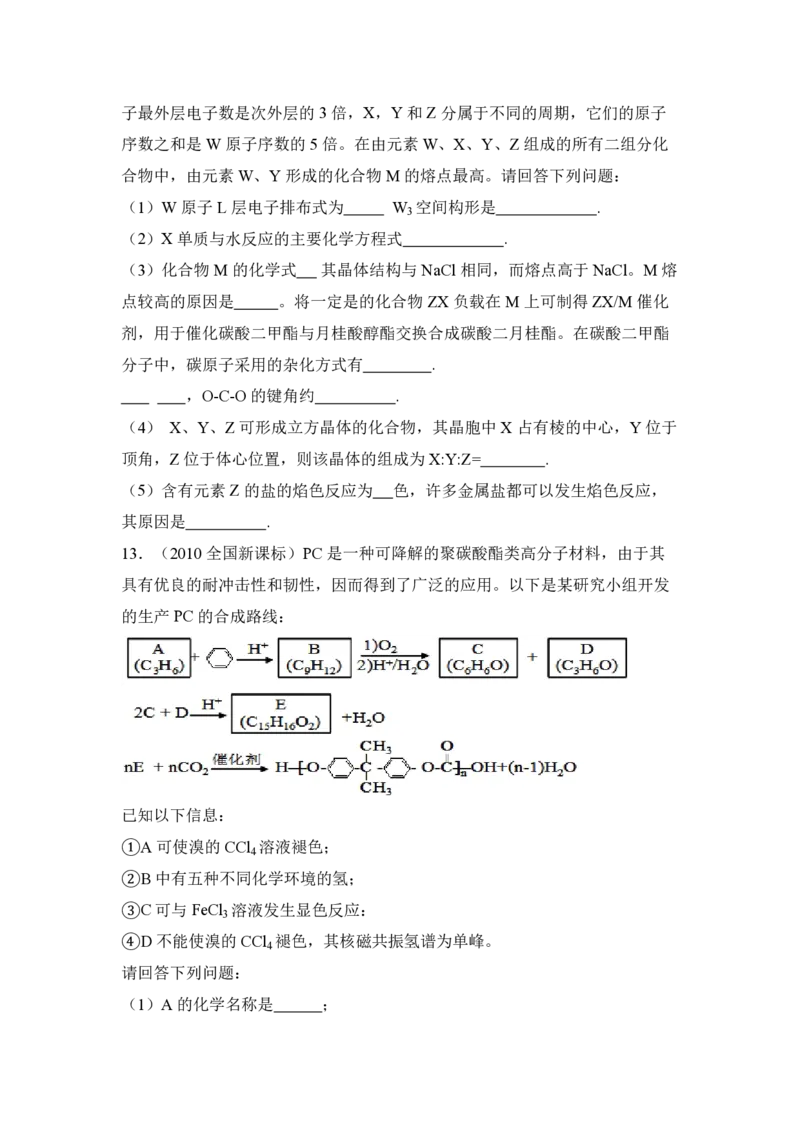
9.(2010全国新课标) 某化学兴趣小组为探究SO 的性质,按下图所示装置
2
进行实验。
请到答F 列问题:
(1)装置A 中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程
式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象
分别说明SO 具有的性质是 和 ;装置 B中发生反应的离子方程式
2
为 ;
(3)装置D 的目的是探究SO 与品红作用的可逆性,请写出实验操作及现
2
象 ;
(4)尾气可采用 溶液吸收。
10.(2010全国新课标)某同学在用稀硫酸与锌制取氢气的实验中,发现加入
少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)实验室中现有Na SO 、MgSO 、Ag SO 、K SO 等4中溶液,可与实验
2 3 4 2 4 2 4
中CuSO 溶液起相似作用的是 ;
4(4)要加快上述实验中气体产生的速率,还可采取的措旌有 (答两
种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一
系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶
中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 A B C D E F
混合溶液
4mol/L H SO /mL 30 V V V V V
2 4 1 2 3 4 5
饱和CuSO 溶液/mL 0 0.5 2.5 5 V 20
4 6
H O/mL V V V V 10 0
2 7 8 9 10
①请完成此实验设计,其中:V = ,V = ,V = ;
1 6 9
②反应一段时间后,实验 A 中的金属呈 色,实验E中的金属呈 色;
③该同学最后得出的结论为:当加入少量 CuSO 溶液时,生成氢气的速率会
4
大大提高。但当加入的CuSO 溶液超过一定量时,生成氢气的速率反而会下
4
降。请分析氢气生成速率下降的主要原
因 .
11.(2010全国新课标)水是一种重要的自然资源,是人类赖以生存不可缺少
的物质,水质优劣直接影响人体健康。请回答下列问题:
(1)天然水中溶解的气体主要有 、 .
(2)天然水在净化处理过程中加入的混凝剂可以是 (填两种物质的名称),
其净水作用的原理是 .
(3)水的净化与软化的区别是 .
(4)硬度为 1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若
某天然水中c(Ca2+)=1.2´10-3mol/L,c(Mg2+)=6´10-4mol/L,则此水的硬度
为 .
(5)若(4)中的天然水还含有c(HCO -)=8´10-4mol/L,现要软化 10m3这种天然水,
3
则需先加入Ca(OH) g ,后加入Na CO g.
2 2 3
12.(2010全国新课标)主族元素W、X、Y、Z的原子序数依次增大,W原子最外层电子数是次外层的3倍,X,Y 和Z分属于不同的周期,它们的原子
序数之和是W原子序数的 5倍。在由元素W、X、Y、Z组成的所有二组分化
合物中,由元素W、Y 形成的化合物 M 的熔点最高。请回答下列问题:
(1)W原子L层电子排布式为 W 空间构形是 .
3
(2)X 单质与水反应的主要化学方程式 .
(3)化合物M 的化学式 其晶体结构与NaCl相同,而熔点高于NaCl。M 熔
点较高的原因是 。将一定是的化合物ZX 负载在M 上可制得ZX/M催化
剂,用于催化碳酸二甲酯与月桂酸醇酯交换合成碳酸二月桂酯。在碳酸二甲酯
分子中,碳原子采用的杂化方式有 .
,O-C-O 的键角约 .
(4) X、Y、Z可形成立方晶体的化合物,其晶胞中X 占有棱的中心,Y 位于
顶角,Z位于体心位置,则该晶体的组成为X:Y:Z= .
(5)含有元素Z的盐的焰色反应为 色,许多金属盐都可以发生焰色反应,
其原因是 .
13.(2010全国新课标)PC 是一种可降解的聚碳酸酯类高分子材料,由于其
具有优良的耐冲击性和韧性,因而得到了广泛的应用。以下是某研究小组开发
的生产PC 的合成路线:
已知以下信息:
①A 可使溴的CCl 溶液褪色;
4
②B 中有五种不同化学环境的氢;
③C 可与FeCl 溶液发生显色反应:
3
④D 不能使溴的CCl 褪色,其核磁共振氢谱为单峰。
4
请回答下列问题:
(1)A 的化学名称是 ;(2)B 的结构简式为 ;
(3)C 与D 反应生成E的化学方程式为 ;
(4)D 有多种同分异构体,其中能发生银镜反应的是 (写出结构简式);
(5)B 的同分异构体中含有苯环的还有 种,其中在核磁共振氢谱中出
现丙两组峰,且峰面积之比为3:1的是 (写出结构简式)。