文档内容
2010年四川省高考理综试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 Ca 40 Mn
55 Fe 56 Co 59 Cu 64 Br 80 Ba 137
1.(2010四川高考)节能减排对发展经济、保护环境有重要意义。下列措施不能减少二
氧化碳排放的是
A.利用太阳能制氢 B.关停小火电企业
C.举行“地球一小时”熄灯活动 D.推广使用煤液化技术
2.(2010四川高考)N 表示阿伏伽德罗常数的值,下列说法正确的是
A
A.标准状况下,22.4L二氯甲烷的分子数约为N 个
A
B.盛有SO 的密闭容器中含有N 个氧原子,则SO 的物质的量为0.5mol
2 A 2
C.17.6g丙烷中所含的极性共价键为4N 个
A
D.电解精炼铜时,若阴极得到电子数为2N 个,则阳极质量减少 64g
A
3.(2010四川高考)下列说法正确的是
A.原子最外层电子数为2的元素一定处于周期表第ⅡA族
B.主族元素X、Y能形成XY 型化合物,则X与Y的原子序数之差可能为2或5
2
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
4.(2010四川高考)下列离子方程式书写正确的是
A.向明矾溶液中加入过量的氢氧化钡溶液:
Al3+ + 2SO2-+2Ba2+ + 4OH-= 2BaSO↓+ AlO-+ 2HO
4 4 2 2
B.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH) + 2H+ = Fe2+ + 2HO
2 2
C.向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH+ + OH-= NH∙HO
4 3 2
D.向CHBrCOOH中加入足量的氢氧化钠溶液并加热:
2
CHBrCOOH + OH-CHBrCOO-+ HO
2 2 2
5.(2010四川高考)有关①100mL0.1mol/LNaHCO、②100mL0.1mol/LNaCO 两种溶液的
3 2 3
叙述不正确的是
A.溶液中水电离出的H+个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO2-)>c(HCO) D.②溶液中:c(HCO-)>c(HCO)
3 2 3 3 2 3
6.(2010四川高考)中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:
下列叙述正确的是
A.M的相对分子质量是180
B.1molM最多能与2molBr 发生反应
2
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为CHONa
9 4 5 4
D.1molM与足量NaHCO 反应能生成2molCO
3 27.(2010四川高考)标准状况下V L氨气溶解在1L水中(水的密度近似为1g/mL),所
得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确
的是
A.ρ = (17V + 22400) / (22.4 + 22.4V) B.ω = 17c / (1000ρ)
C.ω = 17V / (17V + 22400) D.c = 1000Vρ /(17V + 22400)
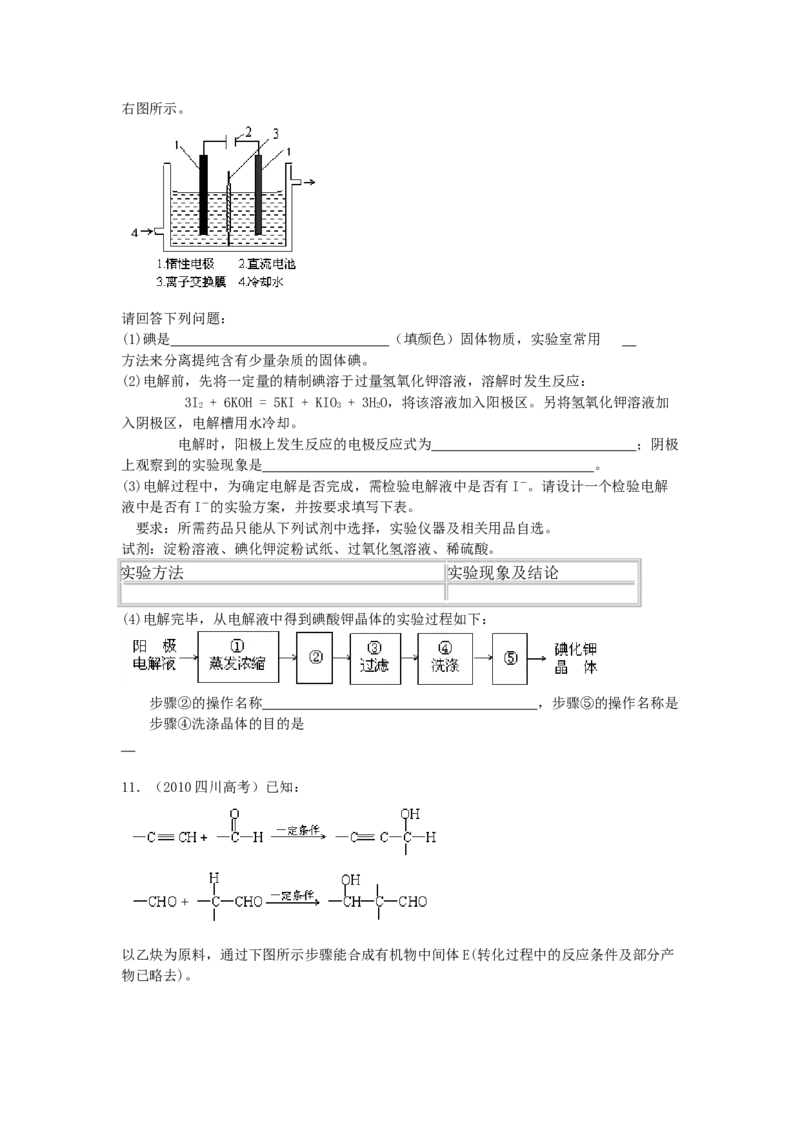
8.(2010四川高考)反应aM(g)+bN(g) cP(g)+dQ(g)达到平衡时。M的体积分数y(M)
与反应条件的关系如图所示。其中z表示反应开始时N的物质的量与M的物质的量之比。
下列说法正确的是
A.同温同压同Z时,加入催化剂,平衡时Q的体积分数增加
B.同压同Z时,升高温度,平衡时Q的体积分数增加
C.同温同Z时,增加压强,平衡时Q的体积分数增加
D.同温同压时,增加Z,平衡时Q的体积分数增加。
9.(2010四川高考)短周期元形成的常见非金属固体单质A与常见金属单质B,在加热条
件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,又能溶于
强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢
氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H
与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第 周期,第 族。
(2)B与氢氧化钠溶液反应的化学方程式为:
(3)C与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化物为
,当生成2mol二氧化氯时,转移电子 mol
(4)溶液F在空气中长期放置生成H的化学方程式为:
。
(5)H的溶液与稀硫酸反应产生的现象为
。
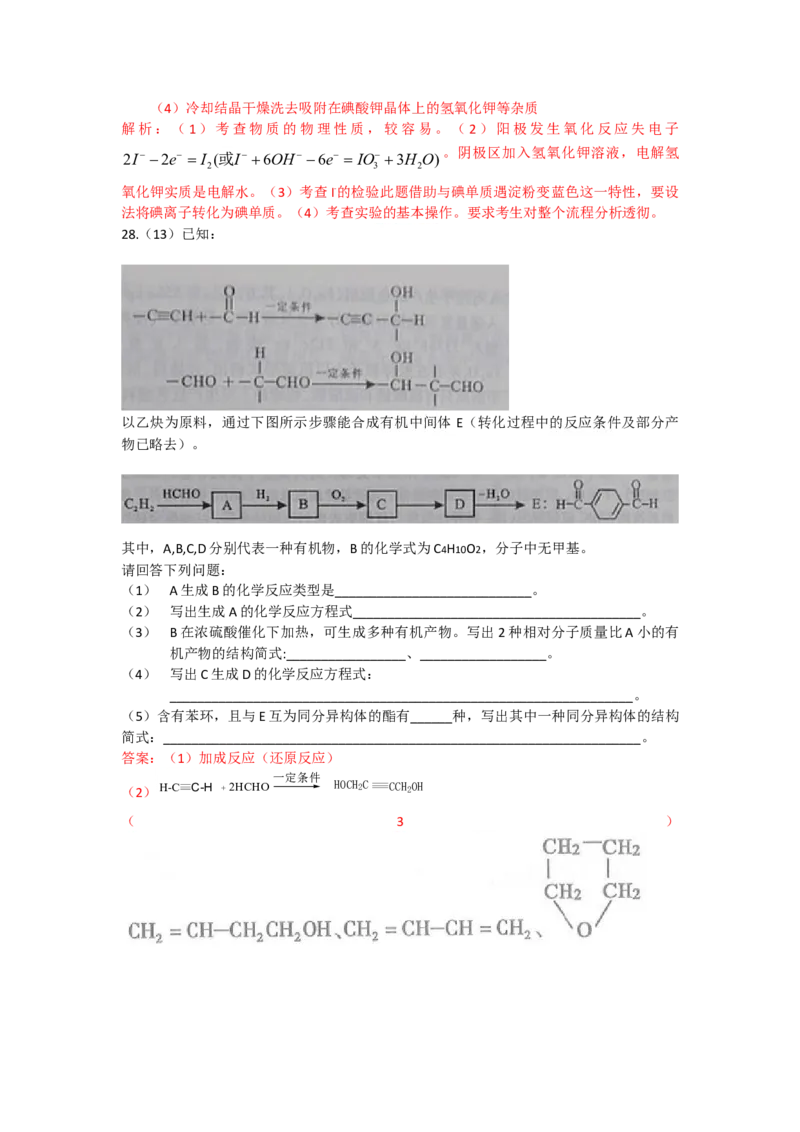
10.(2010四川高考)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸
钾(KIO)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中
3
与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如右图所示。
请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用
方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I + 6KOH = 5KI + KIO + 3HO,将该溶液加入阳极区。另将氢氧化钾溶液加
2 3 2
入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为 ;阴极
上观察到的实验现象是 。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解
液中是否有I-的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
实验方法 实验现象及结论
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
步骤②的操作名称 ,步骤⑤的操作名称是
步骤④洗涤晶体的目的是
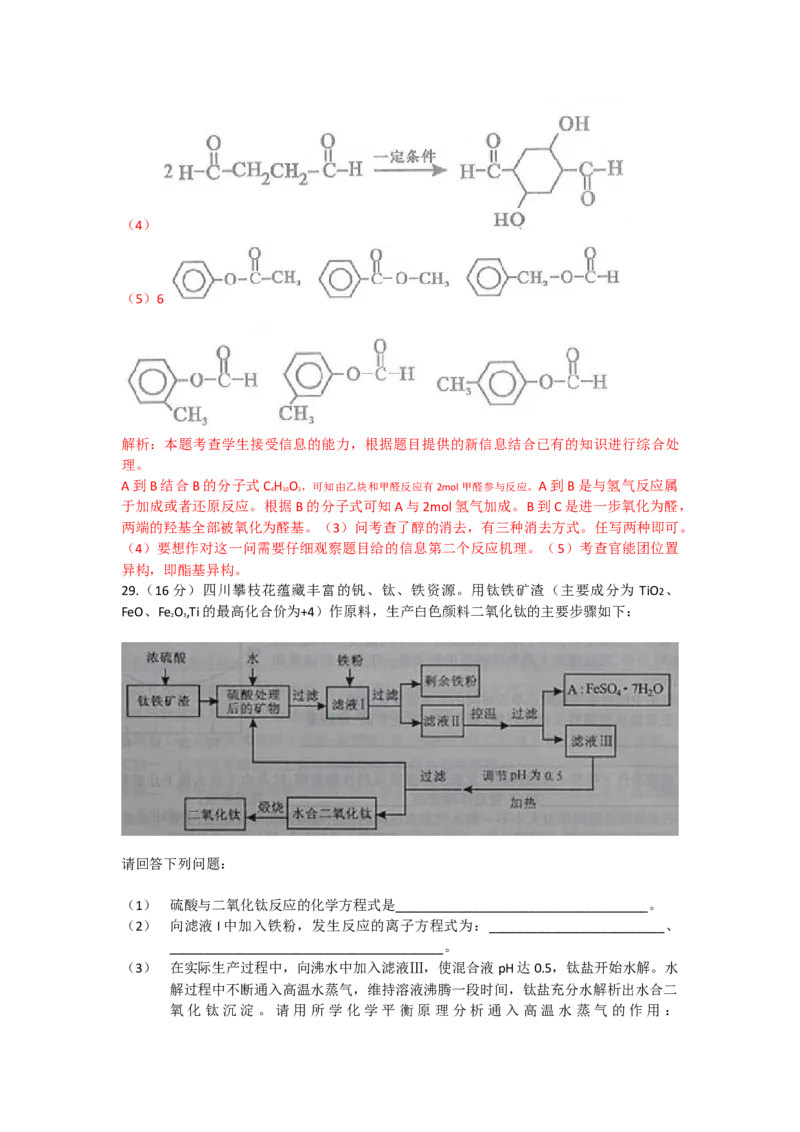
11.(2010四川高考)已知:
以乙炔为原料,通过下图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产
物已略去)。其中,A、B、C、D分别代表一种有机物;B的化学式为CH O,分子中无甲基。
4 10 2
请回答下列问题:
(1)A生成B的化学反应类型是 。
(2)写出生成A的化学方程式: 。
(3)B在浓硫酸催化下加热,可生成多种有机产物。写出两种相对分子质量比A小的有机产
物的结构简式:
、 。
(4)写出C生成D的化学反应方程式: 。
(5)含有苯环,且与E互为同分异构体的酯有 种,写出其中一种同分异构体的
结构简式: 。
12.(2010四川高考)四川攀枝花蕴藏丰富的钒、钛、铁资源。用钛铁矿渣(主要成分为
TiO、FeO、FeO,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的主要步骤如下:
2 2 3
请回答下列问题:
(1)硫酸与二氧化钛反应的化学方程式是 。
(2)向滤液Ⅰ中加入铁粉,发生反应的离子方程式为:
、 。
(3)在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液pH达0.5,钛盐开始水解。水解
过程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二氧化钛沉
淀。请用所学化学平衡原理分析通入高温水蒸气的作用:
。过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐、
、 、 (填化学式),
减少废物排放。
(4)A可用于生产红色颜料(FeO),其方法是:将556a kg A(摩尔质量为278g/mol)溶于水
2 3
中,加入过量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体,再向红
褐色胶体中加入3336b kg A和112c kg铁粉,鼓入足量空气搅拌,反应完全后,有大量
FeO 附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料,若所得滤
2 3
液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料 kg。《2010年四川省高考理综试题》参考答案
1.D
2.B
3.B
4.A
5.C
6.C
7.A
8.B
9.(1)三 ⅥA
(2) 2Al + 2NaOH + 2HO = 2NaAlO + 3H↑
2 2 2
(3)硫酸钠(NaSO) 2
2 4
(4) 4NaS + O + 2HO = 4NaOH + 2NaS
2 2 2 2 2
(或2NaS + O + 2HO = 4NaOH + 2S NaS + S = NaS)
2 2 2 2 2 s
(5)溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
10.(1)紫黑色;升华
(2) 2I-—2e-= I (I-+ 6OH-—6e-= IO-+ 3HO)
2 3 2
有气泡产生
(3)
实验方法 实验现象及结论
取少量阳极区电解液于试管中,加稀硫 如果不变蓝,说明电解液中无I
酸酸化的过氧化氢溶液,再加入几滴淀 -。(如果变蓝,说明电解液中有
粉试液,观察溶液是否变蓝。 I-。)
(4)冷却结晶;干燥;洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
11.(1)加成反应(还原反应)
(2)
(3) CH=CH—CHCHOH、CH=CH—CH=CH、
2 2 2 2 2
(4)
(5) 612.(1) TiO + 2HSO = Ti(SO) + 2HO或TiO + HSO = TiOSO + HO
2 2 4 2 4 2 2 2 2 4 4 2
(2) Fe + 2Fe3+ = 3Fe2+ Fe + 2H+ = Fe2+ + H↑
2
(3)加水促进钛盐水解,加热促进钛盐水解,降低H+浓度促进钛盐水解
HO FeSO HSO
2 4 2 4
(4) 160a + 320b + 160c
2010 年普通高等学校招生全国统一考试(四川卷)
理科综合能力测试(化学部分)
第 I 卷
6.节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是
A.利用太阳能制氢B.关停小火电企业
C.举行“地球一小时”熄灯活动D.推广使用煤液化技术
答案:D
解析:本题考查化学与社会的关系;利用太阳能制氢,减少了化石燃料的使用,同时也减
少了CO 的排放,A项符合;火力发电消耗大量的煤炭资源,同时会排放出CO 及有害气体,
2 2
关停小火电企业,有利用节能减排,B项符合;举行“地球一小时”熄灯活动有效的节约
的能源,C项符合;煤液化技术,提高了煤的利用率,但不能减少CO 的排放,D项不符合。
2
7. 表示阿伏加德罗常数的值,下列说法正确的是
N
w_ww.k#s5_u.co*m
A
A.标准状况下,22.4L二氯甲烷的分子数约为
N
个
A
B.盛有
SO
的密闭容器中含有
N
个氧原子,则
SO
的物质的量为0.5mol
2 A 2
C.17.6g丙烷中所含的极性共价键为 个
4N
AD.电解精炼铜时,若阴极得到电子数为 个,则阳极质量减少64g
2N
A
答案:B
解析:本题考查微粒数与物质的量、物质的质量等的关系;二氯甲烷在标况下为液态,
22.4L不一定为1mol,A项错误;1molSO
2
中含有氧原子2mol,故含有
N
个氧原子的
SO
的
A 2
物质的量为0.5mol,B项正确;17.6g丙烷的物质的量为0.4mol,1mol丙烷中含有极性键
8mol,故0.4mol中含有极性键3.2mol,为3.2N 个,C项错误;精炼铜时,阳极为粗铜,
A
当转移2mol电子时,阳极消耗的质量不一定为64g,D项错误。
8.下列说法正确的是
w_ww.k#s5_u.co*m
A.原子最外层电子数为2的元素一定处于周期表IIA族
B.主族元素X、Y能形成 型化合物,则X与Y的原子序数之差可能为2或5
XY
2
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
答案:B
解析:本题考查物质结构知识;本题可用举例法,氦原子最外层电子数为2,为零族,A项
错误;MgCl 中原子序数之差为5,CO 中原子充数之差为2,B项正确;由于HF中存在氢键,
2 2
故HF的沸点比HCl的高,C项错误;第IA中H O为分子晶体,其它碱金属氧化物为离子晶
2
体,D项错误。
9.下列离子方程式书写正确的是
w_ww.k#s5_u.co*m
A.向明矾溶液中加入过量的氢氧化钡溶液:
Al3 2SO 2 2Ba2 4OH 2BaSO AlO 2H O
4 4 2 2
B.向氢氧化亚铁中加入足量的稀硝酸: FeOH 2H Fe2 2H O
2 2
C.向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:
NH OH NH H O
4 3 2
D.向 中加入足量的氢氧化钠溶液并加热:
CH BrCOOH
2
CH BrCOOH OH CH BrCOO H O
2 2 2
答案:A
解析:本题考查离子方程式正误判断;氢氧化钡溶液过量,Al3+转化为AlO -,SO 2-完全转化
2 4
为沉淀,A项正确;硝酸有强氧化性,可将Fe2+氧化为Fe3+,硝酸被还原为NO,B不符合客
观事实,错误;在磷酸二氢铵中加入足量的氢氧化钠,磷酸二氢根离子中的氢将被中和,C
项错误; 中存在两种官能团,分别是-Br和-COOH,加入足量的氢氧化钠后加
CH BrCOOH
2
热,与-COOH发生中和反应,与-Br发生水解反应,故应该生成CH OHCOO-,D项错误。
2
10.有关①100ml0.1mol/L 、②100ml0.1mol/L 两种溶液的叙述不正确的是
NaHCO Na CO
3 2 3
A.溶液中水电离出的H个数:②>①B.溶液中阴离子的物质的量浓度之和:②>①C.①溶液中:c CO2 cH CO D.②溶液中:c HCO cH CO
3 2 3 3 2 3
答案:C
ww_w.k*s*5*u.co_m
解析:本题考查盐类水解知识;盐类水解促进水的电离,且Na CO 的水解程度更大,碱性更
2 3
强,故水中电离出的H+个数更多,A项正确;B②钠离子的物质的量浓度为0.2mol/L而①
钠离子的物质的量浓度为0.1mol/L根据物料守恒及电荷守恒可知溶液中阴离子的物质的量
浓度之和:②>①,B项正确;C项 水解程度大于电离所以C(H CO )>C(CO2-)D项
NaHCO 2 3 3
3
C0 2-分步水解第一步水解占主要地位且水解大于电离。判断D正确。C、D两项只
Na CO 3
2 3
要写出它们的水解及电离方程式即可判断。
11.中药狼把草的成分之一M具有清炎杀菌作用,M的结构如图所示:
w_ww.k#s5_u.co*m
下列叙述正确的是
A..M的相对分子质量是180
B.1molM最多能与2mol 发生反应
Br
2
C.M与足量的 溶液发生反应时,所得有机产物的化学式为
NaOH C H O Na
9 4 5 4
D.1molM与足量 反应能生成2mol
NaHCO CO w_ww.k#s5_u.co*m,
3 2
答案:C
ww_w.k*s*5*u.co_m
解析:本题考查有机物的性质:A项M的分子式为:C O H 其相对分子质量是 178,B项
9 4 6
1molM最多能与3mol 发生反应,除了酚羟基临位可以发生取代,还有碳碳双键可以
Br
2
发生加成。C项除了酚羟基可以消耗2molNaOH ,酯基水解也消耗1molNaOH ,水解又
生成1mol酚羟基还要消耗1molNaOH 所以共计消耗4molNaOH .D项酚与碳酸氢钠不
反应。所以此题选择C
12.标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为pg/ml,
质量分数为ω,物质浓度为cmol/L,则下列关系中不正确的是
A. p 17V 22400/22.422.4VB. W 17c/1000
C. W 17V /17V 22400D.C=1000Vρ/(17V+22400)
答案:A
解析:本题考查基本概念。考生只要对基本概念熟悉,严格按照基本概念来做,弄清质量
分数与物质的量浓度及密度等之间的转化关系即可。
ww_w.k*s*5*u.co_m
13.反应aM(g)+bN(g) cP(g)+dQ(g)达到平衡时。M的
体积分数y(M)与反应条件的关系如图所示。其中:Z表示反应开始时N的物质的量与M的物质的量之比。下列说法正确的是
A.同温同压Z时,加入催化剂,平衡时Q的体积分数增加
B.同压同Z时,升高温度,平衡时Q的体积分数增加
C.同温同Z时,增加压强,平衡时Q的体积分数增加
D.同温同压时,增加Z,平衡时Q的体积分数增加。
答案:B
解析:本题考查了平衡移动原理的应用。A项加入催化剂只能改变反应速率,不会使平衡
移动。B项由图像(1)知随着温度的升高M的体积分数降低,说明正反应吸热,所以温度
升高平衡正向移动,Q的体积分数增加。C项对比(1)(2)可以看出相同温度条件,压
强增大M的体积分数增大,所以正反应是体积缩小的反应,增大压强Q的体积分数减小。
D项由C项可以判断D也不对。
26.(15分) 短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下
w_ww.k#s5_u.c
反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。
E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠
溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧
化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第 周期,第 族。
w_ww.k#s5_u.co*m
(2)B与氢氧化钠溶液反应的化学方程式为:
。
(1) G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为
,当生成2mol二氧化氯时,转移电子 mol。
(2) 溶液F在空气中长期放置生成H的化学反应方程式为:
。
(3) H的溶液与稀硫酸反应产生的现象为
。
26.答案:(1)三ⅥA
ww_w.k*s*5*u.co_m
(2)
2Al+2NaOH+2H O=2NaAlO 3H
2 2 2
(3)硫酸钠( )2
Na SO
2 4
(4)
4Na S O 2H O 4NaOH 2Na S
2 2 2 2 2
(或 )
2Na S O 2H O 4NaOH 2S Na S S Na S
2 2 2 2 2 2
(5)溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
解析:本题考查的知识点有元素及其化合物的性质、物质结构、氧化还原反应相关计算。
由生成白色沉淀D,D既能溶于强酸,也能溶于强碱,推测D是Al(OH)
3
再逆推可知,B为Al。G在大气中能导致酸雨的形成,可猜测G可能为SO
2
逆推可知:A为S,综合可知C为Al S D为Al(OH) ,E为H S,G为SO
2 3 3 2 2
F为NaS.
2
(1)(2)比较简单,(3)SO 与氯酸钠在酸性条件下反应,SO 为还原剂
2 2
被氧化为SO 2-,根据电子得失可以判断生成2mol二氧化氯时,转移电子2mol。
4由H与过氧化钠的结构和化学性质相似,其溶液显黄色。
结合前面的信息可以推测H为NaS.
2 2
27.(16分)
w_ww.k#s5_u.co*m
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。
碘酸钾(KIO)是国家规定的食盐加碘剂,它的晶体为白色,可溶
3
于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质
碘。以碘为原料,通过电解制备碘酸钾的实验装置如右图所示。
请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用
方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I+6KOH=5KI+KIO+3HO,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽
2 3 2
用水冷却。
电解时,阳极上发生反应的电极反应式为 ;阴
极 上 观 察 到 的 实 验 现 象 是
。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I—。请设计一个检验电解
液中是否有I—的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
w_ww.k#s5_u.co*m
实验方法 实验现象及结论
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
步骤②的操作名称是 ,步骤⑤的操作名称是 。
步骤④洗涤晶体的目的是
。
答案:(1)紫黑色升华
ww_w.k*s*5*u.co_m
(2)
2I 2e I (或I 6OH 6e IO 3H O)
2 3 2
有气泡产生
(3)
实验方法 实验现象及结论
取少量阳极区电解液于试管中,加稀硫酸酸化后加
如果不变蓝,说明无I。(如果
入几滴淀粉试液,观察是否变蓝。 变蓝,说明有I。)(4)冷却结晶干燥洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
解析:(1)考查物质的物理性质,较容易。(2)阳极发生氧化反应失电子
。阴极区加入氢氧化钾溶液,电解氢
2I 2e I (或I 6OH 6e IO 3H O)
2 3 2
氧化钾实质是电解水。(3)考查I-的检验此题借助与碘单质遇淀粉变蓝色这一特性,要设
法将碘离子转化为碘单质。(4)考查实验的基本操作。要求考生对整个流程分析透彻。
28.(13)已知:
w_ww.k#s5_u.co*m
以乙炔为原料,通过下图所示步骤能合成有机中间体 E(转化过程中的反应条件及部分产
物已略去)。
w_ww.k#s5_u.co*m
其中,A,B,C,D分别代表一种有机物,B的化学式为C4H10O2 ,分子中无甲基。
请回答下列问题:
(1) A生成B的化学反应类型是____________________________。
(2) 写出生成A的化学反应方程式_________________________________________。
(3) B在浓硫酸催化下加热,可生成多种有机产物。写出2种相对分子质量比A小的有
机产物的结构简式:_________________、__________________。
(4) 写出C生成D的化学反应方程式:
__________________________________________________________________。
(5)含有苯环,且与E互为同分异构体的酯有______种,写出其中一种同分异构体的结构
简式:____________________________________________________________________。
答案:(1)加成反应(还原反应)
ww_w.k*s*5*u.co_m
一定条件
(2)H-C C-H + 2HCHO HOCH 2 C CCH2OH
( 3 )(4)
(5)6
解析:本题考查学生接受信息的能力,根据题目提供的新信息结合已有的知识进行综合处
理。
A到B结合B的分子式CH O,可知由乙炔和甲醛反应有2mol甲醛参与反应。A到B是与氢气反应属
4 10 2
于加成或者还原反应。根据B的分子式可知A与2mol氢气加成。B到C是进一步氧化为醛,
两端的羟基全部被氧化为醛基。(3)问考查了醇的消去,有三种消去方式。任写两种即可。
(4)要想作对这一问需要仔细观察题目给的信息第二个反应机理。(5)考查官能团位置
异构,即酯基异构。
29.(16分)四川攀枝花蕴藏丰富的钒、钛、铁资源。用钛铁矿渣(主要成分为 TiO2 、
FeO、FeO,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的主要步骤如下:
2 3 w_ww.k#s5_u.co*m
请回答下列问题:
w_ww.k#s5_u.co*m
(1) 硫酸与二氧化钛反应的化学方程式是____________________________________。
(2) 向滤液I中加入铁粉,发生反应的离子方程式为:_________________________、
_______________________________________。
(3) 在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液pH达0.5,钛盐开始水解。水
解过程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二
氧化钛沉淀。请用所学化学平衡原理分析通入高温水蒸气的作用:_______________________________________________。
过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐
___________、______________、_______________________(填化学式),减少废物排放。
(4)A可用于生产红色颜料(FeO),其方法是:将556akgA(摩尔质量为278g/mol)溶于
2 3
水中,加入适量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体;再向
红褐色胶体中加入3336bkgA和112ckg铁粉,鼓入足量空气搅拌,反应完成后,有大量
FeO 附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤
2 3
液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料_______________________kg。
答案:(1) 或
TiO 2H SO Ti(SO ) 2H O TiO H SO TiOSO H O
2 2 4 4 2 2 2 2 4 4 2
(2) Fe2Fe3 3Fe2 Fe2H Fe2 H
2
(3)加水促进钛盐水解,加热促进钛盐水解,降低H浓度促进钛盐水解
H O FeSO H SO
2 4 2 4
(4)160a320b160c
ww_w.k*s*5*u.co_m
解析:本题属于化工生产流程题。(1)考查酸的通性,可以与金属氧化物反应,又知道TI
的化合价,可以写出化学方程式。(2)加入浓硫酸后,浓硫酸可以氧化亚铁离子,再加入
铁粉,铁粉可以还原铁离子。除此外,铁粉还可以与溶液中的H+反应、(3)考查了影响
盐类水解的因素。(4)考虑最后溶质是只有硫酸钠和硫酸铁,根据开始加入 A 为
2a×103mol 加入适量氢氧化钠溶液恰好完全反应.,说明加入氢氧化钠的物质的量为
4a×103mol,后来又加入12b×103mol的A,和2c×103mol的铁。根据电荷守恒,溶质中硫
酸钠消耗硫酸根离子为 2a×103mol,。而溶液中加入的硫酸根离子物质的量共计为
(2a+12b)×103mol,这样剩下的硫酸根就与铁离子结合。可知消耗铁离子为 8b×103mol,
根 据 铁 元 素 守 恒 。 nFe=(2a+4b+2c)×103mol,nFeO=(a+2b+c) ×103mol, 计 算 得 mFeO=
2 3 2 3
160a320b160ckg.