文档内容
2010 年山东省高考化学试卷
参考答案与试题解析
一、选择题(共7小题,每小题4分,满分28分)
1.(4分)(2010•山东)16O和18O是氧元素的两种核素,N 表示阿伏加德罗常数,下列
A
说法正确的是( )
A.16O 与18O 互为同分异构体
2 2
B.16O 与18O 核外电子排布方式不同
2 2
C.通过化学变化可以实现16O与18O间的相互转化
D.标准状况下,1.12L 16O 和1.12L 18O 均含0.1N 个氧原子
2 2 A
2.(4分)(2010•山东)下列与化学反应能量变化相关的叙述正确的是( )
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H (g)+Cl (g)═2HCl(g)在光照和点燃条件下的△H不同
2 2
3.(4分)(2010•山东)下列说法正确的是( )
A.形成离子键的阴阳离子间只存在静电吸引力
B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
4.(4分)(2010•山东)下列叙述错误的是( )
A.乙烯和苯都能使溴水褪色,褪色的原因相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na CO 溶
2 3
液除去
5.(4分)(2010•山东)下列推断正确的是( )
A.SiO 是酸性氧化物,能与NaOH溶液反应
2
B.Na O、Na O 组成元素相同,与CO 反应产物也相同
2 2 2 2
C.CO、NO、NO 都是大气污染气体,在空气中都能稳定存在
2
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
6.(4分)(2010•山东)下列与实验相关的叙述正确的是( )
A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
C.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏高
D.检验某溶液是否含有SO 2﹣时,应取少量该溶液,依次加入BaCl 溶液和稀盐酸
4 2
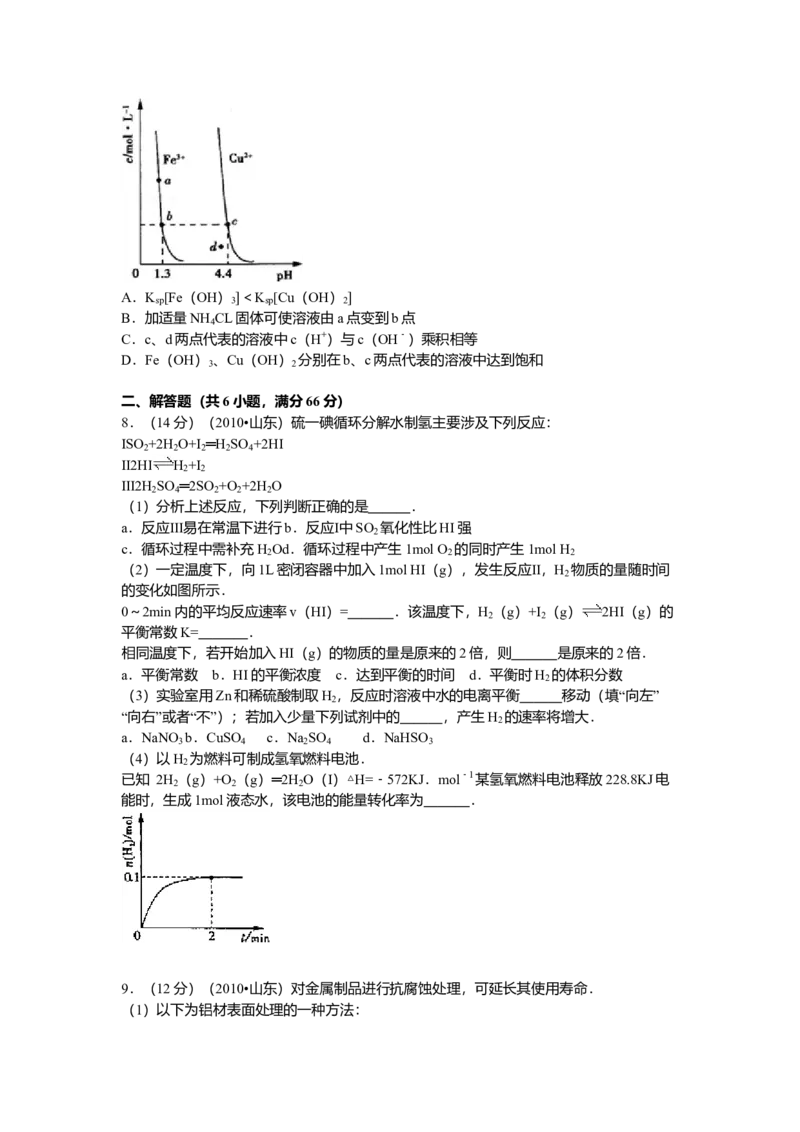
7.(4分)(2010•山东)某温度下,Fe(OH) (s)、Cu(OH) (s)分别在溶液中达
3 2
到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示.据图分析,下列判断
错误的是( )A.K [Fe(OH) <K [Cu(OH)
sp 3 sp 2
B.加适量NH CL固体可使溶液由a点变到b点
4
] ]
C.c、d两点代表的溶液中c(H+)与c(OH﹣)乘积相等
D.Fe(OH) 、Cu(OH) 分别在b、c两点代表的溶液中达到饱和
3 2
二、解答题(共6小题,满分66分)
8.(14分)(2010•山东)硫一碘循环分解水制氢主要涉及下列反应:
ⅠSO +2H O+I ═H SO +2HI
2 2 2 2 4
Ⅱ2HI H +I
2 2
Ⅲ2H SO ═2SO +O +2H O
2 4 2 2 2
(1)分析上述反应,下列判断正确的是 .
a.反应Ⅲ易在常温下进行b.反应Ⅰ中SO 氧化性比HI强
2
c.循环过程中需补充H Od.循环过程中产生1mol O 的同时产生1mol H
2 2 2
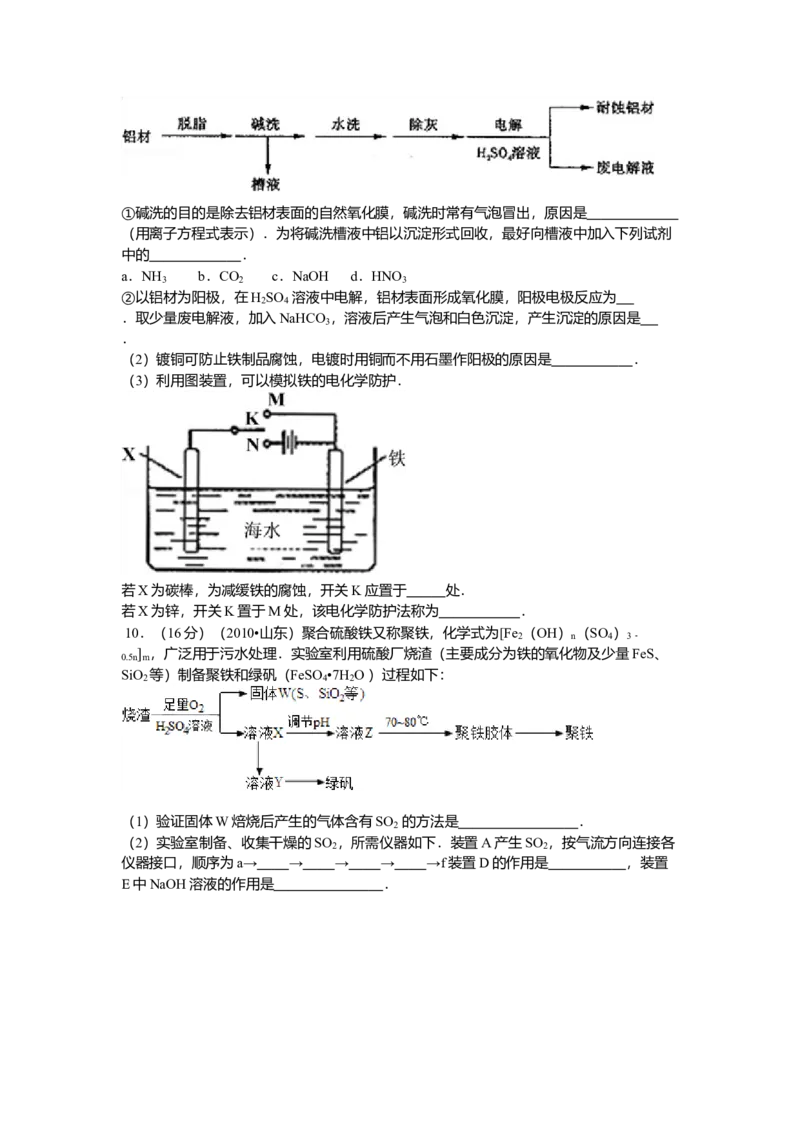
(2)一定温度下,向1L密闭容器中加入1mol HI(g),发生反应Ⅱ,H 物质的量随时间
2
的变化如图所示.
0~2min内的平均反应速率v(HI)= .该温度下,H (g)+I (g) 2HI(g)的
2 2
平衡常数K= .
相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍.
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H 的体积分数
2
(3)实验室用Zn和稀硫酸制取H ,反应时溶液中水的电离平衡 移动(填“向左”
2
“向右”或者“不”);若加入少量下列试剂中的 ,产生H 的速率将增大.
2
a.NaNO b.CuSO c.Na SO d.NaHSO
3 4 2 4 3
(4)以H 为燃料可制成氢氧燃料电池.
2
已知 2H (g)+O (g)═2H O(I)△H=﹣572KJ.mol﹣1某氢氧燃料电池释放228.8KJ电
2 2 2
能时,生成1mol液态水,该电池的能量转化率为 .
9.(12分)(2010•山东)对金属制品进行抗腐蚀处理,可延长其使用寿命.
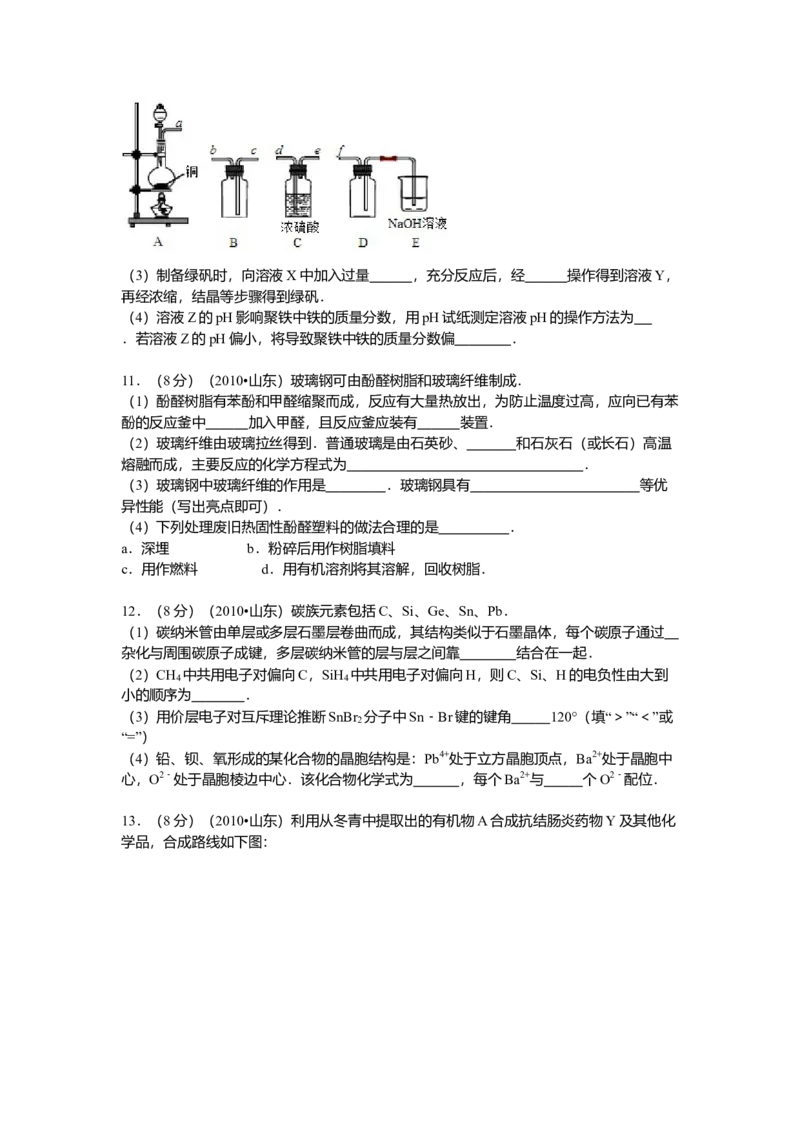
(1)以下为铝材表面处理的一种方法:①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
(用离子方程式表示).为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂
中的 .
a.NH b.CO c.NaOH d.HNO
3 2 3
②以铝材为阳极,在H SO 溶液中电解,铝材表面形成氧化膜,阳极电极反应为
2 4
.取少量废电解液,加入NaHCO ,溶液后产生气泡和白色沉淀,产生沉淀的原因是
3
.
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是 .
(3)利用图装置,可以模拟铁的电化学防护.
若X为碳棒,为减缓铁的腐蚀,开关K应置于 处.
若X为锌,开关K置于M处,该电化学防护法称为 .
10.(16分)(2010•山东)聚合硫酸铁又称聚铁,化学式为[Fe (OH) (SO )
2 n 4 3﹣
,广泛用于污水处理.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、
0.5n m
SiO 等)制备聚铁和绿矾(FeSO •7H O )过程如下:
2 4 2
]
(1)验证固体W焙烧后产生的气体含有SO 的方法是 .
2
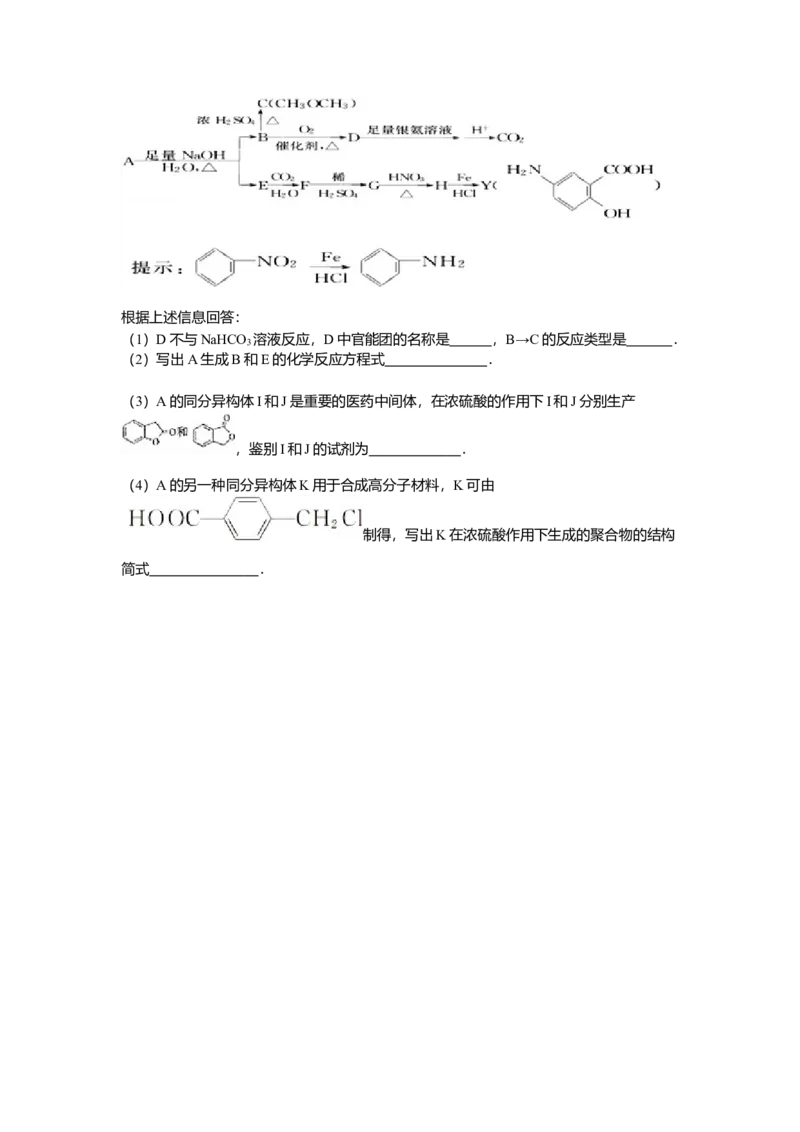
(2)实验室制备、收集干燥的SO ,所需仪器如下.装置A产生SO ,按气流方向连接各
2 2
仪器接口,顺序为a→ → → → →f装置D的作用是 ,装置
E中NaOH溶液的作用是 .(3)制备绿矾时,向溶液X中加入过量 ,充分反应后,经 操作得到溶液Y,
再经浓缩,结晶等步骤得到绿矾.
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为
.若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏 .
11.(8分)(2010•山东)玻璃钢可由酚醛树脂和玻璃纤维制成.
(1)酚醛树脂有苯酚和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向已有苯
酚的反应釜中 加入甲醛,且反应釜应装有 装置.
(2)玻璃纤维由玻璃拉丝得到.普通玻璃是由石英砂、 和石灰石(或长石)高温
熔融而成,主要反应的化学方程式为 .
(3)玻璃钢中玻璃纤维的作用是 .玻璃钢具有 等优
异性能(写出亮点即可).
(4)下列处理废旧热固性酚醛塑料的做法合理的是 .
a.深埋 b.粉碎后用作树脂填料
c.用作燃料 d.用有机溶剂将其溶解,回收树脂.
12.(8分)(2010•山东)碳族元素包括C、Si、Ge、Sn、Pb.
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过
杂化与周围碳原子成键,多层碳纳米管的层与层之间靠 结合在一起.
(2)CH 中共用电子对偏向C,SiH 中共用电子对偏向H,则C、Si、H的电负性由大到
4 4
小的顺序为 .
(3)用价层电子对互斥理论推断SnBr 分子中Sn﹣Br键的键角 120°(填“>”“<”或
2
“=”)
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中
心,O2﹣处于晶胞棱边中心.该化合物化学式为 ,每个Ba2+与 个O2﹣配位.
13.(8分)(2010•山东)利用从冬青中提取出的有机物A合成抗结肠炎药物Y及其他化
学品,合成路线如下图:根据上述信息回答:
(1)D不与NaHCO 溶液反应,D中官能团的名称是 ,B→C的反应类型是 .
3
(2)写出A生成B和E的化学反应方程式 .
(3)A的同分异构体I和J是重要的医药中间体,在浓硫酸的作用下I和J分别生产
,鉴别I和J的试剂为 .
(4)A的另一种同分异构体K用于合成高分子材料,K可由
制得,写出K在浓硫酸作用下生成的聚合物的结构
简式 .