文档内容
2011 年全国普通高等学校招生统一考试
上海化学试卷
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对
后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-l C-12 N-14 O-16 F-19 Na-23 Mg-24 Si-28 S-32 Cu-64
I-127
第I卷 (共66分)
一、选择题(本题共10分,每小题2分,只有一个正确选项,答案涂写在答题卡上。)
1.下列离子在稳定人体血液的pH中起作用的是
A. Na+ B. HCO - C. Fe2+ D. Cl-
3
2.从光合作用的反应原理6CO +6H O C H O +6O 可知碳是农作物生长的必
2 2 6 12 6 2
需元素之一。关于用二氧化碳生产肥料的评价正确的是
A.缓解地球温室效应,抑制农作物营养平衡
B.加剧地球温室效应,促进农作物营养平衡
C.缓解地球温室效应,进农作物营养平衡
D.加剧地球温室效应,抑制农作物营养平衡
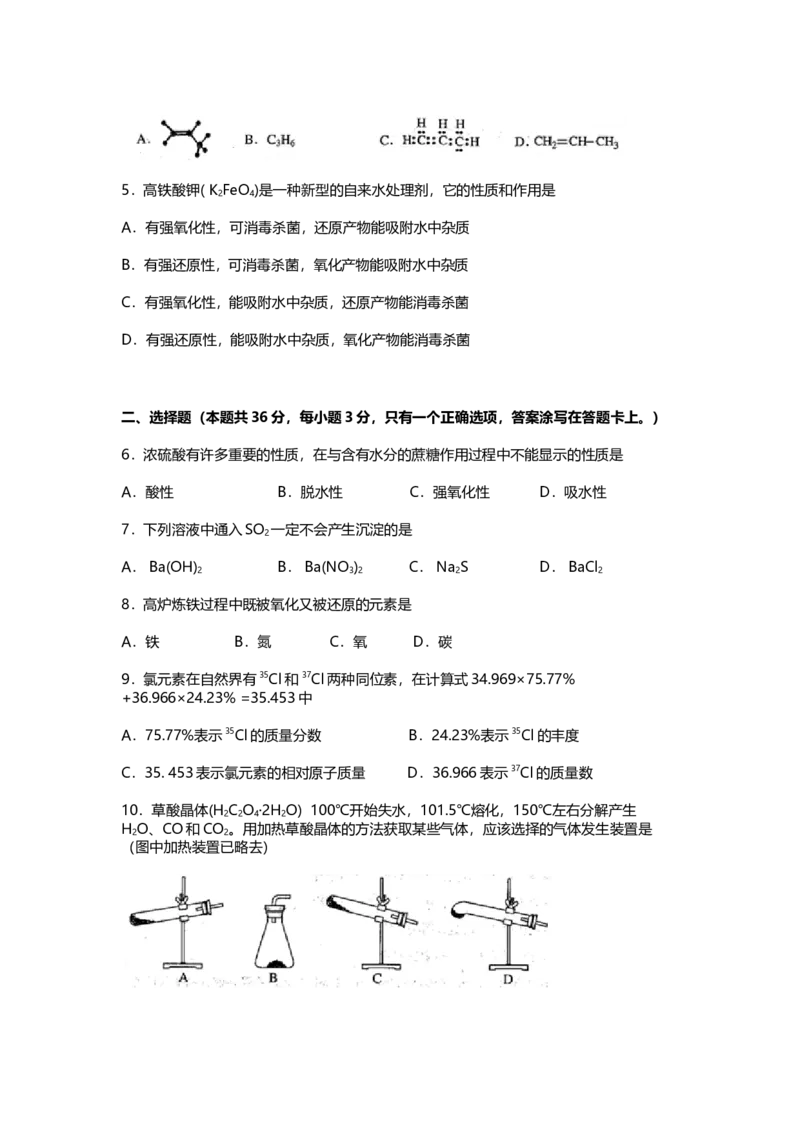
3.据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能
量变化示意图正确的是
4.下列有关化学用语能确定为丙烯的是5.高铁酸钾( K FeO )是一种新型的自来水处理剂,它的性质和作用是
2 4
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌
二、选择题(本题共36分,每小题3分,只有一个正确选项,答案涂写在答题卡上。)
6.浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是
A.酸性 B.脱水性 C.强氧化性 D.吸水性
7.下列溶液中通入SO 一定不会产生沉淀的是
2
A. Ba(OH) B. Ba(NO ) C. Na S D. BaCl
2 3 2 2 2
8.高炉炼铁过程中既被氧化又被还原的元素是
A.铁 B.氮 C.氧 D.碳
9.氯元素在自然界有35Cl和37Cl两种同位素,在计算式34.969×75.77%
+36.966×24.23% =35.453中
A.75.77%表示35Cl的质量分数 B.24.23%表示35Cl的丰度
C.35. 453表示氯元素的相对原子质量 D.36.966表示37Cl的质量数
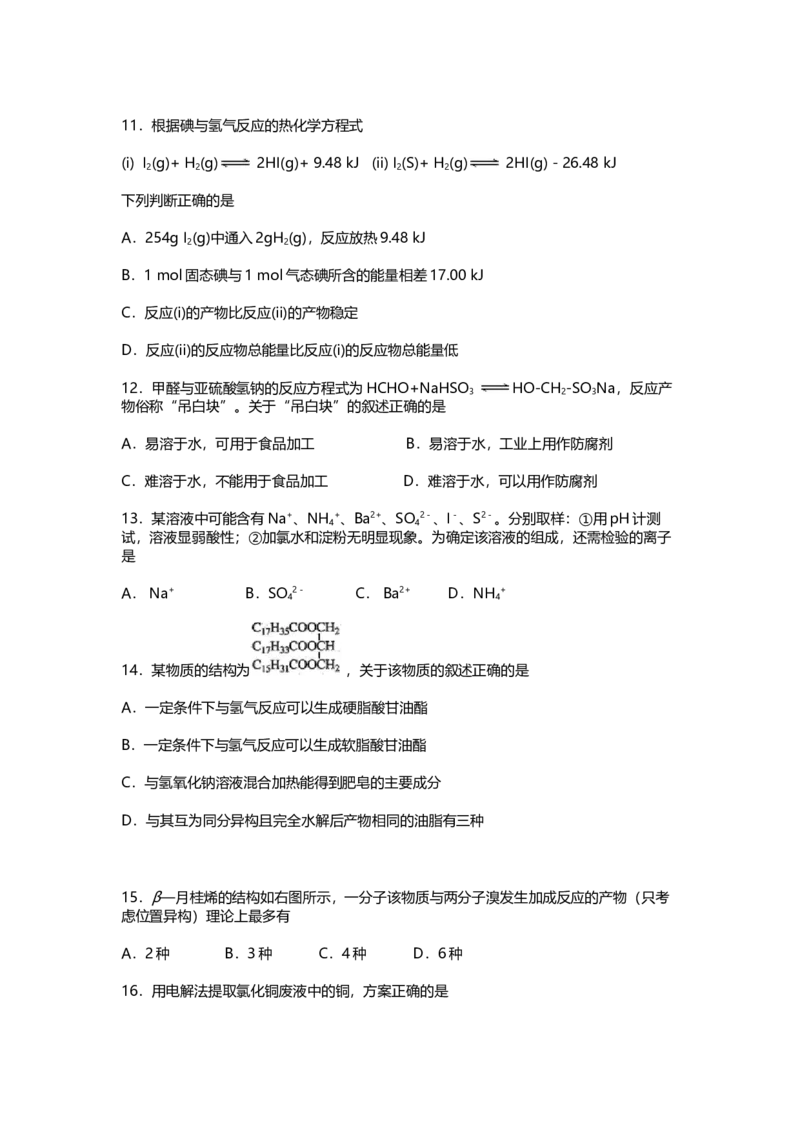
10.草酸晶体(H C O ·2H O) 100℃开始失水,101.5℃熔化,150℃左右分解产生
2 2 4 2
H O、CO和CO 。用加热草酸晶体的方法获取某些气体,应该选择的气体发生装置是
2 2
(图中加热装置已略去)11.根据碘与氢气反应的热化学方程式
(i) I (g)+ H (g) 2HI(g)+ 9.48 kJ (ii) I (S)+ H (g) 2HI(g) - 26.48 kJ
2 2 2 2
下列判断正确的是
A.254g I (g)中通入2gH (g),反应放热9.48 kJ
2 2
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
12.甲醛与亚硫酸氢钠的反应方程式为HCHO+NaHSO HO-CH -SO Na,反应产
3 2 3
物俗称“吊白块”。关于“吊白块”的叙述正确的是
A.易溶于水,可用于食品加工 B.易溶于水,工业上用作防腐剂
C.难溶于水,不能用于食品加工 D.难溶于水,可以用作防腐剂
13.某溶液中可能含有Na+、NH +、Ba2+、SO 2-、I-、S2-。分别取样:①用pH计测
4 4
试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子
是
A. Na+ B.SO 2- C. Ba2+ D.NH +
4 4
14.某物质的结构为 ,关于该物质的叙述正确的是
A.一定条件下与氢气反应可以生成硬脂酸甘油酯
B.一定条件下与氢气反应可以生成软脂酸甘油酯
C.与氢氧化钠溶液混合加热能得到肥皂的主要成分
D.与其互为同分异构且完全水解后产物相同的油脂有三种
15.β—月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考
虑位置异构)理论上最多有
A.2种 B.3种 C.4种 D.6种
16.用电解法提取氯化铜废液中的铜,方案正确的是A.用铜片连接电源的正极,另一电极用铂片 B.用碳棒连接电源的正极,另一电极用铜
片
C.用氢氧化钠溶液吸收阴极产物 D.用带火星的木条检验阳极产物
17.120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是
将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
A.2.0mol/L B.5 mol/L C.0.18 mol/L D.0.24mol/L
三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确
选
项的,多选不给分;有两个正确选项,选对一个给2分,选错一个,该小题不给分,答案
涂写在答题卡上。)
18.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧
化剂又非还原剂等。下列反应与Br +SO +2H O=H SO +2HBr相比较,水的作用不相同
2 2 2 2 4
的是
A.2Na O +2H O=4NaOH+O ↑ B.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 2 2 2 2 3
C.2F +2H O=4HF+O D.2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2 2 2 2
19.常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得
到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是
A.b不可能显碱性 B. a可能显酸性或碱性
C.a不可能显酸性 D.b可能显碱性或酸性
20.过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增
加了28 g,反应中有关物质韵物理量正确的是(N表示阿伏加德罗常数)
A
二氧化碳 碳酸钠 转移的电子
A 1mol N
A
B 22.4L 1mol
C 106 g 1mol
D 106g 2N
A
21.在复盐NH Fe(SO ) 溶液中逐滴加入Ba(OH) 溶液,可能发生的反应的离子方程式是
4 4 2 2
A. Fe2++SO 2-+Ba2++2OH-=BaSO ↓+Fe(OH) ↓
4 4 2B.NH ++Fe3++ 2SO 2-+ 2Ba2++ 4OH-=2BaSO ↓+ Fe(OH) ↓+ NH ·H O
4 4 4 3 3 2
C.2Fe3++ 3SO 2-+ 3Ba2++6OH-=3BaSO ↓+ 2Fe(OH) ↓
4 4 3
D.3NH ++ Fe3++3SO 2-+ 3Ba2++ 6OH-=3BaSO ↓+Fe(OH) ↓+3NH ·H O
4 4 4 3 3 2
22.物质的量为0.10 mol的镁条在只含有CO 和O 混合气体的容器中燃烧(产物不含碳
2 2
酸镁),反应后容器内固体物质的质量不可能为
A.3.2g B.4.0g C.4.2g D.4.6g
第II卷(共84分)
四、(本题共24分)
23.工业上制取冰晶石(Na AlF )的化学方程式如下:
3 6
2Al(OH) + 12HF+ 3Na CO =2Na AlF + 3CO ↑+ 9H O
3 2 3 3 6 2 2
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非极性分子的电子式 ,
属于弱酸的电离方程式 。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性
强弱的是
( 选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离
子方程式为 。
(4) Na CO 俗称纯碱,属于 晶体。工业上制取纯碱的原料是 。
2 3
24.雄黄(AS S )和雌黄(As S )是提取砷的主要矿物原料,二者在自然界中共生。根据题意
4 4 2 3
完成下列填空:
(1)As S 和SnCl 在盐酸中反应转化为As S 和SnCl 并放出H S气体。若As S 和SnCl
2 3 2 4 4 4 2 2 3 2
正好完全反应,As S 和SnCl 的物质的量之比为 。
2 3 2
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。(3) As S 和HNO 有如下反应:As S + 10H++ 10NO —=2H AsO + 3S+10NO ↑+
2 3 3 2 3 3 3 4 2
2H O
2
若生成2mol H AsO ,则反应中转移电子的物质的量为 。若将该反应设计成一原电
3 4
池,则NO 应该在 ( 填“正极”或“负极”)附近逸出。
2
(4)若反应产物NO 与11.2L O (标准状况)混合后用水吸收全部转化成浓HNO ,然后
2 2 3
与过量的碳反应,所产生的CO 的量 ( 选填编号)。
2
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
25.自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增
大约25000~30000 kPa。在地壳内SiO 和HF存在以下平衡:SiO (s) +4HF(g)
2 2
SiF (g)+ 2H O(g)+148.9 kJ
4 2
根据题意完成下列填空:
(1)在地壳深处容易有 气体逸出,在地壳浅处容易有 沉积。
(2)如果上述反应的平衡常数K值变大,该反应 ( 选填编号)。
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, ( 选填编
号)。
a.2v (HF)=v (H O) b.v(H O)=2v(SiF )
正 逆 2 2 4
c.SiO 的质量保持不变 d.反应物不再转化为生成物
2
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,
在这段时间内HF的平均反应速率为 。
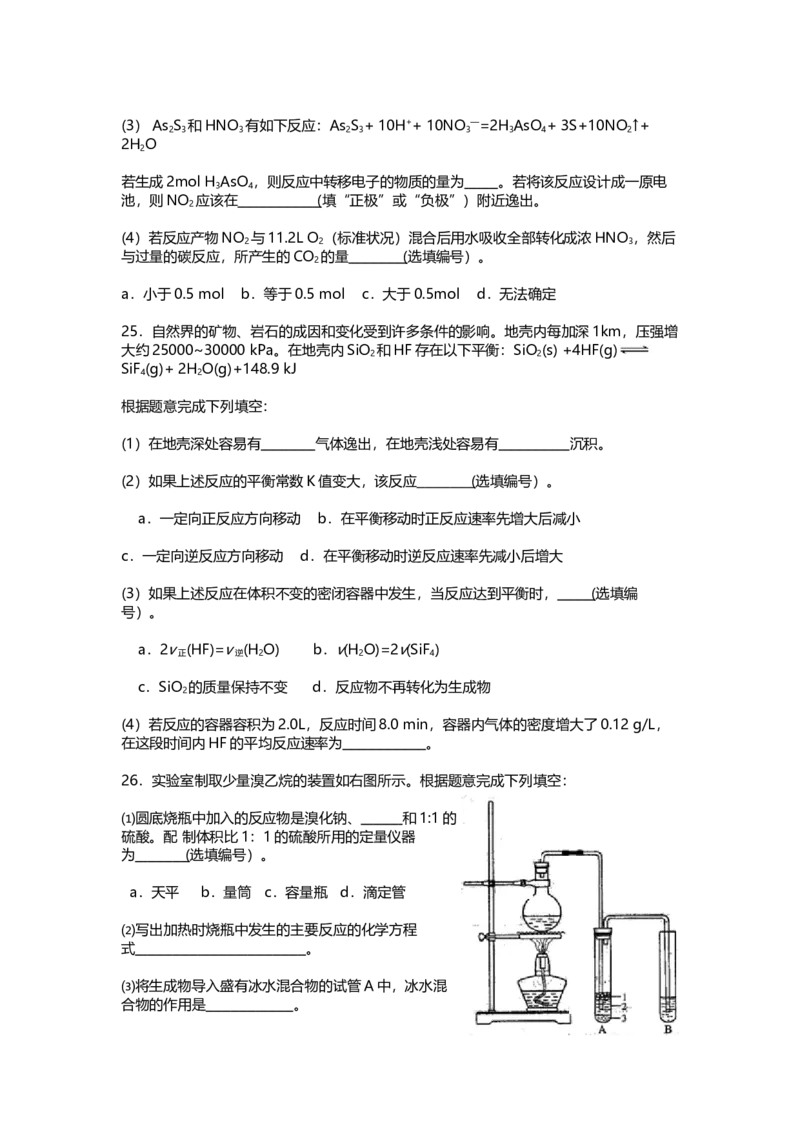
26.实验室制取少量溴乙烷的装置如右图所示。根据题意完成下列填空:
⑴圆底烧瓶中加入的反应物是溴化钠、 和1:1的
硫酸。配 制体积比1:1的硫酸所用的定量仪器
为 ( 选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
⑵写出加热时烧瓶中发生的主要反应的化学方程
式 。
⑶将生成物导入盛有冰水混合物的试管A中,冰水混
合物的作用是 。试管A中的物质分为三层(如图所示),产物在第 层。
⑷试管A中除了产物和水之外,还可能存在 、 (写出化学式)。
⑸用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是
( 选填编号)。
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是 。
⑹实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:
。
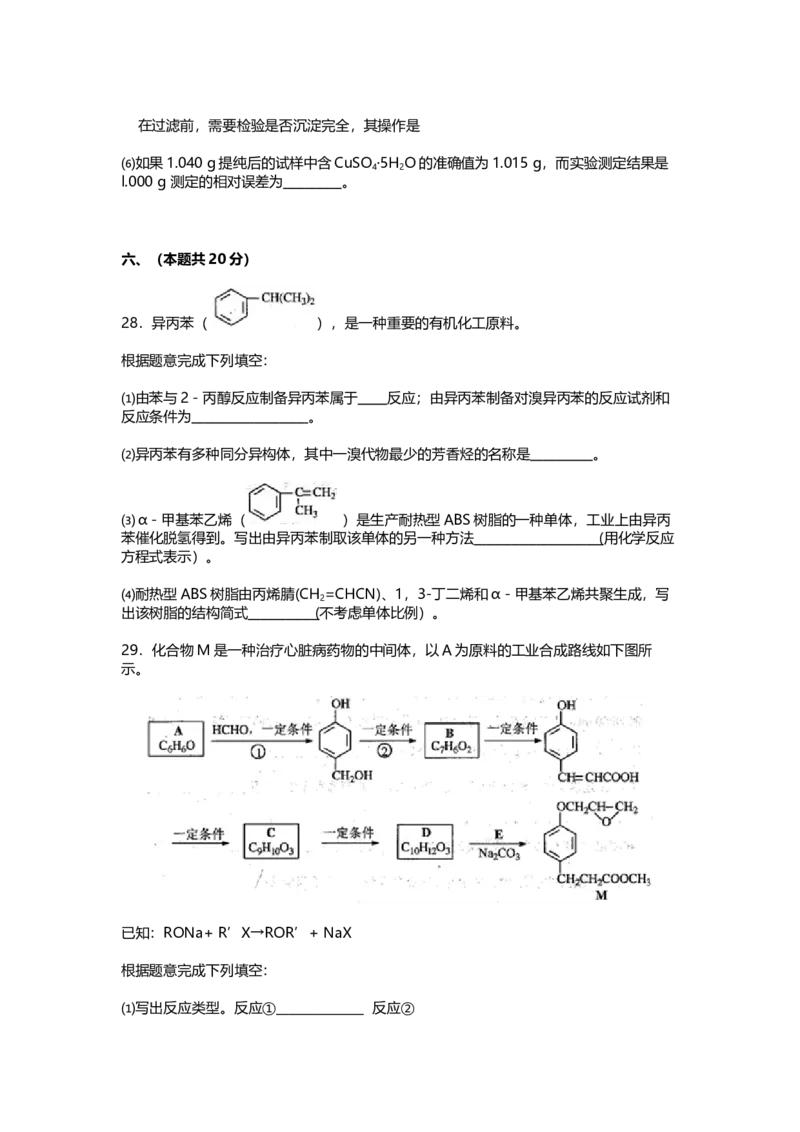
27.CuSO ·5H O是铜的重要化合物,有着广泛的应用。以下是CuSO ·5H O的实验室制
4 2 4 2
备流程图。
根据题意完成下列填空:
⑴向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:
、 。
⑵如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO ·5H O中可能存在的杂质是
4 2
,除去这种杂质的实验操作称为 。
⑶已知:CuSO +2NaOH=Cu(OH) ↓+ Na SO
4 2 2 4
称取0.1000 g提纯后的CuSO ·5H O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶
4 2
液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸
20.16 mL,则0.1000 g该试样中含CuSO ·5H O g。
4 2
⑷上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用 。
在滴定中,准确读数应该是滴定管上蓝线 所对应的刻度。
⑸如果采用重量法测定CuSO ·5H O的含量,完成下列步骤:
4 2
① ②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)在过滤前,需要检验是否沉淀完全,其操作是
⑹如果1.040 g提纯后的试样中含CuSO ·5H O的准确值为1.015 g,而实验测定结果是
4 2
l.000 g 测定的相对误差为 。
六、(本题共20分)
28.异丙苯( ),是一种重要的有机化工原料。
根据题意完成下列填空:
⑴由苯与2-丙醇反应制备异丙苯属于 反应;由异丙苯制备对溴异丙苯的反应试剂和
反应条件为 。
⑵异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的名称是 。
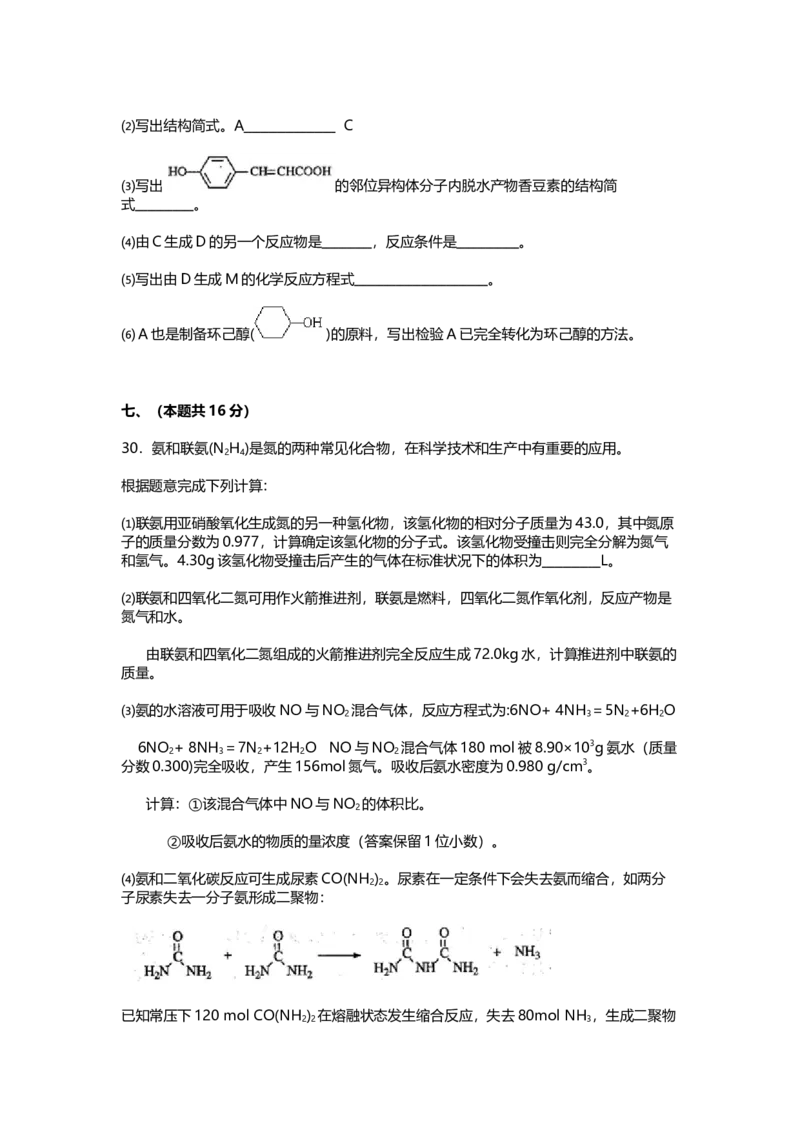
⑶α-甲基苯乙烯( )是生产耐热型ABS树脂的一种单体,工业上由异丙
苯催化脱氢得到。写出由异丙苯制取该单体的另一种方法 ( 用化学反应
方程式表示)。
⑷耐热型ABS树脂由丙烯腈(CH =CHCN)、1,3-丁二烯和α-甲基苯乙烯共聚生成,写
2
出该树脂的结构简式 ( 不考虑单体比例)。
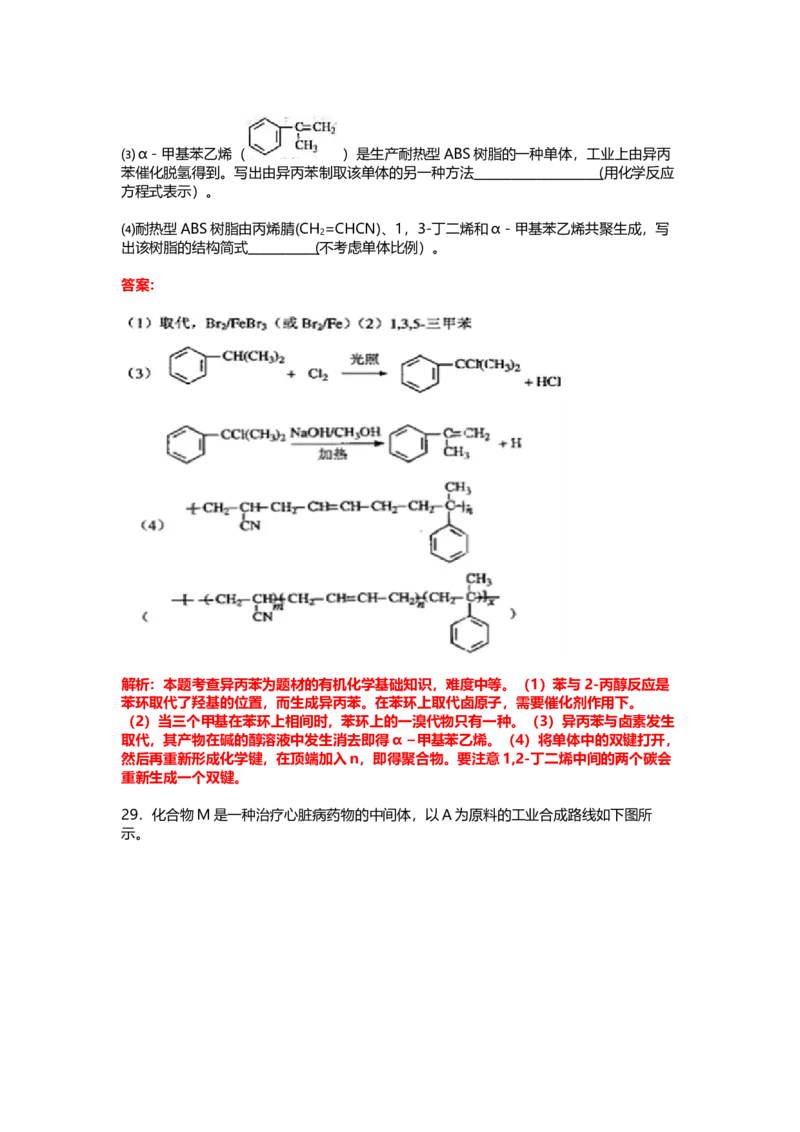
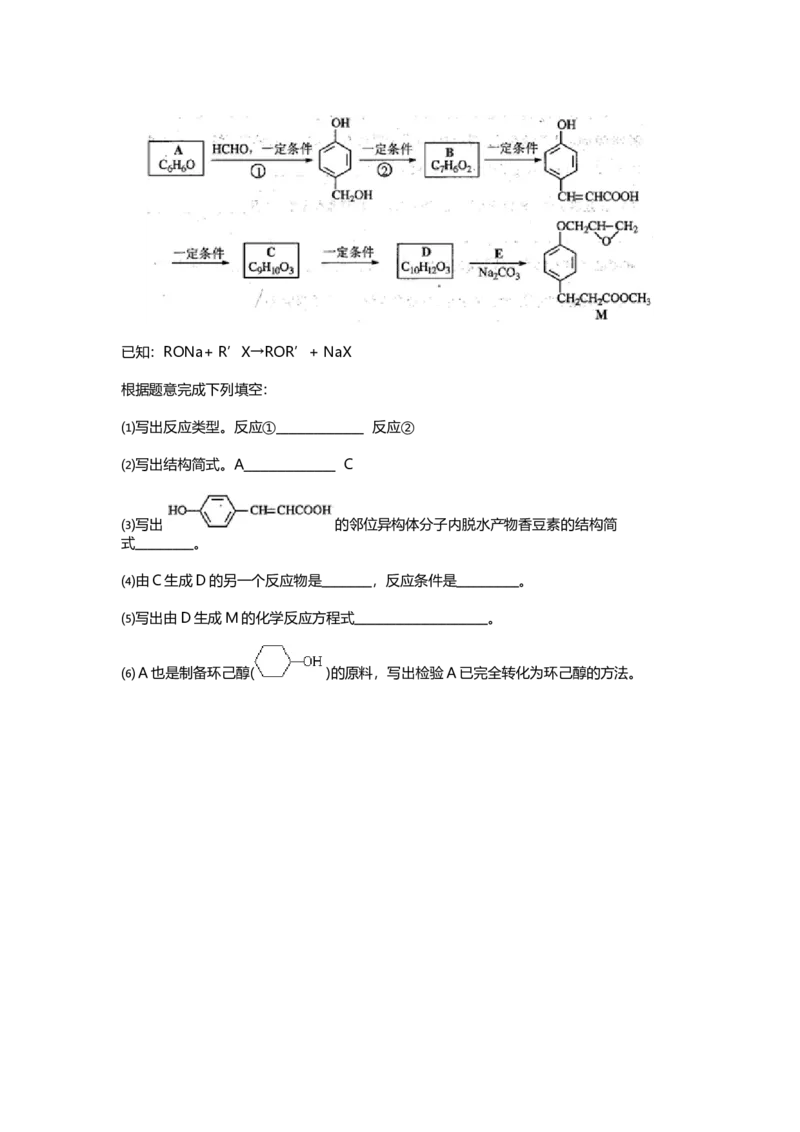
29.化合物M是一种治疗心脏病药物的中间体,以A为原料的工业合成路线如下图所
示。
已知:RONa+ R’X→ROR’+ NaX
根据题意完成下列填空:
⑴写出反应类型。反应① 反应②⑵写出结构简式。A C
⑶写出 的邻位异构体分子内脱水产物香豆素的结构简
式 。
⑷由C生成D的另一个反应物是 ,反应条件是 。
⑸写出由D生成M的化学反应方程式 。
⑹A也是制备环己醇( )的原料,写出检验A已完全转化为环己醇的方法。
七、(本题共16分)
30.氨和联氨(N H )是氮的两种常见化合物,在科学技术和生产中有重要的应用。
2 4
根据题意完成下列计算:
⑴联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原
子的质量分数为0.977,计算确定该氢化物的分子式。该氢化物受撞击则完全分解为氮气
和氢气。4.30g该氢化物受撞击后产生的气体在标准状况下的体积为 L。
⑵联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是
氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0kg水,计算推进剂中联氨的
质量。
⑶氨的水溶液可用于吸收NO与NO 混合气体,反应方程式为:6NO+ 4NH =5N +6H O
2 3 2 2
6NO + 8NH =7N +12H O NO与NO 混合气体180 mol被8.90×103g氨水(质量
2 3 2 2 2
分数0.300)完全吸收,产生156mol氮气。吸收后氨水密度为0.980 g/cm3。
计算:①该混合气体中NO与NO 的体积比。
2
②吸收后氨水的物质的量浓度(答案保留1位小数)。
⑷氨和二氧化碳反应可生成尿素CO(NH ) 。尿素在一定条件下会失去氨而缩合,如两分
2 2
子尿素失去一分子氨形成二聚物:
已知常压下120 mol CO(NH ) 在熔融状态发生缩合反应,失去80mol NH ,生成二聚物
2 2 3(C H N O )和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各
2 5 3 2
缩合物的物质的量之比。2011 年全国普通高等学校招生统一考试
上海化学试卷解析
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对
后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-l C-12 N-14 O-16 F-19 Na-23 Mg-24 Si-28 S-32 Cu-64
I-127
第I卷 (共66分)
一、选择题(本题共10分,每小题2分,只有一个正确选项,答案涂写在答题卡上。)
1.下列离子在稳定人体血液的pH中起作用的是
A. Na+ B. HCO - C. Fe2+ D. Cl-
3
解析:本题考查缓冲溶液的知识,难度较小。HCO -可以结合OH-,也可以结合H+,故可
3
以起到缓冲人体血液pH的作用。人体血液pH恒定在7.35-7.45之间,超出范围即有可
能引起酸中毒或者碱中毒。
2.从光合作用的反应原理6CO +6H O C H O +6O 可知碳是农作物生长的必
2 2 6 12 6 2
需元素之一。关于用二氧化碳生产肥料的评价正确的是
A.缓解地球温室效应,抑制农作物营养平衡
B.加剧地球温室效应,促进农作物营养平衡
C.缓解地球温室效应,进农作物营养平衡
D.加剧地球温室效应,抑制农作物营养平衡
解析:本题考查CO 生产肥料的作用,难度较小。使用CO ,可以减少温室效应,从光合作
2 2
用原理看,使用CO 可促进农作物营养平衡,所以C正确。
2
3.据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能
量变化示意图正确的是解析:本题考查热化学图像知识,难度中等。水分解需要吸热,故产物的总能量大于反应
物的总能量。加入催化剂可以降低反应的活化能,B项正确。
4.下列有关化学用语能确定为丙烯的是
解析:本题考查有关丙烯的化学用语,难度较小。A项,球所代表的不一定是C和H原
子,错;B项,C H 可能为环丙烷,错;C项,甲原子上少一个H原子,错。D项,是丙
3 6
烯的结构简式,正确。
5.高铁酸钾( K FeO )是一种新型的自来水处理剂,它的性质和作用是
2 4
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌
解析:本题考查高铁酸钾的性质,难度中等。高铁酸钾中的铁为+6价,具有强氧化性,
可以杀菌消毒。还原产物为Fe3+,其水解可得Fe(OH) 胶体,具有吸附性。隐性考察了胶
3
体性质。
二、选择题(本题共36分,每小题3分,只有一个正确选项,答案涂写在答题卡上。)
6.浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是
A.酸性 B.脱水性 C.强氧化性 D.吸水性
解析:什么叫酸性?酸转化成了盐。本题考查浓硫酸的性质,难度小。含有水分的蔗糖,
加入浓硫酸,可以吸水。蔗糖可以发生脱水作用,生成C,还可以继续被浓硫酸氧化。过
程中没有盐生成,不表现酸性作用。故选A项。
7.下列溶液中通入SO 一定不会产生沉淀的是
2A. Ba(OH) B. Ba(NO ) C. Na S D. BaCl
2 3 2 2 2
解析:本题考查SO 的性质,难度中等。A中SO 与Ba(OH) 可以生成BaSO ,B中
2 2 2 3
HNO 可以将S氧化成+6价,最终生成BaSO 。C中SO 通入Na S中,先生成H S,
3 4 2 2 2
然后可得到S沉淀。SO 与BaCl 不反应。
2 2
8.高炉炼铁过程中既被氧化又被还原的元素是
A.铁 B.氮 C.氧 D.碳
解析:本题考查高炉炼铁的原理,难度中等。高炉炼铁中涉及C与O2生成CO,CO与
Fe O 生成CO ,CO 与C生成CO。过程中C的化合价有升有降,故既被氧化又被还
2 3 2 2
原。
9.氯元素在自然界有35Cl和37Cl两种同位素,在计算式34.969×75.77%
+36.966×24.23% =35.453中
A.75.77%表示35Cl的质量分数 B.24.23%表示35Cl的丰度
C.35. 453表示氯元素的相对原子质量 D.36.966表示37Cl的质量数
解析:本题考查相对原子质量的求法,难度中等。A项,75.77%表示35Cl的丰度,错;B
项,23.23%表示37Cl的丰度,错;C项,氯元素的相对原子质量是用两种同位素的相对
原子质量分别乘以各自的丰度,正确;D项,36.966表示37Cl的相对原子质量。
10.草酸晶体(H C O ·2H O) 100℃开始失水,101.5℃熔化,150℃左右分解产生
2 2 4 2
H O、CO和CO 。用加热草酸晶体的方法获取某些气体,应该选择的气体发生装置是
2 2
(图中加热装置已略去)
解析:本题考查装置图的选择,难度较大。草酸晶体在没有分解时就已经熔化,故不能直
接用C装置,否则加热过程中液体会流出。D项正确.
11.根据碘与氢气反应的热化学方程式
(i) I (g)+ H (g) 2HI(g)+ 9.48 kJ (ii) I (S)+ H (g) 2HI(g) - 26.48 kJ
2 2 2 2
下列判断正确的是
A.254g I (g)中通入2gH (g),反应放热9.48 kJ
2 2B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
解析:本题考查热化学知识,难度中等。A项,反应为可逆,故反应放热要小于9.48KJ,
错;B项,运用盖斯定律,将两式相减,可得能量相差26.48+9.48=35.96KJ,错;C
项,两个反应的产物相同,错;D项,I (g)的能量比I (s)大,正确。
2 2
12.甲醛与亚硫酸氢钠的反应方程式为HCHO+NaHSO HO-CH -SO Na,反应产
3 2 3
物俗称“吊白块”。关于“吊白块”的叙述正确的是
A.易溶于水,可用于食品加工 B.易溶于水,工业上用作防腐剂
C.难溶于水,不能用于食品加工 D.难溶于水,可以用作防腐剂
解析:本题考查有机物的性质,难度中等。“吊白块”中含有羟基和Na+,故易溶于水。
35%的甲醛水溶液称为福尔马林,可作防腐剂。甲醛有毒,不能用作食品加工,故B项正
确。
13.某溶液中可能含有Na+、NH +、Ba2+、SO 2-、I-、S2-。分别取样:①用pH计测
4 4
试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子
是
A. Na+ B.SO 2- C. Ba2+ D.NH +
4 4
解析:本题考查离子的检验,难度中等。由②知,溶液中不存在I-和S2-。但必须存在阴
离子,所以SO 2-一定存在,而Ba2+则不能存在。由①知,NH +肯定存在,因为其水解
4 4
显酸性。还需要检验的离子为Na+,选A项。
14.某物质的结构为 ,关于该物质的叙述正确的是
A.一定条件下与氢气反应可以生成硬脂酸甘油酯
B.一定条件下与氢气反应可以生成软脂酸甘油酯
C.与氢氧化钠溶液混合加热能得到肥皂的主要成分
D.与其互为同分异构且完全水解后产物相同的油脂有三种
解析:本题考查高级脂肪酸甘油酯的性质,难度中等。从形成的高级脂肪酸看,有3种酸
(硬脂酸、软脂酸和油酸)其结构为混甘油酯,A、B项错;高级脂肪酸在碱性条件下的
水解,得到高级脂肪酸的钠盐和甘油,此反应称为皂化反应,可得肥皂,C项正确;D项
应为两种,错。
15.β—月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有
A.2种 B.3种 C.4种 D.6种
解析:本题考查烯烃的加成反应,难度中等。分子存在三种不同的碳碳双 键,如图
1分子物质与2分子Br 加成时,可以加成①②③,也可以加成①③或②③,
2
还可以在①②发生1,4加成反应,故所得产物共有四种,C项正确。
16.用电解法提取氯化铜废液中的铜,方案正确的是
A.用铜片连接电源的正极,另一电极用铂片 B.用碳棒连接电源的正极,另一电极用铜
片
C.用氢氧化钠溶液吸收阴极产物 D.用带火星的木条检验阳极产物
解析:本题考查电解原理,难度中等。Cu2+在阴极处得电子生成Cu,故阴极采用铜片。
阳极不能用铜电极,否则自身溶解,应用惰性电极,,溶液中的Cl-在阳极处放电生成
Cl ,应用KI试纸检验,综上B项正确。
2
17.120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是
将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
A.2.0mol/L B.5 mol/L C.0.18 mol/L D.0.24mol/L
解析:本题考查碳酸钠与盐酸的互滴反应,难度较大。碳酸钠滴入盐酸中立即有气体产
生,而盐酸滴入碳酸钠中的过程是先反应生成碳酸氢钠,然后再放出CO 气体,反应方程
2
式为Na CO +HCl=NaHCO +NaCl,要放出气体至少需要HCl的浓度为0.2/0.2=
2 3 3
mol·L-1。若Na CO 全部放出CO ,需要盐酸浓度为0.2×2/0.2=2mol·L-1,为使两过
2 3 2
程产生的CO 量不等,故HCl浓度介于1mol·L-1~2mol·L-1,故选B项。
2
三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确
选
项的,多选不给分;有两个正确选项,选对一个给2分,选错一个,该小题不给分,答案
涂写在答题卡上。)
18.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧
化剂又非还原剂等。下列反应与Br +SO +2H O=H SO +2HBr相比较,水的作用不相同
2 2 2 2 4
的是
A.2Na O +2H O=4NaOH+O ↑ B.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 2 2 2 2 3C.2F +2H O=4HF+O D.2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2 2 2 2
解析:本题考查氧化还原反应的分析,难度中等。题干中的H O既不是氧化剂,也不是还
2
原剂。其作用与A、B项相同。C项中H O作还原剂,D项中H O作氧化剂。故选C、D
2 2
项。
19.常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得
到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是
A.b不可能显碱性 B. a可能显酸性或碱性
C.a不可能显酸性 D.b可能显碱性或酸性
解析:本题考查弱电解质的反应,难度较大。所用酸可能是强酸或是弱酸,与NaOH反
应,若为强酸,则生成中性的盐,若为弱酸,则酸过量,溶液呈酸性,A项正确,D项
错;与氨水反应,若为强酸,则碱过量,溶液呈碱性,若为弱酸,则生成的盐为弱酸弱碱
盐,水解后可能为酸性或碱性,B项正确,C项错。
20.过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增
加了28 g,反应中有关物质韵物理量正确的是(N表示阿伏加德罗常数)
A
二氧化碳 碳酸钠 转移的电子
A 1mol N
A
B 22.4L 1mol
C 106 g 1mol
D 106g 2N
A
解析:本题考查过氧化钠与CO 反应的分析,难度较大。
2
2Na O +2CO =2Na CO +O ↑ Δm
2 2 2 2 3 2
2mole- 2mol 2mol 56g
1mole- 1mol 1mol 28g
由上述关系,不能得出A、C项正确。B项,未指明标准状况,错。
21.在复盐NH Fe(SO ) 溶液中逐滴加入Ba(OH) 溶液,可能发生的反应的离子方程式是
4 4 2 2
A. Fe2++SO 2-+Ba2++2OH-=BaSO ↓+Fe(OH) ↓
4 4 2
B.NH ++Fe3++ 2SO 2-+ 2Ba2++ 4OH-=2BaSO ↓+ Fe(OH) ↓+ NH ·H O
4 4 4 3 3 2
C.2Fe3++ 3SO 2-+ 3Ba2++6OH-=3BaSO ↓+ 2Fe(OH) ↓
4 4 3D.3NH ++ Fe3++3SO 2-+ 3Ba2++ 6OH-=3BaSO ↓+Fe(OH) ↓+3NH ·H O
4 4 4 3 3 2
解析:本题考查离子间的反应,难度较大。A项,NH Fe(SO ) 中铁为+3价,故不可能
4 4 2
生成Fe(OH) ,错;B项,当两者为1∶2反应时成立,故正确;C项,当两者为2∶3反
2
应时成立,故正确;D项,意图表示3:3反应,忽视了反应的次序,OH-先与Fe3+反应完
后,再与NH +反应,错。
4
22.物质的量为0.10 mol的镁条在只含有CO 和O 混合气体的容器中燃烧(产物不含碳
2 2
酸镁),反应后容器内固体物质的质量不可能为
A.3.2g B.4.0g C.4.2g D.4.6g
解析:本题考查镁与CO 、O 燃烧产物确定,难度较大,发生的反应为2Mg+
2 2
CO =2MgO+C,2Mg+O =2MgO,若全部发生前一反应,生成的质量为0.05×12+
2 2
0.1×40=4.6g,若全部发生后一反应,生成的质量为0.1×40=4g,即质量不可能超过
4.6g。若混合气体的量不足,生成的产物质量可能很小,最小2.4克(假设镁未消耗),
所以取值范围是(2.4g,4.6g),故A、B、C项是有可能的,D项不可能。有些学生错误地
得出取值范围(4.0,4.6),选择AD.但是回想到2009年的第22题,发现这种思路是错
误的,如果金属镁很多,气体极少,我们可以只考虑剩余固体为镁,即2.4克。看来出题
人有意误导了考生。
第II卷(共84分)
四、(本题共24分)
23.工业上制取冰晶石(Na AlF )的化学方程式如下:
3 6
2Al(OH) + 12HF+ 3Na CO =2Na AlF + 3CO ↑+ 9H O
3 2 3 3 6 2 2
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非极性分子的电子式 ,
属于弱酸的电离方程式 。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性
强弱的是
( 选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离
子方程式为 。
(4) Na CO 俗称纯碱,属于 晶体。工业上制取纯碱的原料是 。
2 3
答案:(1) HF H++F- (2)ac (3)Al(OH) +OH-=== AlO -+
3 2
2H O
2
(4)离子晶体;氯化钠,二氧化碳,氨
解析:本题考查化学基础知识,涉及电子式,电离方程式、元素周期律、化学键等,难度
中等。(1)CO 为非极性分子,C与O之间为两对共用电子对。HF为弱酸,电离方程式
2
用“”相连。(2)O与F为相邻元素,它们的气态氢化物稳定性以及与H 化合得难易程
2
度可以判断非金属性的强弱,O、F无最高正价。(3)Al(OH) 为两性氢氧化物,可以被
3
强碱NaOH溶解。(4)用侯氏制碱法可得纯碱,反应方程式为NH +CO +H O+
3 2 2
NaCl=NaHCO +NH Cl。
3 4
24.雄黄(AS S )和雌黄(As S )是提取砷的主要矿物原料,二者在自然界中共生。根据题意
4 4 2 3
完成下列填空:
(1)As S 和SnCl 在盐酸中反应转化为As S 和SnCl 并放出H S气体。若As S 和SnCl
2 3 2 4 4 4 2 2 3 2
正好完全反应,As S 和SnCl 的物质的量之比为 。
2 3 2
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
(3) As S 和HNO 有如下反应:As S + 10H++ 10NO —=2H AsO + 3S+10NO ↑+
2 3 3 2 3 3 3 4 2
2H O
2
若生成2mol H AsO ,则反应中转移电子的物质的量为 。若将该反应设计成一原电
3 4
池,则NO 应该在 ( 填“正极”或“负极”)附近逸出。
2
(4)若反应产物NO 与11.2L O (标准状况)混合后用水吸收全部转化成浓HNO ,然后
2 2 3
与过量的碳反应,所产生的CO 的量 ( 选填编号)。
2
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
答案:(1)1:1 (2)As S ,氢氧化钠溶液(或硫酸铜溶液) (3)10mol 正极 (4)a
2 3
解析:本题考查氧化还原反应以及电化学知识,难度较大。(1)As S 中为+3价,
2 3
As S 中为+2价,化合价降低1×2。SnCl 中Sn为+2价,SnCl 中Sn为+4价,化合
4 4 2 4
价升高2,故两者物质的量相等时,得失电子才相等。(2)化合价降低作氧化剂。H S可
2
以用NaOH或CuSO 吸收。(3)反应中As和S的化合价均升高,一共失去的电子为2×2
4
+3×2=10mol。N从+5价降为+4价,被还原,可用于原电池的正极反应。(4)4NO
2
+O +2H O=4HNO ,0.5mol O 可得2mol HNO 。C+4HNO (浓)=CO +4NO +
2 2 3 2 3 3 2 2
2H O,若HNO 始终为浓的,则生成的CO 为0.5mol,但随着反应的进行,HNO 变
2 3 2 3稀,则生成的CO 小于0.5mol。
2
25.自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增
大约25000~30000 kPa。在地壳内SiO 和HF存在以下平衡:SiO (s) +4HF(g)
2 2
SiF (g)+ 2H O(g)+148.9 kJ
4 2
根据题意完成下列填空:
(1)在地壳深处容易有 气体逸出,在地壳浅处容易有 沉积。
(2)如果上述反应的平衡常数K值变大,该反应 ( 选填编号)。
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, ( 选填编
号)。
a.2v (HF)=v (H O) b.v(H O)=2v(SiF )
正 逆 2 2 4
c.SiO 的质量保持不变 d.反应物不再转化为生成物
2
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,
在这段时间内HF的平均反应速率为 。
答案:⑴SiF 、H O、 SiO ⑵ad ⑶bc ⑷0.0010mol·L-1·min-1
4 2 2
解析:本题考查化学平衡的移动,平衡状态的判断,化学反应速率的计算等知识,难度中
等。(1)地壳深处的压强大,则生成的SiF 和H O 多。在低压处,SiO 的量多。(2)
4 2 2
平衡常仅与温度有关。平衡常数K 值变大,平衡向正方向移动,该反应为放热反应,则改
变的条件为降低温,降温时反应速率减小,随着反应向正方向进行,v 正减小、V 逆增
大,只至平衡。(3)达到平衡时,A 项,v (H O)前面配2,错;B 项,任一状态时均成
2
立。C 项,SiO 的量保持不变时,可以证明已达平衡。D 项,已达平衡,反应仍在进行,
2
错。(4)气体密度增大,则SiO 的质量减少了为0.12×2/60=0.004mol。由方程式
2
知,HF 的物质的量变化0.004×4=0.016mol,v (HF)=0.016/2/8 =0.001
mol/(L·min)。
26.实验室制取少量溴乙烷的装置如右图所示。根据
题意完成下列填空:
⑴圆底烧瓶中加入的反应物是溴化钠、 和1:1的
硫酸。配 制体积比1:1的硫酸所用的定量仪器
为 ( 选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
⑵写出加热时烧瓶中发生的主要反应的化学方程
式 。⑶将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是 。
试管A中的物质分为三层(如图所示),产物在第 层。
⑷试管A中除了产物和水之外,还可能存在 、 (写出化学式)。
⑸用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是
( 选填编号)。
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是 。
⑹实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:
。
答案:⑴乙醇,b ⑵NaBr+H SO HBr+NaHSO CH CH OH+HBr
2 4 4 3 2
CH CH Br+H O
3 2 2
⑶冷却、液封溴乙烷;3 ⑷HBr 、CH CH OH ⑸d,乙烯 ⑹反应会产生Br ,腐蚀橡胶
3 2 2
解析:本题考查溴乙烷的制备实验,难度中等。(1)配制1:1 的硫酸,只要用量筒分别量
等体积的硫酸和水,然后相混即可。(2)NaBr 与浓硫酸反应生成HBr,HBr 可与乙醇
发生取代反应而生成溴乙烷。(3)冰水可以将溴乙烷冷却,其密度比水大,故沉于底
部。(4)HBr、乙醇易挥发,可能会混入产物中。(5)棕黄色的物质为Br ,可以用
2
Na SO 反应除去。乙醇在浓硫酸作用下发生消去反应生成乙烯,可使KMnO 褪色。
2 3 4
(6)反应中产生Br 可以腐蚀橡胶。
2
27.CuSO ·5H O是铜的重要化合物,有着广泛的应用。以下是CuSO ·5H O的实验室制
4 2 4 2
备流程图。
根据题意完成下列填空:
⑴向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:
、 。
⑵如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO ·5H O中可能存在的杂质是
4 2
,除去这种杂质的实验操作称为 。⑶已知:CuSO +2NaOH=Cu(OH) ↓+ Na SO
4 2 2 4
称取0.1000 g提纯后的CuSO ·5H O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶
4 2
液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸
20.16 mL,则0.1000 g该试样中含CuSO ·5H O g。
4 2
⑷上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用 。
在滴定中,准确读数应该是滴定管上蓝线 所对应的刻度。
⑸如果采用重量法测定CuSO ·5H O的含量,完成下列步骤:
4 2
① ②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)
在过滤前,需要检验是否沉淀完全,其操作是
⑹如果1.040 g提纯后的试样中含CuSO ·5H O的准确值为1.015 g,而实验测定结果是
4 2
l.000 g 测定的相对误差为 。
答案:⑴溶液呈蓝色、有红棕色气体产生 ⑵Cu(NO ) ,重结晶 ⑶0.0980 ⑷标准盐酸
3 2
溶液润洗2-3次 粗细交界点 ⑸称取样品;在上层清液中继续滴加氯化钡溶液,观察有无
沉淀产生
⑹-1.5%(-1.48% )
解析:本题考查实验室制备CuSO ·5H O 的流程,难度中等。(1)铜可以被浓HNO
4 2 3
氧化,生成蓝色的Cu2+,同时有红棕色的NO 气体产物。(2)HNO 与Cu 反应生成
2 3
Cu(NO ) ,除去Cu(NO ) 可采用重结晶的方法。(3)CuSO ·5H O 的质量为
3 2 3 2 4 2
(0.1*28*10-3-0.1*20.16*10-3)250 =0.098g。( 4)滴定管需要用标准液润洗,否则影
响滴定结果。(5)看沉淀是否完全,只要检验是否存在SO 2 -,即继续加入Ba2+观察现
4
象。(6)相对误差为(1.000-1.015)/1.015*100% =-1.48%。
六、(本题共20分)
28.异丙苯( ),是一种重要的有机化工原料。
根据题意完成下列填空:
⑴由苯与2-丙醇反应制备异丙苯属于 反应;由异丙苯制备对溴异丙苯的反应试剂和
反应条件为 。
⑵异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的名称是 。⑶α-甲基苯乙烯( )是生产耐热型ABS树脂的一种单体,工业上由异丙
苯催化脱氢得到。写出由异丙苯制取该单体的另一种方法 ( 用化学反应
方程式表示)。
⑷耐热型ABS树脂由丙烯腈(CH =CHCN)、1,3-丁二烯和α-甲基苯乙烯共聚生成,写
2
出该树脂的结构简式 ( 不考虑单体比例)。
答案:
解析:本题考查异丙苯为题材的有机化学基础知识,难度中等。(1)苯与2-丙醇反应是
苯环取代了羟基的位置,而生成异丙苯。在苯环上取代卤原子,需要催化剂作用下。
(2)当三个甲基在苯环上相间时,苯环上的一溴代物只有一种。(3)异丙苯与卤素发生
取代,其产物在碱的醇溶液中发生消去即得α −甲基苯乙烯。(4)将单体中的双键打开,
然后再重新形成化学键,在顶端加入n,即得聚合物。要注意1,2-丁二烯中间的两个碳会
重新生成一个双键。
29.化合物M是一种治疗心脏病药物的中间体,以A为原料的工业合成路线如下图所
示。已知:RONa+ R’X→ROR’+ NaX
根据题意完成下列填空:
⑴写出反应类型。反应① 反应②
⑵写出结构简式。A C
⑶写出 的邻位异构体分子内脱水产物香豆素的结构简
式 。
⑷由C生成D的另一个反应物是 ,反应条件是 。
⑸写出由D生成M的化学反应方程式 。
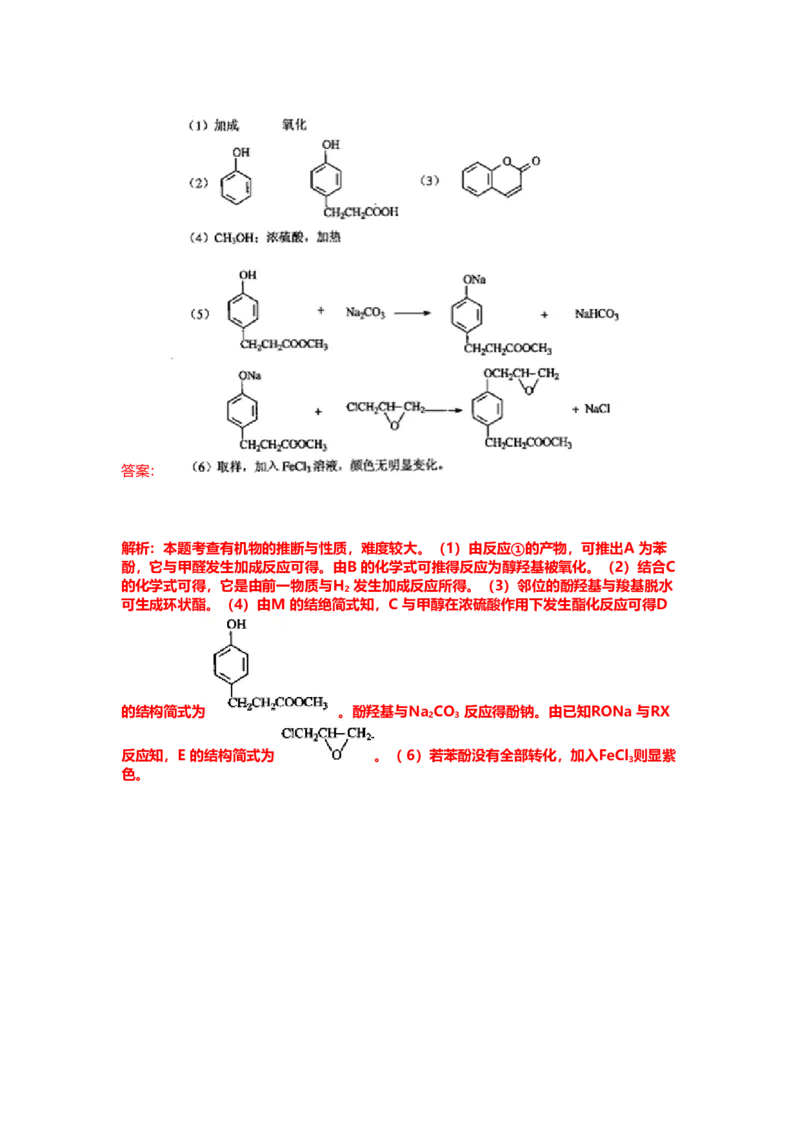
⑹A也是制备环己醇( )的原料,写出检验A已完全转化为环己醇的方法。答案:
解析:本题考查有机物的推断与性质,难度较大。(1)由反应①的产物,可推出A 为苯
酚,它与甲醛发生加成反应可得。由B 的化学式可推得反应为醇羟基被氧化。(2)结合C
的化学式可得,它是由前一物质与H 发生加成反应所得。(3)邻位的酚羟基与羧基脱水
2
可生成环状酯。(4)由M 的结绝简式知,C 与甲醇在浓硫酸作用下发生酯化反应可得D
的结构简式为 。酚羟基与Na CO 反应得酚钠。由已知RONa 与RX
2 3
反应知,E 的结构简式为 。( 6)若苯酚没有全部转化,加入FeCl 则显紫
3
色。七、(本题共16分)
30.氨和联氨(N H )是氮的两种常见化合物,在科学技术和生产中有重要的应用。
2 4
根据题意完成下列计算:
⑴联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原
子的质量分数为0.977,计算确定该氢化物的分子式。该氢化物受撞击则完全分解为氮气
和氢气。4.30g该氢化物受撞击后产生的气体在标准状况下的体积为 L。
⑵联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是
氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0kg水,计算推进剂中联氨的
质量。
⑶氨的水溶液可用于吸收NO与NO 混合气体,反应方程式为:6NO+ 4NH =5N +6H O
2 3 2 2
6NO + 8NH =7N +12H O NO与NO 混合气体180 mol被8.90×103g氨水(质量
2 3 2 2 2
分数0.300)完全吸收,产生156mol氮气。吸收后氨水密度为0.980 g/cm3。
计算:①该混合气体中NO与NO 的体积比。
2
②吸收后氨水的物质的量浓度(答案保留1位小数)。
⑷氨和二氧化碳反应可生成尿素CO(NH ) 。尿素在一定条件下会失去氨而缩合,如两分
2 2
子尿素失去一分子氨形成二聚物:
已知常压下120 mol CO(NH ) 在熔融状态发生缩合反应,失去80mol NH ,生成二聚物
2 2 3
(C H N O )和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各
2 5 3 2
缩合物的物质的量之比。
答案:⑴HN 4.48 ⑵64kg ⑶①V(NO):V(NO )=9:1 ②2.4mol ⑷3:1:1
3 2
解析:(1)该氢化物中N、H 的个数比为:(43*0.977/14) :[43*(1-0.977)/1] =3:
1,则其最简
式为HN ,由于相对分子质量为43.0,则分子式为HN 。根据2HN =3N +H ,则产
3 3 3 2 2
生的气体在标准状况下的体积为4.30g/43.0g / mol×2×22.4L/mol=4.48L。( 2)联
氨和四氧化二氮的反应为:2N H +N O =3N +4H O,根据2N H ~4H O,则推进剂
2 4 2 4 2 2 2 4 2
中联氨的质量为:72.0kg/(18×4)×32×2=64kg。(3)①设该混合气体中NO 与NO
2
的物质的量分别为x、y。则x+y=180, 5/6x+7/6 y=156,解得x=162,y=18,根据同温同压下气体的体积比等于物质的量之比,则NO 与NO 的体积比162:18=
2
9:1。②吸收后氨水中n(NH )=8.90×103g*0.300/17 -162×4/6 -18×8/6 =
3
25.06mol,氨水的质量为8.90×103g-(162×4/6 +18×8/6)×17+(162+
18×2)×18=10220g,故氨水的物质的量浓度为:25.06 mol/10220 g/980 g /L =
2.4mol/L。( 4)三聚物可以看做是1 分子二聚物和1 分子尿素脱去1 分子NH ,有两
3
种结构 (a)(C H N O )、 (b)(C H N O )
3 6 4 3 3 3 3 3
(图片中中间氮原子少了1个氮原子请自行补上)。
设二聚物、三聚物a、三聚物b 的物质的量分别为x、y、z。
则根据碳守恒,有2x+3y+3z=120,
根据氮守恒:3x+4y+3z=120×2-80,
x/(x+y+z) =0.6,解得x=30,y=10,z=10。所以三者的物质的量之比为3:1:1