文档内容
2011 年北京市高考化学试卷
一、选择题(共7小题,每小题3分,满分21分)
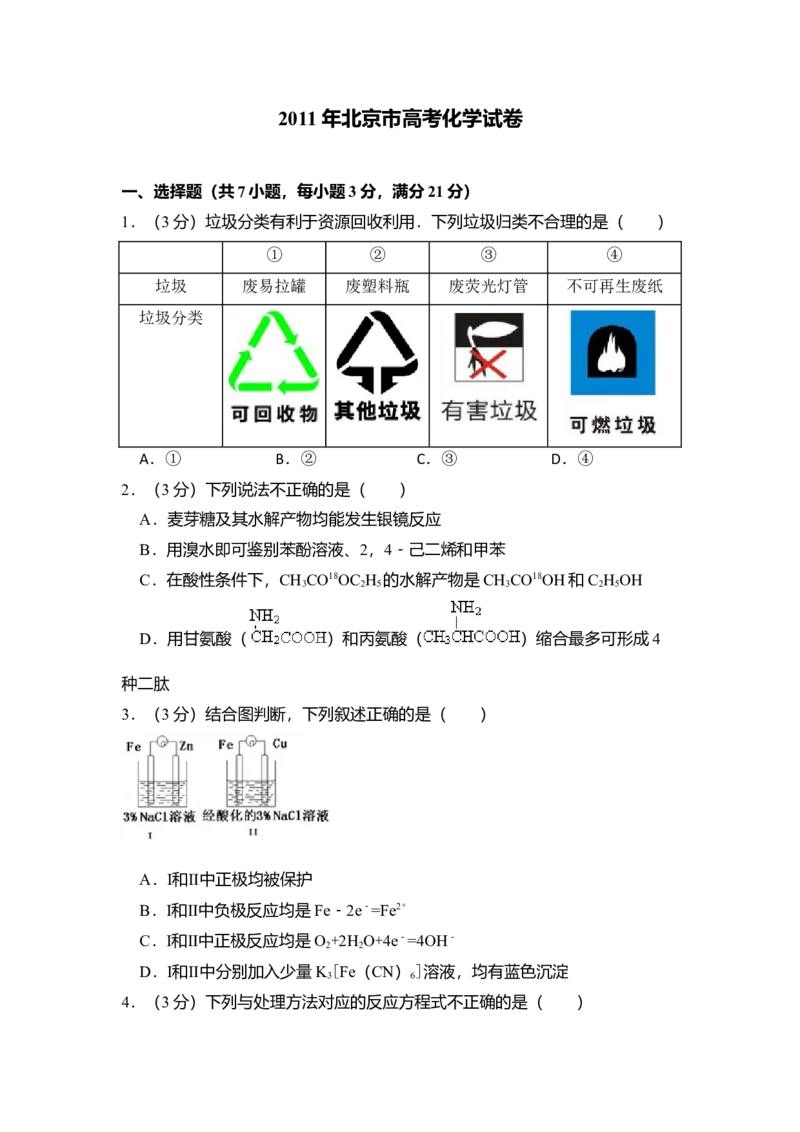
1.(3分)垃圾分类有利于资源回收利用.下列垃圾归类不合理的是( )
① ② ③ ④
垃圾 废易拉罐 废塑料瓶 废荧光灯管 不可再生废纸
垃圾分类
A.① B.② C.③ D.④
2.(3分)下列说法不正确的是( )
A.麦芽糖及其水解产物均能发生银镜反应
B.用溴水即可鉴别苯酚溶液、2,4﹣己二烯和甲苯
C.在酸性条件下,CH CO18OC H 的水解产物是CH CO18OH和C H OH
3 2 5 3 2 5
D.用甘氨酸( )和丙氨酸( )缩合最多可形成4
种二肽
3.(3分)结合图判断,下列叙述正确的是( )
A.Ⅰ和Ⅱ中正极均被保护
B.Ⅰ和Ⅱ中负极反应均是Fe﹣2e﹣=Fe2+
C.Ⅰ和Ⅱ中正极反应均是O +2H O+4e﹣=4OH﹣
2 2
D.Ⅰ和Ⅱ中分别加入少量K [Fe(CN) ]溶液,均有蓝色沉淀
3 6
4.(3分)下列与处理方法对应的反应方程式不正确的是( )A.用Na S去除废水中的Hg2+:Hg2++S2﹣=HgS↓
2
B.用催化法处理汽车尾气中的CO和NO:CO+NO C+NO
2
C.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H O Al(OH)
2 3
(胶体)+3H+
D.用高温催化氧化法去除烃类废气(C H ):C H +(x+ )O xCO +
x y x y 2 2
H O
2
5.(3 分)25℃、101kPa 下:① 2Na(s)+ O (g)=Na O(s)△H=﹣
2 2
414kJ.mol﹣1
②2Na(s)+O (g)=Na O (s)△H=﹣511kJ.mol﹣1
2 2 2
下列说法不正确的是( )
A.①和②产物的阴阳离子个数比相等
B.①和②生成等物质的量的产物,转移电子数相同
C.常温下Na与足量O 反应生成Na O,随温度升高生成Na O的速率逐渐
2 2 2
加快
D.25℃、101kPa下:Na O (s)+2Na(s)=2Na O(s)△H=﹣317kJ.mol
2 2 2
﹣1
6.(3分)下列实验方案中,不能测定Na CO 和NaHCO 混合物中Na CO 质
2 3 3 2 3
量分数( )
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b
克
D.取a克混合物与足量Ba(OH) 溶液充分反应,过滤、洗涤、烘干,得b
2
克固体
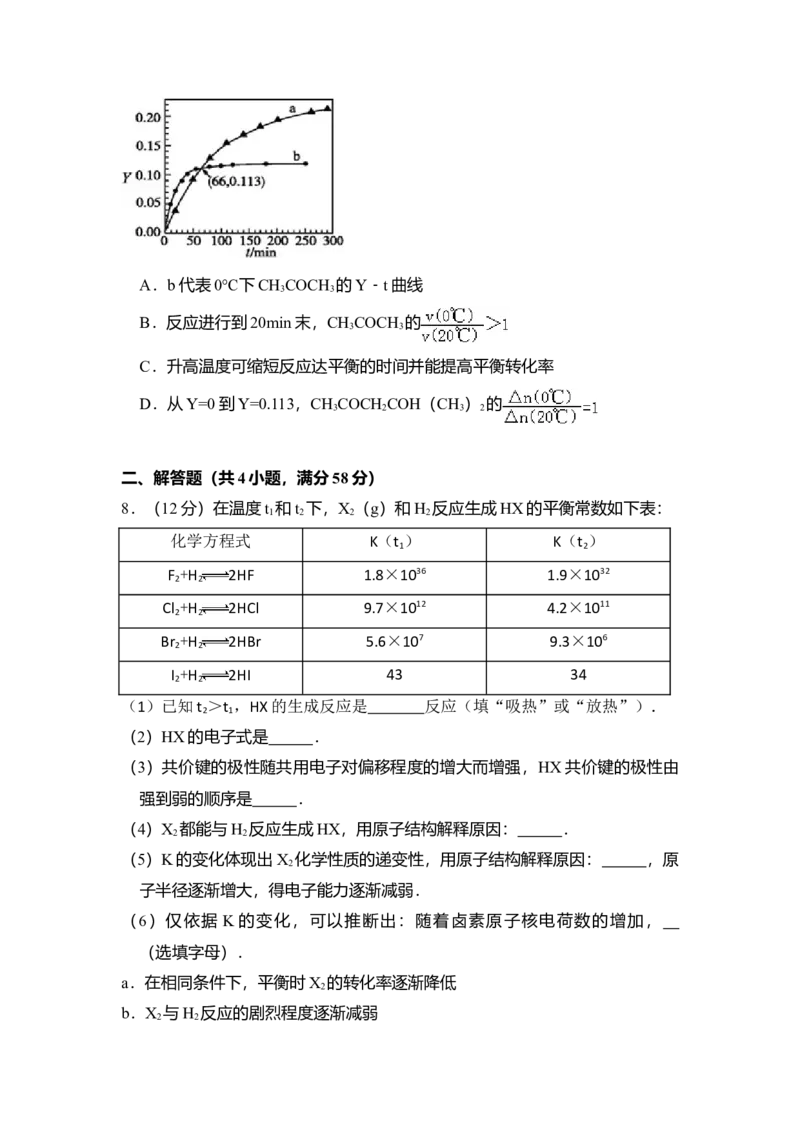
7.(3分)已知反应:2CH COCH (l) CH COCH COH(CH ) (l).取
3 3 3 2 3 2
等量CH COCH ,分别在0℃和20℃下,测得其转化分数随时间变化的关系
3 3 ⇌
曲线(Y﹣t)如图所示.下列说法正确的是( )A.b代表0℃下CH COCH 的Y﹣t曲线
3 3
B.反应进行到20min末,CH COCH 的
3 3
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH COCH COH(CH ) 的
3 2 3 2
二、解答题(共4小题,满分58分)
8.(12分)在温度t 和t 下,X (g)和H 反应生成HX的平衡常数如下表:
1 2 2 2
化学方程式 K(t ) K(t )
1 2
F +H 2HF 1.8×1036 1.9×1032
2 2
Cl +H 2HCl 9.7×1012 4.2×1011
2 2
Br +H 2HBr 5.6×107 9.3×106
2 2
I +H 2HI 43 34
2 2
(1)已知t >t ,HX的生成反应是 反应(填“吸热”或“放热”).
2 1
(2)HX的电子式是 .
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由
强到弱的顺序是 .
(4)X 都能与H 反应生成HX,用原子结构解释原因: .
2 2
(5)K的变化体现出X 化学性质的递变性,用原子结构解释原因: ,原
2
子半径逐渐增大,得电子能力逐渐减弱.
(6)仅依据 K 的变化,可以推断出:随着卤素原子核电荷数的增加,
(选填字母).
a.在相同条件下,平衡时X 的转化率逐渐降低
2
b.X 与H 反应的剧烈程度逐渐减弱
2 2c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱.
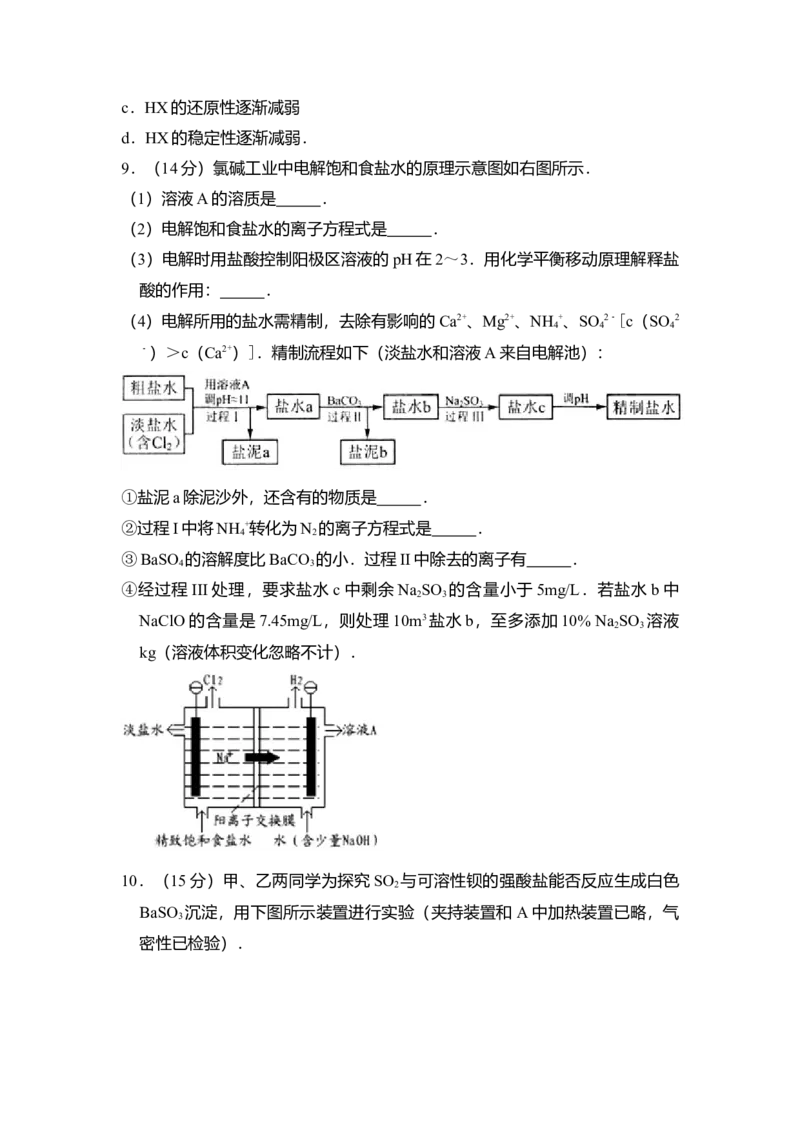
9.(14分)氯碱工业中电解饱和食盐水的原理示意图如右图所示.
(1)溶液A的溶质是 .
(2)电解饱和食盐水的离子方程式是 .
(3)电解时用盐酸控制阳极区溶液的pH在2~3.用化学平衡移动原理解释盐
酸的作用: .
(4)电解所用的盐水需精制,去除有影响的Ca2+、Mg2+、NH +、SO 2﹣[c(SO 2
4 4 4
﹣)>c(Ca2+)].精制流程如下(淡盐水和溶液A来自电解池):
①盐泥a除泥沙外,还含有的物质是 .
②过程I中将NH +转化为N 的离子方程式是 .
4 2
③BaSO 的溶解度比BaCO 的小.过程II中除去的离子有 .
4 3
④经过程III处理,要求盐水c中剩余Na SO 的含量小于5mg/L.若盐水b中
2 3
NaClO的含量是7.45mg/L,则处理10m3盐水b,至多添加10% Na SO 溶液
2 3
kg(溶液体积变化忽略不计).
10.(15分)甲、乙两同学为探究SO 与可溶性钡的强酸盐能否反应生成白色
2
BaSO 沉淀,用下图所示装置进行实验(夹持装置和 A中加热装置已略,气
3
密性已检验).实验操作和现象:
操作 现象
关闭弹簧夹,滴加一定量 A中有白雾生成,铜片表面产生气泡
浓硫酸,加热 B中有气泡冒出,产生大量白色沉淀
C中产生白色沉淀,液面上方略显浅棕色并逐渐消
失
打开弹簧夹,通入N ,停 ﹣﹣﹣
2
止加热,一段时间后关闭
从B、C中分别取少量白色 均未发现白色沉淀溶解
沉淀,加稀盐酸
(1)A中反应的化学方程式是 .
(2)C中白色沉淀是 ,该沉淀的生成表明SO 具有 性.
2
(3)C中液面上方生成浅棕色气体的化学方程式是 .
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认
为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是 ;
乙在A、B间增加洗气瓶D,D中盛放的试剂是 .
②进行实验,B中现象:
甲 大量白色沉淀
乙 少量白色沉淀
检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释实验现象异同的原
因: .
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是 .
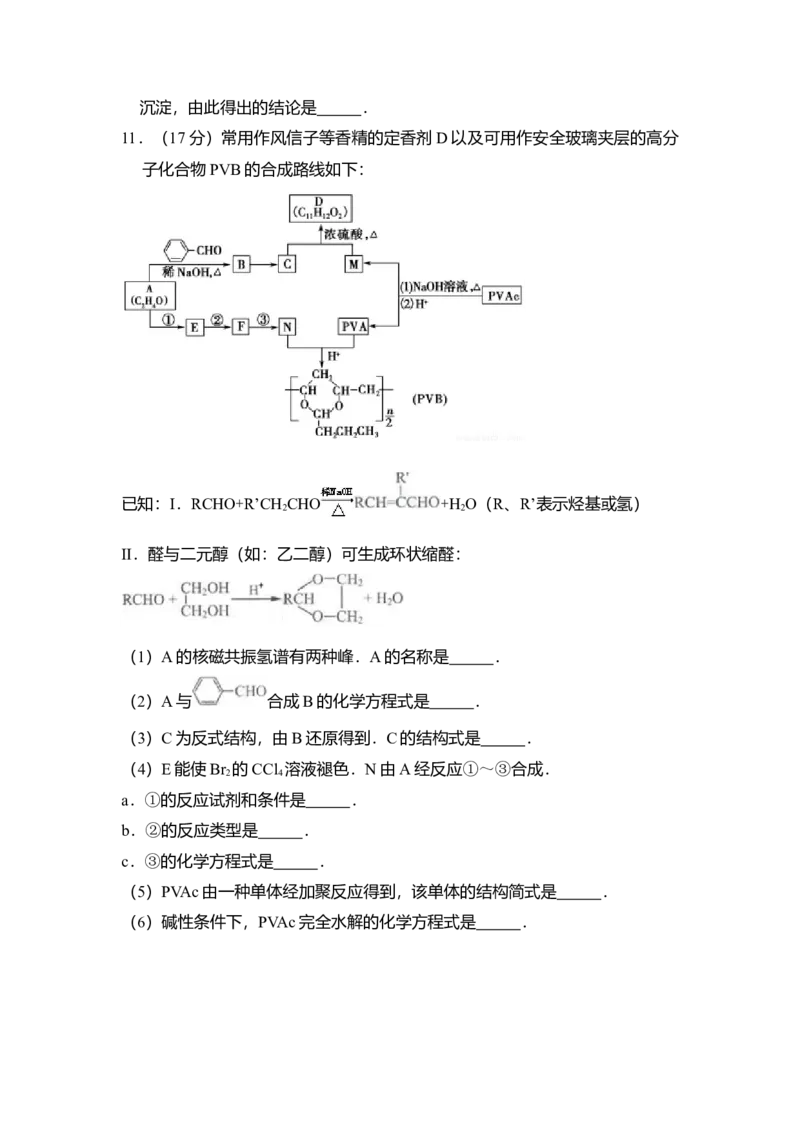
11.(17分)常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分
子化合物PVB的合成路线如下:
已知:Ⅰ.RCHO+R’CH CHO +H O(R、R’表示烃基或氢)
2 2
Ⅱ.醛与二元醇(如:乙二醇)可生成环状缩醛:
(1)A的核磁共振氢谱有两种峰.A的名称是 .
(2)A与 合成B的化学方程式是 .
(3)C为反式结构,由B还原得到.C的结构式是 .
(4)E能使Br 的CCl 溶液褪色.N由A经反应①~③合成.
2 4
a.①的反应试剂和条件是 .
b.②的反应类型是 .
c.③的化学方程式是 .
(5)PVAc由一种单体经加聚反应得到,该单体的结构简式是 .
(6)碱性条件下,PVAc完全水解的化学方程式是 .