文档内容
B.用催化法处理汽车尾气中的CO和NO:CO+NO C+NO
2011 年北京市高考化学试卷 2
C.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H O Al(OH) (胶体)+3H+
2 3
一、选择题(共7小题,每小题3分,满分21分)
D.用高温催化氧化法去除烃类废气(C H ):C H +(x+ )O xCO + H O
x y x y 2 2 2
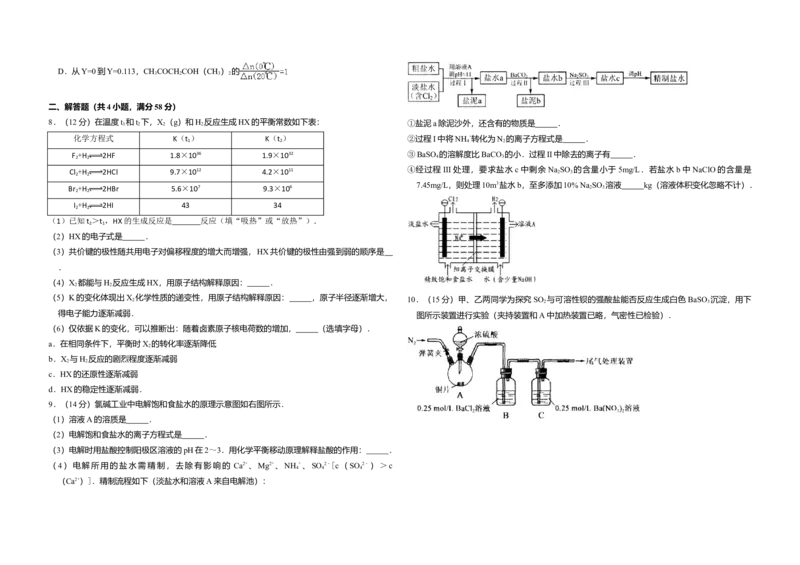
1.(3分)垃圾分类有利于资源回收利用.下列垃圾归类不合理的是( )
① ② ③ ④
5.(3分)25℃、101kPa下:①2Na(s)+ O (g)=Na O(s)△H=﹣414kJ.mol﹣1
2 2
垃圾 废易拉罐 废塑料瓶 废荧光灯管 不可再生废纸
②2Na(s)+O (g)=Na O (s)△H=﹣511kJ.mol﹣1
2 2 2
垃圾分类
下列说法不正确的是( )
A.①和②产物的阴阳离子个数比相等
B.①和②生成等物质的量的产物,转移电子数相同
C.常温下Na与足量O 反应生成Na O,随温度升高生成Na O的速率逐渐加快
2 2 2
A.① B.② C.③ D.④ D.25℃、101kPa下:Na
2
O
2
(s)+2Na(s)=2Na
2
O(s)△H=﹣317kJ.mol﹣1
2.(3分)下列说法不正确的是( ) 6.(3分)下列实验方案中,不能测定Na 2 CO 3 和NaHCO 3 混合物中Na 2 CO 3 质量分数( )
A.麦芽糖及其水解产物均能发生银镜反应 A.取a克混合物充分加热,减重b克
B.用溴水即可鉴别苯酚溶液、2,4﹣己二烯和甲苯 B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.在酸性条件下,CH CO18OC H 的水解产物是CH CO18OH和C H OH C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
3 2 5 3 2 5
D.取a克混合物与足量Ba(OH) 溶液充分反应,过滤、洗涤、烘干,得b克固体
2
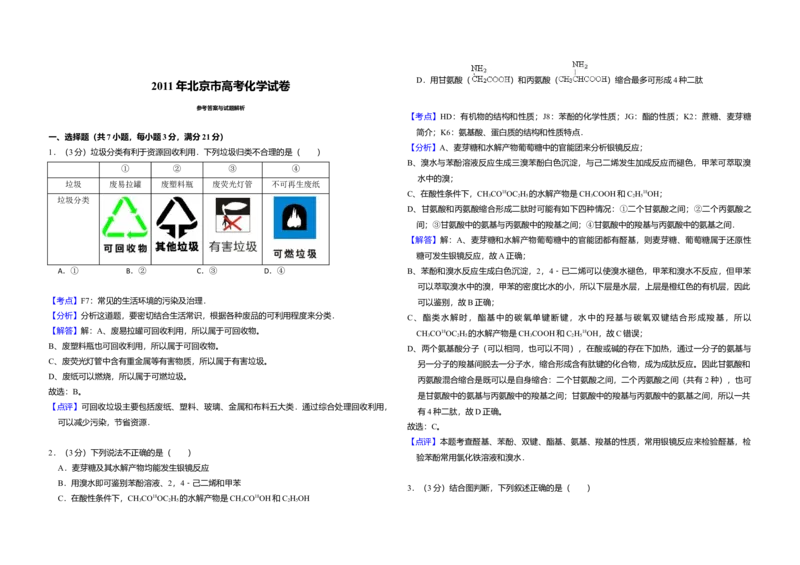
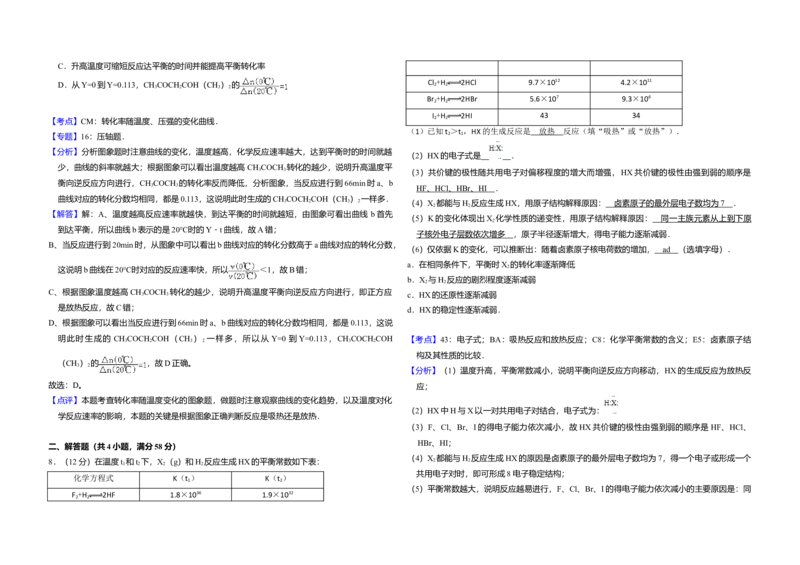
7.(3分)已知反应:2CH COCH (l) CH COCH COH(CH ) (l).取等量CH COCH ,分
D.用甘氨酸( )和丙氨酸( )缩合最多可形成4种二肽 3 3 3 2 3 2 3 3
别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y﹣t)如图所示.下列说法正确
⇌
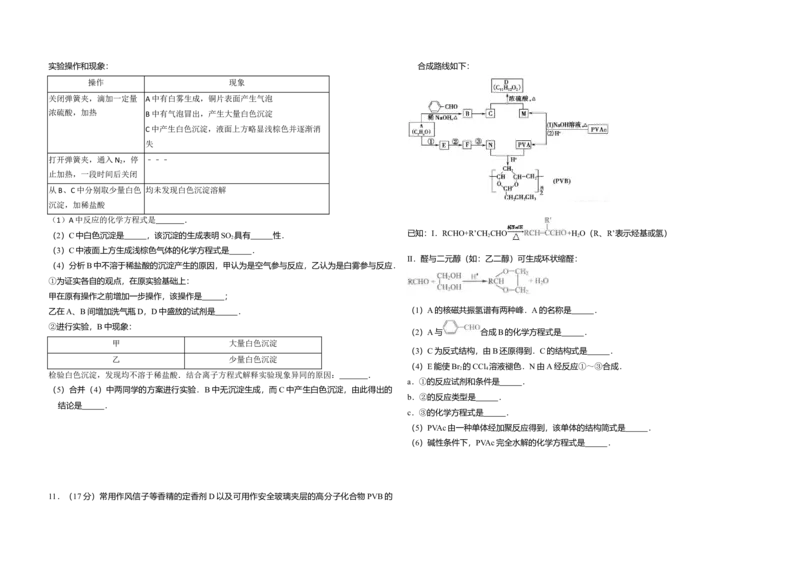
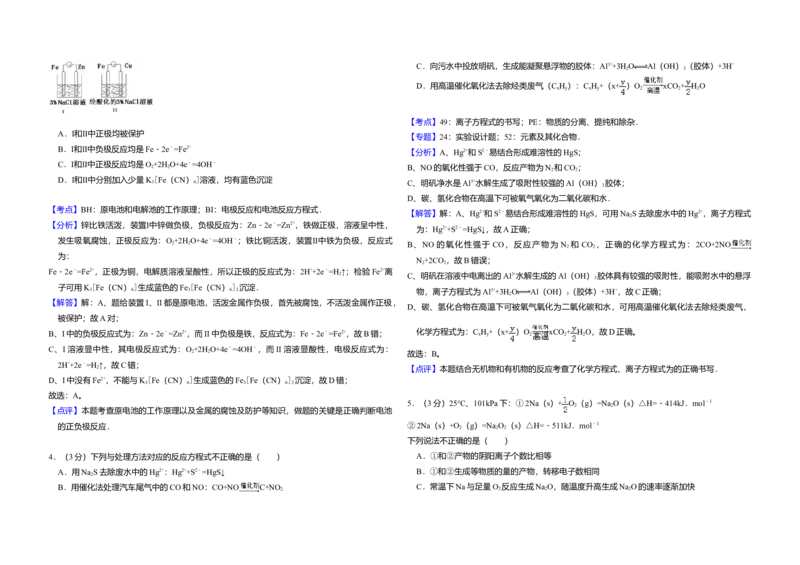
3.(3分)结合图判断,下列叙述正确的是( )
的是( )
A.Ⅰ和Ⅱ中正极均被保护
B.Ⅰ和Ⅱ中负极反应均是Fe﹣2e﹣=Fe2+
C.Ⅰ和Ⅱ中正极反应均是O +2H O+4e﹣=4OH﹣ A.b代表0℃下CH COCH 的Y﹣t曲线
2 2 3 3
D.Ⅰ和Ⅱ中分别加入少量K [Fe(CN) ]溶液,均有蓝色沉淀
3 6 B.反应进行到20min末,CH COCH 的
3 3
4.(3分)下列与处理方法对应的反应方程式不正确的是( )
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
A.用Na S去除废水中的Hg2+:Hg2++S2﹣=HgS↓
2D.从Y=0到Y=0.113,CH COCH COH(CH ) 的
3 2 3 2
二、解答题(共4小题,满分58分)
8.(12分)在温度t 1 和t 2 下,X 2 (g)和H 2 反应生成HX的平衡常数如下表: ①盐泥a除泥沙外,还含有的物质是 .
化学方程式 K(t ) K(t ) ②过程I中将NH +转化为N 的离子方程式是 .
1 2 4 2
F 2 +H 2 2HF 1.8×1036 1.9×1032 ③BaSO 4 的溶解度比BaCO 3 的小.过程II中除去的离子有 .
Cl +H 2HCl 9.7×1012 4.2×1011 ④经过程 III 处理,要求盐水 c 中剩余 Na 2 SO 3 的含量小于 5mg/L.若盐水 b 中 NaClO 的含量是
2 2
7.45mg/L,则处理10m3盐水b,至多添加10% Na SO 溶液 kg(溶液体积变化忽略不计).
Br +H 2HBr 5.6×107 9.3×106 2 3
2 2
I +H 2HI 43 34
2 2
(1)已知t >t ,HX的生成反应是 反应(填“吸热”或“放热”).
2 1
(2)HX的电子式是 .
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是
.
(4)X 都能与H 反应生成HX,用原子结构解释原因: .
2 2
(5)K的变化体现出X 2 化学性质的递变性,用原子结构解释原因: ,原子半径逐渐增大, 10.(15分)甲、乙两同学为探究SO 2 与可溶性钡的强酸盐能否反应生成白色BaSO 3 沉淀,用下
得电子能力逐渐减弱. 图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加, (选填字母).
a.在相同条件下,平衡时X 的转化率逐渐降低
2
b.X 与H 反应的剧烈程度逐渐减弱
2 2
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱.
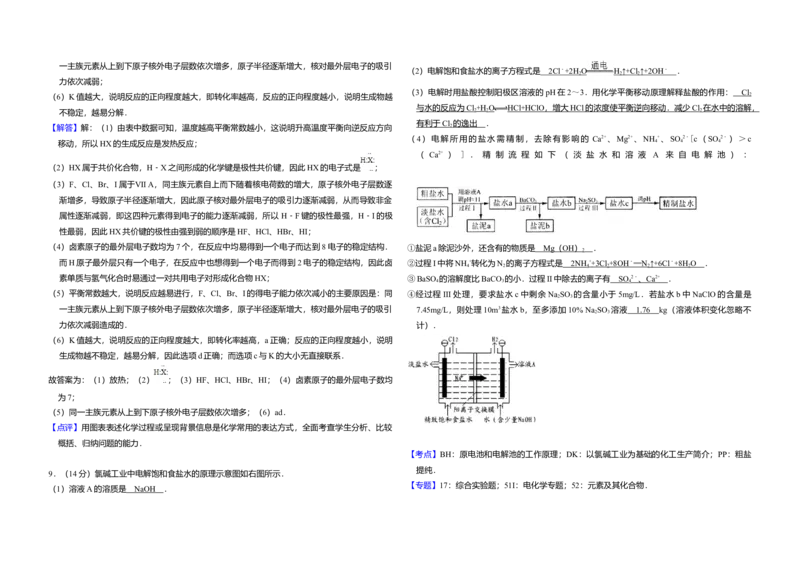
9.(14分)氯碱工业中电解饱和食盐水的原理示意图如右图所示.
(1)溶液A的溶质是 .
(2)电解饱和食盐水的离子方程式是 .
(3)电解时用盐酸控制阳极区溶液的pH在2~3.用化学平衡移动原理解释盐酸的作用: .
(4)电解所用的盐水需精制,去除有影响的 Ca2+、Mg2+、NH +、SO 2﹣[c(SO 2﹣)>c
4 4 4
(Ca2+)].精制流程如下(淡盐水和溶液A来自电解池):实验操作和现象: 合成路线如下:
操作 现象
关闭弹簧夹,滴加一定量 A中有白雾生成,铜片表面产生气泡
浓硫酸,加热 B中有气泡冒出,产生大量白色沉淀
C中产生白色沉淀,液面上方略显浅棕色并逐渐消
失
打开弹簧夹,通入N ,停 ﹣﹣﹣
2
止加热,一段时间后关闭
从B、C中分别取少量白色 均未发现白色沉淀溶解
沉淀,加稀盐酸
(1)A中反应的化学方程式是 .
(2)C中白色沉淀是 ,该沉淀的生成表明SO 2 具有 性. 已知:Ⅰ.RCHO+R’CH 2 CHO +H 2 O(R、R’表示烃基或氢)
(3)C中液面上方生成浅棕色气体的化学方程式是 .
Ⅱ.醛与二元醇(如:乙二醇)可生成环状缩醛:
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是 ;
乙在A、B间增加洗气瓶D,D中盛放的试剂是 . (1)A的核磁共振氢谱有两种峰.A的名称是 .
②进行实验,B中现象:
(2)A与 合成B的化学方程式是 .
甲 大量白色沉淀
(3)C为反式结构,由B还原得到.C的结构式是 .
乙 少量白色沉淀
(4)E能使Br 的CCl 溶液褪色.N由A经反应①~③合成.
2 4
检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释实验现象异同的原因: .
a.①的反应试剂和条件是 .
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的
b.②的反应类型是 .
结论是 .
c.③的化学方程式是 .
(5)PVAc由一种单体经加聚反应得到,该单体的结构简式是 .
(6)碱性条件下,PVAc完全水解的化学方程式是 .
11.(17分)常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分子化合物PVB的D.用甘氨酸( )和丙氨酸( )缩合最多可形成4种二肽
2011 年北京市高考化学试卷
参考答案与试题解析
【考点】HD:有机物的结构和性质;J8:苯酚的化学性质;JG:酯的性质;K2:蔗糖、麦芽糖
简介;K6:氨基酸、蛋白质的结构和性质特点.
一、选择题(共7小题,每小题3分,满分21分) 菁优网版权所有
【分析】A、麦芽糖和水解产物葡萄糖中的官能团来分析银镜反应;
1.(3分)垃圾分类有利于资源回收利用.下列垃圾归类不合理的是( )
B、溴水与苯酚溶液反应生成三溴苯酚白色沉淀,与己二烯发生加成反应而褪色,甲苯可萃取溴
① ② ③ ④
水中的溴;
垃圾 废易拉罐 废塑料瓶 废荧光灯管 不可再生废纸
C、在酸性条件下,CH CO18OC H 的水解产物是CH COOH和C H 18OH;
3 2 5 3 2 5
垃圾分类
D、甘氨酸和丙氨酸缩合形成二肽时可能有如下四种情况:①二个甘氨酸之间;②二个丙氨酸之
间;③甘氨酸中的氨基与丙氨酸中的羧基之间;④甘氨酸中的羧基与丙氨酸中的氨基之间.
【解答】解:A、麦芽糖和水解产物葡萄糖中的官能团都有醛基,则麦芽糖、葡萄糖属于还原性
糖可发生银镜反应,故A正确;
A.① B.② C.③ D.④ B、苯酚和溴水反应生成白色沉淀,2,4﹣已二烯可以使溴水褪色,甲苯和溴水不反应,但甲苯
可以萃取溴水中的溴,甲苯的密度比水的小,所以下层是水层,上层是橙红色的有机层,因此
【考点】F7:常见的生活环境的污染及治理. 可以鉴别,故B正确;
菁优网版权所有
【分析】分析这道题,要密切结合生活常识,根据各种废品的可利用程度来分类. C、酯类水解时,酯基中的碳氧单键断键,水中的羟基与碳氧双键结合形成羧基,所以
【解答】解:A、废易拉罐可回收利用,所以属于可回收物。 CH CO18OC H 的水解产物是CH COOH和C H 18OH,故C错误;
3 2 5 3 2 5
B、废塑料瓶也可回收利用,所以属于可回收物。
D、两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与
C、废荧光灯管中含有重金属等有害物质,所以属于有害垃圾。
另一分子的羧基间脱去一分子水,缩合形成含有肽键的化合物,成为成肽反应。因此甘氨酸和
D、废纸可以燃烧,所以属于可燃垃圾。
丙氨酸混合缩合是既可以是自身缩合:二个甘氨酸之间,二个丙氨酸之间(共有 2种),也可
故选:B。
是甘氨酸中的氨基与丙氨酸中的羧基之间;甘氨酸中的羧基与丙氨酸中的氨基之间,所以一共
【点评】可回收垃圾主要包括废纸、塑料、玻璃、金属和布料五大类.通过综合处理回收利用,
有4种二肽,故D正确。
可以减少污染,节省资源.
故选:C。
【点评】本题考查醛基、苯酚、双键、酯基、氨基、羧基的性质,常用银镜反应来检验醛基,检
2.(3分)下列说法不正确的是( )
验苯酚常用氯化铁溶液和溴水.
A.麦芽糖及其水解产物均能发生银镜反应
B.用溴水即可鉴别苯酚溶液、2,4﹣己二烯和甲苯
3.(3分)结合图判断,下列叙述正确的是( )
C.在酸性条件下,CH CO18OC H 的水解产物是CH CO18OH和C H OH
3 2 5 3 2 5C.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H O Al(OH) (胶体)+3H+
2 3
D.用高温催化氧化法去除烃类废气(C H ):C H +(x+ )O xCO + H O
x y x y 2 2 2
【考点】49:离子方程式的书写;PE:物质的分离、提纯和除杂.
菁优网版权所有
A.Ⅰ和Ⅱ中正极均被保护
【专题】24:实验设计题;52:元素及其化合物.
B.Ⅰ和Ⅱ中负极反应均是Fe﹣2e﹣=Fe2+
【分析】A、Hg2+和S2﹣易结合形成难溶性的HgS;
C.Ⅰ和Ⅱ中正极反应均是O +2H O+4e﹣=4OH﹣
2 2 B、NO的氧化性强于CO,反应产物为N 和CO ;
2 2
D.Ⅰ和Ⅱ中分别加入少量K
3
[Fe(CN)
6
]溶液,均有蓝色沉淀
C、明矾净水是Al3+水解生成了吸附性较强的Al(OH) 胶体;
3
D、碳、氢化合物在高温下可被氧气氧化为二氧化碳和水.
【考点】BH:原电池和电解池的工作原理;BI:电极反应和电池反应方程式.
菁优网版权所有
【解答】解:A、Hg2+和S2﹣易结合形成难溶性的HgS,可用Na
2
S去除废水中的Hg2+,离子方程式
【分析】锌比铁活泼,装置Ⅰ中锌做负极,负极反应为:Zn﹣2e﹣=Zn2+,铁做正极,溶液呈中性,
为:Hg2++S2﹣=HgS↓,故A正确;
发生吸氧腐蚀,正极反应为:O +2H O+4e﹣=4OH﹣;铁比铜活泼,装置Ⅱ中铁为负极,反应式
2 2 B、NO 的氧化性强于 CO,反应产物为 N 和 CO ,正确的化学方程式为:2CO+2NO
2 2
为:
N +2CO ,故B错误;
2 2
Fe﹣2e﹣=Fe2+,正极为铜,电解质溶液呈酸性,所以正极的反应式为:2H++2e﹣=H ↑;检验Fe2+离
2 C、明矾在溶液中电离出的Al3+水解生成的Al(OH) 胶体具有较强的吸附性,能吸附水中的悬浮
3
子可用K [Fe(CN) ]生成蓝色的Fe [Fe(CN) ] 沉淀.
3 6 3 6 2 物,离子方程式为Al3++3H O Al(OH) (胶体)+3H+,故C正确;
2 3
【解答】解:A、题给装置I、II都是原电池,活泼金属作负极,首先被腐蚀,不活泼金属作正极,
D、碳、氢化合物在高温下可被氧气氧化为二氧化碳和水,可用高温催化氧化法去除烃类废气,
被保护;故A对;
B、I中的负极反应式为:Zn﹣2e﹣=Zn2+,而II中负极是铁,反应式为:Fe﹣2e﹣=Fe2+,故B错; 化学方程式为:C
x
H
y
+(x+ )O
2
xCO
2
+ H
2
O,故D正确。
C、I溶液显中性,其电极反应式为:O +2H O+4e﹣=4OH﹣,而II溶液显酸性,电极反应式为:
2 2 故选:B。
2H++2e﹣=H ↑,故C错;
2 【点评】本题结合无机物和有机物的反应考查了化学方程式、离子方程式为的正确书写.
D、I中没有Fe2+,不能与K [Fe(CN) ]生成蓝色的Fe [Fe(CN) ] 沉淀,故D错;
3 6 3 6 2
故选:A。
5.(3分)25℃、101kPa下:①2Na(s)+ O (g)=Na O(s)△H=﹣414kJ.mol﹣1
2 2
【点评】本题考查原电池的工作原理以及金属的腐蚀及防护等知识,做题的关键是正确判断电池
的正负极反应. ②2Na(s)+O 2 (g)=Na 2 O 2 (s)△H=﹣511kJ.mol﹣1
下列说法不正确的是( )
4.(3分)下列与处理方法对应的反应方程式不正确的是( ) A.①和②产物的阴阳离子个数比相等
A.用Na S去除废水中的Hg2+:Hg2++S2﹣=HgS↓ B.①和②生成等物质的量的产物,转移电子数相同
2
B.用催化法处理汽车尾气中的CO和NO:CO+NO C+NO C.常温下Na与足量O 反应生成Na O,随温度升高生成Na O的速率逐渐加快
2 2 2 2D.25℃、101kPa下:Na O (s)+2Na(s)=2Na O(s)△H=﹣317kJ.mol﹣1
2 2 2
【考点】U5:化学实验方案的评价.
菁优网版权所有
【考点】BE:热化学方程式;GE:钠的化学性质. 【专题】16:压轴题.
菁优网版权所有
【专题】517:化学反应中的能量变化;52:元素及其化合物. 【分析】实验方案是否可行,关键看根据测量数据能否计算出结果.
【分析】A、Na O中阴阳离子个数之比为1:2,Na O 中阴阳离子个数之比为1:2; A、此方案利用碳酸氢钠的不稳定性,利用差量法即可计算质量分数;
2 2 2
B、由钠原子的个数及钠元素的化合价分析转移的电子数; B、根据钠守恒,可列方程组求解;
C、常温下Na与足量O 反应生成Na O,随温度升高生成Na O 的速率逐渐加快; C、C项应先把水蒸气排除才合理;
2 2 2 2
D、利用已知的两个反应和盖斯定律来分析; D、根据质量关系,可列方程组求解.
【解答】解:A、在Na O中阳离子是钠离子、阴离子是氧离子,Na O 中阳离子是钠离子、阴离 【解答】解:A、在Na CO 和NaHCO 中,加热能分解的只有NaHCO ,故A项成立;
2 2 2 2 3 3 3
子是过氧根离子,因此阴、阳离子的个数比都是 1:2,①和②产物的阴阳离子个数比相等,故 B、反应后加热、蒸干、灼烧得到的固体产物是NaCl,Na 2 CO 3 和NaHCO 3 转化为NaCl时的固体质
A正确; 量变化不同,由钠元素守恒和质量关系,可列方程组计算,故B项成立;
B、由钠原子守恒可知,①和②生成等物质的量的产物时,钠元素的化合价都是由 0升高到+1价, C、C项中碱石灰可以同时吸收CO
2
和水蒸气,则无法计算,故C项错误;
则转移的电子数相同,故B正确; D、Na 2 CO 3 和NaHCO 3 转化为BaCO 3 时的固体质量变化不同,利用质量关系来计算,故D项成立。
C、常温下Na与足量O 反应生成Na O,随温度升高生成 Na O 的速率逐渐加快,而不是氧化钠, 故选:C。
2 2 2 2
故C错误; 【点评】本题看似是实验设计,实际上是从定性和定量两个角度考察碳酸钠和碳酸氢钠性质的不
D、热化学方程式25℃、101kPa下: 同.
①2Na(s)+ O (g)═Na O(s)△H=﹣414kJ•mol﹣1,
2 2
7.(3分)已知反应:2CH COCH (l) CH COCH COH(CH ) (l).取等量CH COCH ,分
3 3 3 2 3 2 3 3
②2Na(s)+O (g)═Na O (s)△H=﹣511kJ•mol﹣1,
2 2 2 别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y﹣t)如图所示.下列说法正确
⇌
①×2﹣②可得:Na O (s)+2Na(s)═2Na O(s)△H=﹣317kJ•mol﹣1,故D正确;
2 2 2 的是( )
故选:C。
【点评】本题是一综合题,考查化学键类型、氧化还原反应的计算、元素化合物知识、以及盖斯
定律,考查了多个考点,设点全面,题目难度适中.
6.(3分)下列实验方案中,不能测定Na CO 和NaHCO 混合物中Na CO 质量分数( )
2 3 3 2 3
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 A.b代表0℃下CH COCH 的Y﹣t曲线
3 3
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
B.反应进行到20min末,CH COCH 的
3 3
D.取a克混合物与足量Ba(OH) 溶液充分反应,过滤、洗涤、烘干,得b克固体
2C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
Cl +H 2HCl 9.7×1012 4.2×1011
D.从Y=0到Y=0.113,CH COCH COH(CH ) 的 2 2
3 2 3 2
Br +H 2HBr 5.6×107 9.3×106
2 2
I +H 2HI 43 34
2 2
【考点】CM:转化率随温度、压强的变化曲线.
菁优网版权所有
(1)已知t >t ,HX的生成反应是 放热 反应(填“吸热”或“放热”).
【专题】16:压轴题. 2 1
【分析】分析图象题时注意曲线的变化,温度越高,化学反应速率越大,达到平衡时的时间就越
(2)HX的电子式是 .
少,曲线的斜率就越大;根据图象可以看出温度越高 CH COCH 转化的越少,说明升高温度平
3 3 (3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是
衡向逆反应方向进行,CH COCH 的转化率反而降低,分析图象,当反应进行到 66min时a、b
3 3 HF 、 HCl 、 HBr 、 HI .
曲线对应的转化分数均相同,都是0.113,这说明此时生成的CH COCH COH(CH ) 一样多.
3 2 3 2 (4)X 都能与H 反应生成HX,用原子结构解释原因: 卤素原子的最外层电子数均为 7 .
2 2
【解答】解:A、温度越高反应速率就越快,到达平衡的时间就越短,由图象可看出曲线 b首先
(5)K的变化体现出X 化学性质的递变性,用原子结构解释原因: 同一主族元素从上到下原
2
到达平衡,所以曲线b表示的是20℃时的Y﹣t曲线,故A错;
子核外电子层数依次增多 ,原子半径逐渐增大,得电子能力逐渐减弱.
B、当反应进行到20min时,从图象中可以看出b曲线对应的转化分数高于a曲线对应的转化分数,
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加, ad (选填字母).
a.在相同条件下,平衡时X 的转化率逐渐降低
这说明b曲线在20℃时对应的反应速率快,所以 <1,故B错; 2
b.X 与H 反应的剧烈程度逐渐减弱
2 2
C、根据图象温度越高CH COCH 转化的越少,说明升高温度平衡向逆反应方向进行,即正方应
3 3 c.HX的还原性逐渐减弱
是放热反应,故C错;
d.HX的稳定性逐渐减弱.
D、根据图象可以看出当反应进行到66min时a、b曲线对应的转化分数均相同,都是0.113,这说
明此时生成的 CH
3
COCH
2
COH(CH
3
)
2
一样多,所以从 Y=0 到 Y=0.113,CH
3
COCH
2
COH 【考点】43:电子式;BA:吸热反应和放热反应;C8:化学平衡常数的含义;E5:卤素原子结
构及其性质的比较.
(CH ) 的 ,故D正确。 菁优网版权所有
3 2
【分析】(1)温度升高,平衡常数减小,说明平衡向逆反应方向移动,HX的生成反应为放热反
故选:D。 应;
【点评】本题考查转化率随温度变化的图象题,做题时注意观察曲线的变化趋势,以及温度对化
(2)HX中H与X以一对共用电子对结合,电子式为:
学反应速率的影响,本题的关键是根据图象正确判断反应是吸热还是放热.
(3)F、Cl、Br、I的得电子能力依次减小,故 HX共价键的极性由强到弱的顺序是 HF、HCl、
HBr、HI;
二、解答题(共4小题,满分58分)
(4)X 都能与H 反应生成HX的原因是卤素原子的最外层电子数均为 7,得一个电子或形成一个
8.(12分)在温度t 和t 下,X (g)和H 反应生成HX的平衡常数如下表: 2 2
1 2 2 2
共用电子对时,即可形成8电子稳定结构;
化学方程式 K(t ) K(t )
1 2
(5)平衡常数越大,说明反应越易进行,F、Cl、Br、I的得电子能力依次减小的主要原因是:同
F +H 2HF 1.8×1036 1.9×1032
2 2一主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,核对最外层电子的吸引
(2)电解饱和食盐水的离子方程式是 2Cl ﹣ + 2H O H ↑ + Cl ↑ + 2OH ﹣ .
2 2 2
力依次减弱;
(3)电解时用盐酸控制阳极区溶液的pH在2~3.用化学平衡移动原理解释盐酸的作用: Cl
(6)K值越大,说明反应的正向程度越大,即转化率越高,反应的正向程度越小,说明生成物越 2
与水的反应为 Cl + H O HCl + HClO ,增大 HCl 的浓度使平衡逆向移动.减少 Cl 在水中的溶解 ,
不稳定,越易分解. 2 2 2
有利于 Cl 的逸出 .
【解答】解:(1)由表中数据可知,温度越高平衡常数越小,这说明升高温度平衡向逆反应方向 2
(4)电解所用的盐水需精制,去除有影响的 Ca2+、Mg2+、NH +、SO 2﹣[c(SO 2﹣)>c
移动,所以HX的生成反应是发热反应; 4 4 4
( Ca2+ ) ] . 精 制 流 程 如 下 ( 淡 盐 水 和 溶 液 A 来 自 电 解 池 ) :
(2)HX属于共价化合物,H﹣X之间形成的化学键是极性共价键,因此HX的电子式是 ;
(3)F、Cl、Br、I属于ⅦA,同主族元素自上而下随着核电荷数的增大,原子核外电子层数逐
渐增多,导致原子半径逐渐增大,因此原子核对最外层电子的吸引力逐渐减弱,从而导致非金
属性逐渐减弱,即这四种元素得到电子的能力逐渐减弱,所以 H﹣F键的极性最强,H﹣I的极
性最弱,因此HX共价键的极性由强到弱的顺序是HF、HCl、HBr、HI;
(4)卤素原子的最外层电子数均为7个,在反应中均易得到一个电子而达到 8电子的稳定结构. ①盐泥a除泥沙外,还含有的物质是 Mg ( OH ) .
2
而H原子最外层只有一个电子,在反应中也想得到一个电子而得到 2电子的稳定结构,因此卤 ②过程I中将NH +转化为N 的离子方程式是 2NH + + 3C l + 8OH ﹣ ═ N ↑ + 6Cl ﹣ + 8H O .
4 2 4 2 2 2
素单质与氢气化合时易通过一对共用电子对形成化合物HX; ③BaSO 的溶解度比BaCO 的小.过程II中除去的离子有 SO 2﹣ 、 Ca 2 + .
4 3 4
(5)平衡常数越大,说明反应越易进行,F、Cl、Br、I的得电子能力依次减小的主要原因是:同 ④经过程 III 处理,要求盐水 c 中剩余 Na SO 的含量小于 5mg/L.若盐水 b 中 NaClO 的含量是
2 3
一主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,核对最外层电子的吸引 7.45mg/L,则处理10m3盐水b,至多添加10% Na SO 溶液 1.76 kg(溶液体积变化忽略不
2 3
力依次减弱造成的. 计).
(6)K值越大,说明反应的正向程度越大,即转化率越高,a正确;反应的正向程度越小,说明
生成物越不稳定,越易分解,因此选项d正确;而选项c与K的大小无直接联系.
故答案为:(1)放热;(2) ;(3)HF、HCl、HBr、HI;(4)卤素原子的最外层电子数均
为7;
(5)同一主族元素从上到下原子核外电子层数依次增多;(6)ad.
【点评】用图表表述化学过程或呈现背景信息是化学常用的表达方式,全面考查学生分析、比较
概括、归纳问题的能力.
【考点】BH:原电池和电解池的工作原理;DK:以氯碱工业为基础的化工生产简介;PP:粗盐
提纯.
9.(14分)氯碱工业中电解饱和食盐水的原理示意图如右图所示.
菁优网版权所有
【专题】17:综合实验题;51I:电化学专题;52:元素及其化合物.
(1)溶液A的溶质是 NaOH .【分析】(1)根据电极反应判断阴极产物; 添加10% Na SO 溶液50g÷10%=0.5kg,因此至多添加10%Na SO 溶液
2 3 2 3
(2)根据两极的反应书写电解反应式; 的质量为1.26kg+0.5kg=1.76kg.故答案为:1.76.
(3)根据阳极产物和平衡移动原理分析; 【点评】本题考查饱和食盐水的电解和粗盐的提纯,题目较为综合,注意平衡移动原理的应用以
(4)①根据杂质离子和溶液的酸碱性判断能反应生成的沉淀; 及物质的量应用于化学方程式的计算.做题时注意题中所给信息,用守恒的方法解答.
②根据A溶液成分和可能具有的性质,结合氧化还原反应和质量守恒定律书写离子方程式;
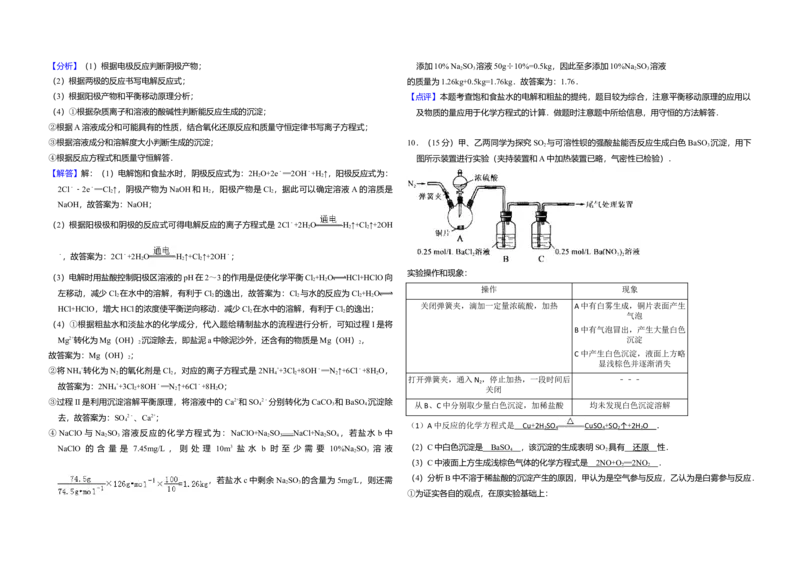
③根据溶液成分和溶解度大小判断生成的沉淀; 10.(15分)甲、乙两同学为探究SO 与可溶性钡的强酸盐能否反应生成白色BaSO 沉淀,用下
2 3
④根据反应方程式和质量守恒解答. 图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).
【解答】解:(1)电解饱和食盐水时,阴极反应式为:2H O+2e﹣═2OH﹣+H ↑,阳极反应式为:
2 2
2Cl﹣﹣2e﹣═Cl ↑,阴极产物为NaOH和H ,阳极产物是 Cl ,据此可以确定溶液 A的溶质是
2 2 2
NaOH,故答案为:NaOH;
(2)根据阳极极和阴极的反应式可得电解反应的离子方程式是 2Cl﹣+2H O H ↑+Cl ↑+2OH
2 2 2
﹣,故答案为:2Cl﹣+2H O H ↑+Cl ↑+2OH﹣;
2 2 2
实验操作和现象:
(3)电解时用盐酸控制阳极区溶液的pH在2~3的作用是促使化学平衡Cl +H O HCl+HClO向
2 2
操作 现象
左移动,减少Cl 在水中的溶解,有利于Cl 的逸出,故答案为:Cl 与水的反应为Cl +H O
2 2 2 2 2
关闭弹簧夹,滴加一定量浓硫酸,加热 A中有白雾生成,铜片表面产生
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl 在水中的溶解,有利于Cl 的逸出;
2 2
气泡
(4)①根据粗盐水和淡盐水的化学成分,代入题给精制盐水的流程进行分析,可知过程 I是将
B中有气泡冒出,产生大量白色
Mg2+转化为Mg(OH) 沉淀除去,即盐泥a中除泥沙外,还含有的物质是Mg(OH) , 沉淀
2 2
故答案为:Mg(OH) ;
C中产生白色沉淀,液面上方略
2
显浅棕色并逐渐消失
②将NH +转化为N 的氧化剂是Cl ,对应的离子方程式是 2NH ++3Cl +8OH﹣═N ↑+6Cl﹣+8H O,
4 2 2 4 2 2 2
打开弹簧夹,通入N ,停止加热,一段时间后 ﹣﹣﹣
2
故答案为:2NH ++3Cl +8OH﹣═N ↑+6Cl﹣+8H O;
4 2 2 2 关闭
③过程II是利用沉淀溶解平衡原理,将溶液中的 Ca2+和SO 2﹣分别转化为CaCO 和BaSO 沉淀除
4 3 4 从B、C中分别取少量白色沉淀,加稀盐酸 均未发现白色沉淀溶解
去,故答案为:SO 2﹣、Ca2+;
4
(1)A中反应的化学方程式是 Cu + 2H SO CuSO + SO ↑ + 2H O .
2 4 4 2 2
④ NaClO 与 Na SO 溶液反应的化学方程式为:NaClO+Na SO NaCl+Na SO ,若盐水 b 中
2 3 2 3 2 4
NaClO 的 含 量 是 7.45mg/L , 则 处 理 10m3 盐 水 b 时 至 少 需 要 10%Na 2 SO 3 溶 液 (2)C中白色沉淀是 BaSO 4 ,该沉淀的生成表明SO 2 具有 还原 性.
(3)C中液面上方生成浅棕色气体的化学方程式是 2NO + O ═ 2NO .
2 2
,若盐水 c中剩余 Na SO 的含量为 5mg/L,则还需
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
2 3
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是 通 N 一段时间,排除装置中的空气 ; (2)A中生成气体SO ,C中的白色沉淀不溶于稀盐酸,说明 C中沉淀为是BaSO ,原因是硝酸
2 2 4
乙在A、B间增加洗气瓶D,D中盛放的试剂是 饱和 NaHSO 溶液 . 根离子在酸性条件下具有强氧化性,能将SO 氧化为SO 2﹣,说明SO 具有还原性;
3 2 4 2
②进行实验,B中现象: (3)C中发生的反应是3SO +3Ba2++2NO ﹣+2H O═3BaSO ↓+2NO↑+4H+,C中液面上方生成浅棕
2 3 2 4
甲 大量白色沉淀 色气体则是硝酸还原生成的 NO 遇 O 生成了红棕色的 NO 之故,化学方程式是
2 2
乙 少量白色沉淀 2NO+O ═2NO ;
2 2
检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释实验现象异同的原因: 甲: SO 2﹣ (4)A中白雾与氯化钡反应能生成BaSO 沉淀,故其可能含有SO 或H SO ,;甲同学为排除装
4 4 3 2 4
+ B a 2 + ═ BaSO ↓ ,乙: 2Ba 2 + + 2SO + O + 2H O ═ 2BaSO ↓ + 4H + ,白雾的量远多于装置中 O 的量 . 置内空气对实验结果的影响,在Cu与浓硫酸反应前,可先通一会儿N ;A中白雾可能含有SO
4 2 2 2 4 2 2 3
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的 或 H SO ,乙同学为除去白雾或 SO 中的 SO ,可在 A、B 间增加一个盛放浓硫酸或饱和
2 4 2 3
结论是 SO 与可溶性钡的强酸盐不能反应生成 BaSO 沉淀 . NaHSO 溶液的洗气瓶;在甲、乙两同学的实验中,B中均出现了不溶于稀盐酸的白色沉淀,说
2 3 3
明该白色沉淀都是BaSO ,由于甲同学没有排除白雾的干扰,故生成BaSO 沉淀的离子方程式
4 4
【考点】F5:二氧化硫的化学性质;U2:性质实验方案的设计. 为 SO 2﹣+Ba2+═BaSO ↓;乙同学没有排除空气的干扰,其生成 BaSO 的离子方程式为 2Ba2+
菁优网版权所有 4 4 4
【专题】16:压轴题. +2SO +O +2H O═2BaSO ↓+4H+,白雾的量远多于装置中氧气的量,所以甲中产生大量白色沉
2 2 2 4
【分析】(1)由题给实验目的和实验可知,A 中发生的反应方程式为:Cu+2H SO 淀,乙中产生少量白色沉淀;
2 4
(5)合并甲、乙两同学的方案进行实验时,B中无沉淀生成,C中产生白色沉淀,说明 SO 与可
2
CuSO +SO ↑+2H O;
4 2 2
溶性钡的强酸盐不能反应生成BaSO 沉淀.
3
(2)C中白色沉淀不溶于稀盐酸,说明沉淀是BaSO ,原因是硝酸根离子在酸性条件下具有强氧
4
故答案为:(1)Cu+2H SO ═CuSO +SO ↑+2H O;
2 4 4 2 2
化性,能将SO 氧化为SO 2﹣,说明SO 具有还原性;
2 4 2
(2)BaSO ,还原;
4
(3)C中液面上方生成浅棕色气体则是硝酸还原生成的NO,遇O 生成了红棕色的NO 之故,化
2 2
(3)2NO+O ═2NO ,
2 2
学方程式是2NO+O ═2NO ;
2 2
(4)①通N 一段时间,排除装置中的空气;饱和NaHSO 溶液;
2 3
(4)甲同学为排除装置内空气对实验结果的影响,在 Cu与浓硫酸反应前,可先通一会儿 N ;乙
2
②甲:SO 2﹣+Ba2+═BaSO ↓,乙:2Ba2++2SO +O +2H O═2BaSO ↓+4H+,白雾的量远多于装置中
4 4 2 2 2 4
同学为除去白雾或SO 中的
2
O 的量;
2
SO ,可在A、B间增加一个盛放浓硫酸或饱和NaHSO 溶液的洗气瓶;
3 3
(5)SO 与可溶性钡的强酸盐不能反应生成BaSO 沉淀.
2 3
由于甲同学没有排除白雾的干扰,生成 BaSO 沉淀的离子方程式为SO 2﹣+Ba2+═BaSO ↓;乙同学
4 4 4
【点评】本题主要考查了SO 的制取、性质及BaSO 、BaSO 的性质知识等,同时考查了学生的实
2 3 4
没有排除空气的干扰,其生成BaSO 的离子方程式为2Ba2++2SO +O +2H O═2BaSO ↓+4H+;
4 2 2 2 4
验设计、分析、检验、推断等基本技能,充分考查了学生的思维分析能力等,综合性强.
(5)合并甲、乙两同学的方案进行实验时,B中无沉淀生成,C中产生白色沉淀,说明 SO 与可
2
溶性钡的强酸盐不能反应生成BaSO 沉淀.
3
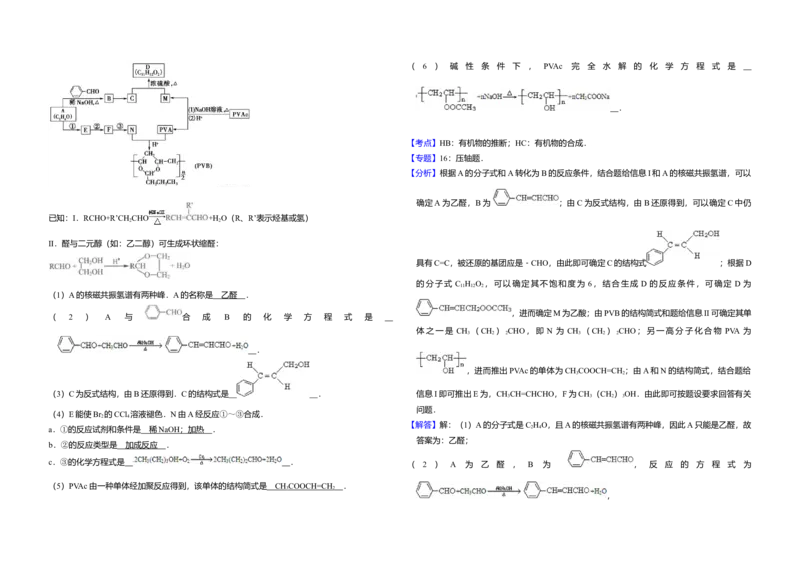
11.(17分)常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分子化合物PVB的
【解答】解:(1)铜和浓硫酸加热条件下生成硫酸铜、二氧化硫和水,化学方程式为:
合成路线如下:
Cu+2H SO CuSO +SO ↑+2H O;
2 4 4 2 2( 6 ) 碱 性 条 件 下 , PVAc 完 全 水 解 的 化 学 方 程 式 是
.
【考点】HB:有机物的推断;HC:有机物的合成.
菁优网版权所有
【专题】16:压轴题.
【分析】根据A的分子式和A转化为B的反应条件,结合题给信息I和A的核磁共振氢谱,可以
确定A为乙醛,B为 ;由C为反式结构,由 B还原得到,可以确定 C中仍
已知:Ⅰ.RCHO+R’CH CHO +H O(R、R’表示烃基或氢)
2 2
Ⅱ.醛与二元醇(如:乙二醇)可生成环状缩醛:
具有C=C,被还原的基团应是﹣CHO,由此即可确定C的结构式 ;根据D
的分子式 C H O ,可以确定其不饱和度为 6,结合生成 D 的反应条件,可确定 D 为
11 12 2
(1)A的核磁共振氢谱有两种峰.A的名称是 乙醛 .
,进而确定M为乙酸;由PVB的结构简式和题给信息II可确定其单
( 2 ) A 与 合 成 B 的 化 学 方 程 式 是
体之一是 CH (CH ) CHO,即 N 为 CH (CH ) CHO;另一高分子化合物 PVA 为
3 2 2 3 2 2
.
,进而推出PVAc的单体为CH COOCH=CH ;由A和N的结构简式,结合题给
3 2
(3)C为反式结构,由B还原得到.C的结构式是 . 信息I即可推出E为,CH CH=CHCHO,F为CH (CH ) OH.由此即可按题设要求回答有关
3 3 2 3
问题.
(4)E能使Br 的CCl 溶液褪色.N由A经反应①~③合成.
2 4
【解答】解:(1)A的分子式是C H O,且A的核磁共振氢谱有两种峰,因此A只能是乙醛,故
a.①的反应试剂和条件是 稀 NaOH ;加热 . 2 4
答案为:乙醛;
b.②的反应类型是 加成反应 .
c.③的化学方程式是 . ( 2 ) A 为 乙 醛 , B 为 , 反 应 的 方 程 式 为
(5)PVAc由一种单体经加聚反应得到,该单体的结构简式是 CH COOCH=CH .
3 2
,故答案为: ;
故答案为: .
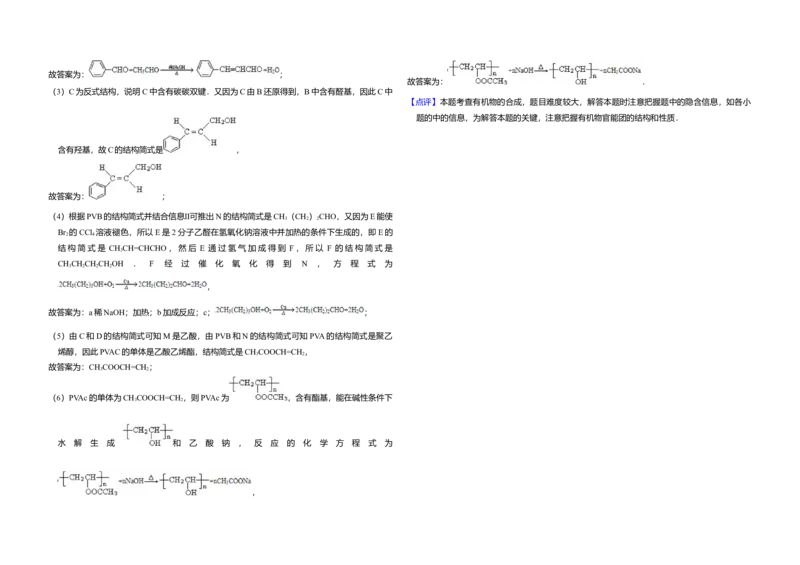
(3)C为反式结构,说明C中含有碳碳双键.又因为C由B还原得到,B中含有醛基,因此C中
【点评】本题考查有机物的合成,题目难度较大,解答本题时注意把握题中的隐含信息,如各小
题的中的信息,为解答本题的关键,注意把握有机物官能团的结构和性质.
含有羟基,故C的结构简式是 ,
故答案为: ;
(4)根据PVB的结构简式并结合信息Ⅱ可推出N的结构简式是CH (CH ) CHO,又因为E能使
3 2 2
Br 的CCl 溶液褪色,所以E是2分子乙醛在氢氧化钠溶液中并加热的条件下生成的,即E的
2 4
结构简式是 CH CH=CHCHO,然后 E 通过氢气加成得到 F,所以 F 的结构简式是
3
CH CH CH CH OH . F 经 过 催 化 氧 化 得 到 N , 方 程 式 为
3 2 2 2
,
故答案为:a稀NaOH;加热;b加成反应;c; ;
(5)由C和D的结构简式可知M是乙酸,由PVB和N的结构简式可知PVA的结构简式是聚乙
烯醇,因此PVAC的单体是乙酸乙烯酯,结构简式是CH COOCH=CH ,
3 2
故答案为:CH COOCH=CH ;
3 2
(6)PVAc的单体为CH COOCH=CH ,则PVAc为 ,含有酯基,能在碱性条件下
3 2
水 解 生 成 和 乙 酸 钠 , 反 应 的 化 学 方 程 式 为
,