文档内容
2011 年高考浙江化学试题及答案
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=
Cu2+
5.(2011浙江高考)褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。
1.(2011浙江高考)下列说法不正确的是
A.化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律
B.原子吸收光谱仪可用于测定物质中的金属元素,红外光谱仪可用于测定化合物的官能团
C.分子间作用力比化学键弱得多,但它对物质熔点、沸点有较大影响,而对溶解度无影响
D.酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对绿色化学、环境保护及节能减排
下列说法不正确的是
具有重要意义
A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点
2.(2011浙江高考)下列说法不正确的是
B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出
A.变色硅胶干燥剂含有CoCl ,干燥剂呈蓝色时,表示不具有吸水干燥功能
2 C.在一定条件下,色氨酸可发生缩聚反应
B.硝基苯制备实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触
D.褪黑素与色氨酸结构相似,也具有两性化合物的特性
C.中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必
6.(2011浙江高考)下列说法不正确的是
须干燥或润洗后方可使用
A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol氢键,且熔化热
D.除去干燥CO 中混有的少量SO ,可将混合气体依次通过盛有酸性KMnO 溶液、浓硫酸的洗气瓶
2 2 4 完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
3.(2011浙江高考)X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,
且最外层电子数之和为15,X与Z可形成XZ 分子;Y与M形成的气态化合物在标准状况下的密度为 0.76 g/L;
2 B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α, ,若加入少量醋酸钠固
W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
体,则CH COOH CH COO-+H+向左移动,α减小,K 变小
A.原子半径:W>Z>Y>X>M 3 3 a
C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265
B.XZ 、X M 、W Z 均为直线型的共价化合物
2 2 2 2 2
kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
C.由X元素形成的单质不一定是原子晶体
D.已知:Fe O (s)+ 3C(石墨)=2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 2 3
4.(2011浙江高考)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心
CO(g)+ O (g)=CO (g),△H=-283.0 kJ/mol;
2 2
区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示。
C(石墨)+O (g)=CO (g),△H=-393.5 kJ/mol;
2 2
导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是
则4Fe(s)+3O (g)=2Fe O (s),△H=-1641.0 kJ/mol
2 2 3
A.液滴中的Cl―由a区向b区迁移
7.(2011浙江高考)海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
B.液滴边缘是正极区,发生的电极反应为:
O +2H O+4e-=4OH-
2 2
C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a 区向b区
迁移,与b区的OH―形成Fe(OH) ,进一步氧化、脱水形成铁锈
2模拟海水中的 Na+ Mg2+ Ca2+ Cl― HCO ― (4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂。请设计实验方案,检验该加碘盐中的
3
离子浓度(mol/L) 0.439 0.050 0.011 0.560 0.001 Fe2+。_______________________________________________________________。
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
9.(2011浙江高考)某研究小组在实验室探究氨基甲酸铵(NH COONH )分解反应平衡常数和水解反应
2 4
已知:K sp (CaCO 3 )=4.96×10-9;K sp (MgCO 3 )=6.82×10-6;K sp [Ca(OH) 2 ]=4.68×10-6;K sp [Mg(OH) 2 ]=5.61×10- 速率的测定。
12。 (1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),
下列说法正确的是 在恒定温度下使其达到分解平衡:NH COONH (s) 2NH (g)+CO (g)。
2 4 3 2
A.沉淀物X为CaCO
3 实验测得不同温度下的平衡数据列于下表:
B.滤液M中存在Mg2+,不存在Ca2+
温度(℃) 15.0 20.0 25.0 30.0 35.0
C.滤液N中存在Mg2+、Ca2+ 平衡总压强(kPa) 5.7 8.3 12.0 17.1 24.0
D.步骤②中若改为加入 4.2 gNaOH固体,沉淀物Y为Ca(OH)
2
和Mg(OH)
2
的混合物 平衡气体总浓度(×10-3mol/
2.4 3.4 4.8 6.8 9.4
L)
8.(2011浙江高考)食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空
①可以判断该分解反应已经达到化学平衡的是___________。
气中的氧气以及光照、受热而引起的。已知:
氧化性:IO ->Fe3+>I ;还原性:S O 2->I-
3 2 2 3 A.2v(NH )=v(CO ) B.密闭容器中总压强不变
3 2
3I +6OH-=IO -+5I-+3H O;KI+I KI
2 3 2 2 3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO 、KI、Mg2+、Fe3+),用适量蒸
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
3
馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足
②根据表中数据,列式计算25.0℃时的分解平衡常数:__________________________。
量KI固体,溶液显淡黄色,用CCl 萃取,下层溶液显紫红色;第三份试液中加入适量KIO 固体后,滴加淀粉试
4 3
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下
剂,溶液不变色。
压缩容器体积,氨基甲酸铵固体的质量______(填“增加”、“减小”或“不变”)。
①加KSCN溶液显红色,该红色物质是_________(用化学式表示);CCl 中显紫红色的物质是
4
___________________(用电子式表示)。
④氨基甲酸铵分解反应的焓变△H____0,熵变△S___0(填>、<或=)。
②第二份试液中加入足量KI固体后,反应的离子方程式为___________________________、
(2)已知:NH COONH +2H O NH HCO +NH ·H O。该研究小组分别用三份不同初始浓度的氨基甲酸
________________。 2 4 2 4 3 3 2
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。
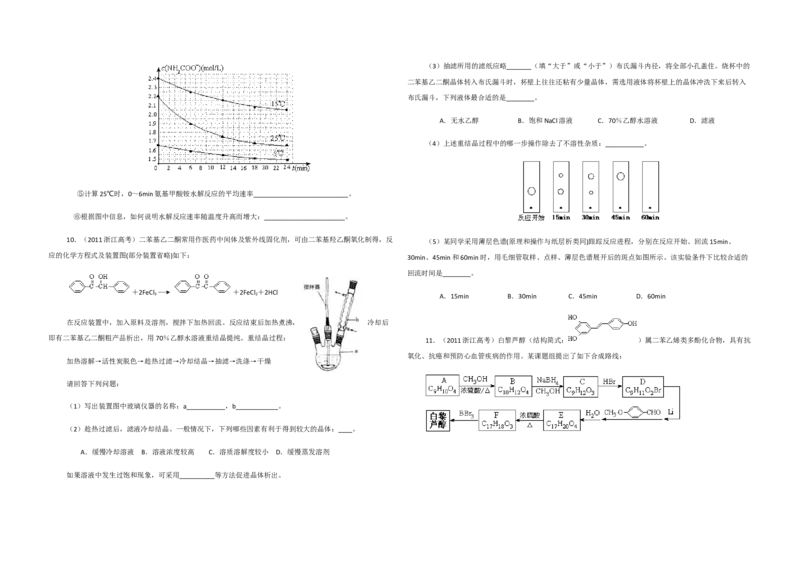
铵溶液测定水解反应速率,得到c(NH
2
COO-)随时间变化趋势如图所示。
写出潮湿环境下KI与氧气反应的化学方程式:_____________________________。
将I 溶于KI溶液,在低温条件下,可制得KI ·H O。该物质作为食盐加碘剂是否合适?______(填“是”或
2 3 2
“否”),并说明理由________________________________________。
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的
是___________________。
A.Na S O B.AlCl C.Na CO D.NaNO
2 2 3 3 2 3 2(3)抽滤所用的滤纸应略_______(填“大于”或“小于”)布氏漏斗内径,将全部小孔盖住。烧杯中的
二苯基乙二酮晶体转入布氏漏斗时,杯壁上往往还粘有少量晶体,需选用液体将杯壁上的晶体冲洗下来后转入
布氏漏斗,下列液体最合适的是________。
A.无水乙醇 B.饱和NaCl溶液 C.70%乙醇水溶液 D.滤液
(4)上述重结晶过程中的哪一步操作除去了不溶性杂质:___________。
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率___________________________。
⑥根据图中信息,如何说明水解反应速率随温度升高而增大:_______________________。
10.(2011浙江高考)二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,反 (5)某同学采用薄层色谱(原理和操作与纸层析类同)跟踪反应进程,分别在反应开始、回流15min、
应的化学方程式及装置图(部分装置省略)如下: 30min、45min和60min时,用毛细管取样、点样、薄层色谱展开后的斑点如图所示。该实验条件下比较合适的
回流时间是________。
+2FeCl +2FeCl +2HCl
3 2 A.15min B.30min C.45min D.60min
在反应装置中,加入原料及溶剂,搅拌下加热回流。反应结束后加热煮沸, 冷却后
即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯。重结晶过程:
11.(2011浙江高考)白黎芦醇(结构简式: )属二苯乙烯类多酚化合物,具有抗
氧化、抗癌和预防心血管疾病的作用。某课题组提出了如下合成路线:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答下列问题:
(1)写出装置图中玻璃仪器的名称:a___________,b____________。
(2)趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体:____。
A.缓慢冷却溶液 B.溶液浓度较高 C.溶质溶解度较小 D.缓慢蒸发溶剂
如果溶液中发生过饱和现象,可采用__________等方法促进晶体析出。C A C B D B A
26.[15分]
I I
(1)①Fe(SCN) ; ;
3
IO
已知: 。 ② 3+5I-+6H+ 3I 2 +3H 2 O、2Fe3++2I― 2Fe2++I 2 。
(2)4KI+O +2H O 2I +4KOH;
2 2 2
否;KI 受热或潮解后产生KI和I ,KI易被O 氧化,I 易升华。
根据以上信息回答下列问题: 3 2 2 2
(3)AC。
(4)方法Ⅰ:取适量食盐,加水溶解,滴加足量氯水(或H O ),再加KSCN溶液至过量,若显血红色说明有Fe2
(1)白黎芦醇的分子式是_________________________。 2 2
+。
方法Ⅱ:取适量食盐,加水溶解,加入K Fe(CN) 溶液,有蓝色沉淀说明有Fe2+。
(2)C→D的反应类型是____________;E→F的反应类型是____________。 3 3
27.[14分]
K=c(CO ) c2(NH )1.63.22109 1.64108
(3)化合物A不与FeCl 溶液发生显色反应,能与NaHCO 反应放出CO ,推测其1H核磁共振谱(H- (1)①BC; ② 2 3 。 ③增加; ④>,>。
3 3 2 (2)⑤0.05 mol L1 min1 ;
NMR)中显示有_____种不同化学环境的氢原子,其个数比为______________。 ⑥标▲与标●的曲线相比,c(初始)小,但同一时间段△c大(即大),说明升温加快反应。
28.[15分]
(4)写出A→B反应的化学方程式:____________________________________________。
(1)三颈烧瓶; (球形)冷凝管。
(2)AD;用玻璃棒摩擦容器内壁或加入晶种。
(5)写出结构简式:D________________、E___________________。
(3)小于;D。
(4)趁热过滤。
(5)C。
(6)化合物 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:
29.[14分](1)C H O 。
14 12 3
_______________________________________________________________。 (2)取代反应;消去反应。
(3)4; 1︰1︰2︰6。
CH O CH O
①能发生银镜反应;②含苯环且苯环上只有两种不同化学环境的氢原子。 3 3
浓硫酸
COOH + HO CH 3 △ COOCH 3 +H 2 O
CH O CH O
(4) 3 3
CH 3 O CH 3 O OH
CH Br CH CH OCH
2 2 3
CH O CH O
(5) 3 ; 3 。
O
HOCH CHO HO CH CHO CH O CH
2 2 3
(6) ; ; 。
2011 年普通高等学校招生全国统一考试(浙江卷)
2011 年普通高等学校招生全国统一考试(浙江卷) 理科综合 化学解析
理科综合 化学答案
一、选择题(本题共17小题,每小题6分,每小题只有一项是符合题目要求的)
一、选择题(本题共17小题,每小题6分,每小题只有一项是符合题目要求的)
7.A.正确,化学反应遵守三大守恒规律
7 8 9 10 11 12 13
B.正确,原子吸收光谱仪也叫元素分析仪,能测定元素的种类和含量。红外光谱仪测定有机物基团对红外光的特征吸收光谱。 D.错误。褪黑素的官能团为酰胺键,结构不相似。
C.错误,分子间作用力(特别是氢键),也能影响物质溶解度。 【评析】本题是一道有机题,考查了氨基酸的性质,特别是等电点的应用,同时能在辨认、区别色氨酸和
D.正确,如模拟生物固氮,细菌法炼铜。 褪黑素的官能团。
【评析】本题主要考查化学与STS联系。 12.A.正确,熔化热只相当于0.3 mol氢键。
目的是引导学生要重视课本知识,学好课本知识,要重视基础知识的掌握。同时也考察学生掌握化学知识面 B.错误。K 只与温度有关,与浓度无关。
a
的宽广度和基础知识的巩固程度,以及注重理论联系实际的能力培养。应该认识到化学是一门与生活、生产密 C.正确。环己烯(l)与环己烷(l)相比,形成一个双键,能量降低169kJ/mol,
切联系的学科,平时就要培养养成勤于观察、注意学科最新发展动向的好习惯,要善于联系、学以致用,运用 苯(l)与环己烷(l)相比,能量降低691kJ/mol,远大于169×3,说明苯环有特殊稳定结构
化学知识解释或解决生活热点问题。 D.正确。热方程式①=(③-②)×3-④÷2,△H也成立。
8.A.错误,无水CoCl 呈蓝色,具有吸水性 【评析】本题为大综合题,主要考察了物质的键能分析应用,化学反应能量变化的盖斯定律的应用,以及
2
B.正确,烧杯底部温度高。 弱电解质溶液的电离平衡分析。
C.正确,滴定管和移液管需考虑残留水的稀释影响。
13.步骤①发生Ca2++OH―+
HCO
3
CaCO ↓+H O,
3 2
D.正确,利用SO 的还原性,用KMnO 酸性溶液除去。 步骤②:K [Mg(OH) ]=c(Mg2+)×(10-3)2=5.6×10-12,c(Mg2+)=5.6×10-6。
2 4 sp 2
【评析】本题考察实验化学内容。 Q[Ca(OH) ]=c(Ca2+)×(10-3)2=10-8<K ,无Ca(OH) 析出
2 sp 2
化学是以实验为基础的自然科学。实验是高考题的重要内容。要解好实验题首先必须要认真做好实验化 A.正确。生成0001 mol CaCO 。
3
学实验,在教学中要重视实验的操作与原理,好的实验考题就是应该让那些不做实验的学生得不到分;让那 B.错误。剩余c(Ca2+)=0.001 mol/L。
些认真做实验的学生得好分。从题目的分析也可以看出,实验题目中的很多细节问题光靠讲学生是会不了 C.错误。c(Mg2+)=5.6×10-6<10-5,无剩余,
的。必须去做实验学生才能会真正领悟。 D.错误。生成0.05 mol Mg(OH) ,余0.005 mol OH―,
2
9.X、Y、Z、M、W依次为C、N、O、H、Na Q[Ca(OH) ]=0.01×0.0052=2.5×10-7<K ,无Ca(OH) 析出
2 sp 2
A.错误,原子半径:C>N>O 【评析】本题考察方式很新颖,主要考察溶度积的计算和分析。
B.错误,W Z 即H O 为折线型分子。 解题时要能结合溶度积计算,分析推断沉淀是否产生,要求较高。
2 2 2 2
C.石墨、C 等为非原子晶体。 非选择题(共58分)
60
D.NH HCO 为离子化合物,符合条件,反例CH -NO 为共价化合物。 26.[15分]
4 3 3 2
【评析】本题为元素周期律与周期表知识题。 (1)①Fe3+与SCN-的配合产物有多种,如 [Fe(SCN)]2 、 [Fe(SCN) 6 ]3 等;
试题在元素周期律的推理判断能力的考查中渗透了结构、性质和用途等基础知识的考查。首先以具体元素推 I 的CCl 溶液显紫红色。
2 4
断为基础,运用周期表,结合周期规律,考虑位、构、性关系推断X、Y、Z、W、M分别是什么元素。在此基础
②应用信息:“氧化性:
IO
3
>Fe3+>I ”,说明
IO
3
和Fe3+均能氧化I-生成I 。
2 2
上应用知识解决题给选项的问题。 (2)KI被潮湿空气氧化,不能写成I-+O +H+→,要联系金属吸氧腐蚀,产物I +KOH似乎不合理(会反应),
2 2
10.液滴边缘O 多,在C粒上发生正极反应O +2H O+4e- 4OH-。 应考虑缓慢反应,微量产物I 会升华和KOH与空气中CO 反应。
2 2 2 2 2
液滴下的Fe发生负极反应,Fe-2e- Fe2+,为腐蚀区(a)。 KI ·H O作加碘剂问题,比较难分析,因为KI 很陌生。从题中:“低温条件下可制得”或生活中并无这一
3 2 3
A.错误。Cl-由b区向a区迁移 使用实例来去确定。再根据信息:“KI+I KI ”解析其不稳定性。
2 3
B.正确。
(3)根据信息“还原性:
S
2
O
3
2
>I-”可判断A,
C.错误。液滴下的Fe因发生氧化反应而被腐蚀。 C比较难分析,应考虑食盐潮解主要是Mg2+、Fe3+引起,加Na CO 能使之转化为难溶物;
2 3
D.错误。Cu更稳定,作正极,反应为O +2H O+4e- 4OH-。 D中NaNO 能氧化I―。
2 2 2
【评析】本题考察电化学内容中金属吸氧腐蚀的原理的分析。 (4)实验方案简答要注意规范性,“如取…加入…现象…结论…”,
老知识换新面孔,高考试题,万变不离其宗,关键的知识内容一定要让学生自己想懂,而不是死记硬背。 本实验I―对Fe2+的检验有干扰,用过量氯水又可能氧化SCN-,当然实际操作能判断,不过对程度好的同
学生把难点真正“消化”了就可以做到一通百通,题目再怎么变换形式,学生也能回答。 学来说,用普鲁士蓝沉淀法确定性强。
11.A.正确。氨基酸形成内盐的熔点较高。 27.[14分]
B.正确。氨基酸在等电点时,形成内盐,溶解度最小,易析出晶体。 (1)①A.不能表示正逆反应速率相等;B.反应进行则压强增大;
C.正确。 C.恒容,反应进行则密度增大;D.反应物是固体,NH 的体积分数始终为2/3
3②需将25℃的总浓度转化为NH 和CO 的浓度;K可不带单位。
3 2
③加压,平衡逆移;④据表中数据,升温,反应正移,△H>0,固体分解为气体,△S>0。
c 2.21.9
= 0.05mol L1 min1
(2)⑤ t 6 ;
⑥图中标▲与标●的曲线相比能确认。
28.[15分]
(1)熟悉化学实验仪器,特别是有机合成的仪器比较特殊。
(2)溶液浓度越高,溶质溶解度越小,蒸发或冷却越快,结晶越小;
过饱和主要是缺乏晶种,用玻璃棒摩擦,加入晶体或将容器进一步冷却能解决。
(3)抽滤涉及的仪器安装,操作细则颇多,要能实际规范操作,仔细揣摩,方能掌握。
用滤液(即饱和溶液)洗涤容器能减少产品的溶解损失。
(4)趁热过滤除不溶物,冷却结晶,抽滤除可溶杂质。
(5)对照反应开始斑点,下面斑点为反应物,上面为生成物,45min反应物基本无剩余。
29.[14分]
先确定A的不饱和度为5,对照白黎芦醇的结构,确定含苯环,间三位,无酚羟基,有羧基。
CH O CH O CH O
3 3 3
COOH COOCH CH OH
3 2
CH O CH O CH O
A: 3 ;B: 3 ;C: 3 ;(应用信息②)
CH 3 O CH 3 O OH
CH Br CH CH OCH
2 2 3
CH O CH O
D: 3 ;E: 3 (应用信息①)
CH O
3
OCH
3
CH O
F: 3 。
(1)熟悉键线式。
(2)判断反应类型。
(3)了解有机化学研究方法,特别是H-NMR的分析。
(4)酯化反应注意细节,如 和H O不能漏掉。
2
(5)分析推断合成流程,正确书写结构简式。
(6)较简单的同分异构体问题,主要分析官能团类别和位置异构。