文档内容
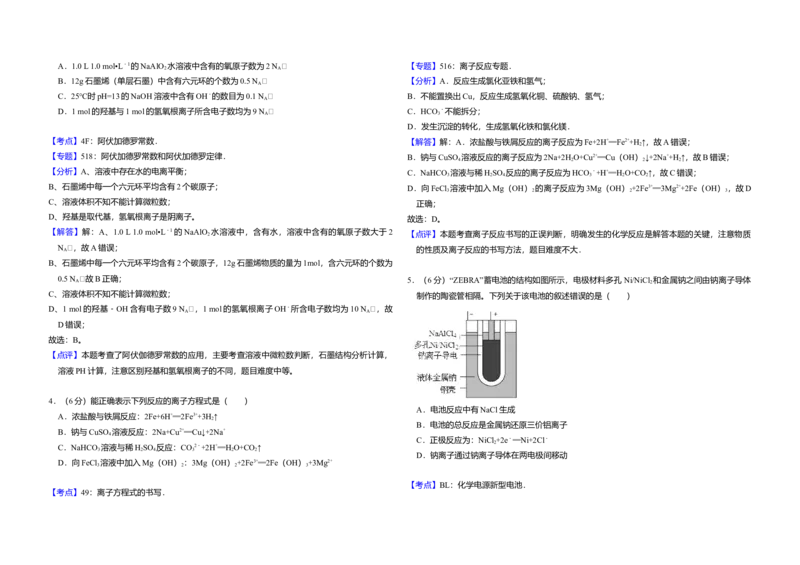
制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
2013年全国统一高考化学试卷(新课标Ⅱ)
一、选择题:本题共7小题,每小题6分.在每小题给出的四个选项中,只有一项是符合题目要
求的.
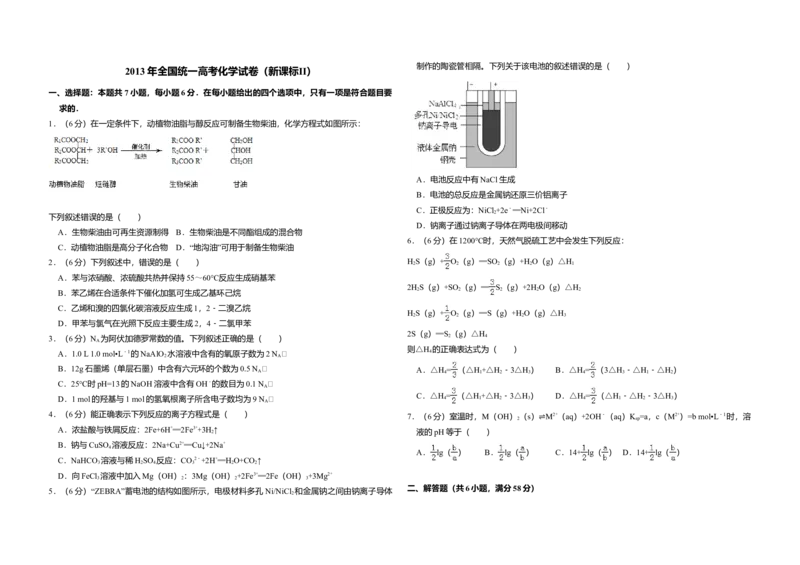
1.(6分)在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如图所示:
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为:NiCl +2e﹣═Ni+2Cl﹣
2
下列叙述错误的是( )
D.钠离子通过钠离子导体在两电极间移动
A.生物柴油由可再生资源制得 B.生物柴油是不同酯组成的混合物
6.(6分)在1200℃时,天然气脱硫工艺中会发生下列反应:
C.动植物油脂是高分子化合物 D.“地沟油”可用于制备生物柴油
2.(6分)下列叙述中,错误的是( ) H 2 S(g)+ O 2 (g)═SO 2 (g)+H 2 O(g)△H 1
A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
2H S(g)+SO (g)═ S (g)+2H O(g)△H
2 2 2 2 2
B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
C.乙烯和溴的四氯化碳溶液反应生成1,2﹣二溴乙烷
H S(g)+ O (g)═S(g)+H O(g)△H
2 2 2 3
D.甲苯与氯气在光照下反应主要生成2,4﹣二氯甲苯
2S(g)═S (g)△H
3.(6分)N 为阿伏加德罗常数的值。下列叙述正确的是( ) 2 4
A
则△H 的正确表达式为( )
A.1.0 L 1.0 mol•L﹣1 的NaAlO 水溶液中含有的氧原子数为2 N 4
2 A
B.12g石墨烯(单层石墨)中含有六元环的个数为0.5 N A A.△H 4 = (△H 1 +△H 2 ﹣3△H 3 ) B.△H 4 = (3△H 3 ﹣△H 1 ﹣△H 2 )
C.25℃时pH=13的NaOH溶液中含有OH﹣的数目为0.1 N
A
C.△H = (△H +△H ﹣3△H ) D.△H = (△H ﹣△H ﹣3△H )
D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9 N 4 1 2 3 4 1 2 3
A
4.(6分)能正确表示下列反应的离子方程式是( ) 7.(6分)室温时,M(OH) (s) M2+(aq)+2OH﹣(aq)K =a,c(M2+)=b mol•L﹣1时,溶
2 sp
A.浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H
2
↑
液的pH等于( ) ⇌
B.钠与CuSO 溶液反应:2Na+Cu2+═Cu↓+2Na+
4
A. lg( ) B. lg( ) C.14+ lg( ) D.14+ lg( )
C.NaHCO 溶液与稀H SO 反应:CO 2﹣+2H+═H O+CO ↑
3 2 4 3 2 2
D.向FeCl 溶液中加入Mg(OH) :3Mg(OH) +2Fe3+═2Fe(OH) +3Mg2+
3 2 2 3
二、解答题(共6小题,满分58分)
5.(6分)“ZEBRA”蓄电池的结构如图所示,电极材料多孔 Ni/NiCl 和金属钠之间由钠离子导体
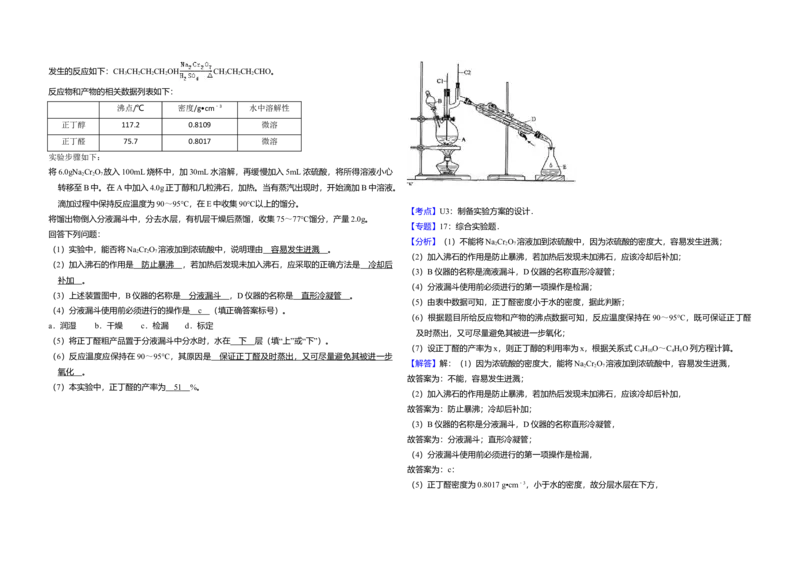
28.(15分)正丁醛是一种化工原料。某实验小组利用如图所示装置合成正丁醛。
发生的反应如下:CH CH CH CH OH CH CH CH CHO。
3 2 2 2 3 2 2
反应物和产物的相关数据列表如下:
沸点/℃ 密度/g•cm﹣3 水中溶解性
正丁醇 117.2 0.8109 微溶
正丁醛 75.7 0.8017 微溶
实验步骤如下:
将6.0gNa Cr O 放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心
2 2 7
9.(14分)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe
转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。
(II)、Mn(II)、Ni(II)等杂质)的流程如图所示:
滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。
回答下列问题:
提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO 。
2
(1)实验中,能否将Na Cr O 溶液加到浓硫酸中,说明理由 。
2 2 7 回答下列问题:
(2)加入沸石的作用是 ,若加热后发现未加入沸石,应采取的正确方法是 。
(1)反应②中除掉的杂质离子是 ,发生反应的离子方程式为 ;在加高锰酸钾溶液前,
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
若pH较低,对除杂的影响是 。
(4)分液漏斗使用前必须进行的操作是 (填正确答案标号)。
(2)反应③的反应类型为 ,过滤得到的滤渣中,除了过量的锌外还有 。
a.润湿 b.干燥 c.检漏 d.标定
(3)反应④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是 。
(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)。
(4)反应④中产物的成分可能是ZnCO •xZn(OH) .取干燥后的滤饼11.2g,锻烧后可得到产品
3 2
(6)反应温度应保持在90~95℃,其原因是 。
8.1g,则x等于 。
(7)本实验中,正丁醛的产率为 %。
10.(14分)在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:A(g) B
(g)+C(g )△H=+85.1kJ•mol﹣1
⇌
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h 0 1 2 4 8 16 20 25 30
总压强p/ 4.91 5.58 6.32 7.31 8.54 9.50 9.52 9.53 9.53
100kPa
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强p和起始压强p 计算反应物A的转化率α(A)的表达式为 ,
0平衡时A的转化率为 ,列式并计算反应的平衡常数K 。
(3)①由总压强p和起始压强p 表示反应体系的总物质的量n 和反应后A的物质的量n(A),
0 总
n = mol,n(A)= mol。
总
②下表为反应物A浓度与反应时间的数据,计算:a= 。
反应时间t/h 0 4 8 16
c(A)/(mol•L﹣1) 0.10 a 0.026 0.0065
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是 ,由此
规律推出反应在12h时反应物的浓度c(A)为 mol•L﹣1。
11.(15分)〔化学﹣﹣选修2:化学与技术〕
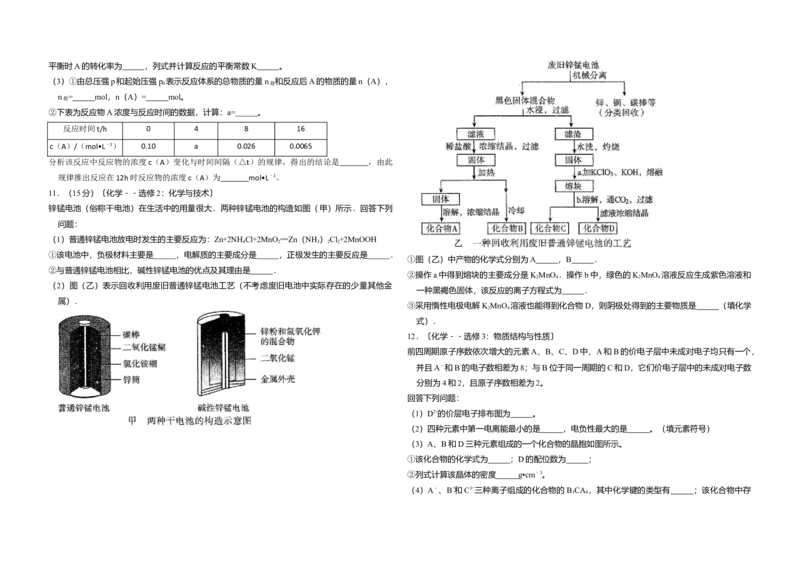
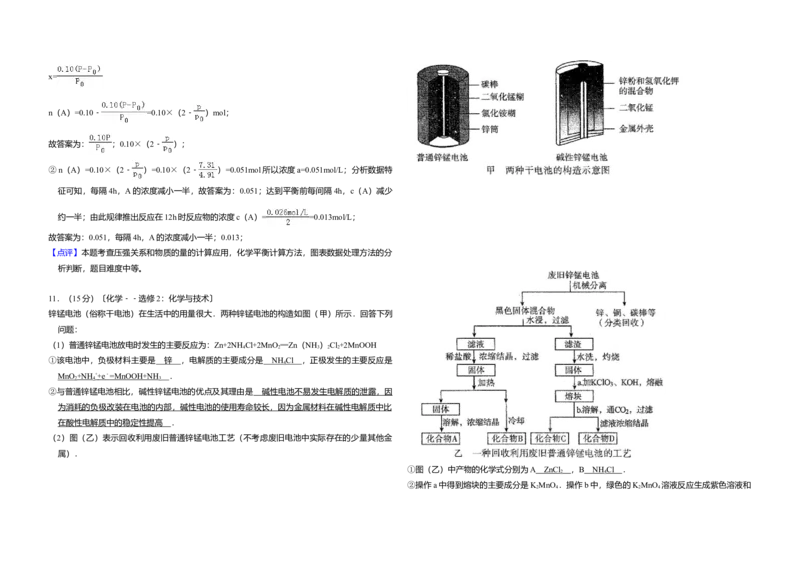
锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(甲)所示.回答下列
问题:
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH Cl+2MnO ═Zn(NH ) Cl +2MnOOH
4 2 3 2 2
①该电池中,负极材料主要是 ,电解质的主要成分是 ,正极发生的主要反应是 .
①图(乙)中产物的化学式分别为A ,B .
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是 .
②操作a中得到熔块的主要成分是K MnO .操作b中,绿色的K MnO 溶液反应生成紫色溶液和
2 4 2 4
(2)图(乙)表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金
一种黑褐色固体,该反应的离子方程式为 .
属).
③采用惰性电极电解K MnO 溶液也能得到化合物D,则阴极处得到的主要物质是 (填化学
2 4
式).
12.〔化学﹣﹣选修3:物质结构与性质〕
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有一个,
并且A﹣和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数
分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为 。
(2)四种元素中第一电离能最小的是 ,电负性最大的是 。(填元素符号)
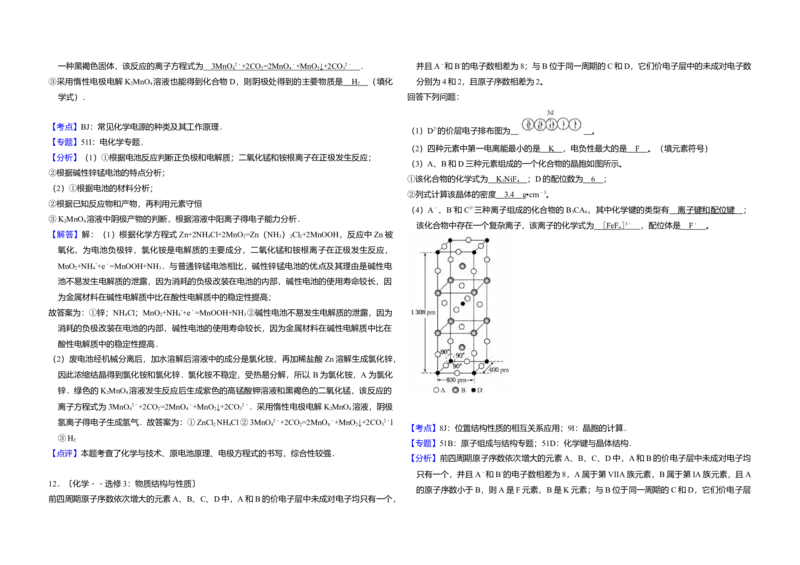
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为 ;D的配位数为 ;
②列式计算该晶体的密度 g•cm﹣3。
(4)A﹣、B+和C3+三种离子组成的化合物的 B CA ,其中化学键的类型有 ;该化合物中存
3 6在一个复杂离子,该离子的化学式为 ,配位体是 。 (3)E的分子式为 .
(4)F生成G的化学方程式为 ,该反应类型为 .
(5)I的结构简式为 .
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有
两个取代基,②既能发生银镜反应,又能与饱和 NaHCO 溶液反应放出 CO ,共有 种
3 2
(不考虑立体异构).J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且
峰面积比为2:2:1,写出J的这种同分异构体的结构简式 .
13.[化学﹣﹣选修5:有机化学基础]
化合物I(C H O )是制备液晶材料的中间体之一,其分子中含有醛基和酯基.I可以用E和H
11 12 3
在一定条件下合成:
已知以下信息:
1.A的核磁共振氢谱表明其只有一种化学环境的氢;
2.R﹣CH=CH R﹣CH CH OH;
2 2 2
3.化合物F苯环上的一氯代物只有两种;
4.通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基.
回答下列问题:
(1)A的化学名称为 .
(2)D的结构简式为 .C.动植物油脂是高分子化合物相对分子质量小于10000,不是高分子化合物,故C错误;
D.“地沟油”中含有动植物油脂,动植物油脂与醇反应可制备生物柴油,故D正确;
2013 年全国统一高考化学试卷(新课标Ⅱ)
故选:C。
参考答案与试题解析
【点评】本题主要考查了油脂的性质与用途,难度不大,根据题目信息即可完成.
一、选择题:本题共7小题,每小题6分.在每小题给出的四个选项中,只有一项是符合题目要
2.(6分)下列叙述中,错误的是( )
求的.
A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
1.(6 分)在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如图所示:
B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
C.乙烯和溴的四氯化碳溶液反应生成1,2﹣二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4﹣二氯甲苯
【考点】HD:有机物的结构和性质;IB:乙烯的化学性质;IH:苯的性质;II:苯的同系物.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
【分析】A.根据苯的硝化反应;
B.根据碳碳双键能发生加成反应,苯环也可发生加成反应;
下列叙述错误的是( ) C.根据碳碳双键能发生加成反应;
A.生物柴油由可再生资源制得 D.根据甲苯与氯气在光照下反应主要发生的是侧链上的氢原子被取代;
B.生物柴油是不同酯组成的混合物 【解答】解:A.苯的硝化反应:苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯,故
C.动植物油脂是高分子化合物 A正确;
D.“地沟油”可用于制备生物柴油 B.碳碳双键能发生加成反应,苯环也可发生加成反应,所以苯乙烯在合适条件下催化加氢可生
成乙基环己烷,故B正确;
【考点】JH:油脂的性质、组成与结构;L1:有机高分子化合物的结构和性质. C.碳碳双键能发生加成反应,所以乙烯和溴的四氯化碳溶液反应生成1,2﹣二溴乙烷,故C正
菁优网版权所有
【专题】534:有机物的化学性质及推断.
确;
【分析】A.生物柴油其原料取自可再生的动植物资源;
D.甲苯与氯气在光照下反应主要发生的是侧链上的氢原子被取代,不能得到苯环上氢原子被取
B.生物柴油通常是指以动植物油脂为原料生产的、以脂肪酸甲酯为主要成份的液体燃料;
代的产物2,4﹣二氯甲苯,故D错误;
C.相对分子质量在10000以上的有机化合物为高分子化合物;
故选:D。
D.“地沟油”中含有动植物油脂,动植物油脂与醇反应可制备生物柴油;
【点评】本题主要考查了物质的结构与性质,注意反应条件对产物结构的影响.
【解答】解:A.生物柴油由可再生资源制得,故A正确;
B.生物柴油通常是指以动植物油脂为原料生产的、以不同脂肪酸甲酯组成的混合物,故B正确;
3.(6分)N 为阿伏加德罗常数的值。下列叙述正确的是( )
AA.1.0 L 1.0 mol•L﹣1 的NaAlO 水溶液中含有的氧原子数为2 N 【专题】516:离子反应专题.
2 A
B.12g石墨烯(单层石墨)中含有六元环的个数为0.5 N 【分析】A.反应生成氯化亚铁和氢气;
A
C.25℃时pH=13的NaOH溶液中含有OH﹣的数目为0.1 N B.不能置换出Cu,反应生成氢氧化铜、硫酸钠、氢气;
A
D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9 N C.HCO ﹣不能拆分;
A 3
D.发生沉淀的转化,生成氢氧化铁和氯化镁.
【考点】4F:阿伏加德罗常数. 【解答】解:A.浓盐酸与铁屑反应的离子反应为Fe+2H+═Fe2++H ↑,故A错误;
菁优网版权所有 2
【专题】518:阿伏加德罗常数和阿伏加德罗定律. B.钠与CuSO 溶液反应的离子反应为2Na+2H O+Cu2+═Cu(OH) ↓+2Na++H ↑,故B错误;
4 2 2 2
【分析】A、溶液中存在水的电离平衡; C.NaHCO 溶液与稀H SO 反应的离子反应为HCO ﹣+H+═H O+CO ↑,故C错误;
3 2 4 3 2 2
B、石墨烯中每一个六元环平均含有2个碳原子; D.向FeCl 溶液中加入Mg(OH) 的离子反应为3Mg(OH) +2Fe3+═3Mg2++2Fe(OH) ,故D
3 2 2 3
C、溶液体积不知不能计算微粒数;
正确;
D、羟基是取代基,氢氧根离子是阴离子。 故选:D。
【解答】解:A、1.0 L 1.0 mol•L﹣1 的NaAlO
2
水溶液中,含有水,溶液中含有的氧原子数大于2
【点评】本题考查离子反应书写的正误判断,明确发生的化学反应是解答本题的关键,注意物质
N
A
,故A错误;
的性质及离子反应的书写方法,题目难度不大.
B、石墨烯中每一个六元环平均含有2个碳原子,12g石墨烯物质的量为1mol,含六元环的个数为
0.5 N A 故B正确; 5.(6分)“ZEBRA”蓄电池的结构如图所示,电极材料多孔 Ni/NiCl 2 和金属钠之间由钠离子导体
C、溶液体积不知不能计算微粒数;
制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
D、1 mol的羟基﹣OH含有电子数9 N ,1 mol的氢氧根离子OH﹣所含电子数均为10 N ,故
A A
D错误;
故选:B。
【点评】本题考查了阿伏伽德罗常数的应用,主要考查溶液中微粒数判断,石墨结构分析计算,
溶液PH计算,注意区别羟基和氢氧根离子的不同,题目难度中等。
4.(6分)能正确表示下列反应的离子方程式是( )
A.电池反应中有NaCl生成
A.浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H ↑
2
B.电池的总反应是金属钠还原三价铝离子
B.钠与CuSO 溶液反应:2Na+Cu2+═Cu↓+2Na+
4
C.正极反应为:NiCl +2e﹣═Ni+2Cl﹣
2
C.NaHCO 溶液与稀H SO 反应:CO 2﹣+2H+═H O+CO ↑
3 2 4 3 2 2
D.钠离子通过钠离子导体在两电极间移动
D.向FeCl 溶液中加入Mg(OH) :3Mg(OH) +2Fe3+═2Fe(OH) +3Mg2+
3 2 2 3
【考点】BL:化学电源新型电池.
【考点】49:离子方程式的书写. 菁优网版权所有
菁优网版权所有【专题】51I:电化学专题. 方程改写分方程,然后求出反应热。
【分析】该原电池中,钠作负极,负极上电极反应式为:Na﹣e﹣=Na+,Ni/NiCl 作正极,正极上
2 【解答】解:根据目标方程,把方程3反写,计量数乘以2;把方程2乘以 ;把方程1乘以 ;
电极反应式为:NiCl +2e﹣=Ni+2Cl﹣,钠离子向正极移动。
2
【解答】解:A.负极上电极反应式为:Na﹣e﹣=Na+,正极上电极反应式为:NiCl +2e﹣=Ni+2Cl
2 然后三者相加;即﹣△H ×2+△H × +△H × = (△H +△H ﹣3△H ),
3 2 1 1 2 3
﹣,所以该原电池中有氯化钠生成,故A正确;
故选:A。
B.根据正负极电极反应式知,金属钠还原NiCl ,故B错误;
2
【点评】本题考查了盖斯定律的应用,要注意方程式计量数的变化,及△H的符号的变化。
C.正极上得电子发生还原反应,电极反应式为:NiCl +2e﹣=Ni+2Cl﹣,故C正确;
2
D.原电池放电时,阳离子向正极移动,钠离子在负极产生,向正极移动,所以钠离子通过钠离
7.(6分)室温时,M(OH) (s) M2+(aq)+2OH﹣(aq)K =a,c(M2+)=b mol•L﹣1时,溶
子导体在两电极间移动,故D正确; 2 sp
液的pH等于( )
故选:B。 ⇌
【点评】本题考查原电池原理,明确正负极上得失电子、离子的移动方向即可分析解答,难点是 A. lg( ) B. lg( ) C.14+ lg( ) D.14+ lg( )
电极反应式的书写,难度中等。
【考点】DA:pH的简单计算;DH:难溶电解质的溶解平衡及沉淀转化的本质.
菁优网版权所有
6.(6分)在1200℃时,天然气脱硫工艺中会发生下列反应:
【专题】51G:电离平衡与溶液的pH专题.
H S(g)+ O (g)═SO (g)+H O(g)△H 【分析】依据Ksp=c(M2+)c2(OH﹣)表达式和题干K =a,C(M2+)=b mol•L﹣1,计算溶液中氢
2 2 2 2 1 sp
氧根离子浓度,结合溶液中离子积计算氢离子浓度和溶液pH;
2H S(g)+SO (g)═ S (g)+2H O(g)△H
2 2 2 2 2 【解答】解:室温时,M(OH) (s) M2+(aq)+2OH﹣(aq),已知K =a,c(M2+)=b mol•L
2 sp
⇌
H S(g)+ O (g)═S(g)+H O(g)△H
2 2 2 3
﹣1,则c(OH﹣)= = mol•L﹣1,
2S(g)═S (g)△H
2 4
则△H 的正确表达式为( )
4
所以c(H+)= = mol•L﹣1,则pH=﹣lgc(H+)=14+ lg( );
A.△H = (△H +△H ﹣3△H ) B.△H = (3△H ﹣△H ﹣△H )
4 1 2 3 4 3 1 2
故选:C。
C.△H = (△H +△H ﹣3△H ) D.△H = (△H ﹣△H ﹣3△H )
4 1 2 3 4 1 2 3
【点评】本题考查了溶度积常数的有关计算和 PH的计算,题目难度不大,注意对 Ksp含义的理
解.
【考点】BF:用盖斯定律进行有关反应热的计算.
菁优网版权所有
【专题】517:化学反应中的能量变化.
二、解答题(共6小题,满分58分)
【分析】利用盖斯定律分析,不管化学反应是一步或分几步完成,其反应热是不变的;根据目标
8.(15分)正丁醛是一种化工原料。某实验小组利用如图所示装置合成正丁醛。发生的反应如下:CH CH CH CH OH CH CH CH CHO。
3 2 2 2 3 2 2
反应物和产物的相关数据列表如下:
沸点/℃ 密度/g•cm﹣3 水中溶解性
正丁醇 117.2 0.8109 微溶
正丁醛 75.7 0.8017 微溶
实验步骤如下:
将6.0gNa Cr O 放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心
2 2 7
转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。
滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分。
【考点】U3:制备实验方案的设计.
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。 菁优网版权所有
【专题】17:综合实验题.
回答下列问题:
【分析】(1)不能将Na Cr O 溶液加到浓硫酸中,因为浓硫酸的密度大,容易发生迸溅;
2 2 7
(1)实验中,能否将Na Cr O 溶液加到浓硫酸中,说明理由 容易发生迸溅 。
2 2 7
(2)加入沸石的作用是防止暴沸,若加热后发现未加沸石,应该冷却后补加;
(2)加入沸石的作用是 防止暴沸 ,若加热后发现未加入沸石,应采取的正确方法是 冷却后
(3)B仪器的名称是滴液漏斗,D仪器的名称直形冷凝管;
补加 。
(4)分液漏斗使用前必须进行的第一项操作是检漏;
(3)上述装置图中,B仪器的名称是 分液漏斗 ,D仪器的名称是 直形冷凝管 。
(5)由表中数据可知,正丁醛密度小于水的密度,据此判断;
(4)分液漏斗使用前必须进行的操作是 c (填正确答案标号)。
(6)根据题目所给反应物和产物的沸点数据可知,反应温度保持在 90~95℃,既可保证正丁醛
a.润湿 b.干燥 c.检漏 d.标定
及时蒸出,又可尽量避免其被进一步氧化;
(5)将正丁醛粗产品置于分液漏斗中分水时,水在 下 层(填“上”或“下”)。
(7)设正丁醛的产率为x,则正丁醇的利用率为x,根据关系式C H O~C H O列方程计算。
4 10 4 8
(6)反应温度应保持在90~95℃,其原因是 保证正丁醛及时蒸出,又可尽量避免其被进一步
【解答】解:(1)因为浓硫酸的密度大,能将Na Cr O 溶液加到浓硫酸中,容易发生迸溅,
2 2 7
氧化 。
故答案为:不能,容易发生迸溅;
(7)本实验中,正丁醛的产率为 51 %。
(2)加入沸石的作用是防止暴沸,若加热后发现未加沸石,应该冷却后补加,
故答案为:防止暴沸;冷却后补加;
(3)B仪器的名称是分液漏斗,D仪器的名称直形冷凝管,
故答案为:分液漏斗;直形冷凝管;
(4)分液漏斗使用前必须进行的第一项操作是检漏,
故答案为:c:
(5)正丁醛密度为0.8017 g•cm﹣3,小于水的密度,故分层水层在下方,故答案为:下;
(6)根据题目所给反应物和产物的沸点数据可知,反应温度保持在 90~95℃,既可保证正丁醛 【考点】GR:常见金属元素的单质及其化合物的综合应用;P8:物质分离和提纯的方法和基本操
及时蒸出,又可尽量避免其被进一步氧化, 作综合应用.
菁优网版权所有
故答案为:保证正丁醛及时蒸出,又可尽量避免其被进一步氧化; 【专题】527:几种重要的金属及其化合物.
(7)设正丁醛的产率为x,则正丁醇的利用率为x,根据关系式, 【分析】(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是 Fe2+和Mn2+,根据
C H O~C H O MnO ﹣+具有氧化性,能将Fe2+和Mn2+氧化,根据电子得失进行配平;加高锰酸钾溶液前,若
4 10 4 8 4
74 72 pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质。
4xg 2g (2)反应③为锌与镍离子的发生反应得到锌离子和镍;得到的滤渣中,除了过量的锌外还有金属
镍。
解得:x= =51%,
(3)检验沉淀是否洗涤干净的方法是最后一次洗涤液,检验表面是否含有硫酸根离子;
故答案为:51。
(4)根据关系式ZnCO •xZn(OH) ~(x+1)ZnO来计算。
3 2
【点评】本题考查有机化学实验、反应原理、基本操作、化学计算等,难度不大,注意计算中正
【解答】解:(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,发
丁醇的转化率等于正丁醛的产率,注意对基础知识的理解掌握。
生 的 离 子 方 程 式 为 MnO ﹣+3Fe2++7H O=3Fe ( OH ) ↓+MnO ↓+5H+ 、 2MnO ﹣+3Mn2+
4 2 3 2 4
+2H O=5MnO ↓+4H+;加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无
2 2
9.(14分)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe
法除去铁和锰杂质;
(II)、Mn(II)、Ni(II)等杂质)的流程如图所示:
故 答 案 为 : Fe2+ 和 Mn2+ ; MnO ﹣+3Fe2++7H O=3Fe ( OH ) ↓+MnO ↓+5H+ 、 2MnO ﹣+3Mn2+
4 2 3 2 4
+2H O=5MnO ↓+4H+;铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
2 2
(2)反应③为锌与镍离子的发生反应得到锌离子和镍,反应类型为置换反应;得到的滤渣中,除
提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO 。
2
了过量的锌外还有金属镍,
回答下列问题:
(1)反应②中除掉的杂质离子是 Fe 2 + 和 Mn 2 + ,发生反应的离子方程式为 MnO ﹣ + 3Fe 2 + 故答案为:置换反应;镍;
4
+ 7H O=3Fe ( OH ) ↓ + MnO ↓ + 5H + 、 2MnO ﹣ + 3Mn 2 + + 2H O=5MnO ↓ + 4H + ;在加高锰酸钾溶液
(3)由于溶液中硫酸根离子属于杂质离子,因此可以检验测定洗涤液中是否存在硫酸根离子,操
2 3 2 4 2 2
作为:取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉
前,若pH较低,对除杂的影响是 铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质
淀生成,则说明沉淀已经洗涤干净,故答案为:取最后一次少量水洗液于试管中,滴入 1~2滴
。
(2)反应③的反应类型为 置换反应 ,过滤得到的滤渣中,除了过量的锌外还有 镍 。 稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净;
(3)反应④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是 取最后一次少量水洗液于试
(4)根据关系式ZnCO
3
•xZn(OH)
2
~(x+1)ZnO
125+99x 81(x+1)
管中,滴入 1 ~ 2 滴盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净 。
11.2g 8.1g
(4)反应④中产物的成分可能是ZnCO •xZn(OH) .取干燥后的滤饼11.2g,锻烧后可得到产品
3 2
解得:x=1
8.1g,则x等于 1 。
故答案为:1。【点评】本题以工业流程为背景,考查了学生分析问题、解决问题,运用知识的能力,难度中等。 ②依据平衡A的浓度计算,依据图表数据分析判断存在的规律;
【解答】解:(1)在一定温度进行如下反应:A(g) B(g)+C(g )△H=+85.1kJ•mol﹣1
10.(14分)在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:A(g) B 反应是吸热反应,反应前后气体体积增大,根据平衡移动原理分析可知,欲提高 A的平衡转化率,
⇌
(g)+C(g )△H=+85.1kJ•mol﹣1 ⇌ 平衡正向进行,可以升温或减压条件下使平衡正向进行;
反应时间(t)与容器内气体总压强(p)的数据见下表: 故答案:升高温度、降低压强;
时间t/h 0 1 2 4 8 16 20 25 30 (2)反应前后气体物质的量增大等于反应的A的量,所以由总压强p和起始压强p 0 计算反应物
总压强p/ 4.91 5.58 6.32 7.31 8.54 9.50 9.52 9.53 9.53
100kPa
A的转化率α(A)的表达式= ×100%=( )×100%;
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 升高温度、降低压强 。
平衡时A的转化率= ×100%=94.1%
(2)由总压强p和起始压强p 计算反应物A的转化率α(A)的表达式为 × 100% ,
0
依据化学平衡三段式 列式得到;
平衡时A的转化率为 94.1% ,列式并计算反应的平衡常数K 1.5mol/L 。
A(g) B(g)+C(g )
(3)①由总压强p和起始压强p 表示反应体系的总物质的量n 和反应后A的物质的量n(A),
0 总 起始量(mol/L) 0.10 0 0
⇌
变化量(mol/L) 0.10×94.1% 0.10×94.1% 0.10×94.1%
n = 0.10 × mol,n(A)= 0.10 × ( 2﹣ ) mol。
总
平衡量(mol/L)0.10(1﹣94.1%) 0.10×94.1% 0.10×94.1%
②下表为反应物A浓度与反应时间的数据,计算:a= 0.051 。
K= = =1.5mol/L
反应时间t/h 0 4 8 16
c(A)/(mol•L﹣1) 0.10 a 0.026 0.0065 故答案为:( )×100%;94.1%; 1.5mol/L
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是 达到平衡前每
(3)①由总压强p和起始压强p 表示反应体系的总物质的量n 和反应物A的物质的量n(A),
0 总
间隔 4h , c ( A )减少约一半 ,由此规律推出反应在 12h时反应物的浓度 c(A)为 0.013
mol•L﹣1。 依据压强之比等于物质的量之比,n :n起始=P:P ,n = ;
总 0 总
A(g) B(g)+C(g )
【考点】CB:化学平衡的影响因素;CP:化学平衡的计算.
菁优网版权所有 起始量(mol) ⇌ 0.10 0 0
【专题】51E:化学平衡专题.
变化量(mol) x x x
【分析】(1)反应是吸热反应,反应前后气体体积增大,结合平衡移动原理分析判断转化率;
某时刻量(mol) 0.10﹣x x x
(2)相同条件下压强之比等于物质的量之比,反应前后物质的量的增大是反应的 A的物质的量,
(0.10+x):0.10=P:P
0
结合转化率概念计算得到;依据化学平衡三段式列式计算平衡浓度达到平衡常数;
(3)①依据相同条件下压强之比等于物质的量之比,结合平衡计算得到;x=
n(A)=0.10﹣ =0.10×(2﹣ )mol;
故答案为: ;0.10×(2﹣ );
②n(A)=0.10×(2﹣ )=0.10×(2﹣ )=0.051mol所以浓度a=0.051mol/L;分析数据特
征可知,每隔4h,A的浓度减小一半,故答案为:0.051;达到平衡前每间隔4h,c(A)减少
约一半;由此规律推出反应在12h时反应物的浓度c(A)= =0.013mol/L;
故答案为:0.051,每隔4h,A的浓度减小一半;0.013;
【点评】本题考查压强关系和物质的量的计算应用,化学平衡计算方法,图表数据处理方法的分
析判断,题目难度中等。
11.(15分)〔化学﹣﹣选修2:化学与技术〕
锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(甲)所示.回答下列
问题:
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH Cl+2MnO ═Zn(NH ) Cl +2MnOOH
4 2 3 2 2
①该电池中,负极材料主要是 锌 ,电解质的主要成分是 NH Cl ,正极发生的主要反应是
4
MnO + NH + + e ﹣ =MnOOH + NH .
2 4 3
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是 碱性电池不易发生电解质的泄露,因
为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比
在酸性电解质中的稳定性提高 .
(2)图(乙)表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金
属).
①图(乙)中产物的化学式分别为A ZnCl ,B NH Cl .
2 4
②操作a中得到熔块的主要成分是K MnO .操作b中,绿色的K MnO 溶液反应生成紫色溶液和
2 4 2 4一种黑褐色固体,该反应的离子方程式为 3MnO 2﹣ + 2CO =2MnO ﹣ + MnO ↓ + 2CO 2﹣ . 并且A﹣和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数
4 2 4 2 3
③采用惰性电极电解K MnO 溶液也能得到化合物D,则阴极处得到的主要物质是 H (填化 分别为4和2,且原子序数相差为2。
2 4 2
学式). 回答下列问题:
【考点】BJ:常见化学电源的种类及其工作原理.
菁优网版权所有 (1)D2+的价层电子排布图为 。
【专题】51I:电化学专题.
(2)四种元素中第一电离能最小的是 K ,电负性最大的是 F 。(填元素符号)
【分析】(1)①根据电池反应判断正负极和电解质;二氧化锰和铵根离子在正极发生反应;
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
②根据碱性锌锰电池的特点分析;
①该化合物的化学式为 K NiF ;D的配位数为 6 ;
2 4
(2)①根据电池的材料分析;
②列式计算该晶体的密度 3.4 g•cm﹣3。
②根据已知反应物和产物,再利用元素守恒
(4)A﹣、B+和C3+三种离子组成的化合物的B CA ,其中化学键的类型有 离子键和配位键 ;
3 6
③K MnO 溶液中阴极产物的判断,根据溶液中阳离子得电子能力分析.
2 4
该化合物中存在一个复杂离子,该离子的化学式为 [ FeF ] 3﹣ ,配位体是 F ﹣ 。
6
【解答】解:(1)根据化学方程式Zn+2NH Cl+2MnO =Zn(NH ) Cl +2MnOOH,反应中Zn被
4 2 3 2 2
氧化,为电池负极锌,氯化铵是电解质的主要成分,二氧化锰和铵根离子在正极发生反应,
MnO +NH ++e﹣=MnOOH+NH .与普通锌锰电池相比,碱性锌锰电池的优点及其理由是碱性电
2 4 3
池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因
为金属材料在碱性电解质中比在酸性电解质中的稳定性提高;
故答案为:①锌;NH Cl;MnO +NH ++e﹣=MnOOH+NH ②碱性电池不易发生电解质的泄露,因为
4 2 4 3
消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在
酸性电解质中的稳定性提高.
(2)废电池经机械分离后,加水溶解后溶液中的成分是氯化铵,再加稀盐酸 Zn溶解生成氯化锌,
因此浓缩结晶得到氯化铵和氯化锌.氯化铵不稳定,受热易分解,所以 B为氯化铵,A为氯化
锌.绿色的K MnO 溶液发生反应后生成紫色的高锰酸钾溶液和黑褐色的二氧化锰,该反应的
2 4
离子方程式为3MnO 2﹣+2CO =2MnO ﹣+MnO ↓+2CO 2﹣.采用惰性电极电解K MnO 溶液,阴极
4 2 4 2 3 2 4
氢离子得电子生成氢气.故答案为:①ZnCl NH Cl②3MnO 2﹣+2CO =2MnO ﹣+MnO ↓+2CO 2﹣l
2 4 4 2 4 2 3
【考点】8J:位置结构性质的相互关系应用;9I:晶胞的计算.
菁优网版权所有
③H
2 【专题】51B:原子组成与结构专题;51D:化学键与晶体结构.
【点评】本题考查了化学与技术、原电池原理、电极方程式的书写,综合性较强.
【分析】前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均
只有一个,并且A﹣和B+的电子数相差为8,A属于第VIIA族元素,B属于第IA族元素,且A
12.〔化学﹣﹣选修3:物质结构与性质〕
的原子序数小于B,则A是F元素,B是K元素;与B位于同一周期的C和D,它们价电子层
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有一个,中的未成对电子数分别为4和2,且原子序数相差为2,且C和D的原子序数大于B,C的原子 ﹣,
序数小于D,则C是Fe元素,D是Ni元素,结合物质结构和性质解答。 故答案为:离子键和配位键;[FeF ]3﹣;F﹣。
6
【解答】解:前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电 【点评】本题考查物质结构和性质,正确推断元素是解本题关键,难度中等,注意化学式的确定
子均只有一个,并且A﹣和B+的电子数相差为8,A属于第VIIA族元素,B属于第IA族元素, 中,各中原子被几个晶胞共用,为易错点,难点是密度的计算。
且A的原子序数小于B,则A是F元素,B是K元素;与B位于同一周期的C和D,它们价电
子层中的未成对电子数分别为4和2,且原子序数相差为2,且C和D的原子序数大于B,C的 13.[化学﹣﹣选修5:有机化学基础]
原子序数小于D,则C是Fe元素,D是Ni元素, 化合物I(C 11 H 12 O 3 )是制备液晶材料的中间体之一,其分子中含有醛基和酯基.I可以用E和H
(1)D2+的价层电子为3d电子,根据能量最低原理、保里不相容原理及洪特规则知,其价电子排 在一定条件下合成:
布图为 ,
故答案为: ; 已知以下信息:
(2)元素的金属性越强其第一电离能越小,元素的非金属性越强,其电负性越大,这四种元素中 1.A的核磁共振氢谱表明其只有一种化学环境的氢;
金属性最强的是K元素,非金属性最强的元素是F,所以第一电离能最小的是K,电负性最大
2.R﹣CH=CH R﹣CH CH OH;
2 2 2
的是F,
3.化合物F苯环上的一氯代物只有两种;
故答案为:K;F;
4.通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基.
(3)①该晶胞中 A 原子个数=16× =8,B 原子个数=8× =4,D 原子个数=8×
回答下列问题:
(1)A的化学名称为 2﹣ 甲基﹣ 2﹣ 氯丙烷 .
,所以该化合物的化学式为 K NiF ,根据晶胞结构知,D 的配位数是 6,故答案为: (2)D的结构简式为 ( CH ) CHCHO .
2 4 3 2
(3)E的分子式为 C H O .
K NiF ;6; 4 8 2
2 4
②该晶胞的体积=(400×10﹣10cm)2(1308×10﹣10cm),ρ= =3.4g•cm﹣3,
(4)F生成G的化学方程式为 ,该反应类型为 取代反应
故答案为:3.4;
.
(4)A﹣、B+和C3+三种离子组成的化合物的K FeF ,该物质中阴阳离子间存在离子键,铁原子和
3 6
氟原子间存在配位键,该化合物中存在一个复杂离子,该离子的化学式为[FeF ]3﹣,配位体是F
6(5)I的结构简式为 . H与E发生酯化反应生成I,其分子中含有醛基和酯基,故I为 ,据
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有 此解答.
两个取代基,②既能发生银镜反应,又能与饱和 NaHCO 溶液反应放出 CO ,共有 18 种 【解答】解:A 的分子式为 C H Cl,核磁共振氢谱表明其只有一种化学环境的氢,则 A 为
3 2 4 9
(不考虑立体异构).J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且 (CH ) CCl,在氢氧化钠醇溶液、加热条件下发生消去反应,生成 B为CH =C(CH ) ,B
3 3 2 3 2
发生信息 2 中的反应生成 C 为(CH ) CHCH OH,C 发生催化氧化生成 D 为(CH )
3 2 2 3
峰面积比为2:2:1,写出J的这种同分异构体的结构简式 . CHCHO,D再与氢氧化铜反应,酸化得到E为(CH ) CHCOOH,
2 3 2
F的分子式为C H O,苯环上的一氯代物只有两种,应含有2个不同的侧链,且处于对位,则F为
7 8
【考点】HB:有机物的推断.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
【分析】A的分子式为 C H Cl,核磁共振氢谱表明其只有一种化学环境的氢,则 A为(CH )
4 9 3
CCl,在氢氧化钠醇溶液、加热条件下发生消去反应,生成 B为CH =C(CH ) ,B发生信息
3 2 3 2
2中的反应生成C为(CH ) CHCH OH,C发生催化氧化生成D为(CH ) CHCHO,D再与 ,与氯气在光照条件下发生取代反应,生成 G为 ,G在氢氧化钠水溶液发生水解反
3 2 2 3 2
氢氧化铜反应,酸化得到E为(CH ) CHCOOH,
3 2
F的分子式为C H O,苯环上的一氯代物只有两种,应含有2个不同的侧链,且处于对位,则F为
7 8
应,酸化得到H,由于同一个碳原子上连有两个羟基不稳定,易脱水形成羰基,故 H为 ,
,与氯气在光照条件下发生取代反应,生成 G为 ,G在氢氧化钠水溶液发生水解反
H与E发生酯化反应生成I,其分子中含有醛基和酯基,故I为 ,
(1)由上述分析可知,A为(CH ) CCl,化学名称为:2﹣甲基﹣2﹣氯丙烷,
3 3
故答案为:2﹣甲基﹣2﹣氯丙烷;
应,酸化得到H,由于同一个碳原子上连有两个羟基不稳定,易脱水形成羰基,故 H为 ,
(2)由上述分析可知,D的结构简式为(CH ) CHCHO,
3 2
故答案为:(CH ) CHCHO;
3 2
(3)E为(CH ) CHCOOH,其分子式为C H O ,
3 2 4 8 2故答案为:C H O ; 1种H原子,产物有2个﹣COOH,应还含有2个﹣CH ﹣,2个侧链相同且处于对位,产物中
4 8 2 2
侧链为﹣CH COOH,故符合条件的同分异构体结构简式为: ,
2
(4)F生成G的化学方程式为 ,该反应类型为取代反应, 故答案为:18; .
【点评】本题考查有机物推断,需要对给予的信息进行利用,能较好的考查学生阅读能力、自学
能力,熟练掌握官能团的性质与转化,利用正推法推断,(6)中同分异构体的书写是易错点、
难点,根据信息确定苯环侧链是关键,难点中等.
故答案为: ;取代反应;
(5)由上述分析可知,I的结构简式为 ,
故答案为: ;
(6)I( )的同系物J比I相对分子质量小14,J比I少一个﹣CH ﹣原
2
子团,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反
应,又能与饱和NaHCO 溶液反应放出CO ,则J的同分异构体含有﹣CHO、﹣COOH,
3 2
侧链为﹣CHO、﹣CH CH COOH,有邻、间、对三种位置,
2 2
侧链为﹣CHO、﹣CH(CH )COOH,有邻、间、对三种位置,
3
侧链为﹣CH CHO、﹣CH COOH,有邻、间、对三种位置,
2 2
侧链为﹣CH CH CHO、﹣COOH,有邻、间、对三种位置,
2 2
侧链为﹣CH(CH )CHO、﹣COOH,有邻、间、对三种位置,
3
侧链为﹣CH 、﹣CH(CHO)COOH,有邻、间、对三种位置,
3
故符合条件的同分异构体有6×3=18种,
J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,而J
的同分异构体发生银镜反应并酸化后的产物苯环侧链至少有 2种H原子,故产物中苯环上只有