文档内容
2013 年北京市高考化学试卷
一、选择题(共7小题,每小题6分,满分42分)
1.(6分)下列设备工作时,将化学能转化为热能的是( )
A B C D
A.a端是直流电源的负极
B.通电使CuCl 发生电离
2
C.阳极上发生的反应:Cu2++2e﹣=Cu
D.通电一段时间后,在阴极附近观察到黄绿色气体
硅太阳能电池 锂离子电池 太阳能集热器 燃气灶 5.(6分)实验:
A.A B.B C.C D.D
①0.1mol•L﹣1AgNO
3
溶液和0.1mol•L﹣1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉
2.(6分)下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
淀c;
A.水中的钢闸门连接电源的负极
②向滤液b中滴加0.1mol•L﹣1KI溶液,出现浑浊;
B.金属护拦表面涂漆
③向沉淀c中滴加0.1mol•L﹣1KI溶液,沉淀变为黄色.
C.汽车底盘喷涂高分子膜 下列分析不正确的是( )
D.地下钢管连接镁块
A.浊液a中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl﹣(aq)
3.(6分)下列解释事实的方程式不准确的是( )
B.滤液b中不含有Ag+
⇌
A.用浓盐酸检验氨:NH +HCl=NH Cl C.③中颜色变化说明AgCl转化为AgI
3 4
B.碳酸钠溶液显碱性:CO 2﹣+H O HCO﹣ +OH﹣ D.实验可以证明AgI比AgCl更难溶
3 2 3
C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe﹣3e﹣=Fe3+ 6.(6分)下列实验事实不能用平衡移动原理解释的是( )
⇌
D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
4.(6分)用石墨电极电解CuCl 溶液(如图).下列分析正确的是( )
2
A. 将NO 球浸泡在冷水和热水中
2
B.
t/℃ 25 50 100
K /10﹣14 1.01 5.47 55.0
W已知:
C.
D.
C(氨水)/(mol•L﹣ 0.1 0.01
1) (1)A的含氧官能团名称是 .
(2)羧酸a的电离方程是 .
pH 11.1 10.6
7.(6分)用如图所示装置检验乙烯时不需要除杂的是( ) (3)B→C的化学方程式是 .
(4)化合物D苯环上的一氯代物有2种,D的结构简式是 .
乙烯的制备 试剂X 试剂Y
(5)E→F中反应①和②的反应类型分别是 .
A CH CH Br与NaOH乙醇溶液共热 水 KMnO 酸性溶液
3 2 4
(6)F的结构简式是 .
B CH CH Br与NaOH乙醇溶液共热 水 Br 的CCl 溶液
3 2 2 4
(7)聚合物P的结构简式是 .
C C H OH与浓H SO 加热至170℃ NaOH溶液 KMnO 酸性溶液
2 5 2 4 4
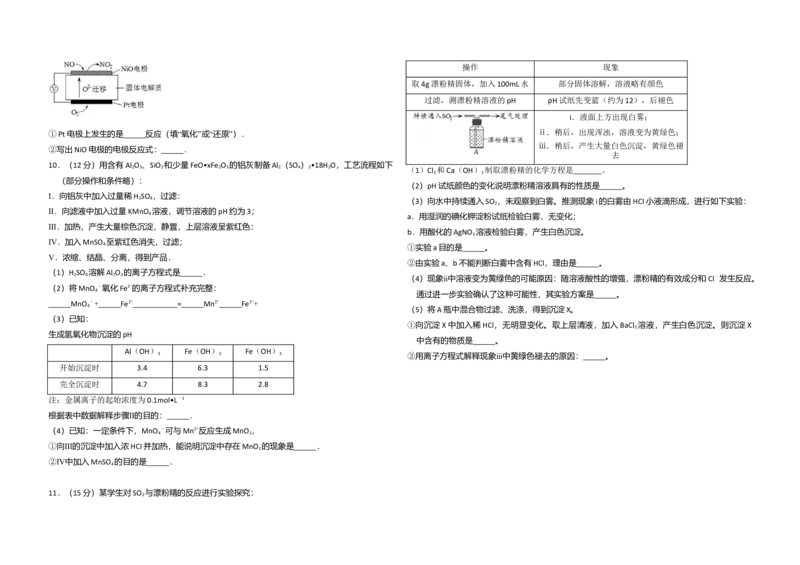
9.(14分)NO 是汽车尾气中的主要污染物之一.
x
D C H OH与浓H SO 加热至170℃ NaOH溶液 Br 的CCl 溶液
2 5 2 4 2 4
(1)NO 能形成酸雨,写出NO 转化为HNO 的化学方程式: .
x 2 3
(2)汽车发动机工作时会引发N 和O 反应,其能量变化示意图如下:
2 2
A.A B.B C.C D.D ①写出该反应的热化学方程式: .
②随温度升高,该反应化学平衡常数的变化趋势是: .
二、解答题(共4小题,满分58分) (3)在汽车尾气系统中装置催化转化器,可有效降低NO 的排放.
X
8.(17分)可降解聚合物P的合成路线如下: ①当尾气中空气不足时,NO 在催化转化器中被还原成N 排出.写出NO被CO还原的化学方程式:
x 2
.
②当尾气中空气过量时,催化转化器中的金属氧化物吸收 NO 生成盐.其吸收能力顺序如下:
x
MgO< CaO< SrO< BaO.原因是: ,元素的金属性逐渐增强,金属氧化物对 NO 的
12 20 38 56 x
吸收能力逐渐增强.
(4)通过NO 传感器可监测NO 的含量,其工作原理示意图如下:
x x操作 现象
取4g漂粉精固体,加入100mL水 部分固体溶解,溶液略有颜色
过滤,测漂粉精溶液的pH pH试纸先变蓝(约为12),后褪色
i.液面上方出现白雾;
①Pt电极上发生的是 反应(填“氧化”或“还原”). ⅱ.稍后,出现浑浊,溶液变为黄绿色;
ⅲ.稍后,产生大量白色沉淀,黄绿色褪
②写出NiO电极的电极反应式: .
去
10.(12分)用含有Al O 、SiO 和少量FeO•xFe O 的铝灰制备Al (SO ) •18H O,工艺流程如下
2 3 2 2 3 2 4 3 2 (1)Cl 和Ca(OH) 制取漂粉精的化学方程是 。
2 2
(部分操作和条件略):
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是 。
Ⅰ.向铝灰中加入过量稀H SO ,过滤:
2 4 (3)向水中持续通入SO ,未观察到白雾。推测现象i的白雾由HCl小液滴形成,进行如下实验:
2
Ⅱ.向滤液中加入过量KMnO 溶液,调节溶液的pH约为3;
4 a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
b.用酸化的AgNO 溶液检验白雾,产生白色沉淀。
3
Ⅳ.加入MnSO 至紫红色消失,过滤;
4 ①实验a目的是 。
Ⅴ.浓缩、结晶、分离,得到产品.
②由实验a、b不能判断白雾中含有HCl,理由是 。
(1)H SO 溶解Al O 的离子方程式是 .
2 4 2 3 (4)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl﹣发生反应。
(2)将MnO ﹣氧化Fe2+的离子方程式补充完整:
4
通过进一步实验确认了这种可能性,其实验方案是 。
MnO ﹣+ Fe2+ = Mn2+ Fe3++
4
(5)将A瓶中混合物过滤、洗涤,得到沉淀X。
(3)已知:
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl 溶液,产生白色沉淀。则沉淀X
2
生成氢氧化物沉淀的pH
中含有的物质是 。
Al(OH) Fe(OH) Fe(OH)
3 2 3 ②用离子方程式解释现象ⅲ中黄绿色褪去的原因: 。
开始沉淀时 3.4 6.3 1.5
完全沉淀时 4.7 8.3 2.8
注:金属离子的起始浓度为0.1mol•L﹣1
根据表中数据解释步骤Ⅱ的目的: .
(4)已知:一定条件下,MnO ﹣可与Mn2+反应生成MnO ,
4 2
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO 的现象是 .
2
②Ⅳ中加入MnSO 的目的是 .
4
11.(15分)某学生对SO 与漂粉精的反应进行实验探究:
2