文档内容
2014年北京市高考化学试卷
一、选择题:共7小题,每小题6分,共120分.在每小题给出的四个选项中,
选出最符合题目要求的一项.
1.(6 分)下列试剂中,标签上应标注 和 的是(
)
A.C H OH B.HNO C.NaOH D.HCl
2 5 3
2.(6分)下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化
的是( )
A.K B.Na C.Fe D.Al
3.(6分)下列电池工作时,O 在正极放电的是( )
2
A. 锌锰电池 B. 氢燃料电池
C. 铅蓄电池 D. 镍镉电池
4.(6分)下列解释事实的方程式不正确的是( )
A.测0.1mol/L氨水的pH为11:NH •H O NH ++OH﹣
3 2 4
B.将Na块放入水中,产生气体:2Na+2H O═2NaOH+H ↑
⇌2 2
C.用CuCl 溶液做导电实验,灯泡发光:CuCl Cu2++2Cl﹣
2 2
D.Al片溶于NaOH溶液中,产生气体:2Al+2OH﹣+2H O═2AlO ﹣+3H ↑
2 2 2
5.(6分)下列说法正确的是( )
A.室温下,在水中的溶解度:丙三醇>苯酚>1﹣氯丁烷
B.用核磁共振氢谱不能区分HCOOCH 和HCOOCH CH
3 2 3C.用Na CO 溶液不能区分CH COOH和CH COOCH CH
2 3 3 3 2 3
D.油脂在酸性或碱性条件下均可发生水解反应,且产物相同
6.(6分)用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能
证实①中反应发生的是( )
①中实验 ②中现象
A 铁粉与水蒸气加热 肥皂水冒泡
B 加热NH Cl和Ca(OH) 混合物 酚酞溶液变红
4 2
C NaHCO 固体受热分解 澄清石灰水变浑浊
3
D 石蜡油在碎瓷片上受热分解 Br 的CCl 溶液褪色
2 4
A.A B.B C.C D.D
7.(6分)一定温度下,10mL 0.40mol/L H O 溶液发生催化分解。不同时刻测
2 2
得生成O 的体积(已折算为标准状况)如下表。
2
t/min 0 2 4 6 8 10
V(O )/ 0.0 9.9 17.2 22.4 26.5 29.9
2
mL
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6min的平均反应速率:v(H O )≈3.3×10﹣2mol/(L•min)
2 2
B.6~10min的平均反应速率:v(H 0 )<3.3×10﹣2mol/(L•min)
2 2
C.反应至6min时,c(H O )=0.30mol/L
2 2
D.反应至6min时,H O 分解了50%
2 2
二、非选择题:共4小题,共180分
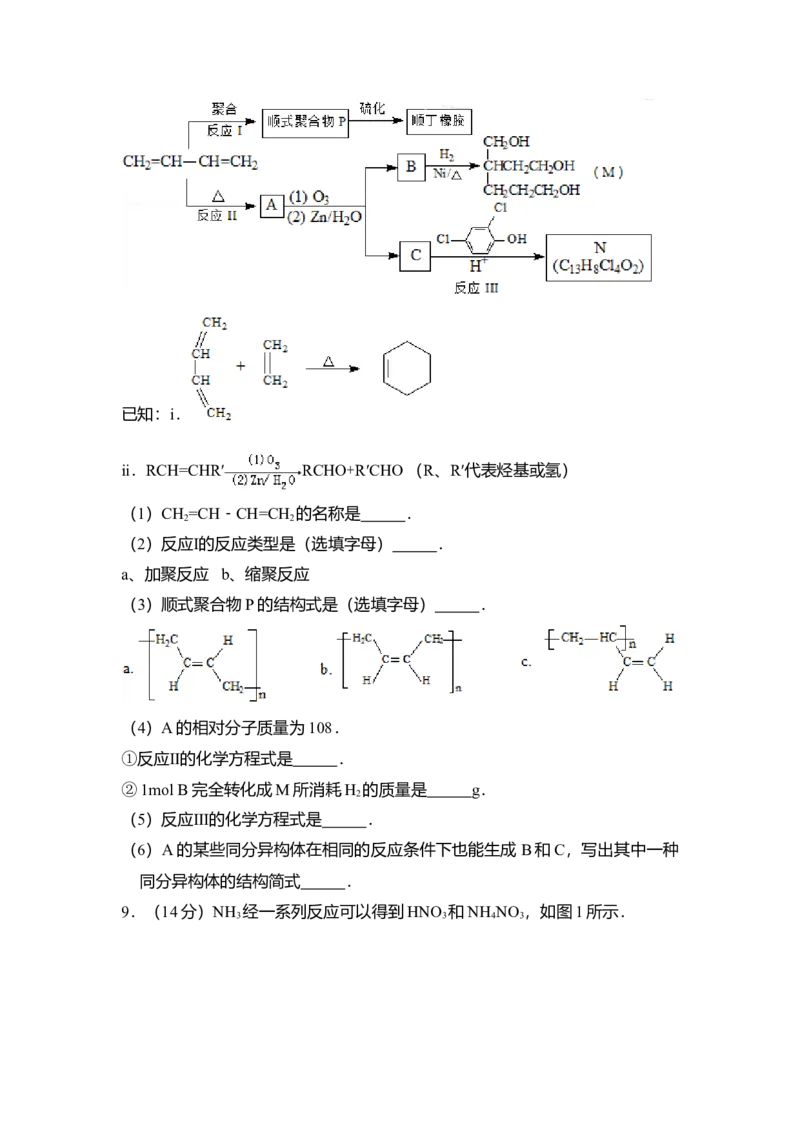
8.(17分)顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:已知:i.
ⅱ.RCH=CHR′ RCHO+R′CHO (R、R′代表烃基或氢)
(1)CH =CH﹣CH=CH 的名称是 .
2 2
(2)反应Ⅰ的反应类型是(选填字母) .
a、加聚反应 b、缩聚反应
(3)顺式聚合物P的结构式是(选填字母) .
(4)A的相对分子质量为108.
①反应Ⅱ的化学方程式是 .
②1mol B完全转化成M所消耗H 的质量是 g.
2
(5)反应Ⅲ的化学方程式是 .
(6)A的某些同分异构体在相同的反应条件下也能生成 B和C,写出其中一种
同分异构体的结构简式 .
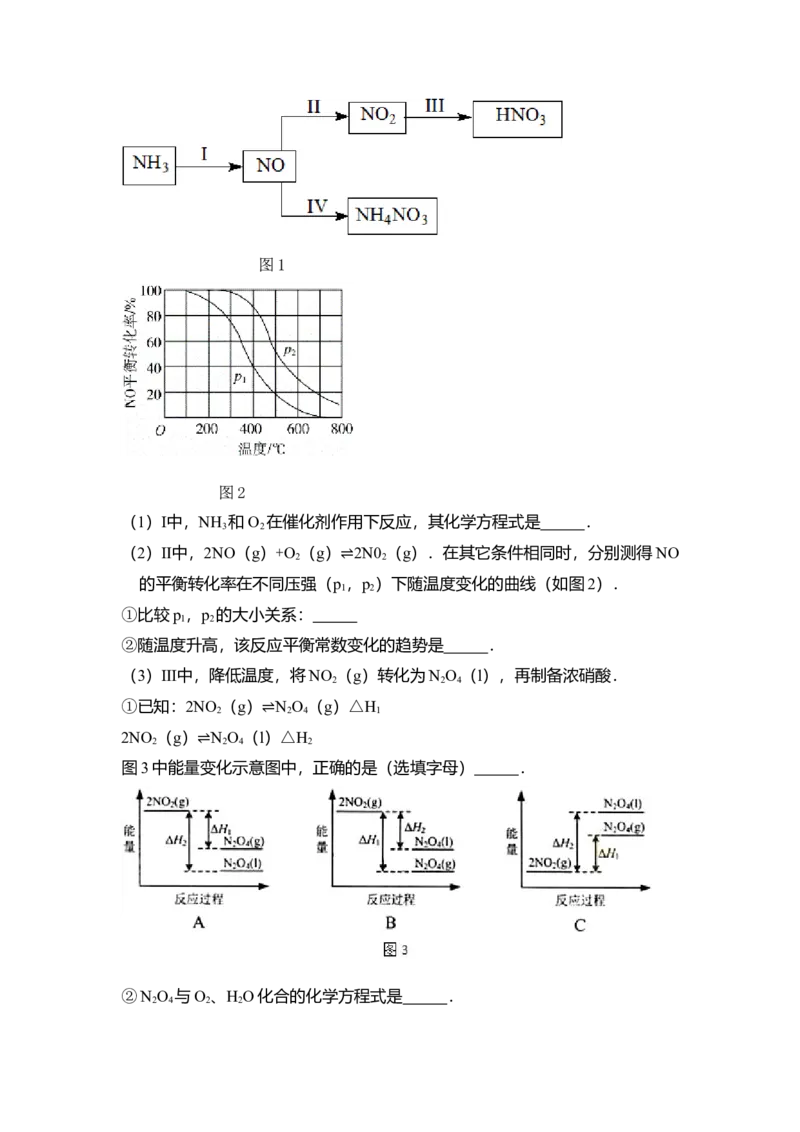
9.(14分)NH 经一系列反应可以得到HNO 和NH NO ,如图1所示.
3 3 4 3图1
图2
(1)Ⅰ中,NH 和O 在催化剂作用下反应,其化学方程式是 .
3 2
(2)Ⅱ中,2NO(g)+O (g) 2N0 (g).在其它条件相同时,分别测得NO
2 2
的平衡转化率在不同压强(p ,p )下随温度变化的曲线(如图2).
⇌1 2
①比较p ,p 的大小关系:
1 2
②随温度升高,该反应平衡常数变化的趋势是 .
(3)Ⅲ中,降低温度,将NO (g)转化为N O (l),再制备浓硝酸.
2 2 4
①已知:2NO (g) N O (g)△H
2 2 4 1
2NO (g) N O (l)△H
2 2 4 ⇌ 2
图3中能量变化示意图中,正确的是(选填字母) .
⇌
②N O 与O 、H O化合的化学方程式是 .
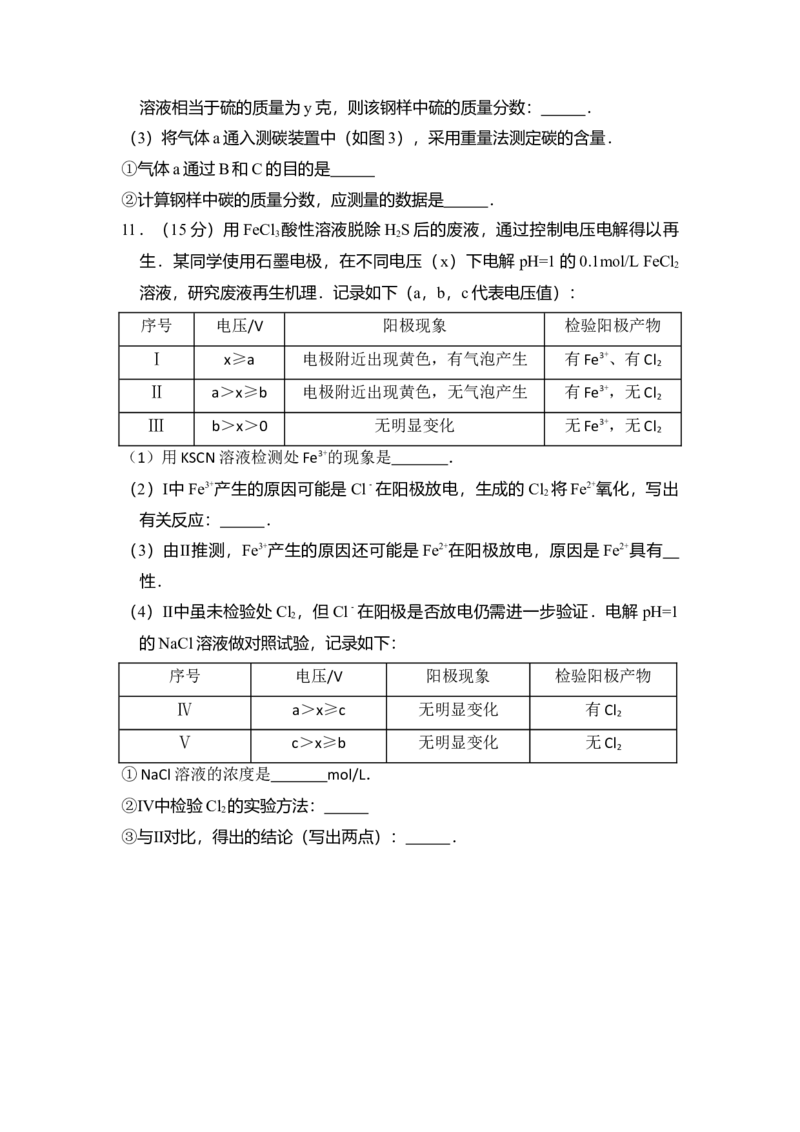
2 4 2 2(4)Ⅳ中,电解NO制备NH NO ,其工作原理如图4所示,为使电解产物全
4 3
部转化为NH NO ,需补充物质A,A是 ,说明理由: .
4 3
图4
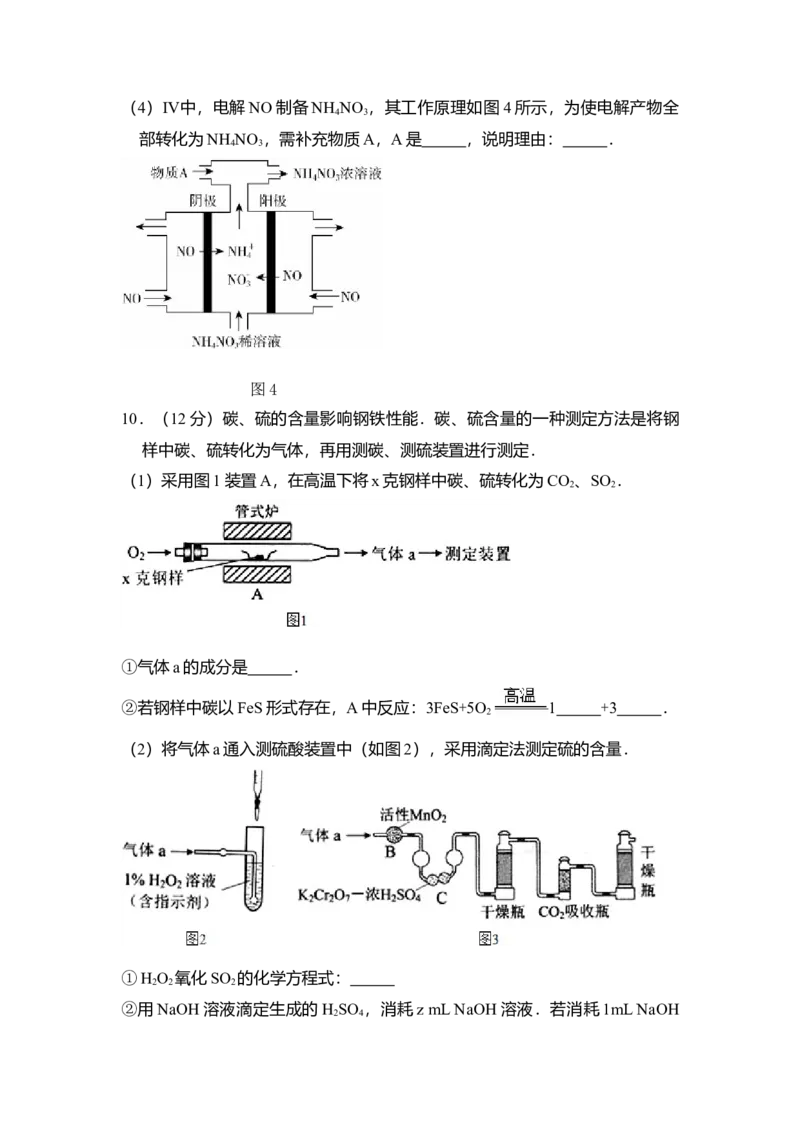
10.(12分)碳、硫的含量影响钢铁性能.碳、硫含量的一种测定方法是将钢
样中碳、硫转化为气体,再用测碳、测硫装置进行测定.
(1)采用图1装置A,在高温下将x克钢样中碳、硫转化为CO 、SO .
2 2
①气体a的成分是 .
②若钢样中碳以FeS形式存在,A中反应:3FeS+5O 1 +3 .
2
(2)将气体a通入测硫酸装置中(如图2),采用滴定法测定硫的含量.
①H O 氧化SO 的化学方程式:
2 2 2
②用NaOH溶液滴定生成的H SO ,消耗z mL NaOH溶液.若消耗1mL NaOH
2 4溶液相当于硫的质量为y克,则该钢样中硫的质量分数: .
(3)将气体a通入测碳装置中(如图3),采用重量法测定碳的含量.
①气体a通过B和C的目的是
②计算钢样中碳的质量分数,应测量的数据是 .
11.(15分)用FeCl 酸性溶液脱除H S后的废液,通过控制电压电解得以再
3 2
生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L FeCl
2
溶液,研究废液再生机理.记录如下(a,b,c代表电压值):
序号 电压/V 阳极现象 检验阳极产物
Ⅰ x≥a 电极附近出现黄色,有气泡产生 有Fe3+、有Cl
2
Ⅱ a>x≥b 电极附近出现黄色,无气泡产生 有Fe3+,无Cl
2
Ⅲ b>x>0 无明显变化 无Fe3+,无Cl
2
(1)用KSCN溶液检测处Fe3+的现象是 .
(2)Ⅰ中Fe3+产生的原因可能是Cl﹣在阳极放电,生成的 Cl 将Fe2+氧化,写出
2
有关反应: .
(3)由Ⅱ推测,Fe3+产生的原因还可能是 Fe2+在阳极放电,原因是 Fe2+具有
性.
(4)Ⅱ中虽未检验处Cl ,但Cl﹣在阳极是否放电仍需进一步验证.电解 pH=1
2
的NaCl溶液做对照试验,记录如下:
序号 电压/V 阳极现象 检验阳极产物
Ⅳ a>x≥c 无明显变化 有Cl
2
Ⅴ c>x≥b 无明显变化 无Cl
2
①NaCl溶液的浓度是 mol/L.
②Ⅳ中检验Cl 的实验方法:
2
③与Ⅱ对比,得出的结论(写出两点): .