文档内容
2014 年天津市高考化学试卷 B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl﹣)=c(I﹣)
C.CO 的水溶液:c(H+)>c(HCO ﹣)=2c(CO 2﹣)
一、选择题(共6小题,每小题6分,满分36分) 2 3 3
D.含等物质的量NaHC O 和Na C O 的溶液:3c(Na+)=2[c(HC O ﹣)+c(C O 2﹣)+c(H C O )]
1.(6分)化学与生产、生活息息相关,下列叙述错误的是( ) 2 4 2 2 4 2 4 2 4 2 2 4
6.(6分)已知:
A.铁表面镀锌可增强其抗腐蚀性
放电
B.用聚乙烯塑料代替聚乳酸塑料可减少白色污染
锂离子电池的总反应为:Li
x
C+Li
1﹣x
CoO
2
⇌C+LiCoO
2
;
充电
放电
C.大量燃烧化石燃料是造成雾霾天气的一种重要因素
锂硫电池的总反应为:2Li+S ⇌Li S
2
充电
D.含重金属离子的电镀废液不能随意排放
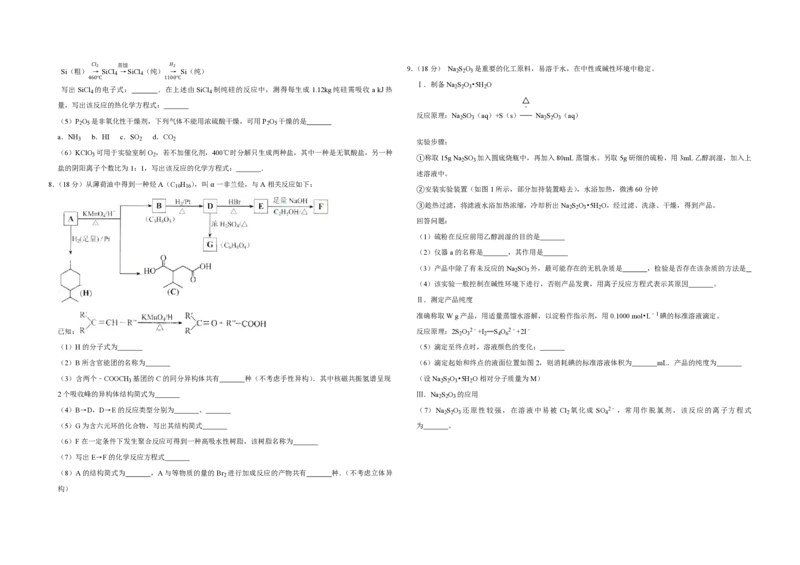
有关上述两种电池说法正确的是( )
2.(6分)实验室制备下列气体时,所用方法正确的是( )
A.锂离子电池放电时,Li+向负极迁移
A.制氧气时,用Na O 或H O 作反应物可选择相同的气体发生装置
2 2 2 2 B.锂硫电池充电时,锂电极发生还原反应
B.制氯气时,用饱和NaHCO 溶液和浓硫酸净化气体
3 C.理论上两种电池的比能量相同
C.制乙烯时,用排水法或向上排空气法收集气体
D.制二氧化氮时,用水或NaOH溶液吸收尾气
3.(6分)运用相关化学知识进行判断,下列结论错误的是( )
D. 图中表示用锂离子电池给锂硫电池充电
A.某吸热反应能自发进行,因此该反应是熵增反应
二、解答题(共4小题,满分64分)
B.NH F水溶液中含有HF,因此NH F溶液不能存放于玻璃试剂瓶中
4 4
7.(14分)元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
(1)按原子序数递增的顺序(稀有气体除外),下列说法正确的是
D.增大反应物浓度可加快反应速度,因此用浓硫酸与铁反应能增大生成H 的速率
2
a.原子半径和离子半径均减小; b.金属性减弱,非金属性增强;
4.(6分)对如图两种化合物的结构或性质描述正确的是( )
c.氧化物对应的水化物碱性减弱,酸性增强; d.单质的熔点降低.
(2)原子最外层电子数与次外层电子数相同的元素名称为 ,氧化性最弱的简单阳离子是
(3)已知:
化合物 MgO Al O MgCl AlCl
2 3 2 3
A.不是同分异构体
类型 离子化合物 离子化合物 离子化合物 共价化合物
B.分子中共平面的碳原子数相同 熔点/℃ 2800 2050 714 191
C.均能与溴水反应 工业制镁时,电解MgCl 而不电解MgO的原因是
2
D.可用红外光谱区分,但不能用核磁共振氢谱区分 制铝时,电解Al O 而不电解AlCl 的原因是
2 3 3
5.(6分)下列有关电解质溶液中粒子浓度关系正确的是( ) (4)晶体硅(熔点1410℃)是良好的半导体材料,由粗硅制纯硅过程如下:
A.pH=1的NaHSO 溶液:c(H+)=c(SO 2﹣)+c(OH﹣)
4 4𝐶𝑙 2 蒸馏 𝐻 2 9.(18分) Na S O 是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
Si(粗) →SiCl →SiCl (纯) → Si(纯) 2 2 3
4 4
460℃ 1100℃
Ⅰ.制备Na S O •5H O
2 2 3 2
写出 SiCl 的电子式: .在上述由 SiCl 制纯硅的反应中,测得每生成 1.12kg纯硅需吸收 a kJ热
4 4
△
量,写出该反应的热化学方程式:
¯
反应原理:Na SO (aq)+S(s) Na S O (aq)
2 3 2 2 3
(5)P O 是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P O 干燥的是
2 5 2 5
a.NH b.HI c.SO d.CO
3 2 2 实验步骤:
(6)KClO 可用于实验室制O ,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种
3 2
①称取15g Na SO 加入圆底烧瓶中,再加入80mL蒸馏水。另取5g研细的硫粉,用3mL乙醇润湿,加入上
2 3
盐的阴阳离子个数比为1:1,写出该反应的化学方程式: .
述溶液中。
8.(18分)从薄荷油中得到一种烃A(C H ),叫α一非兰烃,与A相关反应如下:
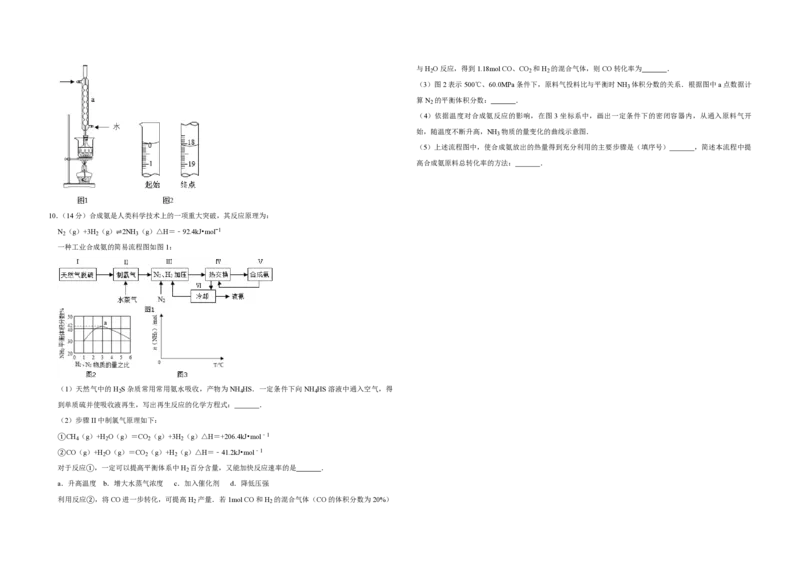
10 16 ②安装实验装置(如图1所示,部分加持装置略去),水浴加热,微沸60分钟
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na S O •5H O,经过滤、洗涤、干燥,得到产品。
2 2 3 2
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是
(2)仪器a的名称是 ,其作用是
(3)产品中除了有未反应的Na SO 外,最可能存在的无机杂质是 ,检验是否存在该杂质的方法是
2 3
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因 。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L﹣1碘的标准溶液滴定。
已知: 反应原理:2S O 2﹣+I ═S O 2﹣+2I﹣
2 3 2 4 6
(1)H的分子式为 (5)滴定至终点时,溶液颜色的变化:
(2)B所含官能团的名称为 (6)滴定起始和终点的液面位置如图2,则消耗碘的标准溶液体积为 mL.产品的纯度为
(3)含两个﹣COOCH 基团的C的同分异构体共有 种(不考虑手性异构).其中核磁共振氢谱呈现 (设Na S O •5H O相对分子质量为M)
3 2 2 3 2
2个吸收峰的异构体结构简式为 Ⅲ.Na S O 的应用
2 2 3
(4)B→D,D→E的反应类型分别为 、 (7)Na S O 还原性较强,在溶液中易被 Cl 氧化成 SO 2﹣,常用作脱氯剂,该反应的离子方程式
2 2 3 2 4
(5)G为含六元环的化合物,写出其结构简式 为 。
(6)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂名称为
(7)写出E→F的化学反应方程式
(8)A的结构简式为 ,A与等物质的量的Br 进行加成反应的产物共有 种.(不考虑立体异
2
构)与H O反应,得到1.18mol CO、CO 和H 的混合气体,则CO转化率为 .
2 2 2
(3)图2表示500℃、60.0MPa条件下,原料气投料比与平衡时NH 体积分数的关系.根据图中a点数据计
3
算N 的平衡体积分数: .
2
(4)依据温度对合成氨反应的影响,在图 3坐标系中,画出一定条件下的密闭容器内,从通入原料气开
始,随温度不断升高,NH 物质的量变化的曲线示意图.
3
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是(填序号) ,简述本流程中提
高合成氨原料总转化率的方法: .
10.(14分)合成氨是人类科学技术上的一项重大突破,其反应原理为:
N (g)+3H (g)⇌2NH (g)△H=﹣92.4kJ•mol‾1
2 2 3
一种工业合成氨的简易流程图如图1:
(1)天然气中的H S杂质常用常用氨水吸收,产物为NH HS.一定条件下向NH HS溶液中通入空气,得
2 4 4
到单质硫并使吸收液再生,写出再生反应的化学方程式: .
(2)步骤II中制氯气原理如下:
①CH (g)+H O(g)=CO (g)+3H (g)△H=+206.4kJ•mol﹣1
4 2 2 2
②CO(g)+H O(g)=CO (g)+H (g)△H=﹣41.2kJ•mol﹣1
2 2 2
对于反应①,一定可以提高平衡体系中H 百分含量,又能加快反应速率的是 .
2
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H 产量.若1mol CO和H 的混合气体(CO的体积分数为20%)
2 2