文档内容
2014 年浙江省高考化学试卷 C.淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
D.CH COOCH CH 与 CH CH COOCH 互为同分异构体,1H﹣NMR 谱显示两者均有三种不同的氢原子
3 2 3 3 2 3
且三种氢原子的比例相同,故不能用1H﹣NMR 来鉴别
一、选择题(共 7小题,每小题 3分,满分 21分)
5.(3分)镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型,NiMH中的 M 表
1.(3分)下列说法不正确的是( )
示金属或合金,该电池在充电过程中的总反应方程式是:Ni(OH) +M═NiOOH+MH
A.光催化还原水制氢比电解水制氢更节能环保、更经济 2
已知:6NiOOH+NH +H O+OH﹣═6Ni(OH) +NO ﹣
B.氨氮废水(含 NH +及NH )可用化学氧化法或电化学氧化法处理 3 2 2 2
4 3
下列说法正确的是( )
C.某种光学检测技术具有极高的灵敏度,可检测到单个细胞(V≈10﹣12L)内的数个目标分子,据
A.NiMH 电池放电过程中,正极的电极反应式为:NiOOH+H O+e﹣═Ni(OH) +OH﹣
此可推算该检测技术能检测细胞内浓度约为10﹣12﹣10﹣11mol•L﹣1的目标分子 2 2
B.充电过程中 OH﹣离子从阳极向阴极迁移
D.向汽油中添加甲醇后,该混合燃料的热值不变
C.充电过程中阴极的电极反应式:H O+M+e﹣═MH+OH﹣,H O 中的H 被M 还原
2.(3分)下列说法正确的是( ) 2 2
D.NiMH 电池中可以用 KOH溶液、氨水等作为电解质溶液
A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
6.(3分)氯在饮用水处理中常用作杀菌剂,且 HClO的杀菌能力比 ClO﹣强,25℃时氯气﹣氯水体
B.用 pH 计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度
系中存在以下平衡关系:
C.邻苯二甲酸氢钾可用于标定 NaOH溶液的浓度,假如称量邻苯二甲酸氢钾时电子天平读数比实
Cl (g)⇌Cl (aq) K =10﹣1.2
际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小 2 2 1
Cl (aq)+H O⇌HClO+H++Cl﹣ K =10﹣3.4
D.向某溶液中加入茚三铜试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质 2 2 2
HClO⇌H++ClO﹣ K =?
3.(3分)如图所示的五中元素中,W、X、Y、Z 为短周期元素,这四种元素的原子最外层电子数 a
其中 Cl (aq)、HClO和 ClO﹣分别在三者中所占分数(α)随 pH 变化的关系如图所示,下列表述正
之和为22,下列说法正确的是( ) 2
确的是( )
A.X、Y、Z 三种元素最低价氢化物的沸点依次升高
B.由 X、Y 和氢三种元素形成的化合物中只有共价键
C.物质WY ,W X ,WZ 均有熔点高,硬度大的特性 A.Cl (g)+H O⇌2H++ClO﹣+Cl﹣ K=10﹣10.9
2 3 4 4 2 2
D.T 元素的单质具有半导体的特性,T 与Z 元素可形成化合物TZ B.在氯处理水体系中,c(HClO)+c(ClO﹣)=c(H+)﹣c(OH﹣)
4
4.(3分)下列说法正确的是( ) C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
A.乳酸薄荷醇酯( )仅能发生水解、氧化、消去反应
7.(3分)雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下可溶性无机离子:
B.乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物
Na+、NH +、Mg2+、Al3+、SO 2﹣、NO ﹣、Cl﹣.某同学收集了该地区的雾霾,经必要的预处理后的试
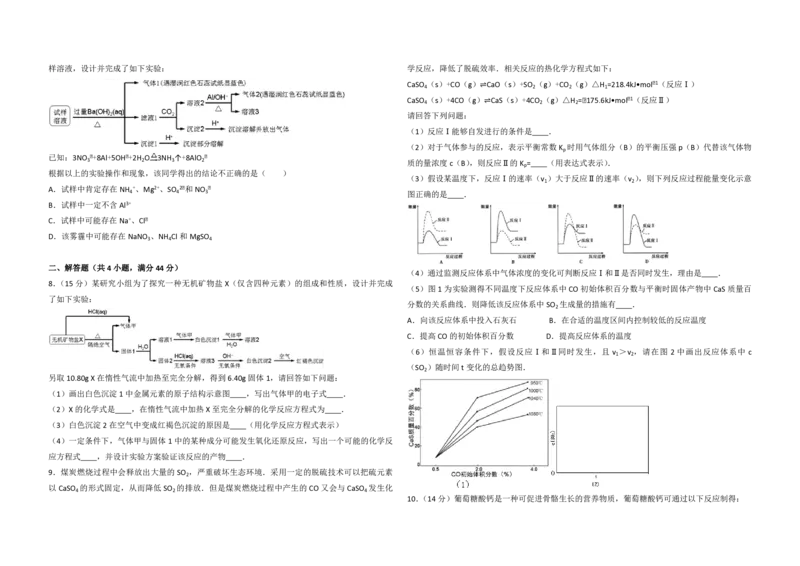
4 4 3样溶液,设计并完成了如下实验: 学反应,降低了脱硫效率.相关反应的热化学方程式如下:
CaSO (s)+CO(g)⇌CaO(s)+SO (g)+CO (g)△H =218.4kJ•mol﹣1(反应Ⅰ)
4 2 2 1
CaSO (s)+4CO(g)⇌CaS(s)+4CO (g)△H =﹣175.6kJ•mol﹣1(反应Ⅱ)
4 2 2
请回答下列问题:
(1)反应Ⅰ能够自发进行的条件是 .
(2)对于气体参与的反应,表示平衡常数 K 时用气体组分(B)的平衡压强 p(B)代替该气体物
p
已知:3NO ﹣+8Al+5OH﹣+2H O 3NH ↑+8AlO ﹣
3 2 3 2 质的量浓度c(B),则反应Ⅱ的K = (用表达式表示).
p
根据以上的实验操作和现象,该同学得出的结论不正确的是( )
(3)假设某温度下,反应Ⅰ的速率(v )大于反应Ⅱ的速率(v ),则下列反应过程能量变化示意
1 2
A.试样中肯定存在 NH +、Mg2+、SO 2﹣和NO ﹣
4 4 3 图正确的是 .
B.试样中一定不含 Al3+
C.试样中可能存在 Na+、Cl﹣
D.该雾霾中可能存在 NaNO 、NH Cl 和MgSO
3 4 4
二、解答题(共 4小题,满分 44分)
(4)通过监测反应体系中气体浓度的变化可判断反应Ⅰ和Ⅱ是否同时发生,理由是 .
8.(15分)某研究小组为了探究一种无机矿物盐 X(仅含四种元素)的组成和性质,设计并完成
(5)图 1为实验测得不同温度下反应体系中 CO 初始体积百分数与平衡时固体产物中 CaS 质量百
了如下实验:
分数的关系曲线.则降低该反应体系中SO 生成量的措施有 .
2
A.向该反应体系中投入石灰石 B.在合适的温度区间内控制较低的反应温度
C.提高CO 的初始体积百分数 D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且 v >v ,请在图 2中画出反应体系中 c
1 2
(SO )随时间t变化的总趋势图.
2
另取10.80g X 在惰性气流中加热至完全分解,得到6.40g固体1,请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图 ,写出气体甲的电子式 .
(2)X 的化学式是 ,在惰性气流中加热 X 至完全分解的化学反应方程式为 .
(3)白色沉淀2在空气中变成红褐色沉淀的原因是 (用化学反应方程式表示)
(4)一定条件下,气体甲与固体 1中的某种成分可能发生氧化还原反应,写出一个可能的化学反
应方程式 ,并设计实验方案验证该反应的产物 .
9.煤炭燃烧过程中会释放出大量的 SO ,严重破坏生态环境.采用一定的脱硫技术可以把硫元素
2
以 CaSO 的形式固定,从而降低 SO 的排放.但是煤炭燃烧过程中产生的 CO 又会与 CaSO 发生化
4 2 4
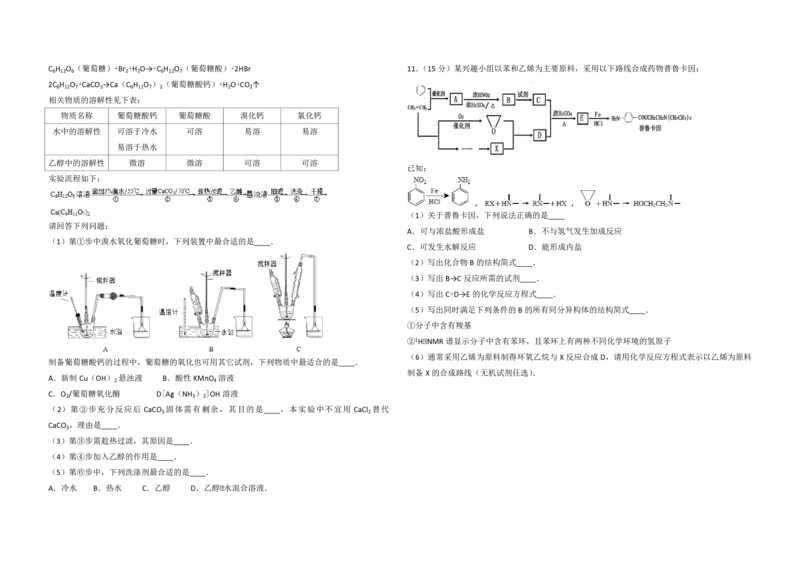
10.(14分)葡萄糖酸钙是一种可促进骨骼生长的营养物质,葡萄糖酸钙可通过以下反应制得:C H O (葡萄糖)+Br +H O→+C H O (葡萄糖酸)+2HBr 11.(15分)某兴趣小组以苯和乙烯为主要原料,采用以下路线合成药物普鲁卡因:
6 12 6 2 2 6 12 7
2C H O +CaCO →Ca(C H O ) (葡萄糖酸钙)+H O+CO ↑
6 12 7 3 6 11 7 2 2 2
相关物质的溶解性见下表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙 氯化钙
水中的溶解性 可溶于冷水 可溶 易溶 易溶
易溶于热水
乙醇中的溶解性 微溶 微溶 可溶 可溶
已知:
实验流程如下:
(1)关于普鲁卡因,下列说法正确的是
请回答下列问题:
A.可与浓盐酸形成盐 B.不与氢气发生加成反应
(1)第①步中溴水氧化葡萄糖时,下列装置中最合适的是 .
C.可发生水解反应 D.能形成内盐
(2)写出化合物B的结构简式 .
(3)写出B→C 反应所需的试剂 .
(4)写出C+D→E的化学反应方程式 .
(5)写出同时满足下列条件的B的所有同分异构体的结构简式 .
①分子中含有羧基
②1H﹣NMR 谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子
(6)通常采用乙烯为原料制得环氧乙烷与 X 反应合成 D,请用化学反应方程式表示以乙烯为原料
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是 .
制备X 的合成路线(无机试剂任选).
A.新制 Cu(OH) 悬浊液 B.酸性KMnO 溶液
2 4
C.O /葡萄糖氧化酶 D[Ag(NH ) ]OH 溶液
2 3 2
(2)第②步充分反应后 CaCO 固体需有剩余,其目的是 ,本实验中不宜用 CaCl 替代
3 2
CaCO ,理由是 .
3
(3)第③步需趁热过滤,其原因是 .
(4)第④步加入乙醇的作用是 .
(5)第⑥步中,下列洗涤剂最合适的是 .
A.冷水 B.热水 C.乙醇 D.乙醇﹣水混合溶液.