文档内容
2014年普通高等学校招生全国统一考试化学(山东卷)
7.下表中对应关系正确的是
A 均为取代反应
CHCH+Cl CHCHCl+HCl
3 3 2 3 2
CH=CH +HCl CHCHCl
2 2 3 2
B 由油脂得到甘油由淀粉得到葡萄糖 均发生了水解反应
C Cl+2Br‾=2Cl‾+Br 均为单质被还原的置换反应
2 2
Zn+Cu2+=Zn2++Cu
D 2NaO+2H O+4NaOH+O ↑ 均为水作还原剂的氧化还原反应
2 2 2 2
Cl+H O=HCl+HClO
2 2
8.根据原子结构及元素周期律的知识,下列推断正确的是
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl‾、S2‾、Ca2+、K+半径逐渐减小
D.Cl与Cl得电子能力相同
9.等质量的下列物质与足量稀硝酸反应,放出NO物质的量最多的是
A.FeO B. Fe O C. FeSO D、Fe O
2 3 4 3 4
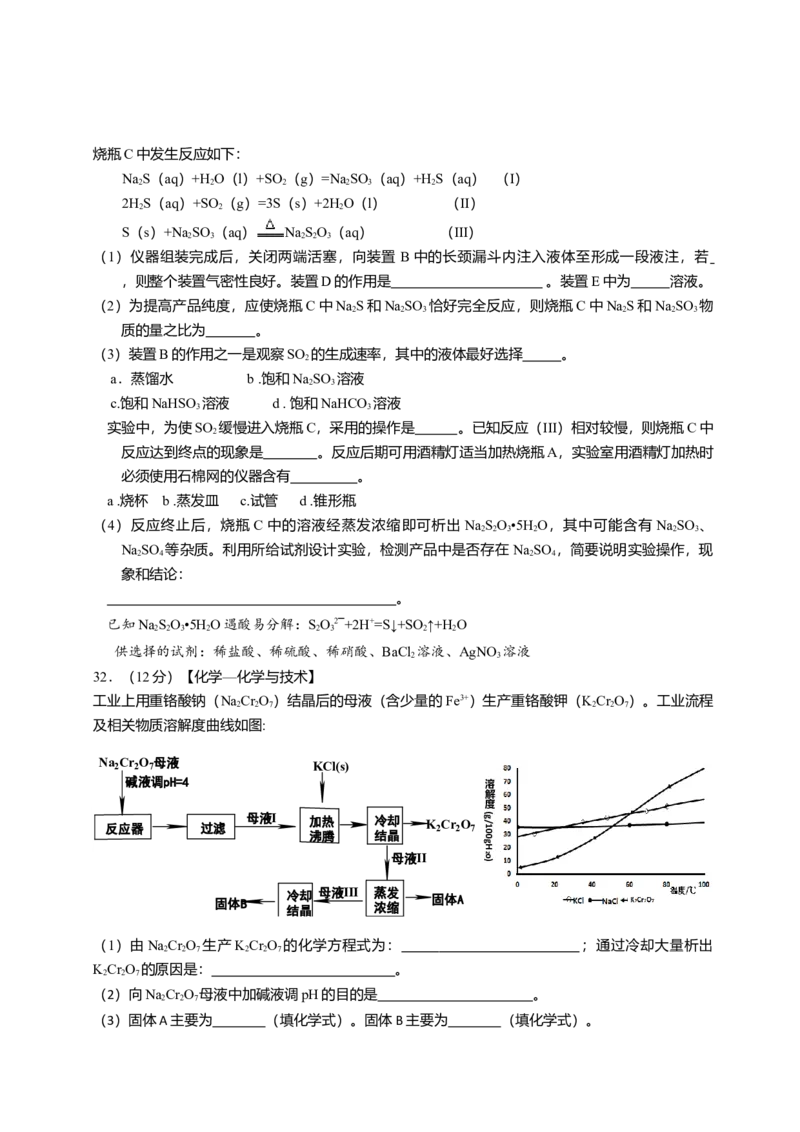
10.下列实验操作或装置(略去部分加持仪器)正确的是
11.苹果酸的结构简式 为下列说法正确的
OH
是
HOOC CH CH COOH
2
A.苹果酸中能发生酯化反应的官能团有2种
B.1mol苹果酸可与3mol NaOH发生中和反应
C.1mol苹果酸与足量金属Na反应生成生成1mol H
2
D.HOOC—CH —CH(OH)—COOH与苹果酸互为同分异构体
2
12.下列有关溶液组成的描述合理的是
A.无色溶液中可能大量存在Al3+、NH +、Cl‾、S2‾
4
B.酸性溶液中可能大量存在Na+、ClO‾、SO 2‾、I‾
4
C.弱碱性溶液中可能大量存在Na+、K+、Cl‾、HCO ‾
3
D.中性溶液中可能大量存在Fe3+、K+、Cl‾、SO 2‾
4
13.已知某温度下 CHCOOH 和 NH •H O 的电离常数相等,现向 10mL 浓度为 0.1mol•L‾1的
3 3 2
CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中
3A.水的电离程度始终增大
B.c(NH +)/c(NH •H O)先增大再减小
4 3 2
C.c(CHCOOH)与c(CHCOO‾)之和始终保持不变
3 3
D.当加入氨水的体积为10mL时,c(NH +)=c(CH COO‾)
4 3
29.(17分)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO (g)+NaCl(s) NaNO (s)+ClNO(g) K ∆H < 0 (I)
2 3 1
2NO(g)+Cl(g) 2ClNO(g) K ∆H < 0 (II)
2 2
(1)4NO (g)+2NaCl(s) 2NaNO (s)+2NO(g)+Cl (g)的平衡常数K= (用K 、
2 3 2 1
K 表示)。
2
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和
0.1mol Cl ,10min时反应(II)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则
2
平衡后n(Cl )= mol,NO的转化率а= 。其它条件保持不变,反应(II)在恒压条
2 1
件下进行,平衡时NO的转化率а а (填“>”“<”或“=”),平衡常数K (填“增大”
2 1 2
“减小”或“不变”。若要使K 减小,可采用的措施是 。
2
(3)实验室可用NaOH溶液吸收NO ,反应为2NO +2NaOH=NaNO +NaNO +H O。含0.2mol NaOH
2 2 3 2 2
的水溶液与0.2mol NO 恰好完全反应得1L溶液A,溶液B为0.1mol•L‾1的CHCOONa溶液,
2 3
则两溶液中c(NO ‾)、c(NO -)和c(CHCOO‾)由大到小的顺序为 。(已知
3 2 3
HNO 的电离常数K=7.1×10-4mol•L‾1,CHCOOH的电离常数K =1.7×10-5mol•L‾1,可使溶液A
2 a 3 a
和溶液B的pH相等的方法是 。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d..向溶液B中加适量NaOH
30.(16分)离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al Cl—和AlCl —组成的离
2 7 4
子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品应接电源的 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴
极电极反应式为 。若改用AlCl 水溶液作电解液,则阴极产物为 。
3
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还
原产物的物质的量为 mol。
(3)用铝粉和Fe O 做铝热反应实验,需要的试剂还有 。
2 3
a.KCl b. KClO c. MnO d. Mg
3 2
取少量铝热反应所得到的固体混合物,将其溶于足量稀 HSO ,滴加KSCN溶液无明显现象,
2 4
(填“能”或“不能”)说明固体混合物中无Fe O,理由是 (用离子方程式说明)。
2 3
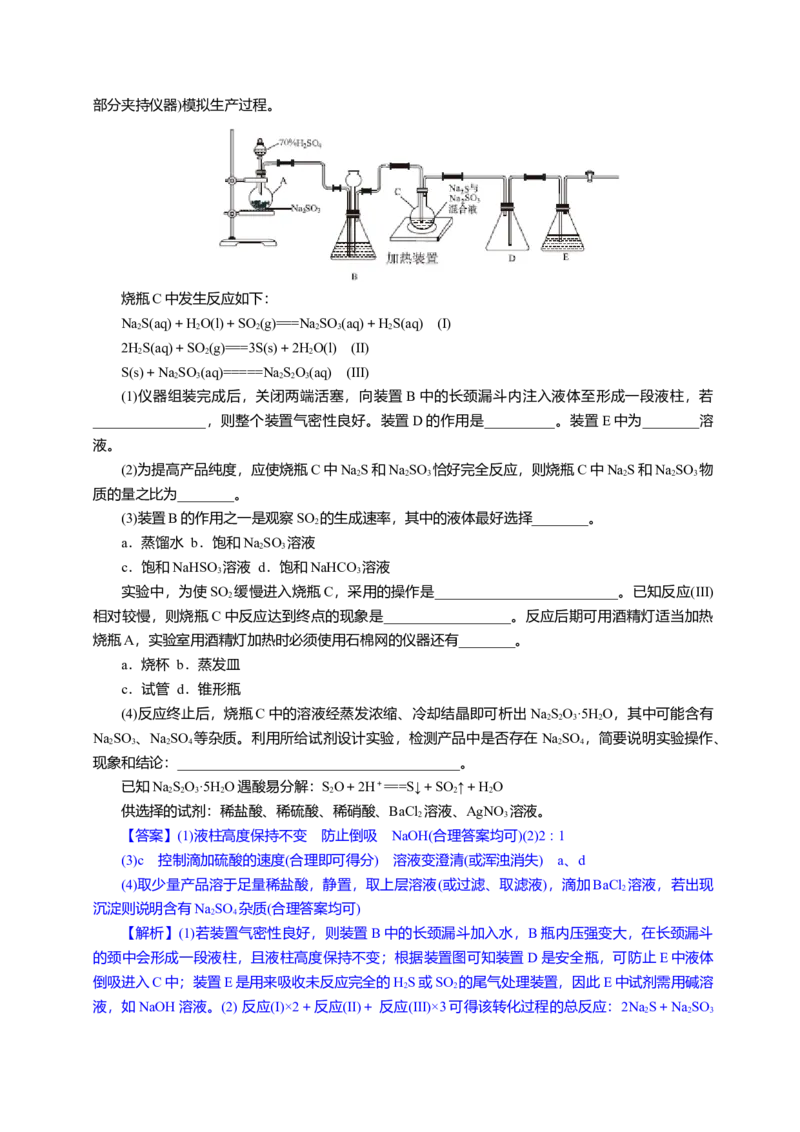
31.(20分)工业上常利用含硫废水生产NaSO•5H O,实验室可用如下装置(略去部分加持仪
2 2 3 2
器)模拟生成过程。烧瓶C中发生反应如下:
NaS(aq)+H O(l)+SO(g)=Na SO (aq)+H S(aq) (I)
2 2 2 2 3 2
2HS(aq)+SO(g)=3S(s)+2H O(l) (II)
2 2 2
S(s)+Na SO (aq) NaSO(aq) (III)
2 3 2 2 3
(1)仪器组装完成后,关闭两端活塞,向装置 B中的长颈漏斗内注入液体至形成一段液注,若
,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中NaS和NaSO 恰好完全反应,则烧瓶C中NaS和NaSO 物
2 2 3 2 2 3
质的量之比为 。
(3)装置B的作用之一是观察SO 的生成速率,其中的液体最好选择 。
2
a.蒸馏水 b .饱和NaSO 溶液
2 3
c.饱和NaHSO 溶液 d . 饱和NaHCO 溶液
3 3
实验中,为使SO 缓慢进入烧瓶C,采用的操作是 。已知反应(III)相对较慢,则烧瓶C中
2
反应达到终点的现象是 。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时
必须使用石棉网的仪器含有 。
a .烧杯 b .蒸发皿 c.试管 d .锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出NaSO•5H O,其中可能含有NaSO 、
2 2 3 2 2 3
NaSO 等杂质。利用所给试剂设计实验,检测产品中是否存在 NaSO ,简要说明实验操作,现
2 4 2 4
象和结论:
。
已知NaSO•5HO遇酸易分解:SO2‾+2H+=S↓+SO ↑+H O
2 2 3 2 2 3 2 2
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl 溶液、AgNO 溶液
2 3
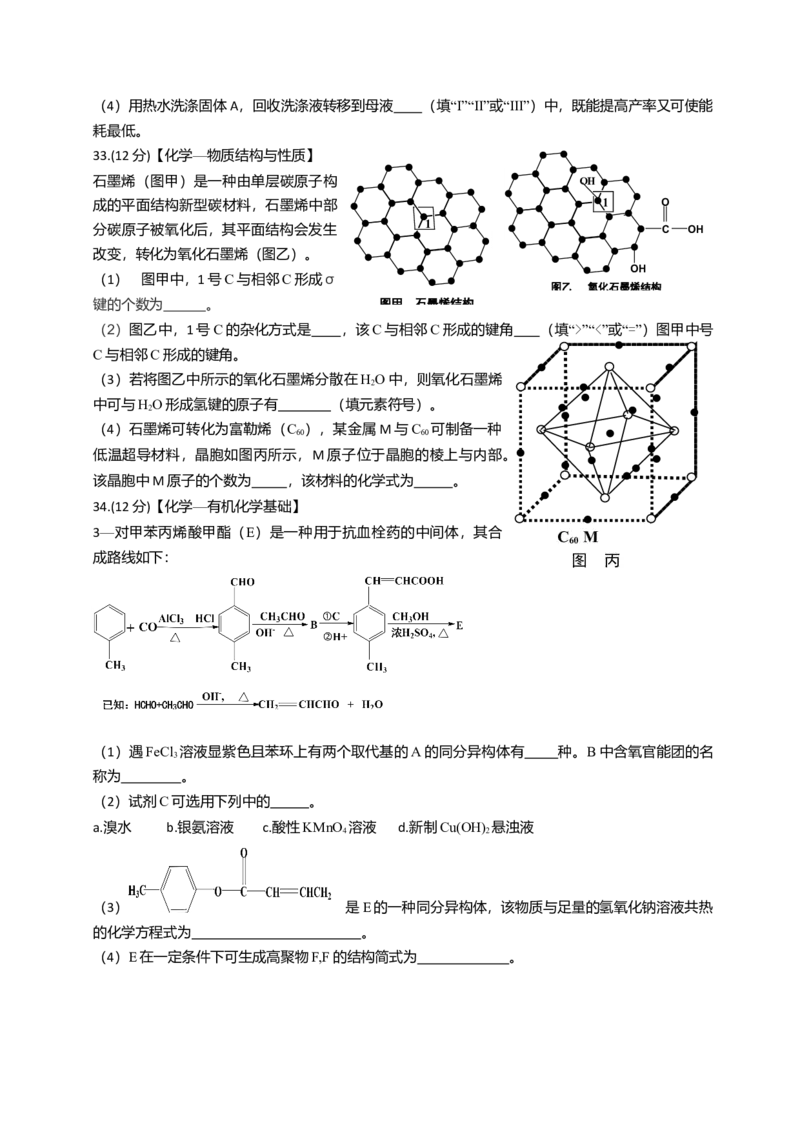
32.(12分)【化学—化学与技术】
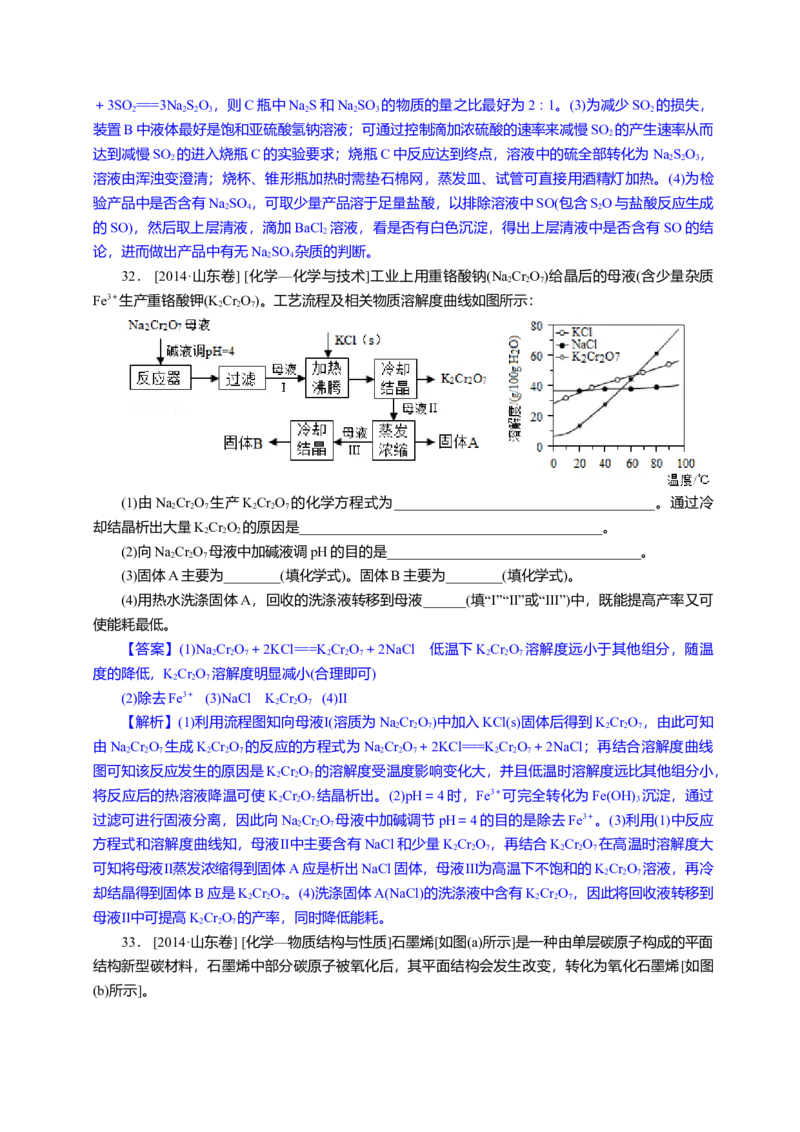
工业上用重铬酸钠(NaCr O)结晶后的母液(含少量的Fe3+)生产重铬酸钾(KCr O)。工业流程
2 2 7 2 2 7
及相关物质溶解度曲线如图:
Na 2 Cr 2 O 7 母液 KCl(s)
碱液调pH=4
溶
解
度
反应器 过滤 母液I 加热 冷却 K 2 Cr 2 O 7
沸腾 结晶
母液II
冷却 母液III 蒸发 固体A
固体B 结晶 浓缩
(1)由NaCr O 生产KCr O 的化学方程式为: ;通过冷却大量析出
2 2 7 2 2 7
KCr O 的原因是: 。
2 2 7
(2)向NaCr O 母液中加碱液调pH的目的是 。
2 2 7
(3)固体A主要为 (填化学式)。固体B主要为 (填化学式)。
(g/100gH2o)(4)用热水洗涤固体A,回收洗涤液转移到母液 (填“Ⅰ”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能
耗最低。
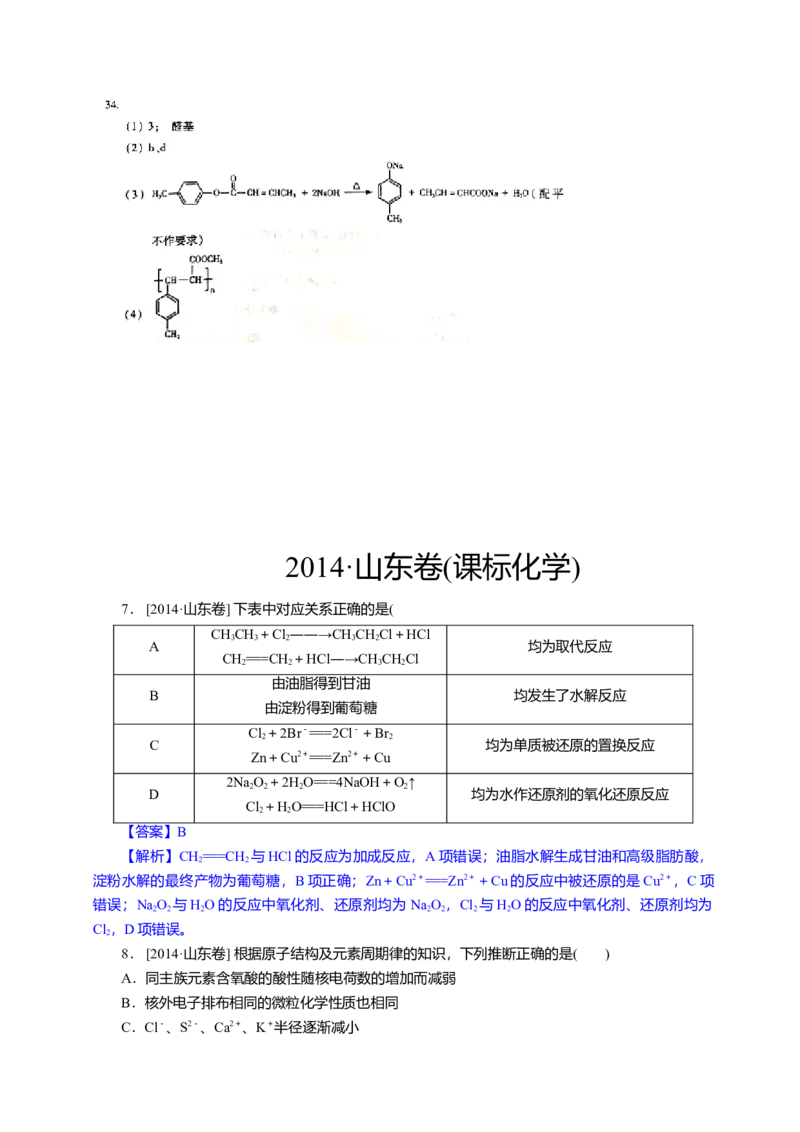
33.(12分)【化学—物质结构与性质】
石墨烯(图甲)是一种由单层碳原子构 OH
成的平面结构新型碳材料,石墨烯中部 1 O
1
分碳原子被氧化后,其平面结构会发生 C OH
改变,转化为氧化石墨烯(图乙)。
OH
(1) 图甲中,1号C与相邻C形成σ
图乙 氧化石墨烯结构
键的个数为 。 图甲 石墨烯结构
(2)图乙中,1号C的杂化方式是 ,该C与相邻C形成的键角 (填“>”“<”或“=”)图甲中号
C与相邻C形成的键角。
(3)若将图乙中所示的氧化石墨烯分散在HO中,则氧化石墨烯
2
中可与HO形成氢键的原子有 (填元素符号)。
2
(4)石墨烯可转化为富勒烯(C ),某金属M与C 可制备一种
60 60
低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。
该晶胞中M原子的个数为 ,该材料的化学式为 。
34.(12分)【化学—有机化学基础】
3—对甲苯丙烯酸甲酯(E)是一种用于抗血栓药的中间体,其合 C M
60
成路线如下: 图 丙
(1)遇FeCl 溶液显紫色且苯环上有两个取代基的A的同分异构体有 种。B中含氧官能团的名
3
称为 。
(2)试剂C可选用下列中的 。
a.溴水 b.银氨溶液 c.酸性KMnO 溶液 d.新制Cu(OH) 悬浊液
4 2
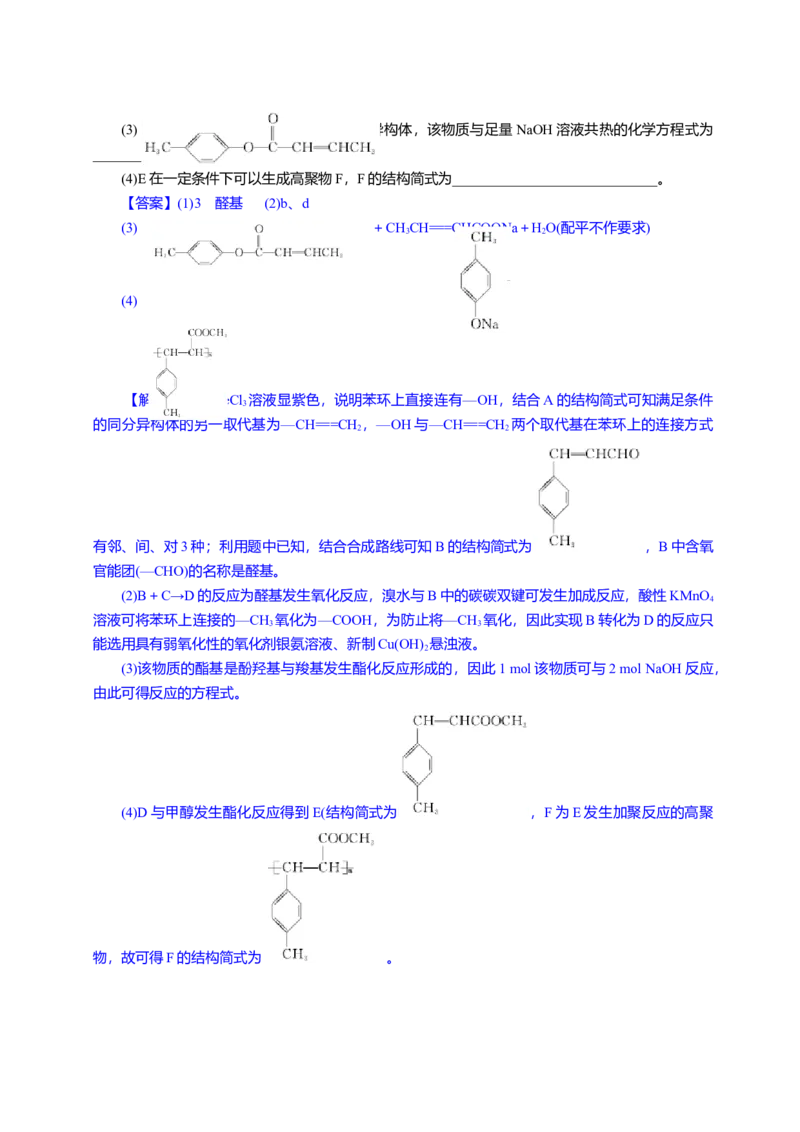
(3) 是E的一种同分异构体,该物质与足量的氢氧化钠溶液共热
的化学方程式为 。
(4)E在一定条件下可生成高聚物F,F的结构简式为 。2014·山东卷(课标化学)
7. [2014·山东卷] 下表中对应关系正确的是(
CHCH+Cl――→CHCHCl+HCl
3 3 2 3 2
A 均为取代反应
CH===CH +HCl―→CHCHCl
2 2 3 2
由油脂得到甘油
B 均发生了水解反应
由淀粉得到葡萄糖
Cl+2Br-===2Cl-+Br
2 2
C 均为单质被还原的置换反应
Zn+Cu2+===Zn2++Cu
2NaO+2HO===4NaOH+O↑
2 2 2 2
D 均为水作还原剂的氧化还原反应
Cl+HO===HCl+HClO
2 2
【答案】B
【解析】CH===CH 与HCl的反应为加成反应,A项错误;油脂水解生成甘油和高级脂肪酸,
2 2
淀粉水解的最终产物为葡萄糖,B项正确;Zn+Cu2+===Zn2++Cu的反应中被还原的是Cu2+,C项
错误;NaO 与HO的反应中氧化剂、还原剂均为 NaO ,Cl 与HO的反应中氧化剂、还原剂均为
2 2 2 2 2 2 2
Cl,D项错误。
2
8. [2014·山东卷] 根据原子结构及元素周期律的知识,下列推断正确的是( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小D. Cl与Cl得电子能力相同
【答案】D
【解析】同主族元素最高价含氧酸的酸性随核电荷数的增加而减弱,A项错误;如Na+、Mg2+
是核外电子排布相同的微粒,二者性质不同,B项错误;核外电子排布相同的简单离子,核电荷数越
大离子半径越小,S2-、Cl-、K+、Ca2+半径逐渐减小,C项错误;Cl与Cl互为同位素,二者化学性
质(得电子能力、化合价等)相同,D项正确。
9. [2014·山东卷] 等质量的下列物质与足量稀硝酸反应,放出 NO物质的量最多的是( )
A.FeO B.Fe O C. FeSO D.Fe O
2 3 4 3 4
【答案】A
【解析】Fe O 与稀硝酸反应不能放出NO,B项错误;1 mol Fe O 中含有1 mol Fe2+,利用得失
2 3 3 4
电子守恒可知生成1 mol NO需消耗FeO、FeSO 、Fe O 的物质的量均为3 mol,FeO、FeSO 、Fe O
4 3 4 4 3 4
的摩尔质量(g/mol)分别为:72、152、232,所以等质量的FeO、FeSO 、Fe O 与足量稀硝酸反应,放
4 3 4
出NO物质的量最多的是FeO。
10. [2014·山东卷] 下列实验操作或装置(略去部分夹持仪器)正确的是( )
A.配制溶液 B.中和滴定 C.制备乙酸乙酯 D.制备收集干燥的氨气
【答案】C
【解析】配制溶液定容时使用胶头滴管,A项错误;中和NaOH待测液需要标准酸溶液,图中盛
酸溶液使用的是碱式滴定管,B项错误;C项正确;收集氨气的导气管应插入试管底部,D项错误。
11. [2014·山东卷] 苹果酸的结构简式为 ,下列说法正确的是(
)
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成1 mol H
2
D. 与苹果酸互为同分异构体
【答案】A
【解析】苹果酸中官能团—OH、—COOH均可发生酯化反应,A项正确;苹果酸中的醇羟基不
能与NaOH反应,只有—COOH可与NaOH反应,1 mol苹果酸可与2 mol NaOH发生中和反应,B项
错误;苹果酸中—OH、—COOH均可与Na发生置换反应,1 mol苹果酸与足量Na反应可生成1.5mol H,C项错误; 与苹果酸是同种物质,D项错误。
2
12. [2014·山东卷] 下列有关溶液组成的描述合理的是( )
A.无色溶液中可能大量存在Al3+、NH、Cl-、S2-
B.酸性溶液中可能大量存在Na+、ClO-、SO、I-
C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO
【答案】C
【解析】Al3+、S2-发生水解互促反应不能大量共存,A项错误;酸性溶液中不能大量存在 ClO
-,B项错误;HCO水解使溶液呈弱碱性,因此弱碱性溶液中可大量存在 Na+、K+、Cl-、HCO,C
项正确;中性溶液中不能大量存在Fe3+,D项错误。
13.H1 H3[2014·山东卷] 已知某温度下CHCOOH和NH ·H O的电离常数相等,现向10 mL浓
3 3 2
度为0.1 mol·L-1的CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B.先增大再减小
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
【答案】D
【解析】水的电离程度先增大,当反应完全后,随氨水的加入,水的电离程度减小,A项错误;
溶液中=,滴定过程中K (NH ·H O)不变,溶液中c(OH-)一直增大,一直减小,B项错误;利用原子
b 3 2
守恒知溶液中n(CHCOOH)与n(CHCOO-)之和不变,滴定过程中溶液体积不断增大,c(CHCOOH)
3 3 3
与 c(CHCOO-)之和不断减小,C 项错误;由 CHCOOH 与 NH ·H O 的电离程度相等可知
3 3 3 2
CHCOONH 溶液呈中性,当加入等体积氨水时,溶液恰好为 CHCOONH 溶液,利用电荷守恒知溶
3 4 3 4
液中c(NH)=c(CHCOO-),D项正确。
3
29. [2014·山东卷] 研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO (g)+NaCl(s) NaNO (s)+ClNO(g) K ΔH<0(Ⅰ)
2 3 1 1
2NO(g)+Cl(g) 2ClNO(g) K ΔH<0(Ⅱ)
2 2 2
(1)4NO (g)+2NaCl(s) 2NaNO (s)+2NO(g)+Cl(g)的平衡常数K=________(用K 、K 表示)。
2 3 2 1 2
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和
0.1 mol Cl ,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,则平衡后
2
n(Cl )=________mol,NO的转化率α=________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,
2 1
平衡时NO的转化率α ________α (填“>”“<”或“=”),平衡常数K ______(填“增大”“减小”或“不变”)。
2 1 2
若要使K 减小,可采取的措施是________。
2
(3)实验室可用NaOH溶液吸收NO ,反应为2NO +2NaOH===NaNO +NaNO +HO。含0.2
2 2 3 2 2
mol NaOH的水溶液与0.2 mol NO 恰好完全反应得1 L溶液A,溶液B为0.1 mol·L-1的CHCOONa
2 3
溶 液 , 则 两 溶 液 中 c(NO) 、 c(NO) 和 c(CHCOO - ) 由 大 到 小 的 顺 序 为
3
____________________________________________。(已知 HNO 电离常数 K =7.1×10-4 mol·L-1,
2 a
CHCOOH的电离常数K=1.7×10-5 mol·L-1)
3 a可使溶液A和溶液B的pH相等的方法是________。
a.向溶液A中加适量水
b.向溶液A中加适量NaOH
c.向溶液B中加适量水
d.向溶液B中加适量NaOH
【答案】(1) (2)2.5×10-2 75% > 不变 升高温度 (3)c(NO)>c(NO)>c(CHCOO-) b、c
3
【解析】(1)反应(Ⅰ)×2-反应(Ⅱ)即得到反应:4NO (g)+2NaCl(s)2NaNO(s)+2NO(g)+
2 3
Cl(g),利用平衡常数定义可知该反应平衡常数 K=。(2)平衡时容器中n(ClNO)=7.5×10-3mol·L-
2
1·min-1×10 min×2 L=0.15 mol,则平衡后n(Cl )=0.1 mol-×0.15 mol=0.025 mol;NO的转化率=
2
×100%=75%;若恒压下达到平衡态相当于将原平衡加压,平衡正向移动,NO的转化率增大;平衡
常数只与温度有关,恒压下达到平衡的平衡常数与原平衡常数相等;因该反应为放热反应,升高温度,
反应逆向进行,反应平衡常数减小 。(3)反应后得到溶液A为物质的量浓度均为0.1 mol/L的NaNO
2
与NaNO 的混合溶液,利用已知电离常数可知CHCOO-水解程度大于NO,NO不发生水解,两溶
3 3
液中c(NO)>c(NO)>c(CHCOO-);利用CHCOO-水解程度大于NO可知溶液B的碱性强于溶液
3 3
A,为使溶液A、B的pH相等,可采取的措施有向溶液A中加适量NaOH或向B溶液中加入适量水
稀释或向B溶液中加入适量稀醋酸等。
30. [2014·山东卷] 离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al Cl和AlCl组
2
成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品接电源的________极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,
阴极电极反应式为__________________________________________。若改用AlCl 水溶液作电解液,
3
则阴极产物为________。
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还
原产物的物质的量为________mol。
(3)用铝粉和Fe O 做铝热反应实验,需要的试剂还有________。
2 3
a.KCl b.KClO c.MnO d.Mg
3 2
取少量铝热反应所得的固体混合物,将其溶于足量稀HSO ,滴加KSCN溶液无明显现象,
2 4
______________(填“能”或“ 不能”)说明固体混合物中无Fe O,理由是________(用离子方程式说明)。
2 3
【答案】(1)负 4Al Cl+3e-===Al+7AlCl H (2)3
2 2
(3)b、d 不能 Fe O+6H+===2Fe3++3HO、Fe+2Fe3+===3Fe2+(或只写Fe+2Fe3+===3Fe2+)
2 3 2
【解析】(1)电镀时,镀件应连接电源负极,作阴极;在阴极上发生还原反应,结合题中“电镀过
程中不产生其他离子且有机阳离子不参与电极反应”可知阴极上的反应式是 4Al Cl+3e-===Al+
2
7AlCl;若改用AlCl 水溶液作电解液,则阴极反应是水电离出的H+得电子还原为H。(2)用NaOH溶
3 2
解铝镀层时发生反应:2Al+2NaOH+2HO===2NaAlO+3H↑,H 是还原产物,当转移6 mol电子时,
2 2 2 2
该反应可得到3 mol还原产物。(3)引发铝粉和Fe O 粉末反应的助燃剂为KClO ,然后插入镁条,点
2 3 3
燃镁条即可使铝热反应发生;混合物中即使含有Fe O ,Fe O 溶于酸后生成的Fe3+与反应生成的Fe
2 3 2 3
发生氧化还原反应生成Fe2+,再加入KSCN溶液后溶液也不显红色,因此不能证明反应后固体不含
Fe O。
2 3
31. (20分)[2014·山东卷] 工业上常利用含硫废水生产NaSO·5H O,实验室可用如下装置(略去
2 2 3 2部分夹持仪器)模拟生产过程。
烧瓶C中发生反应如下:
NaS(aq)+HO(l)+SO (g)===Na SO (aq)+HS(aq) (Ⅰ)
2 2 2 2 3 2
2HS(aq)+SO (g)===3S(s)+2HO(l) (Ⅱ)
2 2 2
S(s)+NaSO (aq)=====NaSO(aq) (Ⅲ)
2 3 2 2 3
(1)仪器组装完成后,关闭两端活塞,向装置 B中的长颈漏斗内注入液体至形成一段液柱,若
________________,则整个装置气密性良好。装置D的作用是__________。装置E中为________溶
液。
(2)为提高产品纯度,应使烧瓶C中NaS和NaSO 恰好完全反应,则烧瓶C中NaS和NaSO 物
2 2 3 2 2 3
质的量之比为________。
(3)装置B的作用之一是观察SO 的生成速率,其中的液体最好选择________。
2
a.蒸馏水 b.饱和NaSO 溶液
2 3
c.饱和NaHSO 溶液 d.饱和NaHCO 溶液
3 3
实验中,为使SO 缓慢进入烧瓶C,采用的操作是__________________________。已知反应(Ⅲ)
2
相对较慢,则烧瓶C中反应达到终点的现象是__________________。反应后期可用酒精灯适当加热
烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有________。
a.烧杯 b.蒸发皿
c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出NaSO·5H O,其中可能含有
2 2 3 2
NaSO 、NaSO 等杂质。利用所给试剂设计实验,检测产品中是否存在 NaSO ,简要说明实验操作、
2 3 2 4 2 4
现象和结论:________________________________________。
已知NaSO·5H O遇酸易分解:SO+2H+===S↓+SO ↑+HO
2 2 3 2 2 2 2
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl 溶液、AgNO 溶液。
2 3
【答案】(1)液柱高度保持不变 防止倒吸 NaOH(合理答案均可)(2)2∶1
(3)c 控制滴加硫酸的速度(合理即可得分) 溶液变澄清(或浑浊消失) a、d
(4)取少量产品溶于足量稀盐酸,静置,取上层溶液(或过滤、取滤液),滴加BaCl 溶液,若出现
2
沉淀则说明含有NaSO 杂质(合理答案均可)
2 4
【解析】(1)若装置气密性良好,则装置B中的长颈漏斗加入水,B瓶内压强变大,在长颈漏斗
的颈中会形成一段液柱,且液柱高度保持不变;根据装置图可知装置D是安全瓶,可防止E中液体
倒吸进入C中;装置E是用来吸收未反应完全的HS或SO 的尾气处理装置,因此E中试剂需用碱溶
2 2
液,如NaOH溶液。(2) 反应(Ⅰ)×2+反应(Ⅱ)+ 反应(Ⅲ)×3可得该转化过程的总反应:2NaS+NaSO
2 2 3+3SO ===3Na SO ,则C瓶中NaS和NaSO 的物质的量之比最好为2∶1。(3)为减少SO 的损失,
2 2 2 3 2 2 3 2
装置B中液体最好是饱和亚硫酸氢钠溶液;可通过控制滴加浓硫酸的速率来减慢SO 的产生速率从而
2
达到减慢SO 的进入烧瓶C的实验要求;烧瓶C中反应达到终点,溶液中的硫全部转化为NaSO ,
2 2 2 3
溶液由浑浊变澄清;烧杯、锥形瓶加热时需垫石棉网,蒸发皿、试管可直接用酒精灯加热。(4)为检
验产品中是否含有NaSO ,可取少量产品溶于足量盐酸,以排除溶液中SO(包含SO与盐酸反应生成
2 4 2
的SO),然后取上层清液,滴加BaCl 溶液,看是否有白色沉淀,得出上层清液中是否含有 SO的结
2
论,进而做出产品中有无NaSO 杂质的判断。
2 4
32. [2014·山东卷] [化学—化学与技术]工业上用重铬酸钠(Na Cr O)给晶后的母液(含少量杂质
2 2 7
Fe3+生产重铬酸钾(K Cr O)。工艺流程及相关物质溶解度曲线如图所示:
2 2 7
(1)由NaCr O 生产KCr O 的化学方程式为_____________________________________。通过冷
2 2 7 2 2 7
却结晶析出大量KCr O 的原因是___________________________________________。
2 2 2
(2)向NaCr O 母液中加碱液调pH的目的是____________________________________。
2 2 7
(3)固体A主要为________(填化学式)。固体B主要为________(填化学式)。
(4)用热水洗涤固体A,回收的洗涤液转移到母液______(填“Ⅰ”“Ⅱ”或“Ⅲ”)中,既能提高产率又可
使能耗最低。
【答案】(1)Na Cr O +2KCl===K Cr O +2NaCl 低温下KCr O 溶解度远小于其他组分,随温
2 2 7 2 2 7 2 2 7
度的降低,KCr O 溶解度明显减小(合理即可)
2 2 7
(2)除去Fe3+ (3)NaCl KCr O (4)Ⅱ
2 2 7
【解析】(1)利用流程图知向母液Ⅰ(溶质为NaCr O)中加入KCl(s)固体后得到KCr O ,由此可知
2 2 7 2 2 7
由NaCr O 生成KCr O 的反应的方程式为NaCr O +2KCl===K Cr O +2NaCl;再结合溶解度曲线
2 2 7 2 2 7 2 2 7 2 2 7
图可知该反应发生的原因是KCr O 的溶解度受温度影响变化大,并且低温时溶解度远比其他组分小,
2 2 7
将反应后的热溶液降温可使KCr O 结晶析出。(2)pH=4时,Fe3+可完全转化为Fe(OH) 沉淀,通过
2 2 7 3
过滤可进行固液分离,因此向NaCr O 母液中加碱调节pH=4的目的是除去Fe3+。(3)利用(1)中反应
2 2 7
方程式和溶解度曲线知,母液Ⅱ中主要含有NaCl和少量KCr O ,再结合KCr O 在高温时溶解度大
2 2 7 2 2 7
可知将母液Ⅱ蒸发浓缩得到固体A应是析出NaCl固体,母液Ⅲ为高温下不饱和的KCr O 溶液,再冷
2 2 7
却结晶得到固体B应是KCr O。(4)洗涤固体A(NaCl)的洗涤液中含有KCr O,因此将回收液转移到
2 2 7 2 2 7
母液Ⅱ中可提高KCr O 的产率,同时降低能耗。
2 2 7
33. [2014·山东卷] [化学—物质结构与性质]石墨烯[如图(a)所示]是一种由单层碳原子构成的平面
结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图
(b)所示]。(a)石墨烯结构 (b)氧化石墨烯结构
(1)图(a)中,1号C与相邻C形成σ键的个数为________。
(2)图(b)中,1号C的杂化方式是________,该C与相邻C形成的键角________(填“>”“<”或“=”)
图(a)中1号C与相邻C形成的键角。
(3)若将图(b)所示的氧化石墨烯分散在HO中,则氧化石墨烯中可与HO形成氢键的原子有
2 2
________(填元素符号)。
(4)石墨烯可转化为富勒烯(C ),某金属M与C 可制备一种低温超导材料,晶胞如图所示,M原
60 60
子位于晶胞的棱上与内部。该晶胞中M原子的个数为________,该材料的化学式为________。
【答案】(1)3 (2)sp3 < (3)O、H (4)12 MC
3 60
【解析】(1)由图(a)可知,1号C与另外3个碳原子形成3个σ键。(2)图(b)中1号C与3个碳原子、
1个氧原子共形成4个σ键,其价层电子对数为4,C的杂化方式为sp3;该C与相邻C的键角约为
109°28′,图(a)中1号C采取sp2杂化,碳原子间夹角为120°。(3)氧化石墨烯中“—OH”的O可与HO
2
中的H形成氢键、氧化石墨烯中“—OH”的H可与HO中的O形成氢键,氧化石墨烯中可与HO形成
2 2
氢键的原子有O、H。(4)利用“均摊法”可知该晶胞棱上12个M完全属于该晶胞的M为12×=3,位于
晶胞内的9个M完全属于该晶胞,故该晶胞中M原子的个数为12;该晶胞中含有C 的个数为8×+
60
6×=4,因此该晶胞的化学式为MC 。
3 60
34. [2014·山东卷] [化学—有机化学基础]3对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间
体,其合成路线如下:
已知:HCHO+CHCHO――→CH===CHCHO+HO
3 2 2
(1)遇FeCl 溶液显紫色且苯环上有两个取代基的A的同分异构体有____________种,B中含氧官
3
能团的名称为________。
(2)试剂C可选用下列中的________。
a.溴水 b.银氨溶液
c.酸性KMnO 溶液 d.新制Cu(OH) 悬浊液
4 2(3) 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
____________________。
(4)E在一定条件下可以生成高聚物F,F的结构简式为_____________________________。
【答案】(1)3 醛基 (2)b、d
(3) +2NaOH――→ +CHCH===CHCOONa+HO(配平不作要求)
3 2
(4)
【解析】(1)遇FeCl 溶液显紫色,说明苯环上直接连有—OH,结合A的结构简式可知满足条件
3
的同分异构体的另一取代基为—CH===CH ,—OH与—CH===CH 两个取代基在苯环上的连接方式
2 2
有邻、间、对3种;利用题中已知,结合合成路线可知B的结构简式为 ,B中含氧
官能团(—CHO)的名称是醛基。
(2)B+C→D的反应为醛基发生氧化反应,溴水与B中的碳碳双键可发生加成反应,酸性KMnO
4
溶液可将苯环上连接的—CH 氧化为—COOH,为防止将—CH 氧化,因此实现B转化为D的反应只
3 3
能选用具有弱氧化性的氧化剂银氨溶液、新制Cu(OH) 悬浊液。
2
(3)该物质的酯基是酚羟基与羧基发生酯化反应形成的,因此1 mol该物质可与2 mol NaOH反应,
由此可得反应的方程式。
(4)D与甲醇发生酯化反应得到E(结构简式为 ,F为E发生加聚反应的高聚
物,故可得F的结构简式为 。