文档内容
2015 年全国统一高考化学试卷(新课标Ⅱ)
一、选择题(共 7小题,每小题 6分,满分 42分)
1.(6分)食品干燥剂应无毒、无味、无腐蚀性及环境友好.下列说法错误的是( )
A.硅胶可用作食品干燥剂
B.P O 不可用作食品干燥剂
2 5
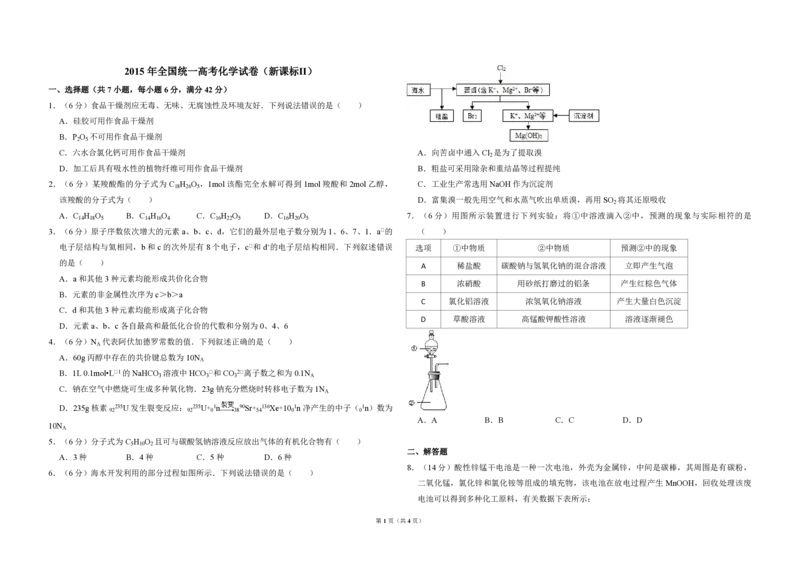
C.六水合氯化钙可用作食品干燥剂 A.向苦卤中通入Cl 是为了提取溴
2
D.加工后具有吸水性的植物纤维可用作食品干燥剂 B.粗盐可采用除杂和重结晶等过程提纯
2.(6 分)某羧酸酯的分子式为 C H O ,1mol该酯完全水解可得到 1mol羧酸和 2mol乙醇, C.工业生产常选用NaOH 作为沉淀剂
18 26 5
该羧酸的分子式为( ) D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
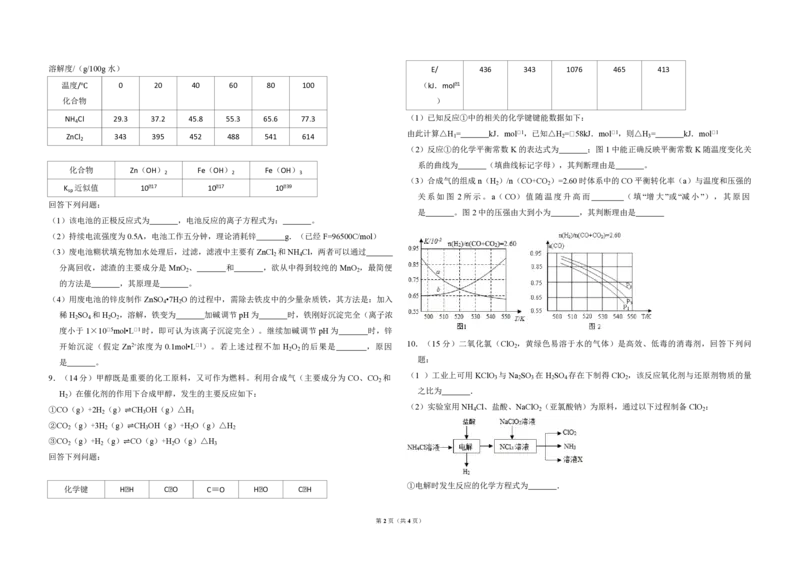
A.C H O B.C H O C.C H O D.C H O 7.(6分)用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
14 18 5 14 16 4 16 22 5 16 20 5
3.(6 分)原子序数依次增大的元素 a、b、c、d,它们的最外层电子数分别为 1、6、7、1.a﹣的 ( )
电子层结构与氦相同,b和 c的次外层有 8个电子,c﹣和 d+的电子层结构相同.下列叙述错误 选项 ①中物质 ②中物质 预测②中的现象
的是( )
A 稀盐酸 碳酸钠与氢氧化钠的混合溶液 立即产生气泡
A.a和其他3种元素均能形成共价化合物
B 浓硝酸 用砂纸打磨过的铝条 产生红棕色气体
B.元素的非金属性次序为c>b>a
C 氯化铝溶液 浓氢氧化钠溶液 产生大量白色沉淀
C.d和其他3种元素均能形成离子化合物
D 草酸溶液 高锰酸钾酸性溶液 溶液逐渐褪色
D.元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
4.(6分)N 代表阿伏加德罗常数的值.下列叙述正确的是( )
A
A.60g丙醇中存在的共价键总数为10N
A
B.1L 0.1mol•L﹣1的NaHCO 溶液中HCO ﹣和CO 2﹣离子数之和为0.1N
3 3 3 A
C.钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1N
A
D.235g核素 235U 发生裂变反应: 235U+ 1n 90Sr+ 136Xe+10 1n净产生的中子( 1n)数为
92 92 0 38 54 0 0
A.A B.B C.C D.D
10N
A
5.(6分)分子式为C H O 且可与碳酸氢钠溶液反应放出气体的有机化合物有( )
5 10 2
二、解答题
A.3种 B.4 种 C.5种 D.6种
8.(14分)酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,
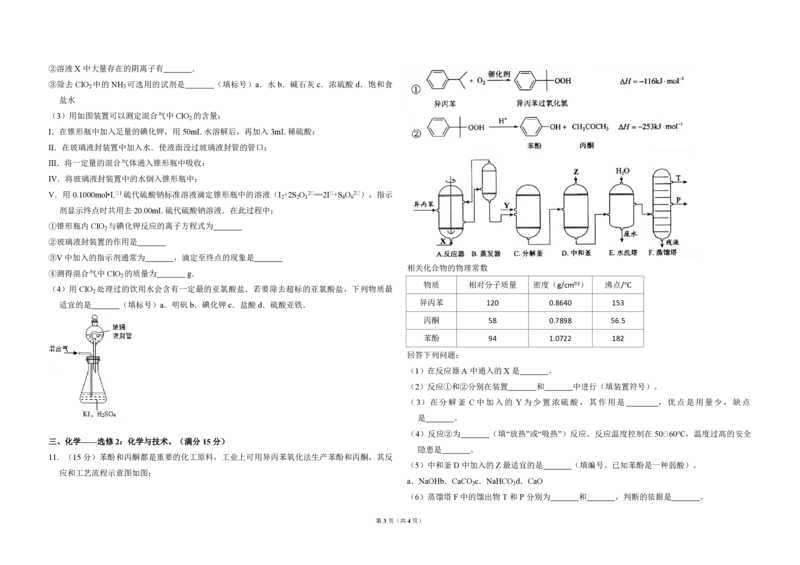
6.(6分)海水开发利用的部分过程如图所示.下列说法错误的是( )
二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生 MnOOH,回收处理该废
电池可以得到多种化工原料,有关数据下表所示:
第1页(共4页)溶解度/(g/100g水) E/ 436 343 1076 465 413
温度/℃ 0 20 40 60 80 100 (kJ.mol﹣1
化合物 )
NH Cl 29.3 37.2 45.8 55.3 65.6 77.3 (1)已知反应①中的相关的化学键键能数据如下:
4
由此计算△H = kJ.mol﹣1,已知△H =﹣58kJ.mol﹣1,则△H = kJ.mol﹣1
ZnCl 343 395 452 488 541 614 1 2 3
2
(2)反应①的化学平衡常数 K 的表达式为 ;图 1中能正确反映平衡常数 K 随温度变化关
系的曲线为 (填曲线标记字母),其判断理由是 。
化合物 Zn(OH) Fe(OH) Fe(OH)
2 2 3
(3)合成气的组成 n(H )/n(CO+CO )=2.60时体系中的 CO 平衡转化率(a)与温度和压强的
2 2
K 近似值 10﹣17 10﹣17 10﹣39
sp
关系如图 2所示。a(CO)值随温度升高而 (填“增大”或“减小”),其原因
回答下列问题:
是 。图2中的压强由大到小为 ,其判断理由是
(1)该电池的正极反应式为 ,电池反应的离子方程式为: 。
(2)持续电流强度为0.5A,电池工作五分钟,理论消耗锌 g.(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有 ZnCl 和 NH Cl,两者可以通过
2 4
分离回收,滤渣的主要成分是 MnO 、 和 ,欲从中得到较纯的 MnO ,最简便
2 2
的方法是 ,其原理是 。
(4)用废电池的锌皮制作 ZnSO •7H O 的过程中,需除去铁皮中的少量杂质铁,其方法是:加入
4 2
稀 H SO 和 H O ,溶解,铁变为 加碱调节 pH 为 时,铁刚好沉淀完全(离子浓
2 4 2 2
度小于 1×10﹣5mol•L﹣1时,即可认为该离子沉淀完全)。继续加碱调节 pH 为 时,锌
10.(15分)二氧化氯(ClO ,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问
开始沉淀(假定 Zn2+浓度为 0.1mol•L﹣1)。若上述过程不加 H O 的后果是 ,原因 2
2 2
是 。
題:
(1 )工业上可用 KClO 与 Na SO 在 H SO 存在下制得 ClO ,该反应氧化剂与还原剂物质的量
9.(14 分)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为 CO、CO 和 3 2 3 2 4 2
2
H )在催化剂的作用下合成甲醇,发生的主要反应如下:
之比为 .
2
①CO(g)+2H (g)⇌CH OH(g)△H
(2)实验室用NH
4
Cl、盐酸、NaClO
2
(亚氯酸钠)为原料,通过以下过程制备ClO
2
:
2 3 1
②CO (g)+3H (g)⇌CH OH(g)+H O(g)△H
2 2 3 2 2
③CO (g)+H (g)⇌CO(g)+H O(g)△H
2 2 2 3
回答下列问题:
①电解时发生反应的化学方程式为 .
化学键 H﹣H C﹣O C≡O H﹣O C﹣H
第2页(共4页)②溶液X 中大量存在的阴离子有 .
③除去 ClO 中的 NH 可选用的试剂是 (填标号)a.水 b.碱石灰 c.浓硫酸 d.饱和食
2 3
盐水
(3)用如图装置可以测定混合气中ClO 的含量:
2
Ⅰ.在锥形瓶中加入足量的碘化钾,用 50mL水溶解后,再加入3mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水.使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用 0.1000mol•L﹣1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I +2S O 2﹣═2I﹣+S O 2﹣),指示
2 2 3 4 6
剂显示终点时共用去20.00mL硫代硫酸钠溶液.在此过程中:
①锥形瓶内ClO 与碘化钾反应的离子方程式为
2
②玻璃液封装置的作用是
③V 中加入的指示剂通常为 ,滴定至终点的现象是
相关化合物的物理常数
④测得混合气中ClO 的质量为 g.
2
物质 相对分子质量 密度(g/cm﹣3) 沸点/℃
(4)用 ClO 处理过的饮用水会含有一定最的亚氯酸盐.若要除去超标的亚氯酸盐,下列物质最
2
适宜的是 (填标号)a.明矾b.碘化钾c.盐酸d.硫酸亚铁. 异丙苯 120 0.8640 153
丙酮 58 0.7898 56.5
苯酚 94 1.0722 182
回答下列问题:
(1)在反应器A 中通入的X 是 。
(2)反应①和②分别在装置 和 中进行(填装置符号)。
(3)在分解釜 C中加入的 Y 为少置浓硫酸,其作用是 ,优点是用量少,缺点
是 。
(4)反应②为 (填“放热”或“吸热”)反应。反应温度控制在 50﹣60℃,温度过高的安全
三、化学——选修 2:化学与技术。(满分 15分)
隐患是 。
11.(15分)苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反
(5)中和釜D 中加入的Z最适宜的是 (填编号。已知苯酚是一种弱酸)。
应和工艺流程示意图如图:
a.NaOHb.CaCO c.NaHCO d.CaO
3 3
(6)蒸馏塔F 中的馏出物T和P 分别为 和 ,判断的依据是 。
第3页(共4页)(7)用该方法合成苯酚和丙酮的优点是 。
四、化学-选修 3:物质结构与性质。(满分 15分)
12.(15分)A、B、C、D 为原子序数依次增大的四种元素,A2﹣和 B+具有相同的电子构型;
C、D 为同周期元素,C核外电子总数是最外层电子数的 3倍;D 元素最外层有一个未成对电 已知:
子.回答下列问题: ①烃A 的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢
(1)四种元素中电负性最大的是 (填元素符号),其中 C原子的核外电子排布式 ②化合物B 为单氯代烃:化合物C的分子式为C H
5 8
为 . ③E、F 为相对分子质量差14的同系物,F 是福尔马林的溶质
(2)单质 A 有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;A 和
B的氢化物所属的晶体类型分别为 和 . ④
(3)C和 D 反应可生成组成比为 1:3的化合物 E,E的立体构型为 ,中心原子的杂化轨 冋答下列问题:
道类型为 . (1)A 的结构简式为 .
(4)化合物 D A 的立体构型为 ,中心原子的价层电子对数为 ,单质 D 与湿润的 (2)由B 生成C 的化学方程式为 .
2
Na CO 反应可制备D A,其化学方程式为 . (3)由E和F 生成G 的反应类型为 ,G 的化学名称为 .
2 3 2
(5)A 和 B能够形成化合物 F,其晶胞结构如图所示,晶胞边长 a=0.566nm,F 的化学式 (4)①由D 和H 生成PPG 的化学方程式为:
为 ;晶胞中 A 原子的配位数为 ;列式计算晶体 F 的密度(g•cm﹣3 ) ②若PPG 平均相对分子质量为 10000,则其平均聚合度约为 (填标号).
(保留小数点后两位数字). a. 48b. 58c. 76 d.122
(5)D 的同分异构体中能同时满足下列条件的共有 种(不含立体异构):
①能与饱和NaHCO 溶液反应产生气体②既能发生银镜反应,又能发生水解反应
3
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 (写结构简式)
D 的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是
(填标号).
五、化学一选修 5:有机化学基础(满分 15分) a.质谱仪 b.红外光谱仪 c.元素分析仪d.核磁共振仪.
13.(15分)聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容
性方面有很好的应用前景. PPG 的一种合成路线如下:
第4页(共4页)