文档内容
2012 山西省高中阶段教育学校招生统一考试
理科综合(化学部分)
第Ⅰ卷 选择题(共50分)
可能用到的相对原子质量:H-1,C-12,O-16,Cl-35.5,Ca-40
一、选择题(在每小题给出的四个选项中,只有一项符合题目要求,请选出并在答题卡上
将该选项涂黑,每小题2分)
1.下列变化中属于化学变化的是( )
A.黄瓜切成段 B.布料裁成衣 C.葡萄酿成酒 D.钢锭轧成板
2.下列物质属于混合物的是( )
A.海水 B.干冰 C.液氧 D.冰水
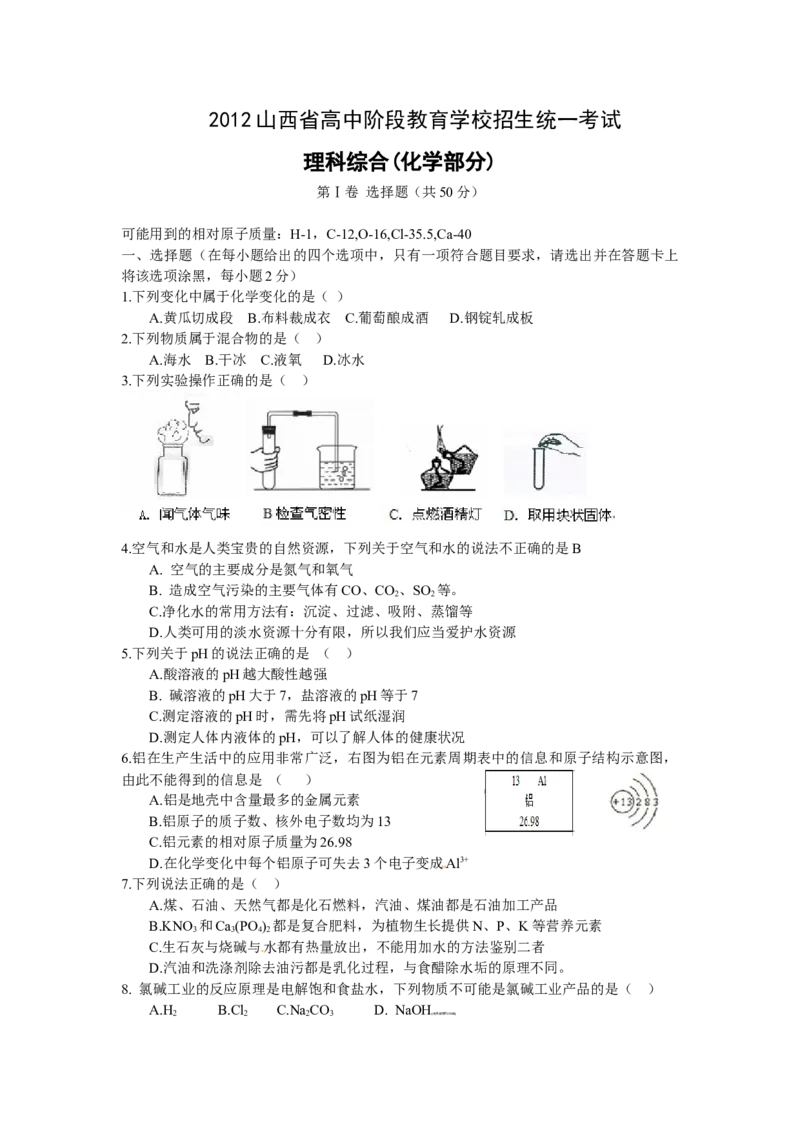
3.下列实验操作正确的是( )
4.空气和水是人类宝贵的自然资源,下列关于空气和水的说法不正确的是B
A. 空气的主要成分是氮气和氧气
B. 造成空气污染的主要气体有CO、CO、SO 等。
2 2
C.净化水的常用方法有:沉淀、过滤、吸附、蒸馏等
D.人类可用的淡水资源十分有限,所以我们应当爱护水资源
5.下列关于pH的说法正确的是 ( )
A.酸溶液的pH越大酸性越强
B. 碱溶液的pH大于7,盐溶液的pH等于7
C.测定溶液的pH时,需先将pH试纸湿润
D.测定人体内液体的pH,可以了解人体的健康状况
6.铝在生产生活中的应用非常广泛,右图为铝在元素周期表中的信息和原子结构示意图,
由此不能得到的信息是 ( )
A.铝是地壳中含量最多的金属元素
B.铝原子的质子数、核外电子数均为13
C.铝元素的相对原子质量为26.98
D.在化学变化中每个铝原子可失去3个电子变成Al3+
7.下列说法正确的是( )
A.煤、石油、天然气都是化石燃料,汽油、煤油都是石油加工产品
B.KNO 和Ca (PO ) 都是复合肥料,为植物生长提供N、P、K等营养元素
3 3 4 2
C.生石灰与烧碱与水都有热量放出,不能用加水的方法鉴别二者
D.汽油和洗涤剂除去油污都是乳化过程,与食醋除水垢的原理不同。
8. 氯碱工业的反应原理是电解饱和食盐水,下列物质不可能是氯碱工业产品的是( )
A.H B.Cl C.Na CO D. NaOH
2 2 2 3 [来源:学科网ZXXK]9. 下列实验方案能达到目的的是 ( )
A探究燃烧条件 B探究铁生锈的条件 C探究二氧化锰对反 D探究溶解性的影响
应速率的影响 因素
10. 实验室制取氧气时,在试管中加热一定量高锰酸钾固体,随着反应的发生,纵坐标表
示的是( )
A.高锰酸钾的质量 B.氧气的质量
C.锰元素的质量分数 D.固体物质的质量
第Ⅱ卷 非选择题
三、填空题(化学方程式每空2分,其余每空1分,共17分)
21. 用化学用语填空
氢元素____;五氧化二磷中磷元素的化合价______;2个氮分子_______;
钙离子_____;甲烷燃烧的化学方程式_____________________________。
22. 某实验室欲配制一定溶质质量分数的 KNO 溶液,现实验室只有含少量NaCl的KNO
3 3
固体药品。
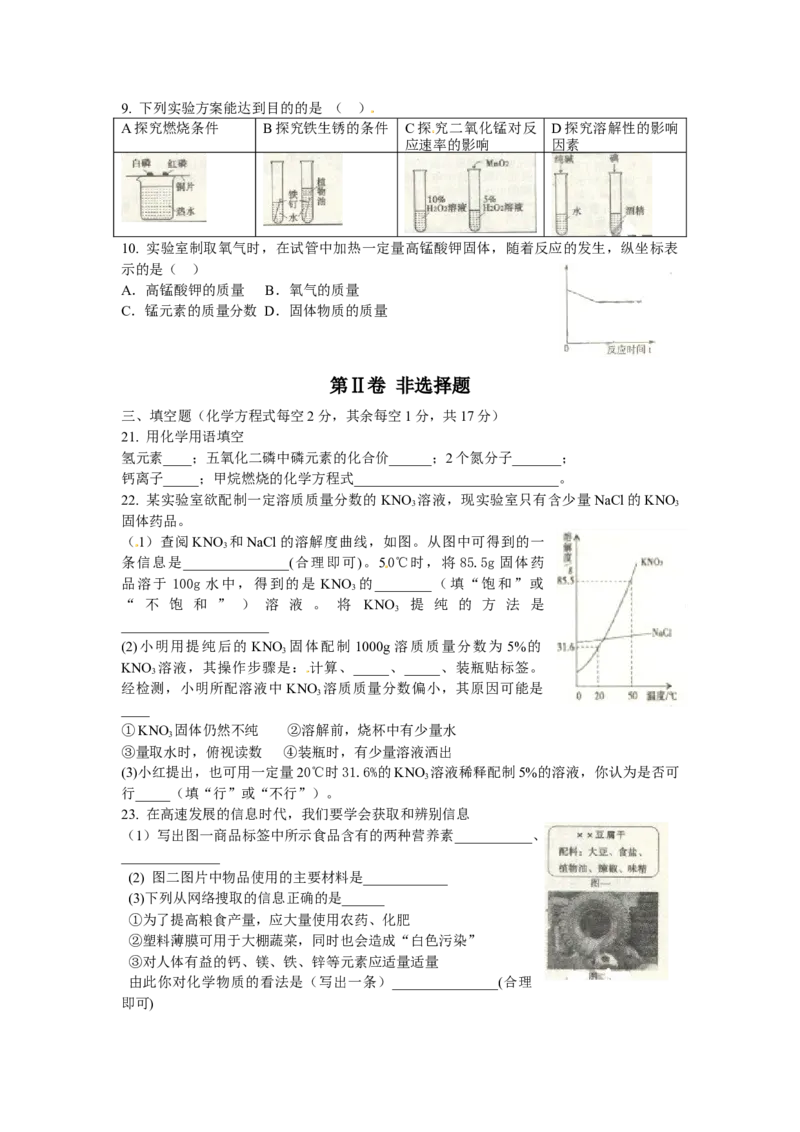
(1)查阅KNO 和NaCl的溶解度曲线,如图。从图中可得到的一
3
条信息是_______________(合理即可)。50℃时,将 85.5g 固体药
品溶于 100g 水中,得到的是 KNO 的________(填“饱和”或
3
“ 不 饱 和 ” ) 溶 液 。 将 KNO 提 纯 的 方 法 是
3
_____________________
(2)小明用提纯后的 KNO 固体配制 1000g 溶质质量分数为 5%的
3
KNO 溶液,其操作步骤是:计算、_____、_____、装瓶贴标签。
3
经检测,小明所配溶液中 KNO 溶质质量分数偏小,其原因可能是
3
____
①KNO 固体仍然不纯 ②溶解前,烧杯中有少量水
3
③量取水时,俯视读数 ④装瓶时,有少量溶液洒出
(3)小红提出,也可用一定量20℃时31.6%的KNO 溶液稀释配制5%的溶液,你认为是否可
3
行_____(填“行”或“不行”)。
23. 在高速发展的信息时代,我们要学会获取和辨别信息
(1)写出图一商品标签中所示食品含有的两种营养素___________、
______________
(2) 图二图片中物品使用的主要材料是____________
(3)下列从网络搜取的信息正确的是______
①为了提高粮食产量,应大量使用农药、化肥
②塑料薄膜可用于大棚蔬菜,同时也会造成“白色污染”
③对人体有益的钙、镁、铁、锌等元素应适量适量
由此你对化学物质的看法是(写出一条)_______________(合理
即可)四、简答题(化学方程式每空2分,其余每空1分,共12分)
24.
(1) 图一中从微观角度你获得的一条信息___________________________。
(2) 图二所示反应的化学方程式为__________________,该反应的微观过程是:①氢分
子和氧分子分裂为氢原子和氧原子,则②表示_______________________________
(3) 图三所示反应为:C(石墨) C(金刚石),你对该化学变化的微观解释是
_______________________________________________________________________
(4) 请你再写出一组反应物,其反应的微观实质与上述都不同:___________(合理即
可)
25. 同学们在学习酸碱的化学性质时构建了如右图知识网络,
A、B、C、D是不同类别的无机化合物,“—”表示物质
在一定条件下可以发生化学反应。请回答下列问题:
( 1 ) 反 应 ① 的 化 学 方 程 式 为 :
___________________________, 实 验 现 象 为
__________________________________________
(2) 写出图中一个中和反应的化学方程式_______________________________________
(3)物质C应具备的条件是__________________________________________________
五、实验探究题(化学方程式每空2分,其余每空1分,共14分)
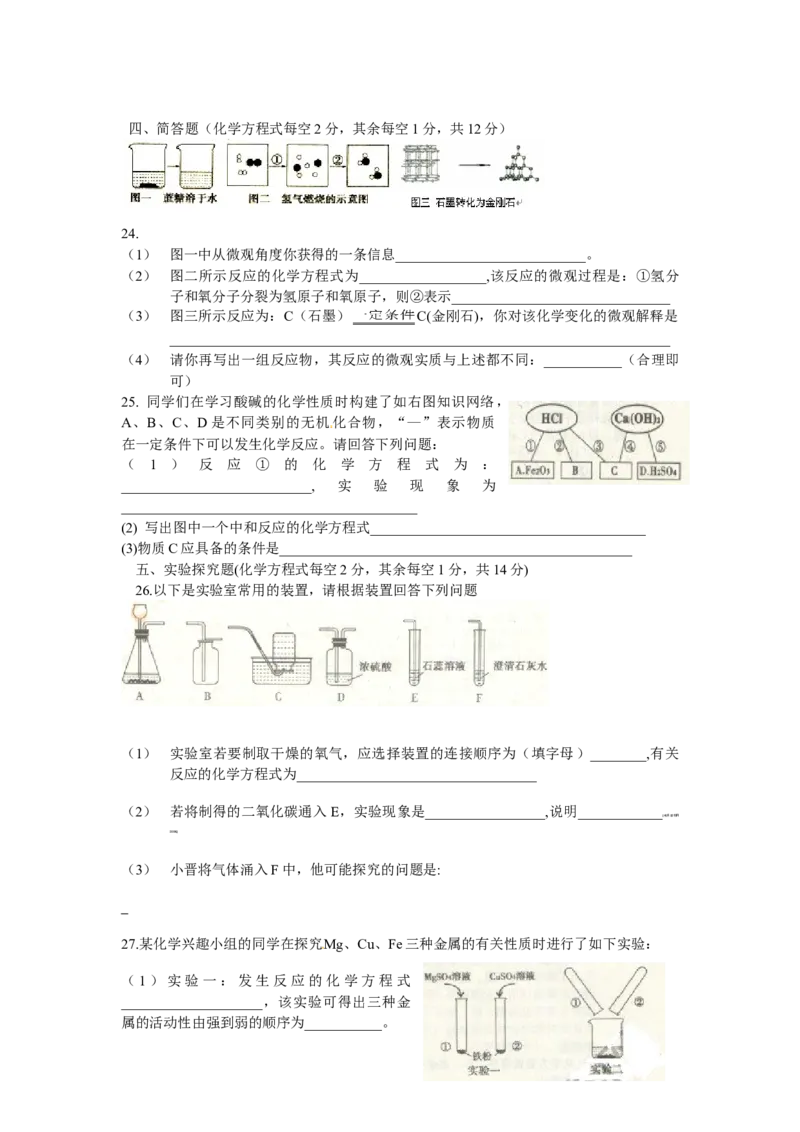
26.以下是实验室常用的装置,请根据装置回答下列问题
(1) 实验室若要制取干燥的氧气,应选择装置的连接顺序为(填字母)________,有关
反应的化学方程式为__________________________________
(2) 若将制得的二氧化碳通入E,实验现象是_________________,说明____________
[来源:学科网
ZXXK]
(3) 小晋将气体涌入F中,他可能探究的问题是:
27.某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:
(1)实验一:发生反应的化学方程式
____________________,该实验可得出三种金
属的活动性由强到弱的顺序为___________。(2)实验二:将实验一后①、②试管内的物质倒入烧杯中,发现烧杯内的红色固体明显增
多,一段时间后过滤。滤渣中一定含有的物质是__________,可能有的物质是____,为了
进一步确定可能有的物质是否存在,同学们设计了如下方案:
实验步骤 实验现象 结论
取少量滤渣于试管中,向其中滴加______ 没有气泡产生 _________________
[来源:学科网ZXXK]
滤液中含有的金属离子可能是____
① Mg2+②Mg2+、Fe2+③Mg2+、Fe3+④Cu2+、Fe2+⑤Mg2+、Fe2+、Cu2+
六、计算题(7分)
28.某化学兴趣小组的同学采集了一些大理石样品,为测定该样品中碳酸钙的质量分数,取
样品6g粉碎成粉末状置于烧杯中,向其中加入10%的稀盐酸并不断搅拌,恰好不再有气泡
产生时(已知杂质不与稀盐酸反应),共用去稀盐酸36.5g。
(1)该实验中能否用稀硫酸代替稀盐酸____(填“能”或“不能”)。
(2)用质量分数为36%的浓盐酸100g能配制所需10%的稀盐酸____g。
(3)计算样品中碳酸钙的质量分数。(结果保留到0.1%)2012 山西理科综合化学部分参考答案
一、 选择题
选项 1 2 3 4 5 6 7 8 9 10
答案 C A B B D A A C C D
[来源:Z#xx#k.Com]
三、填空题
+5
21.H PO Ca2+ CH+2O CO+2H O
2 5 4 2 2 2
22.(1)20℃时KNO 的溶解度为31.6g(其他合理即可) 不饱和 降温结晶(冷却热的
3
饱和溶液)
(2)称量、溶解 ①② (3)不行
23.(1)蛋白质 无机盐或维生素
(2)合成橡胶(或合成材料或有机高分子材料)
(3)②③ 要科学合理的使用化学物质
24.(1)分子在不断运动(分子间有间隔或分子很小)
(2)2H+O 2HO 氢原子和氧原子结合成水分子(或每两个氢原子与一个氧原子结
2 2 2
合成一个水分子)
(3)碳原子排列方式发生了改变(或碳原子排列方式不同)
(4)NaOH和HCl
25.(1) Fe O+6HCl= 2FeCl +3H O 红色(或红棕色)固体不断溶解,溶液由无色变成黄色
2 3 3 2
(2)Ca(OH) +2HCl=CaCl +2H O (或HCl和任意一种碱)
2 2 2
(3)(可溶性)盐,且和Ca(OH) 、HCl反应符合复分解反应发生的条件
2
26.(1) ADB 2HO 2HO+O↑
2 2 2 2
(2) 紫色石蕊变红 二氧化碳与水反应生成了碳酸(或二氧化碳与水生成了酸性物质)
(3)该气体是否为二氧化碳(或该气体能与澄清石灰水反应吗)
27.(1)Fe+CuSO4= FeSO4+Cu Mg、Fe、Cu
(2) Cu Fe 稀盐酸 滤渣中没有铁 ②⑤
[来源:Z§xx§k.Com]
六、计算题
28.解:(1)能
(2)360
(3)设6g样品中CaCO3的质量为x
CaCO + 2HCl = CaCl + CO↑ + HO
3 2 2 2
100 73
x 36.5g×10%=
x=5g
样品中碳酸钙的质量分数为: ×100%=83.3%
答:样品中碳酸钙的质量分数为83.3%。