文档内容
2015年高考化学试题 [广东卷]
7.化学是你,化学是我,化学深入我们生活,下列说法正确的是( )
A.木材纤维和土豆淀粉遇碘水均显蓝色
B.食用花生油和鸡蛋清都能发生水解反应
C.包装用材料聚乙烯和聚氯乙烯都属于烃
D.PX项目的主要产品对二甲苯属于饱和烃
8.水溶液中能大量共存的一组离子是( )
A.NH + 、Ba2+、Br-、CO2- B.Cl-、SO 2-、Fe2+、H+
4 3 3
C.K+、Na+、SO 2-、MnO - D.Na+、H+、NO -、HCO -
4 4 3 3
9.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A 1-己醇的沸点比己烷的沸点高 1-己醇和己烷可通过蒸馏初步分离
B 原电池可将化学能转化为电能 原电池需外接电源才能工作
C 乙二酸可与KMnO 溶液发生反应 乙二酸具有酸性
4
D Na在Cl 中燃烧的生成物含离子键 NaCl固体可导电
2
10.设n 为阿伏伽德罗常数的数值,下列说法正确的是( )
A
A. 23g Na 与足量HO反应完全后可生成n 个H 分子
2 A 2
B.1 molCu和足量热浓硫酸反应可生成n 个SO 分子
A 3
C.标准状况下,22.4L N 和H 混合气中含n 个原子
2 2 A
D.3mol单质Fe完全转变为Fe O,失去8n 个电子
3 4 A
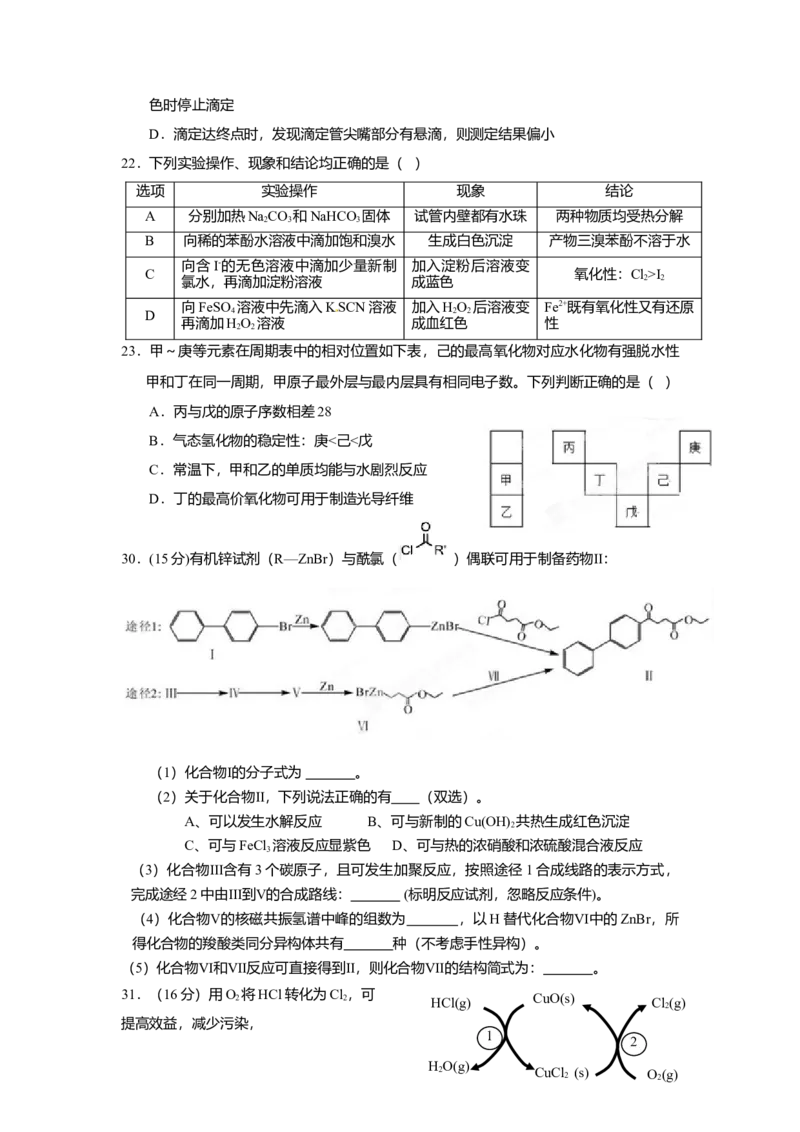
11.一定温度下,水溶液中H+和OH-的浓度变化曲线如图2,下列说法正确的是( )
A.升高温度,可能引起有c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
12.准确移取 20.00mL 某待测 HCl 溶液于锥形瓶中,
用0.1000mol·L-1NaOH溶液滴定,下列说法正确的
是( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着 NaOH 溶液滴入,锥形瓶中溶液 pH由小 O c(OH - )/mol -
1·L - 1 - )·mol -
变大 1·L-1)
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无
L·1-
lom/)+
H(c -1-
7-01×0.1
a
b
c
d
1.0×10-7
图2色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
22.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A 分别加热NaCO 和NaHCO 固体 试管内壁都有水珠 两种物质均受热分解
2 3 3
B 向稀的苯酚水溶液中滴加饱和溴水 生成白色沉淀 产物三溴苯酚不溶于水
向含I-的无色溶液中滴加少量新制 加入淀粉后溶液变
C 氧化性:Cl>I
氯水,再滴加淀粉溶液 成蓝色 2 2
向FeSO 溶液中先滴入KSCN溶液 加入HO 后溶液变 Fe2+既有氧化性又有还原
D 4 2 2
再滴加HO 溶液 成血红色 性
2 2
23.甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性
甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
A.丙与戊的原子序数相差28
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丁的最高价氧化物可用于制造光导纤维
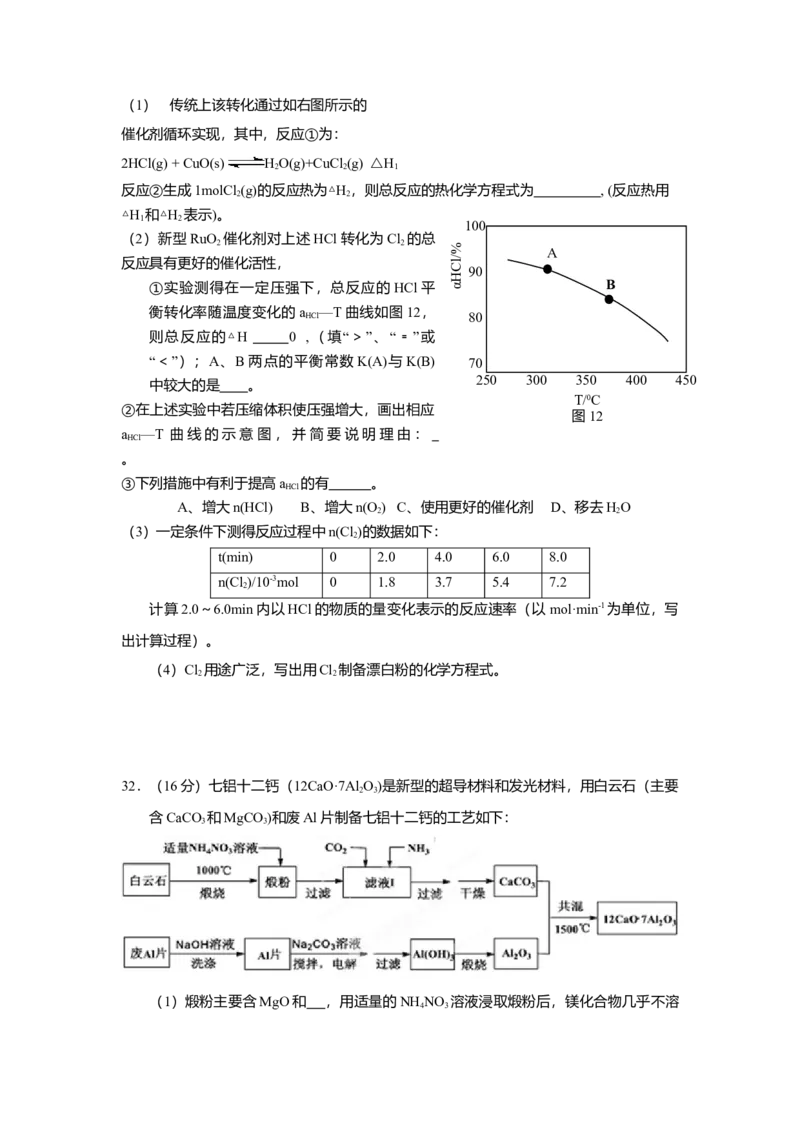
30.(15分)有机锌试剂(R—ZnBr)与酰氯( )偶联可用于制备药物Ⅱ:
(1)化合物Ⅰ的分子式为 。
(2)关于化合物Ⅱ,下列说法正确的有 (双选)。
A、可以发生水解反应 B、可与新制的Cu(OH) 共热生成红色沉淀
2
C、可与FeCl 溶液反应显紫色 D、可与热的浓硝酸和浓硫酸混合液反应
3
(3)化合物Ⅲ含有3个碳原子,且可发生加聚反应,按照途径1合成线路的表示方式,
完成途经2中由Ⅲ到Ⅴ的合成路线: (标明反应试剂,忽略反应条件)。
(4)化合物Ⅴ的核磁共振氢谱中峰的组数为 ,以H替代化合物Ⅵ中的ZnBr,所
得化合物的羧酸类同分异构体共有 种(不考虑手性异构)。
(5)化合物Ⅵ和Ⅶ反应可直接得到Ⅱ,则化合物Ⅶ的结构简式为: 。
[来源:学§科§网]
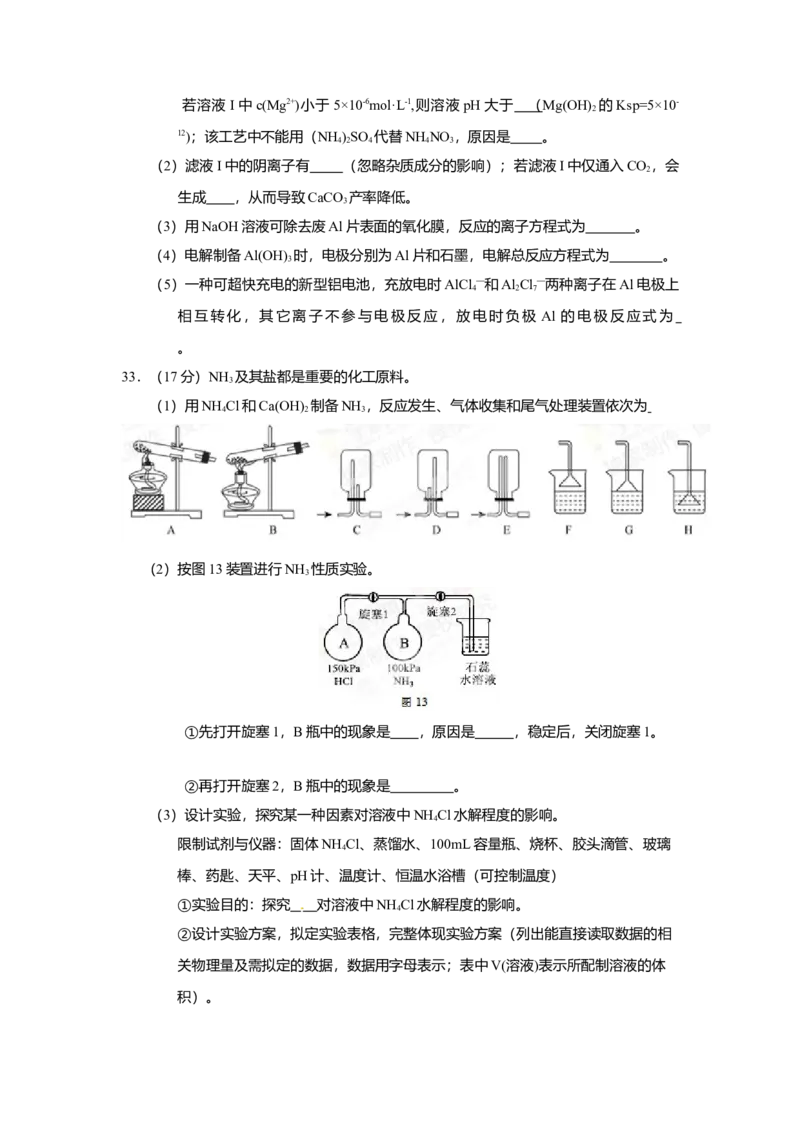
31.(16分)用O 2 将HCl转化为Cl 2 ,可 HCl(g) CuO(s) Cl (g)
2
提高效益,减少污染,
1
2
H O(g)
2 CuCl 2 (s) O 2 (g)(1) 传统上该转化通过如右图所示的
催化剂循环实现,其中,反应①为:
2HCl(g) + CuO(s) HO(g)+CuCl (g) △H
2 2 1
反应②生成1molCl (g)的反应热为△H,则总反应的热化学方程式为 , (反应热用
2 2
△H 和△H 表示)。
1 2
100
(2)新型RuO 催化剂对上述HCl转化为Cl 的总
2 2
反应具有更好的催化活性,
90
①实验测得在一定压强下,总反应的 HCl平
衡转化率随温度变化的a —T曲线如图12,
HCl 80
则总反应的△H 0 ,(填“>”、“﹦”或
“<”);A、B两点的平衡常数 K(A)与K(B) 70
250 300 350 400 450
中较大的是 。
②在上述实验中若压缩体积使压强增大,画出相应
a —T 曲线的示意图,并简要说明理由:
HCl
。
③下列措施中有利于提高a 的有 。
HCl
A、增大n(HCl) B、增大n(O ) C、使用更好的催化剂 D、移去HO
2 2
(3)一定条件下测得反应过程中n(Cl )的数据如下:
2
t(min) 0 2.0 4.0 6.0 8.0
n(Cl )/10-3mol 0 1.8 3.7 5.4 7.2
2
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率(以mol·min-1为单位,写
出计算过程)。
(4)Cl 用途广泛,写出用Cl 制备漂白粉的化学方程式。
2 2
32.(16分)七铝十二钙(12CaO·7Al O)是新型的超导材料和发光材料,用白云石(主要
2 3
含CaCO 和MgCO )和废Al片制备七铝十二钙的工艺如下:
3 3
(1)煅粉主要含MgO和 ,用适量的NH NO 溶液浸取煅粉后,镁化合物几乎不溶
4 3
%/lCHα
A
B
T/0C
图12若溶液I中c(Mg2+)小于5×10-6mol·L-1,则溶液pH大于 (Mg(OH) 的Ksp=5×10-
2
12);该工艺中不能用(NH )SO 代替NH NO ,原因是 。
4 2 4 4 3
(2)滤液I中的阴离子有 (忽略杂质成分的影响);若滤液I中仅通入CO ,会
2
生成 ,从而导致CaCO 产率降低。
3
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为 。
(4)电解制备Al(OH) 时,电极分别为Al片和石墨,电解总反应方程式为 。
3
(5)一种可超快充电的新型铝电池,充放电时AlCl —和Al Cl—两种离子在Al电极上
4 2 7
相互转化,其它离子不参与电极反应,放电时负极 Al 的电极反应式为
。
33.(17分)NH 及其盐都是重要的化工原料。
3
(1)用NH Cl和Ca(OH) 制备NH ,反应发生、气体收集和尾气处理装置依次为
4 2 3
(2)按图13装置进行NH 性质实验。
3
①先打开旋塞1,B瓶中的现象是 ,原因是 ,稳定后,关闭旋塞1。
[来源:Z。
xx。k.Com]
②再打开旋塞2,B瓶中的现象是 。
(3)设计实验,探究某一种因素对溶液中NH Cl水解程度的影响。
4
限制试剂与仪器:固体NH Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃
4
棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究 对溶液中NH Cl水解程度的影响。
4
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相
关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体
积)。物理量 V(溶液)/ ……
mL
实验序号
1 100
2 100
③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH Cl
4
水解反应得平衡转化率为 (只列出算式,忽略水自身电离的影响)。
2015年高考化学试题 [广东卷]参考答案
7.【答案】B 【解析】木材纤维主要成分是纤维素,遇碘水不变蓝色,A错;花生油属于
酯类,可以发生水解反应,鸡蛋主要成分是蛋白质,水解生成氨基酸,B对;聚氯乙烯中
有氯原子,不属于烃类,C错;对二甲苯中有苯环,不属于饱和烃,D错。
8.【答案】C【解析】Ba2+和CO2-反应生成BaCO 沉淀,不能大量共存,A错;SO 2-和
3 3 3
H+反应生成SO ,不能大量共存,B错;C中四种离子不反应,可以大量共存,C对;H+和
2
HCO -会反应生成CO、HO,不能大量共存,D错。
3 2 2
9.【答案】A 【解析】互溶的液体物质沸点相差较大的,可以用蒸馏的方法分离,A对;
原电池不需外接电源,B错;乙二酸可与KMnO 溶液发生反应体现的是还原性而不是酸性,
4
C错;NaCl固体中没有自由移动的离子,不能导电,D错。
10. 【答案】D 【解析】23g Na完全反应时转移电子为 1mol,生成H 为0.5mol,个数为
2
0.5n 个,A错;Cu和足量热浓硫酸反应生成的是 SO ,不是SO ,B错;标准状况下,
A 2 3
22.4L N 和H 混合气的物质的量为1mol,含有的分子数目是n 个,由于N 和H 都是双原
2 2 A 2 2
子分子,故原子的物质的量为2mol,个数为2n 个,C错;Fe O 看成Fe O·FeO,3mol单
A 3 4 2 3
质Fe完全转变为Fe O,失去8n 个电子,D对。
3 4 A
11. 【答案】C 【解析】温度升高,水的离子积增大,c(H+)、c(OH-)都增大,表示的点就
不在曲线上,A错;水的离子积常数K=c(H+)·c(OH-),从图可知离子积是1.0×10-11,不
是1.0×10-13,B错;加入FeCl ,水解使得溶液酸性增强,c(H+)增大,那么c(OH-)减小,
3
故可能引起由b向a的变化,C对;温度不变水的离子积不变,稀释溶液后所表示的
点还在曲线上,不可能引起由c向d的变化,D错。
12. 【答案】B 【解析】滴定管用蒸馏水洗涤后,没有用标准液洗涤,装入 NaOH溶液进行
滴定会造成NaOH溶液的浓度变小,用量增多,结果偏大,A错;酸中滴入碱,溶液的碱
性增强,酸性减弱,溶液pH由小变大,B对;用酚酞作指示剂,锥形瓶溶液开始是无色的,当锥形瓶中溶液由无色变红色,而且半分钟内不褪色时,证明滴定达到了滴定终点,C错;
滴定达终点时,发现滴定管尖嘴部分有悬滴,造成碱的用量偏多,则测定结果偏大,D对。
22. 【答案】BC 【解析】NaCO 加热时产生的水珠是空气中的水凝结形成,不是分解生成
2 3
的,A错;苯酚溶液中滴加饱和溴水生成白色沉淀,说明产物三溴苯酚不溶于水,B对;
淀粉溶液变成蓝色则生成了I ,说明氯水把I—氧化成了I , 故氧化性:Cl>I ,C对;
2 2 2 2
FeSO 溶液中先滴入KSCN溶液再滴加HO 溶液,溶液变成血红色,说明HO 把Fe2+氧化
4 2 2 2 2
为Fe3+,体现了Fe2+的还原性,没有体现氧化性,D错。
23. 【答案】AD 【解析】己的最高氧化物对应水化物有强脱水性为浓硫酸,则己是S元素,
可以推出庚是F元素,戊是As元素,丁是Si元素,丙是B元素,甲和丁在同一周期,甲
原子最外层与最内层具有相同电子数,甲是 Mg,乙是Ca。A.丙与戊的原子序数相差
(8+18+2)=28,对;B.非金属性越强,气态氢化物越稳定,气态氢化物的稳定性:庚>
己>戊,B错;甲单质与水反应不剧烈,C错;丁是Si元素,二氧化硅可用于制造光导纤
维,D对。
30. 【答案】(1)C HBr (2)AD (3)CH =CHCOOH BrCHCHCOOH
12 9 2 2 2
BrCHCHCOOCH CH (4) 4 、 4 (5)
2 2 2 3
【解析】(1)根据化合物Ⅰ的结构简式可写出其分子式为C HBr;(2)根据化合物Ⅱ的结
12 9
构简式,其含有酯基,可发生水解反应,含有苯环,发生苯环上的硝化反应,没有醛基,
不可与新制的Cu(OH) 共热生成红色沉淀,没有酚羟基,不可与FeCl 溶液反应显紫色,所
2 3
以A、D正确,选择AD;(3)根据Ⅵ的结构简式及途径Ⅰ的信息,可推出Ⅴ的结构简式为
BrCHCHCOOCH CH ,从而可知Ⅴ是由Ⅳ与乙醇发生酯化反应得到,可推出Ⅳ的结构简
2 2 2 3
式为BrCHCHCOOH,而化合物Ⅲ含有3个碳原子,且可发生加聚反应,从而可知化合物
2 2
Ⅲ的结构简式为 CH=CHCOOH,从而可得其合成路线;(4)化合物Ⅴ的结构为
2
BrCHCHCOOCH CH ,每个碳原子上的氢都相同,不同碳原子上的H原子不相同,所以
2 2 2 3
应有 4 组峰;以氢原子 H 替代化合物Ⅵ中的 ZnBr,所得化合物的结构简式为
CHCHCOOCH CH ,其属于羧酸类的结构应为 C HCOOH,C H—为丁基,丁基有4种
3 2 2 3 4 9 4 9
不同的结构的H原子,所以C HCOOH的同分异构体共有4种;(5)根据题目信息,有
4 9机锌试剂(R—ZnBr)与酰氯( )偶联可用于制备药物Ⅱ,因此化合物Ⅵ为
BrZnCH CHCOOCH CH,则要合成Ⅱ,Ⅶ为酰氯,根据Ⅱ的结构及途径Ⅰ合成化合物药物Ⅱ
2 2 2 3
的方式,可推知Ⅶ的结构为 。
31. 【答案】(1) 2HCl(g) + 1/2O (g) HO(g)+Cl (g) △H=△H +△H
2 2 2 1 2
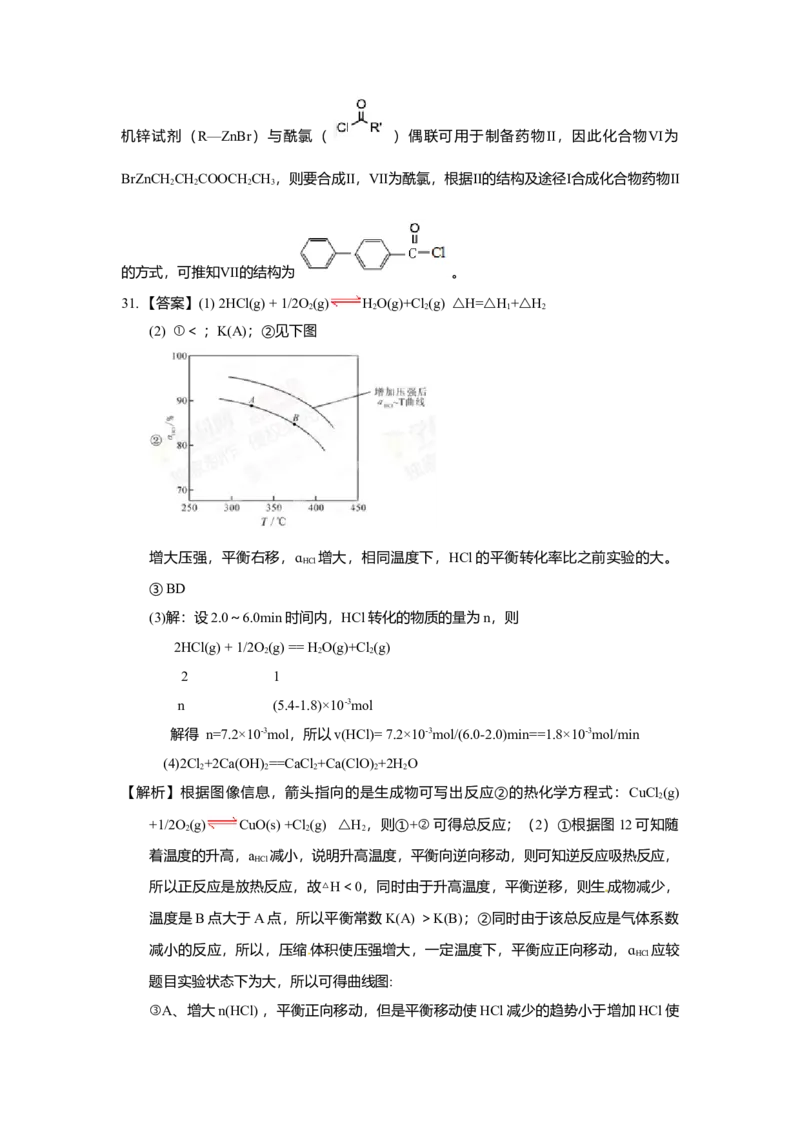
(2) ①< ;K(A);②见下图
增大压强,平衡右移,ɑ 增大,相同温度下,HCl的平衡转化率比之前实验的大。
HCl
③BD
(3)解:设2.0~6.0min时间内,HCl转化的物质的量为n,则
2HCl(g) + 1/2O(g) == H O(g)+Cl (g)
2 2 2
2 1
n (5.4-1.8)×10-3mol
解得 n=7.2×10-3mol,所以v(HCl)= 7.2×10-3mol/(6.0-2.0)min==1.8×10-3mol/min
(4)2Cl +2Ca(OH) ==CaCl +Ca(ClO) +2H O
2 2 2 2 2
【解析】根据图像信息,箭头指向的是生成物可写出反应②的热化学方程式:CuCl (g)
2
+1/2O (g) CuO(s) +Cl (g) △H ,则①+②可得总反应;(2)①根据图12可知随
2 2 2
着温度的升高,a 减小,说明升高温度,平衡向逆向移动,则可知逆反应吸热反应,
HCl
所以正反应是放热反应,故△H<0,同时由于升高温度,平衡逆移,则生成物减少,
温度是B点大于A点,所以平衡常数K(A) >K(B);②同时由于该总反应是气体系数
减小的反应,所以,压缩体积使压强增大,一定温度下,平衡应正向移动,ɑ 应较
HCl
题目实验状态下为大,所以可得曲线图:
③A、增大n(HCl) ,平衡正向移动,但是平衡移动使HCl减少的趋势小于增加HCl使增大的趋势,所以HCl的转化率减小,错;B、增大n(O ) ,反应物的浓度增大,平衡
2
向正向移动,HCl转化率增大,对;C、使用更好的催化剂,不能使化学平衡发生移动,
实验HCl的转化率不变,错; D、移去HO,及减小了生成物的浓度,平衡向正反应
2
方向移动,HCl转化率增大。对。故答案是选项B、D。(3)题目中给出的是n(Cl )的
2
数据,要求的是以HCl的物质的量变化表示的反应速率,所以根据方程式进行计算,
注意是2.0~6.0min内的速率,单位是mol·min-1:设2.0~6.0min内,HCl转化的物质
的量为n,则:
2HCl(g) + 1/2O(g)=HO(g)+Cl (g)
2 2 2
2 1
n (5.4-1.8)×10-3mol
解得 n=7.2×10-3mol,所以v(HCl)= 7.2×10-3mol/(6.0-2.0)min==1.8×10-3mol/min
(4)Cl 与石灰乳发生反应制取漂白粉,反应的化学方程式为:2Cl+2Ca(OH) =
2 2 2
CaCl +Ca(ClO) +2H O。
2 2 2
32. 【答案】(1)CaO;11;加入(NH )SO 会生成CaSO 微溶物,在过滤时会被除去,
4 2 4 4
造成生成的CaCO 减少。(2)NO —、OH—;Ca(HCO ) (3)2OH—+AlO =2AlO—
3 3 3 2 2 3 2
+H O(4)2Al+6H 0 2Al(OH) ↓+3H ↑
2 2 3 2
(5) Al-3e-+7 AlCl —=4 Al Cl—
4 2 7
【解析】(1)煅烧时CaCO 会发生分解生成CaO和CO ;煅烧MgCO 分解生成MgO和
3 2 3
CO;故煅粉主要含MgO和CaO;Ksp= c(Mg2+)∙c2(OH—),5×10-12=5×10-6 ×c2(OH—),得
2
c(OH—)= 10-3mol·L-1, pH=11。由于溶液I中c(Mg2+)小于5×10-6mol·L-1,所以溶液pH
大于11;不能用(NH )SO 代替NH NO 的原因是加入(NH )SO 会生成CaSO 微溶
4 2 4 4 3 4 2 4 4
物,在过滤时会被除去,从而造成生成的CaCO 减少。(2)从流程中看出NO —没有
3 3
被除去,故滤液I中的阴离子有NO —,CaO溶于水生成Ca(OH) ,故溶液中还有OH
3 2
—;若滤液I中仅通入CO ,过量的CO 会与CaCO 生成Ca(HCO ) 从而导致CaCO 产
2 2 3 3 2 3
率降低。(3)Al表面的氧化膜的成分是Al O ,该物质是两性氧化物,NaOH可以与
2 3
之发生反应。NaOH溶液与Al O 反应的离子方程式为:2OH—+AlO =2AlO—+H O;
2 3 2 3 2 2
(4)电解制备Al(OH) 时,电极分别为Al片和石墨,Al作阳极,石墨作阴极。Al在
3
阳极放电,溶液中的H+在阴极放电,破坏了水的电离平衡,使的溶液中的OH—浓度增
大 , 与 产 生 的 Al3+ 结 合 生 成 Al(OH) , 总 反 应 方 程 式 为 : 2Al+6H O
3 22Al(OH) ↓+3H ↑。(5)根据题意,充电和放电时AlCl —和Al Cl—两种离子在Al电极
3 2 4 2 7
上相互转化,放电时负极Al失去电子变为Al3+,与溶液中的AlCl —结合,发生反应产
4
生的Al Cl—电极反应式为:Al-3e-+7 AlCl —=4 Al Cl—。
2 7 4 2 7
33. 【答案】(1)A、C、G。
(2)①产生白烟;打开旋塞1,氯化氢与氨气混合反应生成了白色氯化铵固体小颗粒,
形成白烟。②烧杯中的石蕊溶液会倒流进入到B瓶中,形成红色溶液。
(3)①温度(或浓度)
②
物理量 V(溶液)/ NH Cl质量(g) 温 度 pH ……
4
mL (℃)
实验序号
1 100 m T Y
1
2 100 m T Z
2
或
物理量 V(溶液)/ NH Cl质量(g) 温 度 pH ……
4
mL (℃)
实验序号
1 100 m T Y
2 100 m T Z
2
③(10-Y×5.35)/m
【解析】(1)NH Cl和Ca(OH) 制备NH 是固体混合物加热制取气体的反应,有水生成,
4 2 3
试管口应向下倾斜,发生装置选A,NH 密度比空气小,用向下排空气法收集,收集
3
装置选C,氨气极易溶于水,要用防倒吸装置,但不能距离水太远,也不能插入液面
以下,选G,故选A、C、G。(2)①先打开旋塞1,B瓶中的现象是产生白色的烟;
原因是先打开旋塞1,氯化氢与氨气挥发出来,氯化氢与氨气反应生成了氯化铵小颗
粒,氯化铵小颗粒形成白烟。②再打开旋塞 2,B瓶中的现象是烧杯中的石蕊溶液会
倒流进入到B瓶中,是因为气体参与反应后使得烧瓶内的压强变小,打开旋塞2后,
大气压就会把烧杯中的溶液压到烧瓶中来,同时由于 A中的HCl不可能全部进入B中,
A中HCl过量,就算不能完全进入B瓶,B中的氨气也应能完全反应,形成氯化铵,
石蕊溶液进入B中,B中的NH Cl溶于石蕊溶液,溶液显酸性,所以石蕊试液显红色。
4
(3)主要采用控制变量的方法,根据给出的仪器,有可控制温度水浴槽,那么可以完
成温度对NHCl水解程度的影响,天平可以称出不同质量NH Cl,那么可以配制出不
4 4
同浓度的溶液,就可以探究浓度对NH Cl水解程度的影响,故答案为温度或浓度。如
4果探究温度的影响那么控制浓度相同,改变温度,如果探究浓度相同,那么就要控制
温度相同,不管哪一种探究都需要配制一定浓度的NH Cl溶液,那么需要称量NH Cl
4 4
的质量,但不管探究的是哪种因素的影响,都需要使用 pH计通过测量水解后溶液的
pH来判断其水解程度,所以在表格中都应有一项为pH值。若探究温度对NH Cl水解
4
程度的影响时数据为:
物理量 V(溶液)/ NH Cl质量(g) 温 度 pH ……
4
mL (℃)
实验序号
[来源:学科网ZXXK]
1 100 m T Y
1
2 100 m T Z
2
若探究浓度对NH Cl水解程度的影响时数据为:
4
物理量 V(溶液)/ NH Cl质量(g) 温 度 pH ……
4
mL (℃)
实验序号
1 100 m T Y
1[来源:学|科|网Z|X|X|K]
2 100 m T Z
2
如果pH 为Y,那么c(H+)=10-Ymol/L,物质的量为10-Ymol/L×0.1L=10-Y-1mol,那么水解的
NH Cl的物质的量也为10-Y-1mol,质量为10-Y-1mol×53.5g/mol=10-Y×5.35g,则NH Cl水
4 4
解反应得平衡转化率为:( 10-Y×5.35)/m。