文档内容
绝密★考试结束前
2015 年 10 月浙江省普通高校招生选考科目考试
化学试题
考生须知:
1.本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。
其中加试题部分为30分,用【加试题】标出。
2.考生答题前,务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔填写在答题
纸上。
3.选择题的答案须用2B铅笔将答题纸上对应题目的答案标号涂黑,如要改动,须将
原填涂处用橡皮擦净。
4.非选择题的答案须用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可
先使用2B铅笔,确定后须用黑色字迹的签字笔或钢笔描黑,答案写在本试题卷上无效。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Si 28 S 32
Ca 40 Fe 56 Cu 64 Zn 65
一、选择题(本大题共25小题,每小题2分,共50分。每个小题列出的四个备选项中只
有一个是符合题目要求的,不选、多选、错选均不得分)
1.下列属于酸性氧化物的是
A.CO B.CaO C.K SO D.NaOH
2 2 4
2.仪器名称为“容量瓶”的是
A. B. C. D.
3.常温下能与水反应的金属单质是
A.SiO B.Br C.Na O D.Na
2 2 2
4.HCl+NaOH=NaCl+H O的反应类型是
2
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
5.下列物质中,属于可再生的能源是
A.氢气 B.石油 C.煤 D.天然气
6.硅元素在周期表中的位置是
A.第二周期ⅣA族 B.第三周期ⅣA族
C.第三周期ⅥA族 D.第二周期ⅥA族
7.下列化学用语表述正确的是
O ‥
A.水分子的结构式: / \ B.氯化钠的电子式:Na︰Cl︰
H H ‥
C.氯气的比例模型: D.硫原子的结构示意图: +16 2 8 8
8.能产生“丁达尔效应”的是
A.饱和食盐水 B.Fe(OH) 胶体 C.盐酸 D.硫酸铜溶液
3
9.下列说法不正确的是
A.核素21H的中子数是0
B.12C和14C互为同位素
C.金刚石、石墨和富勒烯互为同素异形体
D.CH CH OH和CH OCH 互为同分异构体
3 2 3 310.实验室有两瓶失去标签的溶液,其中一瓶是稀H SO 溶液,另一瓶是蔗糖溶液。鉴别
2 4
时,下列选用的试纸或试剂不正确的是
A.pH试纸 B.KCl溶液 C.BaCl 溶液 D.Na CO 固体
2 2 3
11.下列物质的水溶液因水解呈酸性的是
A.NaOH B.Na CO C.NH Cl D.HCl
2 3 4
12.已知1 mol CH 气体完全燃烧生成气态CO 和液态H O,放出890.3 kJ热量,则表示
4 2 2
该反应的热化学方程式正确的是
A.CH (g)+2O (g)=CO (g)+2H O(g) ΔH=+890.3 kJ·molˉ1
4 2 2 2
B.CH (g)+2O (g)=CO (g)+2H O(l) ΔH=-890.3 kJ·molˉ1
4 2 2 2
C.CH (g)+2O (g)=CO (g)+2H O(l) ΔH=+890.3 kJ·molˉ1
4 2 2 2
D.CH (g)+2O (g)=CO (g)+2H O(g) ΔH=-890.3 kJ·molˉ1
4 2 2 2
13.有关SO 的性质,下列说法不正确的是
2
A.能使品红溶液褪色 B.能与NaOH溶液反应
C.能与H O反应生成H SO D.一定条件下能与O 反应生成SO
2 2 4 2 3
14.有关苯的结构与性质,下列说法正确的是
A.分子中含有碳碳双键
B.易被酸性KMnO 溶液氧化
4
C.与溴水发生加成反应而使溴水褪色
D.在一定条件下可与浓硝酸和浓硫酸的混合酸反应生成硝基苯
15.下列说法正确的是
A.HCl属于共价化合物,溶于水能电离出H+和Clˉ
B.NaOH是离子化合物,该物质中只含有离子键
C.HI气体受热分解的过程中,只需克服分子间作用力
D.石英和干冰均为原子晶体
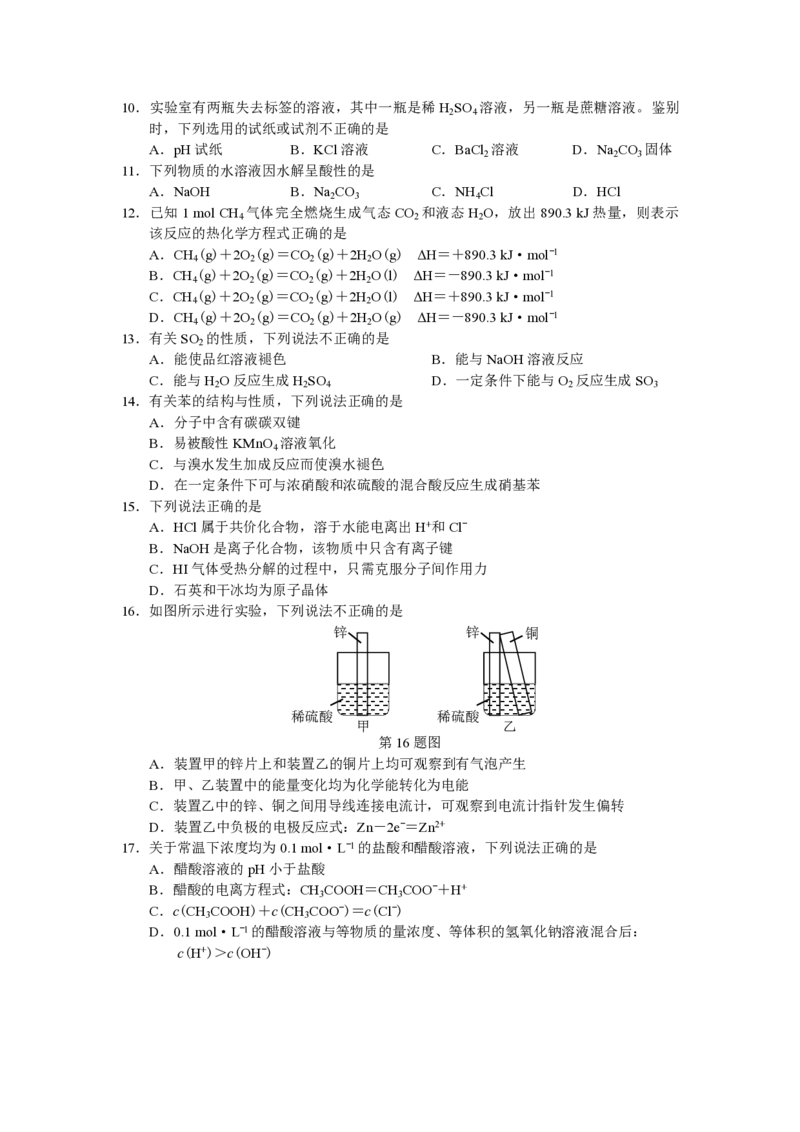
16.如图所示进行实验,下列说法不正确的是
锌 锌 铜
稀硫酸 稀硫酸
甲 乙
第16题图
A.装置甲的锌片上和装置乙的铜片上均可观察到有气泡产生
B.甲、乙装置中的能量变化均为化学能转化为电能
C.装置乙中的锌、铜之间用导线连接电流计,可观察到电流计指针发生偏转
D.装置乙中负极的电极反应式:Zn-2eˉ=Zn2+
17.关于常温下浓度均为0.1 mol·Lˉ1的盐酸和醋酸溶液,下列说法正确的是
A.醋酸溶液的pH小于盐酸
B.醋酸的电离方程式:CH COOH=CH COOˉ+H+
3 3
C.c(CH COOH)+c(CH COOˉ)=c(Clˉ)
3 3
D.0.1 mol·Lˉ1的醋酸溶液与等物质的量浓度、等体积的氢氧化钠溶液混合后:
c(H+)>c(OHˉ)18.下列离子方程式正确的是
A.硫酸钠溶液与氢氧化钡溶液反应:SO24ˉ+Ba2+=BaSO ↓
4
B.大理石与稀硝酸反应:CO23ˉ+2H+=CO ↑+H O
2 2
C.氯化铁溶液与碘化钾溶液反应:Fe3++2Iˉ=Fe2++I
2
D.氯化镁溶液与氨水反应:Mg2++2OHˉ=Mg(OH) ↓
2
19.下列说法不正确的是
A.钠和钾的合金可用于快中子反应堆作热交换剂
B.可用超纯硅制造的单晶硅来制造芯片
C.可利用二氧化碳制造全降解塑料
D.氯气有毒,不能用于药物的合成
20.某温度时,2NO(g)+O (g)=2NO (g)反应2 s后,NO的浓度减少了0.06 mol·Lˉ1,
2 2
则以O 表示该时段的化学反应速率是
2
A.0.03 mol·Lˉ1·sˉ1 B.0.015 mol·Lˉ1·sˉ1
C.0.12 mol·Lˉ1·sˉ1 D.0.06 mol·Lˉ1·sˉ1
21.下列说法正确的是
A.棉花和蚕丝的主要成分都是纤维素
B.蛋白质在一定条件下发生水解反应生成葡萄糖
C.煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程
D.食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物
22.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.N 个氧分子与N 个氢分子的质量比为8∶l
A A
B.100 mL 1.0 mol·Lˉ1 FeCl 溶液与足量Cu反应,转移的电子数为0.2 N
3 A
C.标淮状况下,11.2 L CCl 中含有C-Cl键的数目为2 N
4 A
D.N 个D O分子中,含有10 N 个电子
A 2 A
23.右图为元素周期表中短周期主族非金属元素的一部分,下列说法不正确的是
A.W的原子序数可能是Y的两倍
X Y
B.Z的原子半径比X的大
Z W
C.Y元素的非金属性比Z元素的强
第23题图
D.Z的最高价氧化物对应水化物的酸性比W的强
24.下列说法不正确的是
A.定容时,因不慎使液面高于容量瓶的刻度线,可用滴管将多余液体吸出
B.焰色反应时,先用稀盐酸洗涤铂丝并在酒精灯火焰上灼烧,然后再进行实验
C.将新制氯水滴入紫色石蕊溶液中,可以看到石蕊溶液先变红后褪色
D.取少量晶体放入试管中,再加入适量NaOH溶液,加热,在试管口用湿润的红色
石蕊试纸检验,若试纸变蓝,则可证明该晶体中含有NH +4
25.已知氧化性Br >Fe3+。向含溶质a mol的FeBr 溶液中通入b mol Cl ,充分反应。下
2 2 2
列说法不正确的是
A.离子的还原性强弱:Fe2+>Brˉ>Clˉ
B.当a≥2b时,发生的离子反应:2Fe2++Cl =2Fe3++2Clˉ
2
C.当a=b时,反应后的离子浓度之比:c(Fe3+)∶c(Brˉ) ∶c(Clˉ)=1∶2∶2
D.当3a≤2b时,发生的离子反应:2Fe2++4Brˉ+3Cl =2Fe3++2Br +6Clˉ
2 2二、非选择题(本大题共7小题,共50分)
26.(4分)气态烃 A中碳元素与氢元素的质量比为 6∶l。淀粉在一定条件下水解可生成
B,B在人体组织中发生缓慢氧化,放出热量,提供生命活动所需能量。有关物质的
转化关系如下图:
H O/催化剂
2
A
①
O /Cu,△
乙醇 2 乙醛
③
酒化酶
B
②
请回答:
(1) ①的反应类型是________。
(2) 向试管中加入2 mL 10%氢氧化钠溶液,滴加4~5滴5%硫酸铜溶液,振荡后加入
2 mL 10% B溶液,加热。写出加热后观察到的现象________。
(3) 反应③的化学方程式是________。
27.(6分)某酸性废液中含有Fe3+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对该
废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
沉淀a
①铁屑 ①H O 溶液
废液 2 2 红褐色沉淀b
②过滤 ②NaOH溶液
溶液A 沉淀c
③过滤 ①Na CO 溶液
溶液B 2 3
②过滤
溶液C
请回答:
(1) 沉淀a中含有的单质是________。
(2) 沉淀c的化学式是________。
(3) 溶液A与H O 溶液在酸性条件下反应的离子方程式是________。
2 2
28.(6分)右图为实验室制取乙酸乙酯的装置。
请回答:
(1) 检验该装置气密性的方法是________。
(2) 浓硫酸的作用是________。
(3) 下 列 有 关 该 实 验 的 说 法 中 , 正 确 的 是
________。
A.向a试管中加入沸石,其作用是防止加热时
液体暴沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明、密度比水大的油状液体
D.若原料为CH COOH和CH CH 18OH,则乙酸乙酯中不含18O
3 3 2
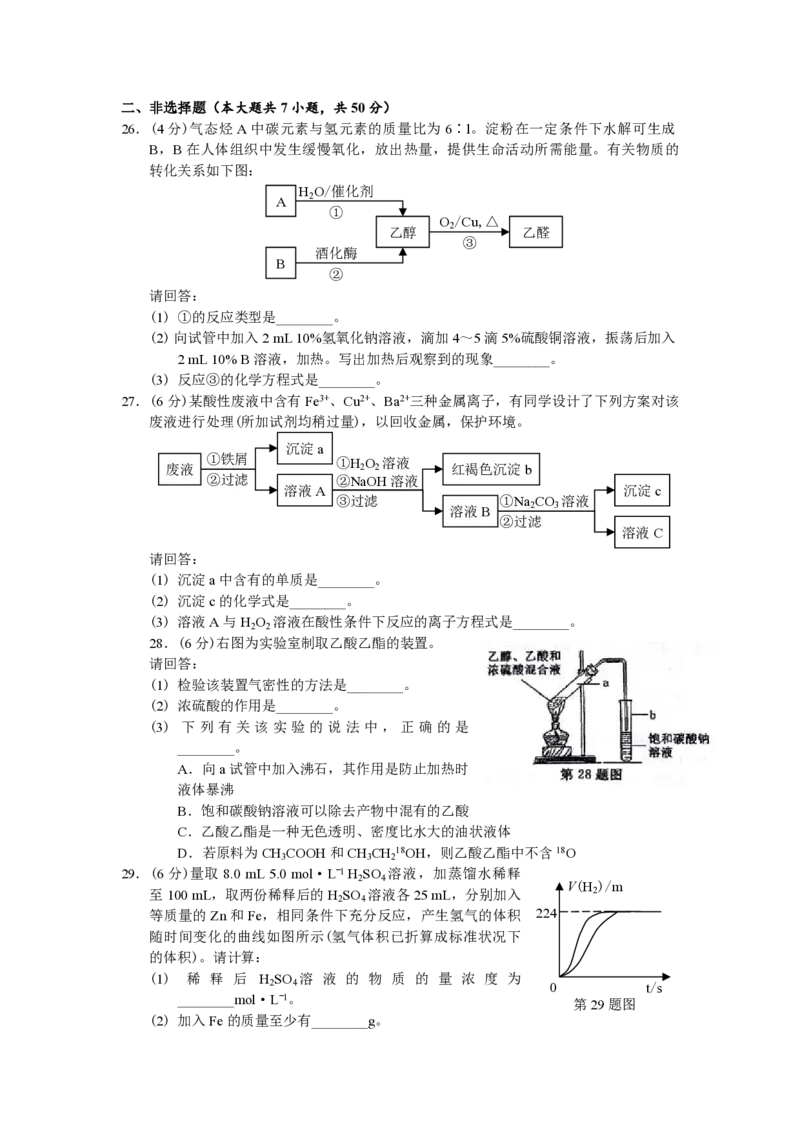
29.(6分)量取 8.0 mL 5.0 mol·Lˉ1H SO 溶液,加蒸馏水稀释
2 4
V(H )/m
至100 mL,取两份稀释后的H SO 溶液各25 mL,分别加入 2
2 4
L
等质量的Zn和Fe,相同条件下充分反应,产生氢气的体积 224
随时间变化的曲线如图所示(氢气体积已折算成标准状况下
的体积)。请计算:
(1) 稀 释 后 H SO 溶 液 的 物 质 的 量 浓 度 为
2 4 0 t/s
________mol·Lˉ1。
第29题图
(2) 加入Fe的质量至少有________g。30.【加试题】(10分)由某精矿石(MCO ·ZCO )可以制备单质M,制备过程中排放出的
3 3
二氧化碳可以作为原料制备甲醇。取该矿石样品1.84 g,高温灼烧至恒重,得到0.96
g仅含两种金属氧化物的固体,其中m(M)∶m(O)=3∶5。请回答:
(1) 该矿石的化学式为________。
(2) ①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单
质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2∶
1)。写出该反应的化学方程式________。
②单质M还可以通过电解熔融MCl 得到。不能用电解MCl 溶液的方法制备M
2 2
的理由是________。
(3) 一定条件下,由CO 和H 制备甲醇的过程中含有下列反应:
2 2
反应1: CO (g)+H (g) CO(g)+H O(g) ΔH
2 2 2 1
反应2: CO(g)+2H (g) CH OH(g) ΔH
2 3 2
反应3: CO (g)+3H (g) CH OH(g)+H O(g) ΔH
2 2 3 2 3
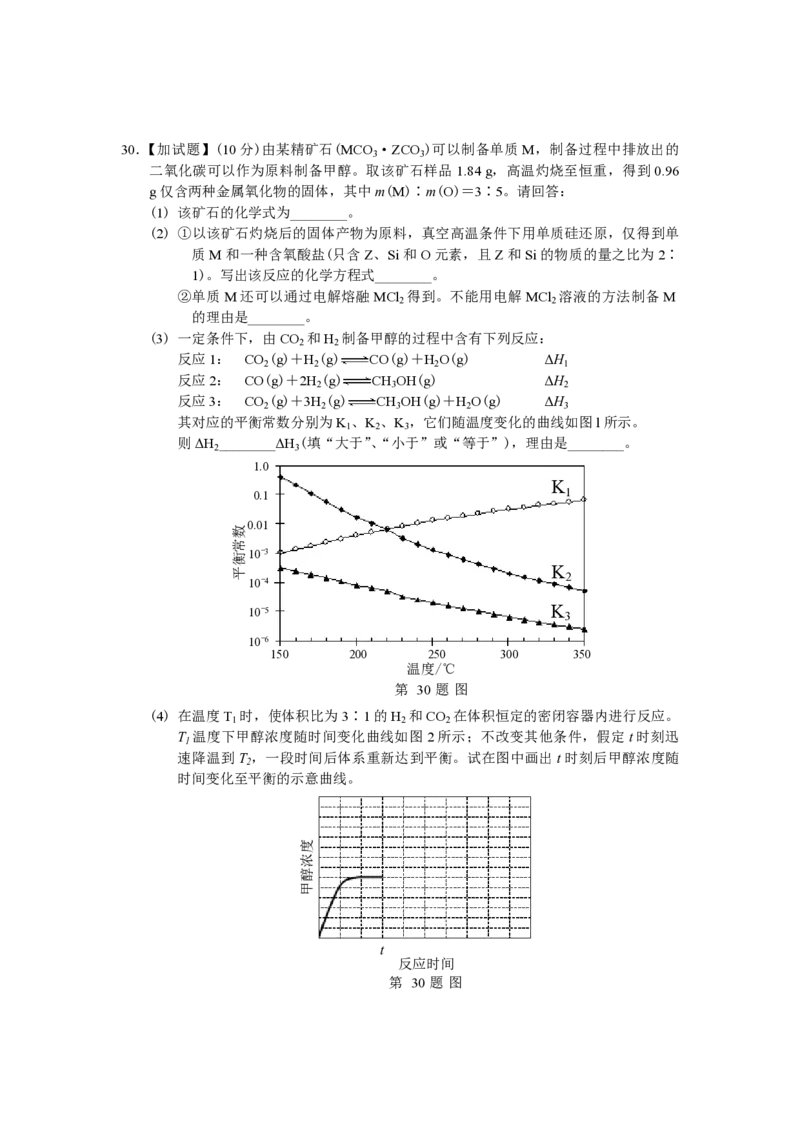
其对应的平衡常数分别为K 、K 、K ,它们随温度变化的曲线如图l所示。
1 2 3
则ΔH ________ΔH (填“大于”、“小于”或“等于”),理由是________。
2 3
1.0
0.1
0.01
10ˉ3
10ˉ4
10ˉ5
10ˉ6
150 200 250 300 350
温度/℃
第 30题 图
1
数常衡平
K
1
K
2
K
3
(4) 在温度T 时,使体积比为3∶1的H 和CO 在体积恒定的密闭容器内进行反应。
1 2 2
T 温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t时刻迅
1
速降温到T ,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随
2
时间变化至平衡的示意曲线。
t
反应时间
第 30题 图
2
度浓醇甲31.【加试题】(10分)纳米CdSe(硒化镉)可用作光学材料。在一定条件下,由Na SO 和
2 3
Se
(硒,与S为同族元素)反应生成Na SeSO (硒代硫酸钠);再由CdCl 形成的配合物与
2 3 2
Na SeSO 反应制得CdSe纳米颗粒。流程图如下:
2 3
NaSO 溶液
2 3 加热回流 抽滤
Na SeSO 溶液
2 3
过量硒粉
调节pH=9~10 避光加热 分离提纯
CdSe纳米颗粒
CdCl 溶液
2
[Cd(L)]Cl 溶液
n 2
配位剂L
注:①CdCl 能与配位剂L形成配合物[Cd(L) ]Cl
2 n 2
[Cd(L) ]Cl =[Cd(L) ]2++2Clˉ;[Cd(L) ]2+ Cd2++nL
n 2 n n
②纳米颗粒通常指平均粒径为1~100nm的粒子
请回答:
(1) 图l加热回流装置中,仪器a的名称是________,进水口为________(填1或2)。
(2) ①分离CdSe纳米颗粒不宜采用抽滤的方法,理由是________。
②有关抽滤,下列说法正确的是________。
A.滤纸应比漏斗内径略小,且能盖住所有小孔
B.图2抽滤装置中只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
C.抽滤得到的滤液应从吸滤瓶的支管口倒出
D.抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒
吸
(3) 研究表明,CdSe的生成分成两步:①SeSO23ˉ在碱性条件下生成HSeˉ;②HSeˉ与
Cd2+反应生成CdSe。
完成第①步反应的离子方程式SeSO23ˉ+________=HSeˉ+________
写出第②步反应的离子方程式________。
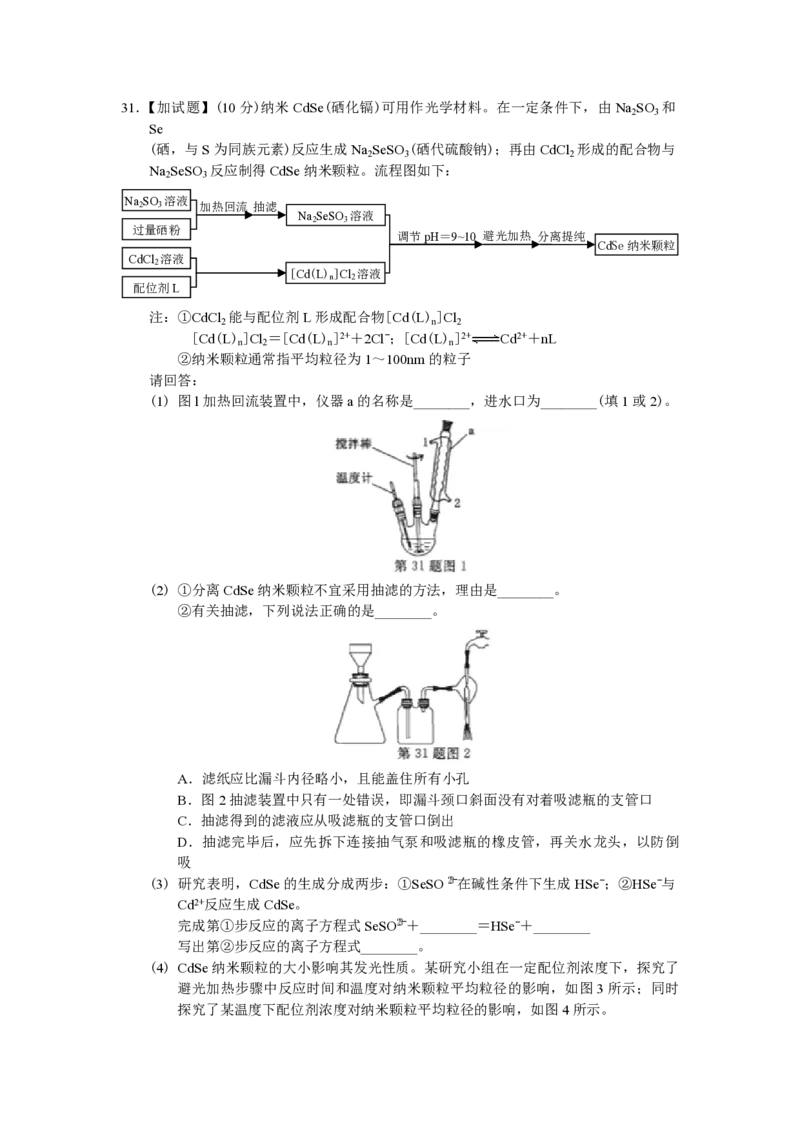
(4) CdSe纳米颗粒的大小影响其发光性质。某研究小组在一定配位剂浓度下,探究了
避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,如图3所示;同时
探究了某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图4所示。3.6
3.4
3.2
3.0
2.8
2.6
2.4
2.2
0 10 20 30 40 50
反应时间/h
第 31题 图
3
mn/径直均平粒颗
100℃ 3.
0
2.
60℃
9
2.
8
0 05 10 15 20
2.
配 位 剂 浓 度
7
/第% 31题 图
2. 4
6
2.
5
mn/径直均平粒颗
下列说法正确的是________。
A.改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒
B.在图3所示的两种温度下,只有60℃反应条件下可得到2.7 nm的CdSe纳米
颗粒
C.在其他条件不变时,若要得到较大的CdSe纳米颗粒,可采用降低温度的方法
D.若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法
32.【加试题】(10分)乙酰基扁桃酰氯是一种医药中间体。某研究小组以甲苯和乙醇为主
要原料,按下列路线合成乙酰基扁桃酰氯。
O
O
CH Cl
3
Cl 2 NaOH/H 2 O O 2 ①NaHSO 3 H 2 O/H+ O
A B C D E
光照 催化剂 ②NaCN SOCl 2
G
F
CH CH OH …… 乙酰基扁桃酰氯
3 2 C H ClO
2 3
H2O/H+
已知:RCHO;RCN ―――→ RCOOH;
SOCl2 R'OH
RCOOH ――→ RCOCl ――→ RCOOR'
请回答:
(1) D的结构简式________。
(2) 下列说法正确的是________。
A.化合物A不能发生取代反应
B.化合物B能发生银镜反应
C.化合物C能发生氧化反应
D.从甲苯到化合物C的转化过程中,涉及到的反应类型有取代反应、加成反应
和氧化反应
(3) E+F→G的化学方程式是________。
(4) 写出化合物D同时符合下列条件的所有可能的同分异构体的结构简式________。
①红外光谱检测表明分子中含有氰基(-CN);
②1H-NMR谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子。
(5) 设计以乙醇为原料制备F的合成路线(用流程图表示;无机试剂任选)________。