文档内容
2015 年普通高等学校招生全国统一考试
浙江卷·理科综合·化学部分
7.下列说法不正确的是
A.液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性
B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关
C.石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化
D.燃料的脱硫脱氮、SO 的回收利用和NO 的催化转化都是减少酸雨产生的措施
2 x
8.下列说法正确的是
A.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 A.在pH=9.0时,c(NH4+)>c(HCOˉ3)>c(NH COOˉ)>c(CO23ˉ)
2
B.做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加 B.不同pH的溶液中存在关系:
热,冷却后补加 c(NH4+)+c(H+)=2c(CO23ˉ)+c(HCOˉ3)+c(NH COOˉ)+c(OHˉ)
2
C.在未知溶液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO24ˉ或SO c(OHˉ)
2 C.随着CO 的通入, 不断增大
23ˉ 2 c(NH3·H2O)
D.提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 D.在溶液中pH不断降低的过程中,有含NH COOˉ的中间产物生成
2
9.右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列
说法正确的是 13.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe O 、SiO 、Al O ,不考虑其他杂质) 制取七水合硫酸亚
X 2 3 2 2 3
A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次 递增 铁(FeSO ·7H O) ,设计了如下流程:
Y Z W 4 2
B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧 化物的水化物的酸性
T 固体1
依次递增 足量酸 NaOH溶液
第9题表 烧渣 固体2
C.YX 晶体熔化、液态WX 气化均需克服分子间作用力 试剂X 控制pH
2 3 溶液1
D.根据元素周期律,可以推测T元素的单质具有半导体特性,T X 具有氧化性和还原性
2 3 溶液2 FeSO ·7H O
4 2
10.下列说法不正确的是 下列说法不正确的是
A.己烷有4种同分异构体,它们的熔点、沸点各不相同 A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 B.固体1中一定含有SiO ,控制pH是为了使Al3+转化为Al(OH) ,进入固体2
2 3
C.油脂皂化反应得到高级脂肪酸盐与甘油 C.从溶液2得到FeSO ·7H O产品的过程中,须控制条件防止其氧化和分解
4 2
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到
D.聚合物(—[CH2—CH2—CH—CH2—]n)可由单体CH CH=CH 和CH =CH 加聚制得
| 3 2 2 2 FeSO ·7H O
CH3 4 2
11.在固态金属氧化物电解池中,高温共电解H O- CO 混合气体制备
2 2
H 和CO是一种新的能源利用方式,基本原理如 图所示。下列说法
2
不正确的是
A.X是电源的负极
B.阴极的反应式是:H O+2eˉ=H +O2ˉ
2 2
CO +2eˉ=CO+O2ˉ
2
C.总反应可表示为:H O+CO H +CO+O
2 2= 2 2
D.阴、阳两极生
成的气体的物质的量之比是1︰1
12.40℃时,在氨-水体系中不断通入CO ,各种离子的变化趋势如下图所示。下列说法不正确的是
226.(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成: Ⅱ.(12分) 化合物甲和NaAlH 都是重要的还原剂。一定条件下金属钠和H 反应生成甲。甲与水反应可产
4 2
生 H ,甲与 AlCl 反应可得到 NaAlH 。将 4.80g甲加热至完全分解,得到金属钠和 2.24 L(已折算成标准状
2 3 4
况) 的H 。
2
请推测并回答:
(1) 甲的化学式__________。
(2) 甲与AlCl 反应得到NaAlH 的化学方程式__________。
3 4
(3) NaAlH 与水发生氧化还原反应的化学方程式__________。
4
(4) 甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O ) 脱锈过程发生的化学方程式
2 3
___________。
(5) 某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠
反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H ,即可证明得到的甲一定是
2
已知:RXROH;RCHO+CH COOR-RCH=CHCOOR’ 纯净的。
3
请回答: 判断该同学设想的制备和验纯方法的合理性并说明理由___________。
(1) E中官能团的名称是 。(2) B+D→F的化学方程式 。 28.(15分)乙苯催化脱氢制苯乙烯反应:
(3) X的结构简式 。
(4) 对于化合物X,下列说法正确的是 。
A.能发生水解反应 B.不与浓硝酸发生取代反应
C.能使Br /CCl 溶液褪色 D.能发生银镜反应 (1)已知:
2 4
(5) 下列化合物中属于F的同分异构体的是 。 化学键 C-H C-C C=C H-H
键能/kJ·molˉ1 412 348 612 436
计算上述反应的△H=________ kJ·mol-1。
A. CH OCH CH CHO
2 2 2
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知
乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________(用α等符号表示)。
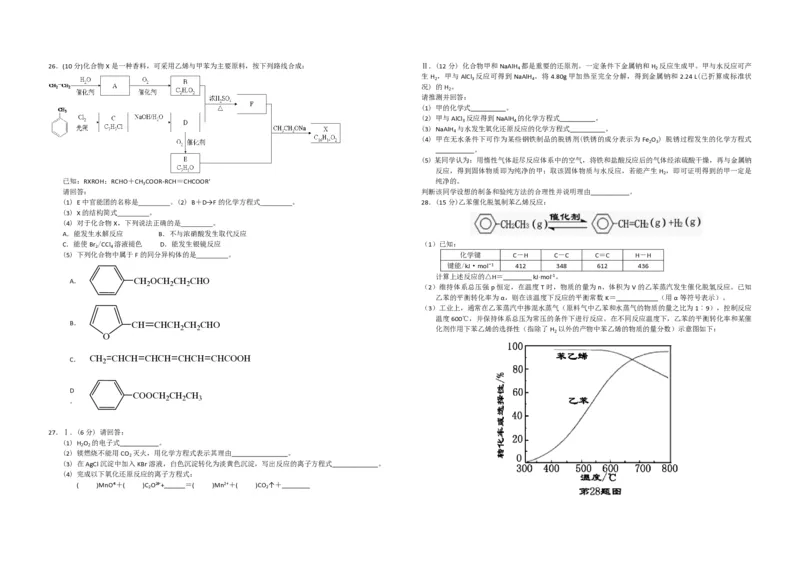
(3)工业上,通常在乙苯蒸汽中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应
温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催
B. CH CHCH CH CHO
2 2 化剂作用下苯乙烯的选择性(指除了H 以外的产物中苯乙烯的物质的量分数)示意图如下:
2
O
C. CH
2
CHCH CHCH CHCH CHCOOH
D
COOCH CH CH
2 2 3
.
27.Ⅰ.(6分) 请回答:
(1) H O 的电子式___________。
2 2
(2) 镁燃烧不能用CO 灭火,用化学方程式表示其理由________________。
2
(3) 在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_____________。
(4) 完成以下氧化还原反应的离子方程式:
( )MnOˉ4+( )C O24ˉ+______=( )Mn2++( )CO ↑+________
2 2①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___________。
②控制反应温度为600℃的理由是____________。
(3)某研究机构用CO 代替水蒸气开发了绿色化学合成工艺----乙苯-二氧化碳耦合催化脱氢制苯乙烯。保
2
持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中
还能够发生反应:CO +H =CO+H O,CO +C=2CO。新工艺的特点有_________(填编号)。
2 2 2 2
①CO 与H 反应,使乙苯脱氢反应的化学平衡右移
2 2
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO 资源利用
2
29.(15分)某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
取0.0100 mol·Lˉ1的AgNO
3
标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测
定碘含量。测的的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表: ②该次滴定终点时用去 AgNO 溶液的体积为 mL,计算得海带中碘的百分含量为
3
V(AgNO )/mL 15.00 19.00 19.80 19.98 20.00 20.02 21.00 23.00 25.00 %。
3
E/mV -225 -200 -150 -100 50.0 175 275 300 325 (3) ①分液漏斗使用前须检漏,检漏方法为 。
实验(二) 碘的制取 ②步骤X中,萃取后分液漏斗内观察到的现象是 。
另制海带浸取原液,甲、乙两种实验方案如下: ③下列有关步骤Y的说法,正确的是 。
A.应控制NaOH溶液的浓度和体积
B.将碘转化呈离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
④实验(二) 中操作Z的名称是 。
(4) 方案甲中采用蒸馏不合理,理由是 。
已知:3I +6NaOH=5NaI+NaIO +3H O
2 3 2
请回答:
(1) 实验(一) 中的仪器名称:仪器A , 仪器 B 。
(2) ①根据表中数据绘制滴定曲线:可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27
S 32 Fe 56 Ag 108 I 127
7.下列说法不正确的是
A.液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性
B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 考点:物质结构 元素周期律
C.石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 10.下列说法不正确的是
D.燃料的脱硫脱氮、SO 的回收利用和NO 的催化转化都是减少酸雨产生的措施 A.己烷有4种同分异构体,它们的熔点、沸点各不相同
2 x
【答案】C B.在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
【解析】 C.油脂皂化反应得到高级脂肪酸盐与甘油
试题分析:C.纳米银粒子的聚集属于物理变化。
D.聚合物(—[CH2—CH2—CH—CH2—]n)可由单体CH CH=CH 和CH =CH 加聚制得
考点:考查液晶的性质、氢键、化学变化、减少酸雨的措施 | 3 2 2 2
CH3
8.下列说法正确的是 【答案】A
A.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 【解析】
B.做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加 试题分析: A.己烷有5种同分异构体,分别是己烷(CH CH CH CH CH CH )、2—甲基戊烷
3 2 2 2 2 3
热,冷却后补加 [(CH ) CH CH CH CH ]、3—甲基戊烷[CH CH CH(CH )CH CH ]、2,3—甲基丁烷[(CH ) CHCH(CH ) ]、2,2—
3 2 2 2 2 3 3 2 3 2 3 3 2 3 2
C.在未知溶液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO 2-或 甲基丁烷[(CH ) CCH CH ],A不正确。
2 4 3 3 2 3
SO 2- 考点:有机物结构与性质 基本营养物质
3
D.提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 11.在固态金属氧化物电解池中,高温共电解H O-CO 混合气体制备H 和CO是一种新的能源利用方式,
2 2 2
【答案】B 基本原理如图所示。下列说法不正确的是
考点:化学实验基本操作 物质检验
9.右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核 电荷数为X元素的2倍。下
列说法正确的是
A.X是电源的负极
X B.阴极的反应式是:H O+2eˉ=H +O2ˉ
2 2
Y Z W CO +2eˉ=CO+
2
T
通电
第9题表 A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 C.总反应可表示为:H 2 O+CO 2 = = = =H 2 +CO+O 2
B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 D.阴、阳两极生成的气体的物质的量之比是1︰1
C.YX 晶体熔化、液态WX 气化均需克服分子间作用力 【答案】D
2 3
D.根据元素周期律,可以推测T元素的单质具有半导体特性,T X 具有氧化性和还原性
2 3
【答案】D固体1
足量酸 NaOH溶液
烧渣 固体2
试剂X 控制pH
溶液1
溶液2 FeSO ·7H O
4 2
下列说法不正确的是
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO
2
,控制pH是为了使Al3+转化为Al(OH)
3
,进入固体2
考点:电化学基础知识 C.从溶液2得到FeSO ·7H O产品的过程中,须控制条件防止其氧化和分解
4 2
12.40℃时,在氨-水体系中不断通入CO ,各种离子的变化趋势如下图所示。下列说法不正确的是 D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到
2
FeSO ·7H O
4 2
【答案】D
考点:离子反应,物质分离、元素及化合物
26.(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
A.在pH=9.0时,c(NH +)>c(HCOˉ3)>c(NH COOˉ)>c(CO 2-)
4 2 3
B.不同pH的溶液中存在关系:c(NH +)+c(H+)=2c(CO 2-)+c(HCO -)+c(NH COOˉ)+c(OHˉ)
4 3 3 2
c(OHˉ)
C.随着CO 的通入, 不断增大
2
c(NH3·H2O)
D.在溶液中pH不断降低的过程中,有含NH COOˉ的中间产物生成
2
【答案】C
NaOH/H2O CH3CH2ONa
已知:RX―――――→ROH;RCHO+CH COOR’――――――→RCH=CHCOOR’
3
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
考点:电解质溶液 (3)X的结构简式 。
13.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe O 、SiO 、Al O ,不考虑其他杂质)制取七水合硫 (4)对于化合物X,下列说法正确的是 。
2 3 2 2 3
酸亚铁(FeSO ·7H O),设计了如下流程: A.能发生水解反应 B.不与浓硝酸发生取代反应
4 2
C.能使Br /CCl 溶液褪色 D.能发生银镜反应
2 4
(5)下列化合物中属于F的同分异构体的是 。【答案】(1)醛基 (2)
(3) (4)AC (5)BC
考点:化学基本概
念、离子反应、氧化还原反应
Ⅱ.(12分) 化合物甲和NaAlH 都是重要的还原剂。一定条件下金属钠和H 反应生成甲。甲与水反应可产生
4 2
H ,甲与AlCl 反应可得到NaAlH 。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)
2 3 4
的H 。
2
请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl 反应得到NaAlH 的化学方程式__________。
3 4
(3)NaAlH 与水发生氧化还原反应的化学方程式__________。
4
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O ),脱锈过程发生反应的
2 3
。
考点:有机合成与有 (5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属
机推断
钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H ,即可证明得到的甲一定
2
27.Ⅰ.(6分) 请回答:
是纯净的。
(1)H O 的电子式___________。
2 2
判断该同学设想的制备和验纯方法的合理性并说明理由___________。
(2)镁燃烧不能用CO 灭火,用化学方程式表示其理由________________。
2
【答案】(12分)(1)NaH (2) 4NaH+AlCl ==NaAlH +3NaCl
3 4
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(3) NaAlH +2H O==NaAlO +4H ↑ (4) 3NaH+Fe O ==2Fe+3NaOH
4 2 2 2 2 3
_____________。
(5) 制备过程不合理,因为盐酸易挥发,H
2
中混有HCl,导致产物中有NaCl
验纯方法不合理,如果有Na残留,Na与水反应也产生H ;没有考虑混入的NaCl
2
(4)完成以下氧化还原反应的离子方程式:
【解析】
( )MnO -+( )C O 2-+______=( )Mn2++( )CO ↑+________
4 2 4 2
【答案】(6分) (1) (2)
(3) AgCl + Br-== AgBr + Cl-
(4) 2MnO - + 5C O 2- + 16H+ == 2Mn2+ + 10CO ↑+ 8H O
4 2 4 2 2① CO 与H 反应,使乙苯脱氢反应的化学平衡右移
2 2
② 不用高温水蒸气,可降低能量消耗
③ 有利于减少积炭
④ 有利于CO 资源利用
2
2 n2
【答案】(15分)(1)124 (2) K p或K
p 12 c (12)V
(3) ① 正反应方向气体分子数增加,加入水蒸气起稀释,相当于起减压的效果
②600℃时,乙苯的转化率和苯乙烯的选择性均较高。温度过低,反应速率慢,转化率低;温度过高,
选择性下降。高温还可能使催化剂失活,且能耗大
(4) ①②③④
考点:元素及化合物
28.(15分)乙苯催化脱氢制苯乙烯反应:
(1)已知:
化学键 C-H C-C C=C H-H
键能/kJ·molˉ1 412 348 612 436
计算上述反应的△H=________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知
乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________ (用α等符号表示)。
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温
度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化
剂作用下苯乙烯的选择性(指除了H 以外的产物中苯乙烯的物质的量分数)示意图如下:
2
性下降。高温还可能使催化剂失活,且能耗大。(4) ①乙苯催化脱氢制苯乙烯反应为可逆反应,CO 与H
2 2
反应,可使生成物浓度减小,化学平衡右移;②不用高温水蒸气,必然降低能耗;③由于发生反应
CO +C=2CO,可减少积炭;④CO 得到有效利用,可减少 CO 排放并作为资源得到利用。故选择
2 2 2
①②③④。
考点:化学反应与能量 化学反应速率 化学平衡
29.(15分)某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___________。
②控制反应温度为600℃的理由是____________。 取0.0100 mol·Lˉ1的AgNO
3
标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含
(4)某研究机构用CO 代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。 量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
2
保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺 V(AgNO )/mL 15.00 19.00 19.80 19.98 20.00 20.02 21.00 23.00 25.00
3
中还能够发生反应:CO +H =CO+H O,CO +C=2CO。新工艺的特点有_________(填编号)。 E/mV -225 -200 -150 -100 50.0 175 275 300 325
2 2 2 2实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
已知:3I +6NaOH=5NaI+NaIO +3H O。
2 3 2
【答案】(1)坩埚 500mL容量瓶 (2) ① ② 20.00mL
请回答:
(1)实验(一) 中的仪器名称:仪器A , 仪器 B 。 0.635% (3)①向分液漏斗中加入少量水,检查旋塞处是否漏水;将漏斗倒转过来,检查玻璃塞是
(2)①根据表中数据绘制滴定曲线: 否漏水 ②液体分上下两层,下层呈紫红色 ③AB ④过滤 (4)主要由于碘易升华,会
导致碘的损失
②该次滴定终点时用去AgNO 溶液的体积为 mL,计算得海带中碘的百分含量为 %。
3
(3)①分液漏斗使用前须检漏,检漏方法为 。
②步骤X中,萃取后分液漏斗内观察到的现象是 。
③下列有关步骤Y的说法,正确的是 。
A.应控制NaOH溶液的浓度和体积 考点:定量实验 实验设计与评价
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
④实验(二) 中操作Z的名称是 。
(4)方案甲中采用蒸馏不合理,理由是 。