文档内容
绝密★启封并使用完毕前
2016 年普通高等学校招生全国统一考试
理科综合能力测试(化学)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
2.答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。
3.全部答案在答题卡上完成,答在本试题上无效。
4.考试结束后,将本试题和答题卡一并交回。
第Ⅰ卷
(选择题共126分)
本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:
一、选择题:本大题共13小题,每小题6分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
7.下列关于燃料的说法错误的是
A.燃料燃烧产物CO 是温室气体之一
2
B.化石燃料完全燃烧不会造成大气污染
C.以液化石油气代替燃油可减少大气污染
D.燃料不完全燃烧排放的CO是大气污染物之一
8.下列各组中的物质均能发生就加成反应的是
A.乙烯和乙醇
B.苯和氯乙烯
C.乙酸和溴乙烷
D.丙烯和丙烷
9.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+的电子层结构相同,d与b同族。下列叙
述错误的是学.科.网
A.a与其他三种元素形成的二元化合物中其化合价均为+1
B.b与其他三种元素均可形成至少两种二元化合物
C.c的原子半径是这些元素中最大的
D.d与a形成的化合物的溶液呈弱酸性
10.分子式为C HCl 的有机物共有(不含立体异构)
4 8 2
A.7种 B.8种 C.9种 D.10种
11.Mg–AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A.负极反应式为Mg–2e–=Mg2+B.正极反应式为Ag+ e–=Ag
+
C.电池放电时Cl–由正极向负极迁移
D.负极会发生副反应Mg+2H O=Mg(OH) +H ↑
2 2 2
12.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解:再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,震荡后仍有固体存在。
该白色粉末可能为
A.NaHCO 、Al(OH) B.AgCl、NaHCO C.Na SO 、BaCO D.NaCO、CuSO
3 3 3 2 3 3 2 3 4
13.下列实验操作能达到实验目的的是
实验目的 实验操作
A. 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和FeCl 溶液中
3 3
B. 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C. 除去Cu粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥
D. 比较水与乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
第II卷
(非选择题共174分)
三、非选择题:包括必考题和选考题两部分。第 22题~第32题为必考题,每个试题考生都必
须做答。第33题~第40题为选考题,考生根据要求做答。
26.(14分)
联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
2 4
(1)联氨分子的电子式为_______,其中氮的化合价为_________。
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_________。
(3)①2O(g)+N(g)==N O(l) ΔH
2 2 2 4 1
②N(g)+2H(g)==N H(l) ΔH
2 2 2 4 2
③O(g)+2H(g)==2H O(g) ΔH
2 2 2 3
④2NH(l)+N O(l)==3N(g)+4HO(g)ΔH=-1048.9 kJ·mol-1
2 4 2 4 2 2 4
上述反应热效应之间的关系式为ΔH=_______,联氨和NO 可作为火箭推进剂的主要原因为________。
4 2 4
(4)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为_____(已知:
NH+H+ NH+的K=8.7×107;K =1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为________。
2 4 2 5 w
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是_______。联
氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1 kg的联氨可除去水中溶解的O_______kg;
2
与使用NaSO 处理水中溶解的O 相比,联氨的优点是_____。学科&网
2 3 2
27.(14分)
丙烯腈(CH=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产。主要副产物有丙烯
2
醛(CH=CHCHO)和异径(CHCN)和副产物丙烯醛(C HO)的热化学方程式如下:
2 3 3 4
①C H(g)+NH(g)+ O(g) C HN(g)+3H O(g)ΔH = −515 kJ·mol−1
3 6 3 2 3 3 2
②C H(g)+O(g) C HO(g)+H O(g)ΔH = −353 kJ·mol−1
3 6 2 3 4 2
两个反应在热力学上趋势均很大,其原因是__________;有利于提高丙烯腈平衡产率的反应条件是
_____________;提高丙烯腈反应选择性的关键因素是___________。
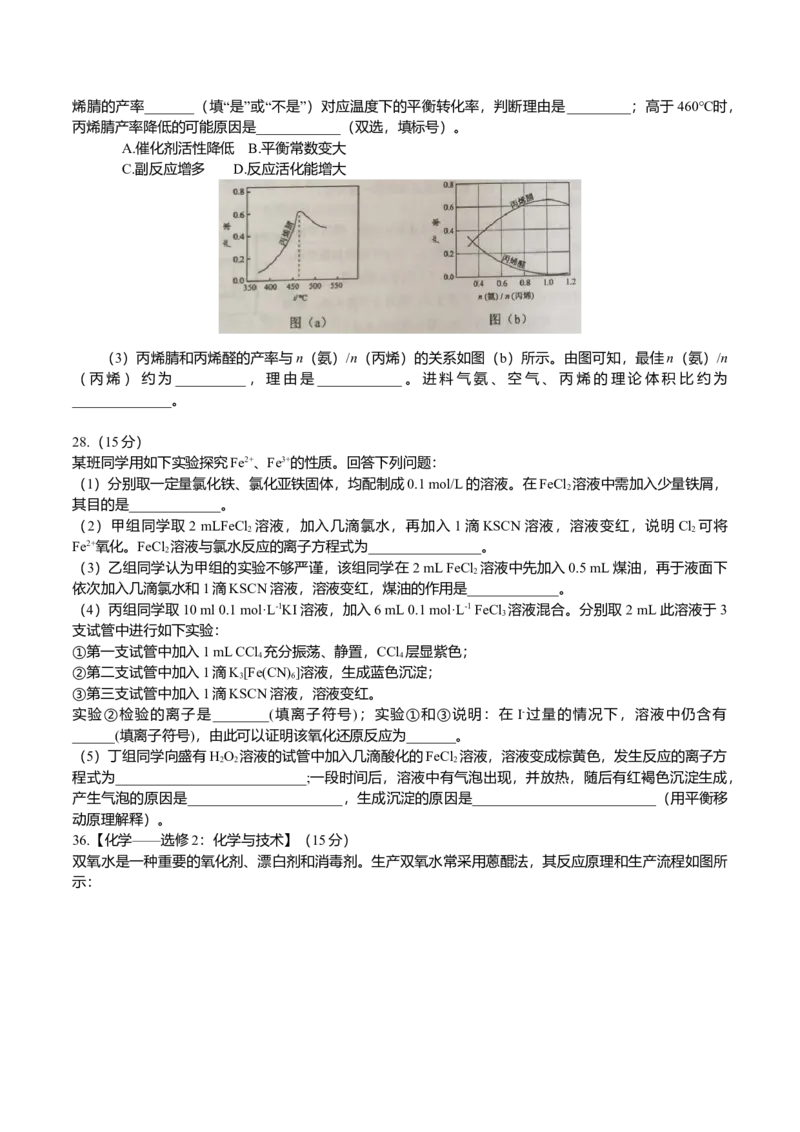
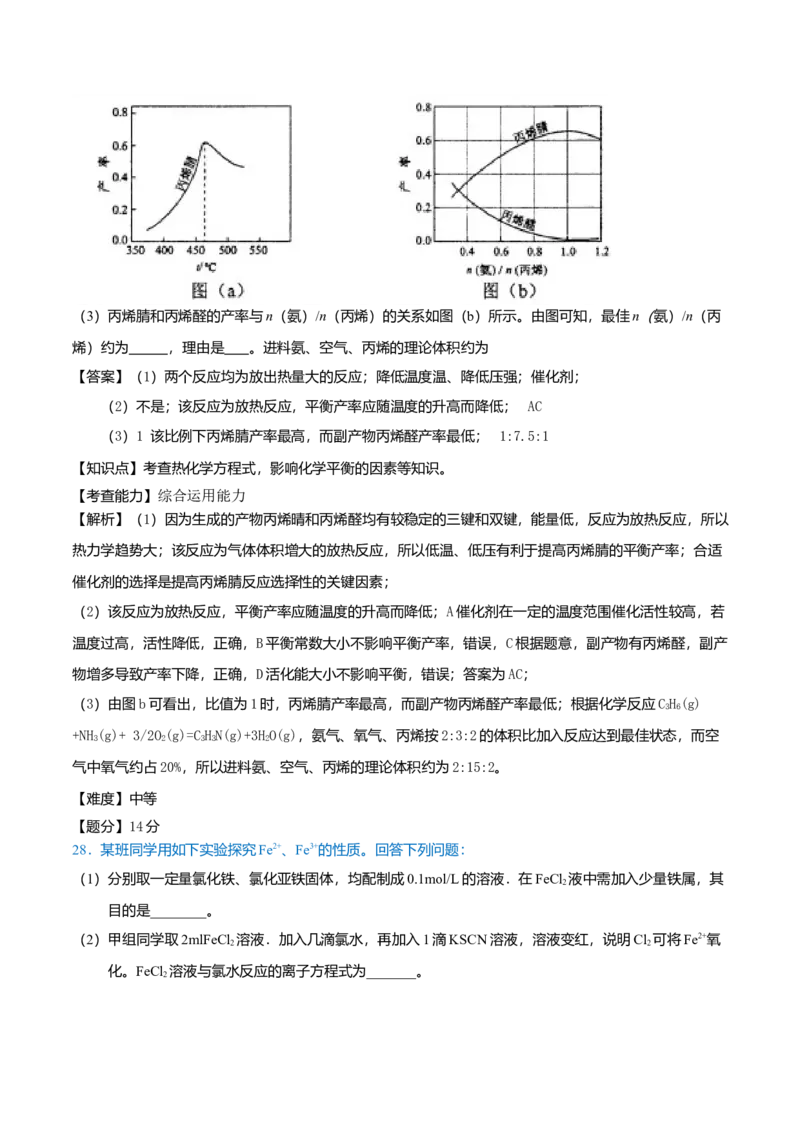
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃。低于460℃时,丙烯腈的产率_______(填“是”或“不是”)对应温度下的平衡转化率,判断理由是_________;高于460℃时,
丙烯腈产率降低的可能原因是____________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大
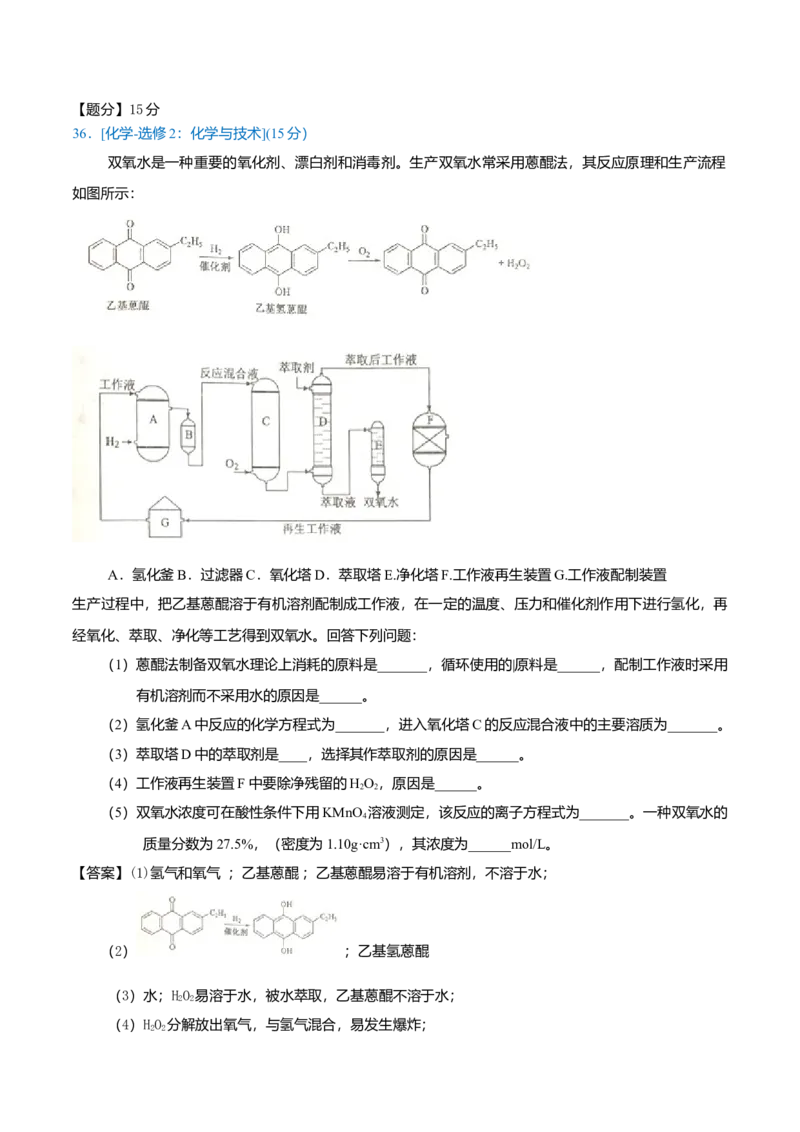
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n
(丙烯)约为__________,理由是____________。进料气氨、空气、丙烯的理论体积比约为
______________。
28.(15分)
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl 溶液中需加入少量铁屑,
2
其目的是_____________。
(2)甲组同学取2 mLFeCl 溶液,加入几滴氯水,再加入 1滴KSCN溶液,溶液变红,说明Cl 可将
2 2
Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为________________。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在 2 mL FeCl 溶液中先加入0.5 mL 煤油,再于液面下
2
依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________。
(4)丙组同学取10 ml 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl 溶液混合。分别取 2 mL 此溶液于3
3
支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在 I-过量的情况下,溶液中仍含有
______(填离子符号),由此可以证明该氧化还原反应为_______。
(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生反应的离子方
2 2 2
程式为___________________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,
产生气泡的原因是______________________,生成沉淀的原因是__________________________(用平衡移
动原理解释)。
36.【化学——选修2:化学与技术】(15分)
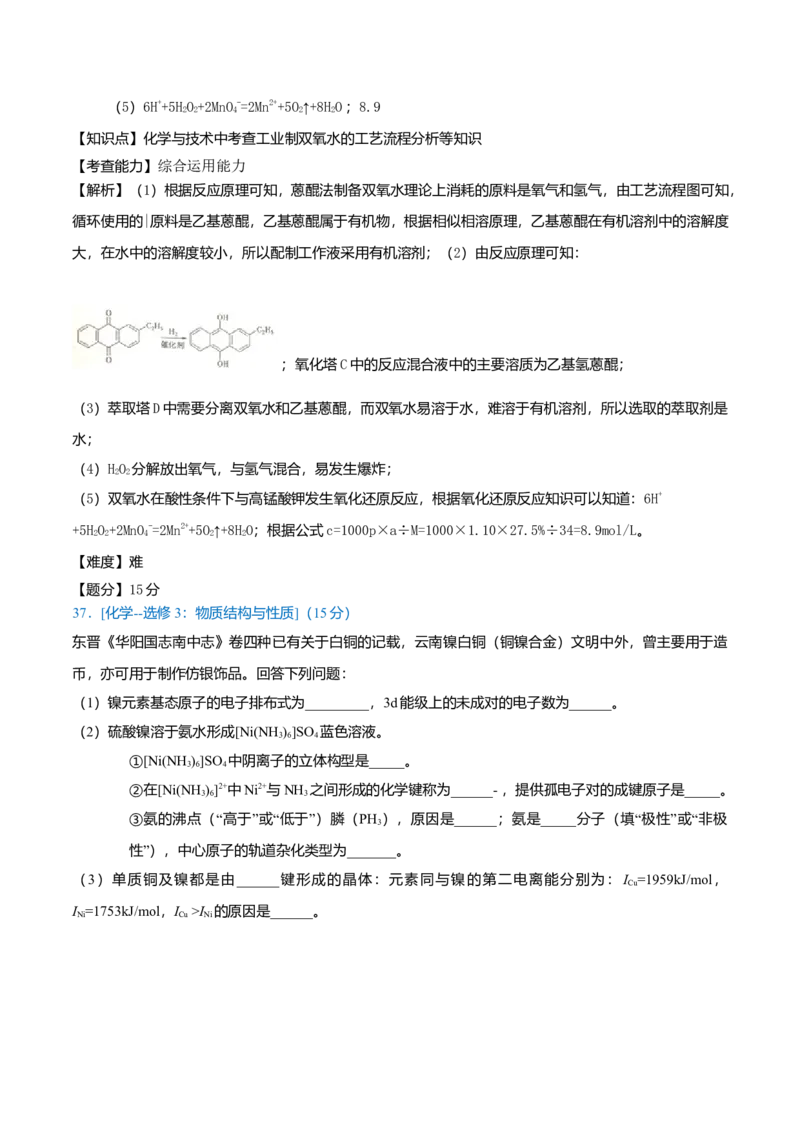
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所
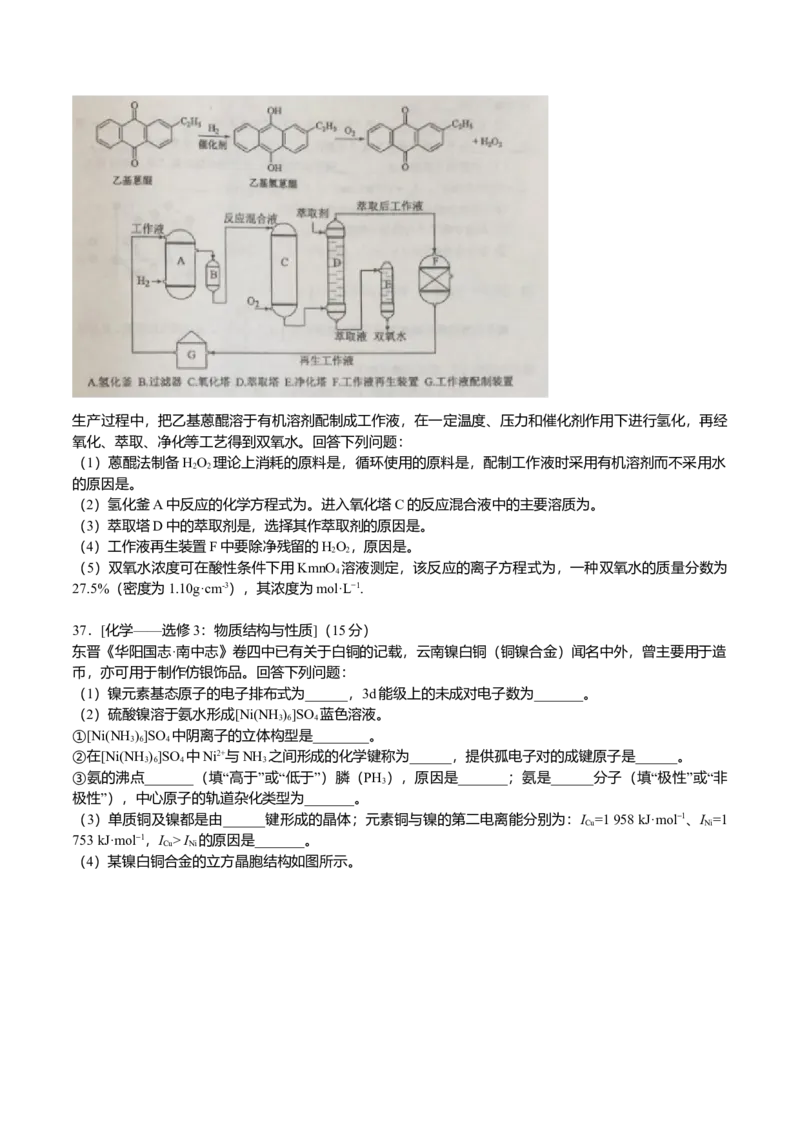
示:生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定温度、压力和催化剂作用下进行氢化,再经
氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备HO 理论上消耗的原料是,循环使用的原料是,配制工作液时采用有机溶剂而不采用水
2 2
的原因是。
(2)氢化釜A中反应的化学方程式为。进入氧化塔C的反应混合液中的主要溶质为。
(3)萃取塔D中的萃取剂是,选择其作萃取剂的原因是。
(4)工作液再生装置F中要除净残留的HO,原因是。
2 2
(5)双氧水浓度可在酸性条件下用KmnO 溶液测定,该反应的离子方程式为,一种双氧水的质量分数为
4
27.5%(密度为1.10g·cm-3),其浓度为mol·L−1.
37.[化学——选修3:物质结构与性质](15分)
东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造
币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______,3d能级上的未成对电子数为_______。
(2)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液。
3 6 4
①[Ni(NH )]SO 中阴离子的立体构型是________。
3 6 4
②在[Ni(NH )]SO 中Ni2+与NH 之间形成的化学键称为______,提供孤电子对的成键原子是______。
3 6 4 3
③氨的沸点_______(填“高于”或“低于”)膦(PH ),原因是_______;氨是______分子(填“极性”或“非
3
极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体;元素铜与镍的第二电离能分别为:I =1 958 kJ·mol–1、I =1
Cu Ni
753 kJ·mol–1,I > I 的原因是_______。
Cu Ni
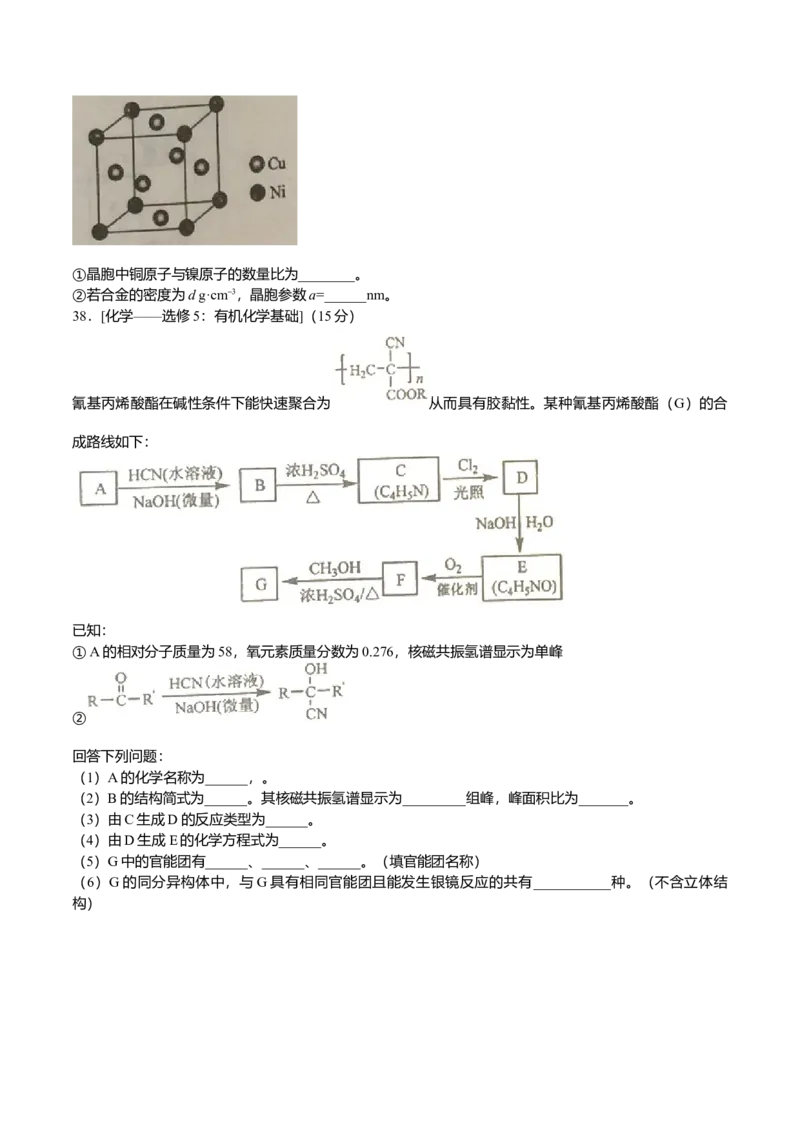
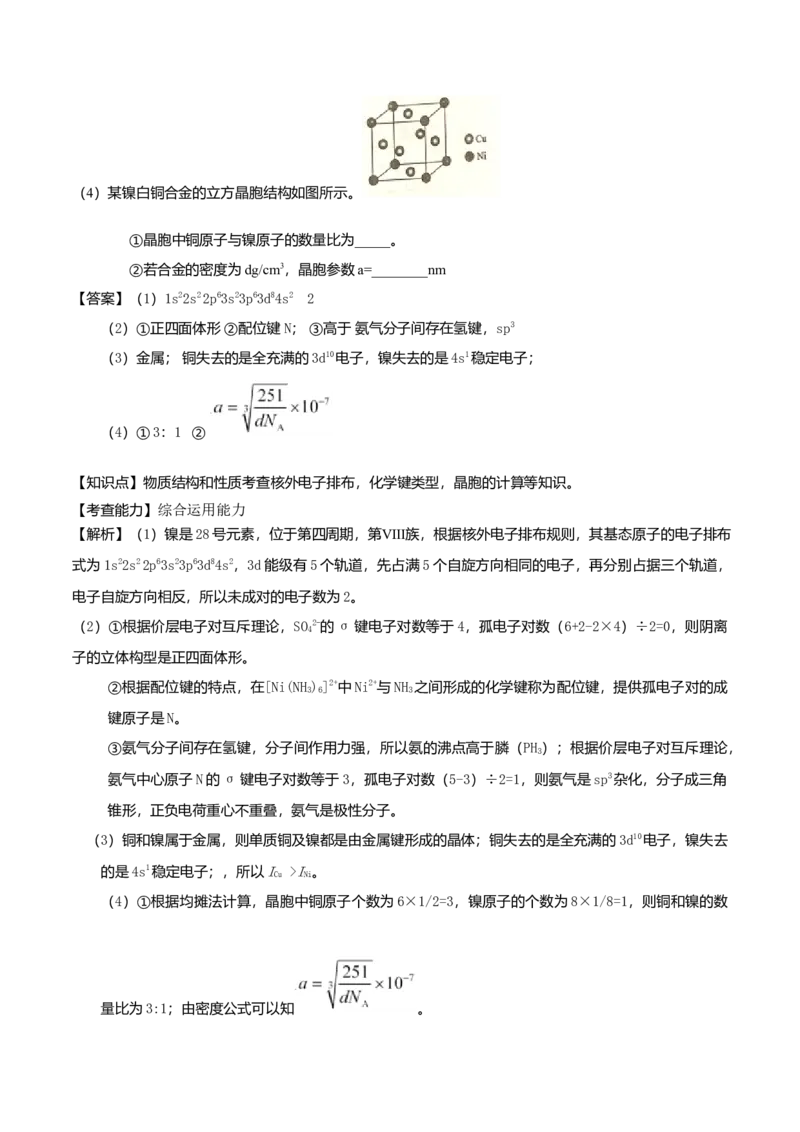
(4)某镍白铜合金的立方晶胞结构如图所示。①晶胞中铜原子与镍原子的数量比为________。
②若合金的密度为d g·cm–3,晶胞参数a=______nm。
38.[化学——选修5:有机化学基础](15分)
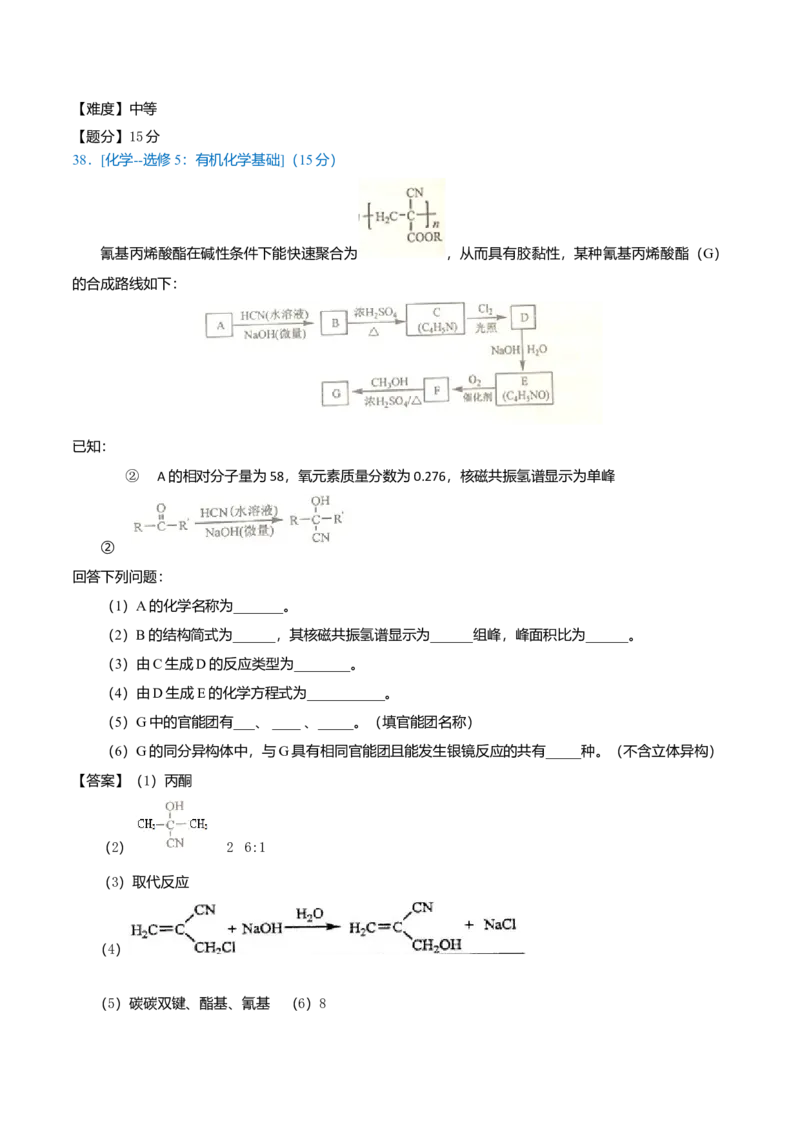
氰基丙烯酸酯在碱性条件下能快速聚合为 从而具有胶黏性。某种氰基丙烯酸酯(G)的合
成路线如下:
已知:
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A 的化学名称为______,。
(2)B的结构简式为______。其核磁共振氢谱显示为_________组峰,峰面积比为_______。
(3)由C生成D的反应类型为______。
(4)由D生成E的化学方程式为______。
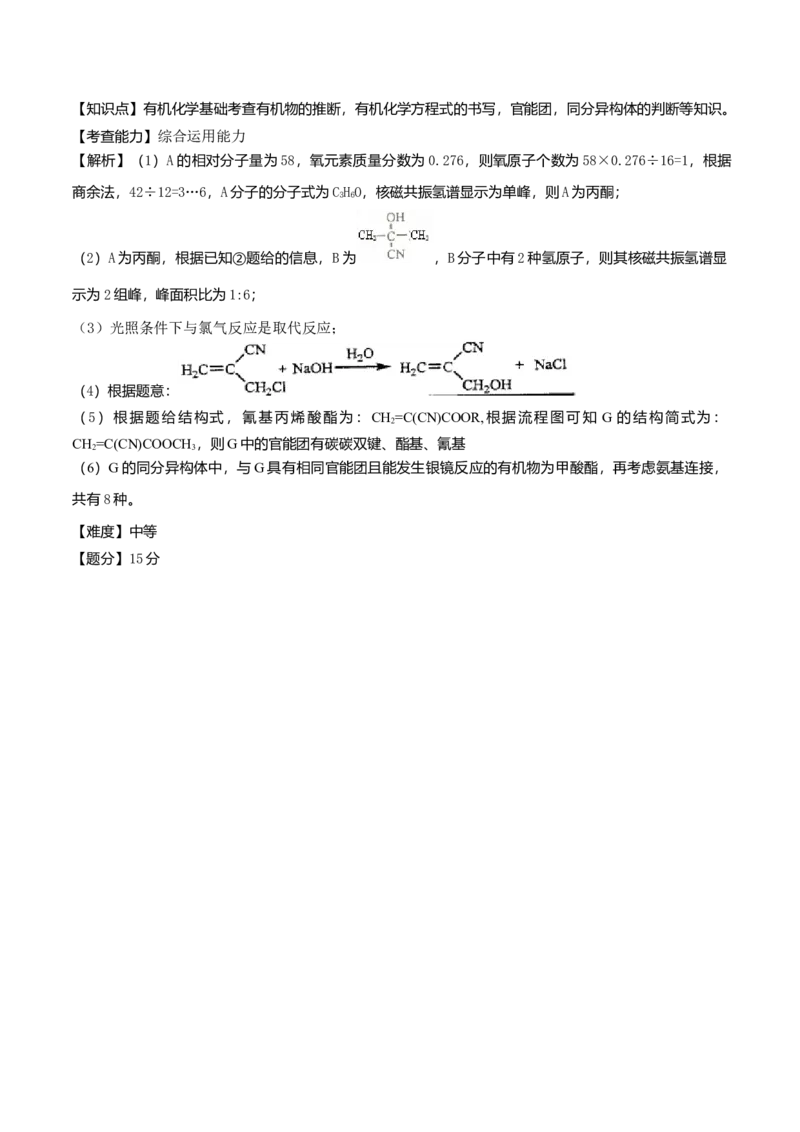
(5)G中的官能团有______、______、______。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有___________种。(不含立体结
构)2016年普通高等学校招生全国统一考试 (全国Ⅱ卷) 理综化学
第Ⅰ卷
7.下列有关燃料的说法错误的是
A.燃料燃烧产物CO 是温室气体之一
2
B.化石燃料完全燃烧不会造成大气污染
C.以液化石油气代替燃油可减少大气污染
D.燃料不完全燃烧排放的CO是大气污染物之一
【答案】B
【知识点】考查燃料燃烧,环境污染与防治等知识
【考查能力】获取信息的能力
【解析】化学燃料完全燃烧生成的二氧化碳会导致温室效应,另外也会产生其他污染气体,答案选B
【难度】简单
【题分】6分
8.下列各组中的物质均能发生加成反应的是
A.乙烯和乙醇 B.苯和氯乙烯 C.乙酸和溴乙烷 D.丙烯和丙烷
【答案】B
【知识点】考查有机反应类型
【考查能力】理解能力
【解析】苯和氯乙烯中均含有不饱和键,能与氢气发生加成反应,乙醇、溴乙烷和丙烷分子 中均是饱和键,
只能发生取代反应,不能发生加成反应,答案选B
【难度】简单
【题分】6分
9.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和C+离子的电子层结构相同,d与b同族。下
列叙述错误的是A.a与其他三种元素形成的二元化合物中其化合价均为+1
B.b与其他三种元素均可形成至少两种二元化合物
C.c的原子半径是这些元素中最大的
D.d和a形成的化合物的溶液呈弱酸性
【答案】A
【知识点】元素的推断,元素周期律的应用等知识
【考查能力】综合运用能力
【解析】a的原子中只有1个电子,则a为氢元素,a、b、c、d为短周期元素,b2-和C+离子的电子层结构
相同,则b为氧元素,C为Na元素,d与b同族,则d为硫元素,据此解答。A. H与O、S形成化合物
为HO和HS,氢元素的化合价为+1,而NaH中氢元素的化合价为-1价,A项错误;B.氧元素与其他元
2 2
素能形成HO、HO、SO、SO、NaO、NaO ,B项正确;C.同周期元素,从左到右原子半径逐渐减小,
2 2 2 2 3 2 2 2
电子层数越多,原子半径越大,原子半径:Na>S>O>H,C项正确;D.d和a形成的化合物为HS,硫化
2
氢的溶液呈弱酸性,D项正确;答案选A
【难度】中等
【题分】6分
10.分子式为CHCl 的有机物共有(不含立体异构)
4 8 2
A. 7种 B.8种 C.9种 D.10种
【答案】C
【知识点】同分异构体的判断
【考查能力】综合运用能力
【解析】根据同分异构体的书写方法,一共有9种,分别为1,2-二氯丁烷;1,3-二氯丁烷;1,4-二氯
丁烷;1,1-二氯丁烷;2,2-二氯丁烷;2,3-二氯丁烷;2-甲基-1,1-二氯丙烷;2-甲基-1,2-二
氯丙烷;2-甲基-1,3-二氯丙烷。答案选C
【难度】中等
【题分】6分
11.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2HO=Mg(OH)+H↑
2 2 2
【答案】B
【知识点】原电池的工作原理【考查能力】理解能力
【解析】由题意,电池总反应式为:Mg+2AgCl=MgCl+2Ag,正极反应为:2AgCl+2e-= 2Cl-+ 2Ag,负极反应
2
为:Mg-2e-=Mg2+,A项正确,B项错误;对原电池来说,阴离子由正极移向负极,C项正确;由于镁
是活泼金属,则负极会发生副反应Mg+2HO=Mg(OH)+H↑,D项正确;答案选B
2 2 2
【难度】中等
【题分】6分
12.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。该白色粉末可能为
A. NaHCO、Al(OH) B.AgCl、NaHCO C.NaSO 、BaCO D.NaCO、CuSO
3 3 3 2 3 3 2 3 4
【答案】C
【知识点】物质的推断和性质
【考查能力】实验与探究能力
【解析】A. NaHCO 、Al(OH) 中加入足量稀硫酸有气泡产生,生成硫酸钠、硫酸铝、二氧化碳和水,最终
3 3
无固体存在,A项错误;B.AgCl不溶于酸,固体不能全部溶解,B项错误;C.亚硫酸钠和碳酸钡溶于
水,碳酸钡不溶于水使部分固体不溶解,加入稀盐酸,碳酸钡与盐酸反应生成氯化钡、二氧化碳和水,
固体全部溶解,再将样品加入足量稀硫酸,稀硫酸和碳酸钡反应生成硫酸钡沉淀和二氧化碳和水,符
合题意,C项正确;D. NaCO、CuSO 中加热足量稀硫酸,振荡后无固体存在,D项错误;答案选C。
2 3 4
【难度】中等
【题分】6分
13. 列实验操作能达到实验目的的是
实验目的 实验操作
A 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和的FeCl 溶液中
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C 除去Cu粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥
D 比较水和乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
【答案】D
【知识点】考查化学实验基本操作。
【考查能力】实验与探究能力
【解析】A.向沸水中滴入饱和氯化铁溶液制备氢氧化铁胶体,A项错误;B.氯化镁是强酸弱碱盐,MgCl 溶
2
液水解产生的HCl易挥发,所以由MgCl 溶液制备无水MgCl 要在HCl气流中加热蒸干,B项错误;C.铜与稀
2 2
硝酸反应,应该用稀盐酸,C项错误;D. 分别将少量钠投入到盛有水和乙醇的烧杯中,反应剧烈的是水,
反应平缓的是乙醇,利用此反应比较水和乙醇中氢的活泼性,D项正确;答案选D。【难度】中等
【题分】6分
第Ⅱ卷
26.联氨(又称联肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
2 4
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O(g)+N(g)=NO(l) △H
2 2 2 4 1
②N(g)+2H(g)=NH(l) △H
2 2 2 4 2
③O(g)+2H(g)=2HO(g) △H
2 2 2 3
④2 NH(l) + NO(l)= 3N(g)+ 4HO(g) △H=-1048.9kJ/mol
2 4 2 4 2 2 4
上述反应热效应之间的关系式为△H=________________,联氨和NO 可作为火箭推进剂的主要原因为
4 2 4
_________________________________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为
___________________(已知:NH+H+ NH+的K=8.7×107;K =1.0×10-14)。联氨与硫酸形成的酸式盐
2 4 2 5 W
的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 。联氨
可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O kg;与使
2
用NaSO 处理水中溶解的O 相比,联氨的优点是 。
2 3 2
【答案】(1) -2价
;
(2)NaClO+2NH=NH+NaCl+HO (3)△H=2△H-2△H-△H ;反应放热量大,产生大量气体;
3 2 4 2 4 3 2 1
(4)8.7×10-7,NH(HSO)
2 6 4 2
(5)固体逐渐变黑,并有气泡产生; 1 NH 的用量少,不产生其他杂质(氧化产物为N,对环境无污染,
2 4 2
而NaSO 的氧化产物为NaSO);
2 3 2 4
【知识点】考查电子式,化合价,盖斯定律的应用,弱电解质的电离、氧化还原反应、化学计算等知识。
【考查能力】综合运用能力
【解析】(1)联氨是有两种非金属元素构成的共价化合物,电子式为 ,根据化合价代数和
为零,氮化合价为-2价;
(2)次氯酸钠溶液与氨气反应制备联氨,根据氧化还原反应的规律,可得到NaClO+2NH=NH+NaCl+HO ;
3 2 4 2
(3)根据盖斯定律,反应热之间的关系为△H=2△H-2△H-△H ;联胺有强还原性,NO 有强氧化性,两者在
4 3 2 1 2 4
一起易发生自发地氧化还原反应,产生大量热和气体,所有联氨和NO 可以作为火箭推进剂。
2 4
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,则联氨第一步电离的方程式为NH+HO NH+
2 4 2 2 5
+OH-,已知:NH+H+ NH+的K=8.7×107;K=1.0×10-14,平衡常数K=8.7×107×1.0×10-14=8.7×10-7
2 4 2 5 W
;联氨为二元弱碱,酸碱发生中和反应生成盐,则联氨与硫酸形成酸式盐的化学式为NH(HSO)。
2 6 4 2
(5)联氨是一种常用的还原剂,AgBr具有氧化性,两者发生氧化还原反应生成银,则向装有少量AgBr的
试管中加入联氨溶液,可观察到固体变黑,并且有气泡产生;联氨可用于处理高压锅炉水中的氧,防止锅
炉被腐蚀,发生的反应为NH+O=N+2HO,理论上1kg的联氨可除去水中溶解的氧气为1kg÷32g/
2 4 2 2 2
mol×32g/moL=1kg;与使用NaSO 处理水中溶解的O 相比,联氨的优点是氧化产物为N,对环境无污染,
2 3 2 2
而NaSO 的氧化产物为NaSO,易生成硫酸盐沉淀,影响锅炉的安全使用。
2 3 2 4
【难度】中等
【题分】14分
27.丙烯腈(CH=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛
2
(CH=CHCHO)和乙腈CHCN等,回答下列问题:
2 3
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(CHN)和副产物丙烯醛(CHO)的热化学
3 3 3 4
方程式如下:
①CH(g)+NH(g)+ 3/2O(g)=CHN(g)+3HO(g) △H=-515kJ/mol
3 6 3 2 3 3 2
CH(g)+ O(g)=CHO(g)+HO(g) △H=-353kJ/mol
3 6 2 3 4 2
两个反应在热力学上趋势均很大,其原因是 ;有利于提高丙烯腈平衡产率的反应条件是 ;提高丙
烯腈反应选择性的关键因素是 。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460OC.低于460OC时,丙烯腈的
产率 (填“是”或者“不是”)对应温度下的平衡产率,判断理由是 ;高于460OC时,丙烯腈产率降低的
可能原因是 (双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙
烯)约为 ,理由是 。进料氨、空气、丙烯的理论体积约为
【答案】(1)两个反应均为放出热量大的反应;降低温度温、降低压强;催化剂;
(2)不是;该反应为放热反应,平衡产率应随温度的升高而降低; AC
(3)1 该比例下丙烯腈产率最高,而副产物丙烯醛产率最低; 1:7.5:1
【知识点】考查热化学方程式,影响化学平衡的因素等知识。
【考查能力】综合运用能力
【解析】(1)因为生成的产物丙烯晴和丙烯醛均有较稳定的三键和双键,能量低,反应为放热反应,所以
热力学趋势大;该反应为气体体积增大的放热反应,所以低温、低压有利于提高丙烯腈的平衡产率;合适
催化剂的选择是提高丙烯腈反应选择性的关键因素;
(2)该反应为放热反应,平衡产率应随温度的升高而降低;A催化剂在一定的温度范围催化活性较高,若
温度过高,活性降低,正确,B平衡常数大小不影响平衡产率,错误,C根据题意,副产物有丙烯醛,副产
物增多导致产率下降,正确,D活化能大小不影响平衡,错误;答案为AC;
(3)由图b可看出,比值为1时,丙烯腈产率最高,而副产物丙烯醛产率最低;根据化学反应CH(g)
3 6
+NH(g)+ 3/2O(g)=CHN(g)+3HO(g),氨气、氧气、丙烯按2:3:2的体积比加入反应达到最佳状态,而空
3 2 3 3 2
气中氧气约占20%,所以进料氨、空气、丙烯的理论体积约为2:15:2。
【难度】中等
【题分】14分
28.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl 液中需加入少量铁属,其
2
目的是________。
(2)甲组同学取2mlFeCl 溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将Fe2+氧
2 2
化。FeCl 溶液与氯水反应的离子方程式为_______。
2(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl 溶液中先加入0.5ml煤油,再于液面下依
2
次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是______。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl 溶液混合。分别取2mL此溶液于3 支试
3
管中进行如下实验:
① 第一支试管中加入1mLCCl 充分振荡、静置,CCl 层呈紫色;
4 4
② 第二只试管中加入1滴K[Fe(CN) ] 溶液,生成蓝色沉淀:
3 6
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_____(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有
______(填离子符号),由此可以证明该氧化还原反应为______。
(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液·变成棕黄色,发生反应的离子
2 2 3
方程式为________;一段时间后.溶液中有气泡出现,并放热.随后有红褐色沉淀生成。产生气泡
的原因是______;生成沉淀的原因是______(用平衡移动原理解释)。
【答案】(1)防止Fe2+被氧化 (2)2Fe2++Cl=2Fe3++2Cl-
2
(3)隔绝空气,
(4)Fe2+;Fe3+;可逆反应;
(5)HO+2Fe2++2H+=2Fe3++2HO,Fe3+催化HO 分解产生O;
2 2 2 2 2 2
HO 分解反应放热,促使Fe3+水解平衡正向移动。
2 2
【知识点】考查铁离子和亚铁离子的性质,离子的检验,盐类的水解等知识。
【考查能力】实验与探究能力
【解析】(1)亚铁离子具有还原性,能被空气中的氧气氧化,所以在配制的 FeCl 溶液中加入少量铁属的
2
目的是防止Fe2+被空气氧化。
(2)Cl 可将Fe2+氧化成铁离子,自身得电子生成氯离子,反应的离子方程式为2Fe2++Cl=2Fe3+
2 2
+2Cl-。
(3)防止空气中的氧气将Fe2+氧化,产生干扰,所以煤油的作用是隔绝空气。
(4)根据Fe2+的检验方法,向溶液中加入1滴K[Fe(CN)] 溶液,生成蓝色沉淀,一定含有亚铁离子;则
3 6
实验②检验的离子是Fe2+;碘易溶于CCl,在CCl 中呈紫色,Fe3+遇KSCN溶液显血红色,实验①和说明,
4 4
在碘离子过量情况下,溶液中仍然含有Fe3+,由此可知该反应为可逆反应。
(5)双氧水溶液中加入几滴酸化的氯化铁溶液,溶液变成黄色,发生反应为HO+2Fe2++2H+=2Fe3++2HO,
2 2 2
一段时间后产生气泡,Fe3+催化HO 分解产生O,并且HO 分解反应放热,促使Fe3+水解平衡正向移动,生
2 2 2 2 2
成氢氧化铁沉淀。
【难度】中等【题分】15分
36.[化学-选修2:化学与技术](15分)
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程
如图所示:
A.氢化釜B.过滤器C.氧化塔D.萃取塔E.净化塔F.工作液再生装置G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再
经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______,循环使用的|原料是______,配制工作液时采用
有机溶剂而不采用水的原因是______。
(2)氢化釜A中反应的化学方程式为_______,进入氧化塔C的反应混合液中的主要溶质为_______。
(3)萃取塔D中的萃取剂是____,选择其作萃取剂的原因是______。
(4)工作液再生装置F中要除净残留的HO,原因是______。
2 2
(5)双氧水浓度可在酸性条件下用KMnO 溶液测定,该反应的离子方程式为_______。一种双氧水的
4
质量分数为27.5%,(密度为1.10g·cm3),其浓度为______mol/L。
【答案】(1)氢气和氧气 ;乙基蒽醌 ;乙基蒽醌易溶于有机溶剂,不溶于水;
(2) ;乙基氢蒽醌
(3)水;HO 易溶于水,被水萃取,乙基蒽醌不溶于水;
2 2
(4)HO 分解放出氧气,与氢气混合,易发生爆炸;
2 2(5)6H++5HO+2MnO-=2Mn2++5O↑+8HO ;8.9
2 2 4 2 2
【知识点】化学与技术中考查工业制双氧水的工艺流程分析等知识
【考查能力】综合运用能力
【解析】(1)根据反应原理可知,蒽醌法制备双氧水理论上消耗的原料是氧气和氢气,由工艺流程图可知,
循环使用的|原料是乙基蒽醌,乙基蒽醌属于有机物,根据相似相溶原理,乙基蒽醌在有机溶剂中的溶解度
大,在水中的溶解度较小,所以配制工作液采用有机溶剂;(2)由反应原理可知:
;氧化塔C中的反应混合液中的主要溶质为乙基氢蒽醌;
(3)萃取塔D中需要分离双氧水和乙基蒽醌,而双氧水易溶于水,难溶于有机溶剂,所以选取的萃取剂是
水;
(4)HO 分解放出氧气,与氢气混合,易发生爆炸;
2 2
(5)双氧水在酸性条件下与高锰酸钾发生氧化还原反应,根据氧化还原反应知识可以知道:6H+
+5HO+2MnO-=2Mn2++5O↑+8HO;根据公式c=1000p×a÷M=1000×1.10×27.5%÷34=8.9mol/L。
2 2 4 2 2
【难度】难
【题分】15分
37.[化学--选修3:物质结构与性质](15分)
东晋《华阳国志南中志》卷四种已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造
币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液。
3 6 4
①[Ni(NH )]SO 中阴离子的立体构型是_____。
3 6 4
②在[Ni(NH )]2+中Ni2+与NH 之间形成的化学键称为______- ,提供孤电子对的成键原子是_____。
3 6 3
③氨的沸点(“高于”或“低于”)膦(PH ),原因是______;氨是_____分子(填“极性”或“非极
3
性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素同与镍的第二电离能分别为:I =1959kJ/mol,
Cu
I =1753kJ/mol,I >I 的原因是______。
Ni Cu Ni(4)某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm
【答案】(1)1s22s2 2p63s23p63d84s2 2
(2)①正四面体形 ②配位键 N; ③高于 氨气分子间存在氢键,sp3
(3)金属; 铜失去的是全充满的3d10电子,镍失去的是4s1稳定电子;
(4)①3:1 ②
【知识点】物质结构和性质考查核外电子排布,化学键类型,晶胞的计算等知识。
【考查能力】综合运用能力
【解析】(1)镍是28号元素,位于第四周期,第Ⅷ族,根据核外电子排布规则,其基态原子的电子排布
式为1s22s2 2p63s23p63d84s2,3d能级有5个轨道,先占满5个自旋方向相同的电子,再分别占据三个轨道,
电子自旋方向相反,所以未成对的电子数为2。
(2)①根据价层电子对互斥理论,SO2-的σ键电子对数等于4,孤电子对数(6+2-2×4)÷2=0,则阴离
4
子的立体构型是正四面体形。
②根据配位键的特点,在[Ni(NH)]2+中Ni2+与NH 之间形成的化学键称为配位键,提供孤电子对的成
3 6 3
键原子是N。
③氨气分子间存在氢键,分子间作用力强,所以氨的沸点高于膦(PH );根据价层电子对互斥理论,
3
氨气中心原子N的σ键电子对数等于3,孤电子对数(5-3)÷2=1,则氨气是sp3杂化,分子成三角
锥形,正负电荷重心不重叠,氨气是极性分子。
(3)铜和镍属于金属,则单质铜及镍都是由金属键形成的晶体;铜失去的是全充满的3d10电子,镍失去
的是4s1稳定电子;,所以I >I。
Cu Ni
(4)①根据均摊法计算,晶胞中铜原子个数为6×1/2=3,镍原子的个数为8×1/8=1,则铜和镍的数
量比为3:1;由密度公式可以知 。【难度】中等
【题分】15分
38.[化学--选修5:有机化学基础](15分)
氰基丙烯酸酯在碱性条件下能快速聚合为 ,从而具有胶黏性,某种氰基丙烯酸酯(G)
的合成路线如下:
已知:
② A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)由C生成D的反应类型为________。
(4)由D生成E的化学方程式为___________。
(5)G中的官能团有___、 ____ 、_____。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____种。(不含立体异构)
【答案】(1)丙酮
(2) 2 6:1
(3)取代反应
(4)
(5)碳碳双键、酯基、氰基 (6)8【知识点】有机化学基础考查有机物的推断,有机化学方程式的书写,官能团,同分异构体的判断等知识。
【考查能力】综合运用能力
【解析】(1)A的相对分子量为58,氧元素质量分数为0.276,则氧原子个数为58×0.276÷16=1,根据
商余法,42÷12=3…6,A分子的分子式为CHO,核磁共振氢谱显示为单峰,则A为丙酮;
3 6
(2)A为丙酮,根据已知②题给的信息,B为 ,B分子中有2种氢原子,则其核磁共振氢谱显
示为2组峰,峰面积比为1:6;
(3)光照条件下与氯气反应是取代反应;
(4)根据题意:
(5)根据题给结构式,氰基丙烯酸酯为:CH=C(CN)COOR,根据流程图可知 G 的结构简式为:
2
CH=C(CN)COOCH ,则G中的官能团有碳碳双键、酯基、氰基
2 3
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的有机物为甲酸酯,再考虑氨基连接,
共有8种。
【难度】中等
【题分】15分