文档内容
2017 年北京市高考化学试卷
一、本部分共 7小题,每小题 6分,共 42分.在每小题列出的四个选项中,选出最符合题目要
求的一项.
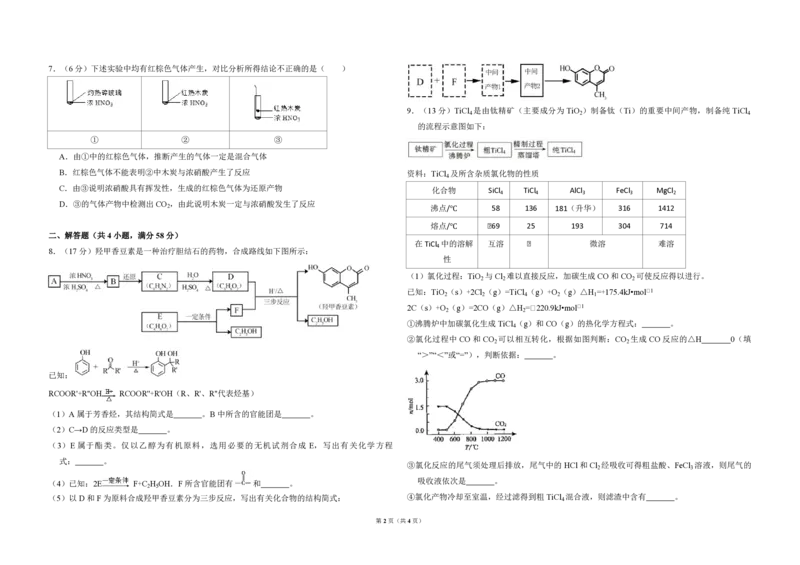
1.(6分)古丝绸之路贸易中的下列商品,主要成分属于无机物的是( )
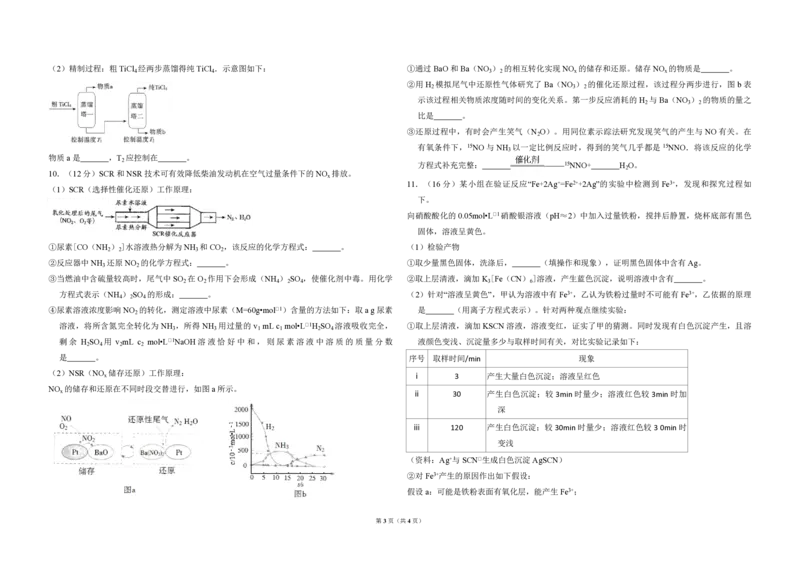
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C ~C 的烃类混合物
5 11
A. 瓷器 B. 丝绸
D.图中a的名称是2﹣甲基丁烷
5.(6分)根据SO 通入不同溶液中实验现象,所得结论不正确的是( )
2
实验 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
C. 茶叶 D. 中草药
B H S 溶液 产生黄色沉淀 SO 有氧化性
2 2
2.(6分)2016年 IUPAC 命名 117号元素为 Ts(中文名“ ”,tián),Ts的原子核外最外层
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
电子数是7,下列说法不正确的是( )
D Na SiO 溶液 产生胶状沉淀 酸性:H SO >H SiO
2 3 2 3 2 3
A.Ts是第七周期第ⅦA 族元素
A.A B.B C.C D.D
B.Ts 的同位素原子具有相同的电子数
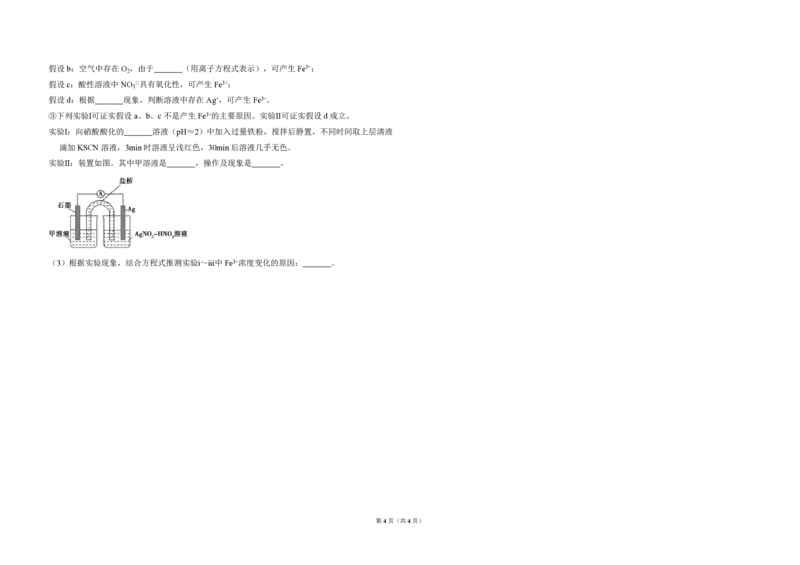
6.(6分)聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与 HI 形成聚维
C.Ts 在同族元素中非金属性最弱 3
D.中子数为176的Ts核素符号是 Ts
3.(6分)下列变化中,气体被还原的是( )
酮碘,其结构表示如下
A.二氧化碳使Na O 固体变白
2 2
(图中虚线表示氢键)下列说法不正确的是( )
B.氯气使 KBr 溶液变黄
C.乙烯使 Br 的四氯化碳溶液褪色
2
D.氨气使AlCl 溶液产生白色沉淀
3
4.(6 分)我国在 CO 催化加氢制取汽油方面取得突破性进展,CO 转化过程示意图如下:下列
A.聚维酮的单体是
2 2
说法不正确的是( ) B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮在一定条件下能发生水解反应
第1页(共4页)7.(6分)下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
9.(13分)TiCl 是由钛精矿(主要成分为 TiO )制备钛(Ti)的重要中间产物,制备纯 TiCl
4 2 4
的流程示意图如下:
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应 资料:TiCl 及所含杂质氯化物的性质
4
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
化合物 SiCl TiCl AlCl FeCl MgCl
4 4 3 3 2
D.③的气体产物中检测出CO ,由此说明木炭一定与浓硝酸发生了反应
2 沸点/℃ 58 136 181(升华) 316 1412
熔点/℃ ﹣69 25 193 304 714
二、解答题(共 4小题,满分 58分)
在TiCl 中的溶解 互溶 ﹣ 微溶 难溶
4
8.(17分)羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
性
(1)氯化过程:TiO 与Cl 难以直接反应,加碳生成CO 和CO 可使反应得以进行。
2 2 2
已知:TiO (s)+2Cl (g)=TiCl (g)+O (g)△H =+175.4kJ•mol﹣1
2 2 4 2 1
2C(s)+O (g)=2CO(g)△H =﹣220.9kJ•mol﹣1
2 2
①沸腾炉中加碳氯化生成TiCl (g)和CO(g)的热化学方程式: 。
4
②氯化过程中 CO 和 CO 可以相互转化,根据如图判断:CO 生成 CO 反应的△H 0(填
2 2
“>”“<”或“=”),判断依据: 。
已知:
RCOOR'+R''OH RCOOR''+R'OH(R、R'、R''代表烃基)
(1)A 属于芳香烃,其结构简式是 。B中所含的官能团是 。
(2)C→D 的反应类型是 。
(3)E属于酯类。仅以乙醇为有机原料,选用必要的无机试剂合成 E,写出有关化学方程
式: 。
③氯化反应的尾气须处理后排放,尾气中的 HCl和 Cl 经吸收可得粗盐酸、FeCl 溶液,则尾气的
2 3
(4)已知:2E F+C H OH.F 所含官能团有 和 。
吸收液依次是 。
2 5
(5)以D 和F 为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构简式: ④氯化产物冷却至室温,经过滤得到粗TiCl
4
混合液,则滤渣中含有 。
第2页(共4页)(2)精制过程:粗TiCl 经两步蒸馏得纯TiCl .示意图如下: ①通过BaO和 Ba(NO ) 的相互转化实现NO 的储存和还原。储存NO 的物质是 。
4 4 3 2 x x
②用 H 模拟尾气中还原性气体研究了 Ba(NO ) 的催化还原过程,该过程分两步进行,图 b表
2 3 2
示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 H 与 Ba(NO ) 的物质的量之
2 3 2
比是 。
③还原过程中,有时会产生笑气(N O)。用同位素示踪法研究发现笑气的产生与 NO 有关。在
2
有氧条件下,15NO 与 NH 以一定比例反应时,得到的笑气几乎都是 15NNO.将该反应的化学
3
物质a是 ,T 应控制在 。
2
方程式补充完整: 15NNO+ H O。
2
10.(12分)SCR 和NSR 技术可有效降低柴油发动机在空气过量条件下的NO 排放。
x
11.(16分)某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到 Fe3+,发现和探究过程如
(1)SCR(选择性催化还原)工作原理:
下。
向硝酸酸化的 0.05mol•L﹣1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色
固体,溶液呈黄色。
①尿素[CO(NH ) ]水溶液热分解为NH 和CO ,该反应的化学方程式: 。 (1)检验产物
2 2 3 2
②反应器中NH 还原NO 的化学方程式: 。 ①取少量黑色固体,洗涤后, (填操作和现象),证明黑色固体中含有Ag。
3 2
③当燃油中含硫量较高时,尾气中 SO 在 O 作用下会形成(NH ) SO ,使催化剂中毒。用化学 ②取上层清液,滴加K [Fe(CN) ]溶液,产生蓝色沉淀,说明溶液中含有 。
2 2 4 2 4 3 6
方程式表示(NH ) SO 的形成: 。 (2)针对“溶液呈黄色”,甲认为溶液中有 Fe3+,乙认为铁粉过量时不可能有 Fe3+,乙依据的原理
4 2 4
④尿素溶液浓度影响 NO 的转化,测定溶液中尿素(M=60g•mol﹣1)含量的方法如下:取 a g尿素 是 (用离子方程式表示)。针对两种观点继续实验:
2
溶液,将所含氮完全转化为 NH ,所得 NH 用过量的 v mL c mol•L﹣1H SO 溶液吸收完全, ①取上层清液,滴加 KSCN 溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶
3 3 1 1 2 4
剩余 H SO 用 v mL c mol•L﹣1NaOH 溶液恰好中和,则尿素溶液中溶质的质量分数 液颜色变浅、沉淀量多少与取样时间有关,对比实验记录如下:
2 4 2 2
是 。 序号 取样时间/min 现象
(2)NSR(NO
x
储存还原)工作原理:
ⅰ 3 产生大量白色沉淀;溶液呈红色
NO 的储存和还原在不同时段交替进行,如图a所示。
x ⅱ 30 产生白色沉淀;较 3min 时量少;溶液红色较 3min 时加
深
ⅲ 120 产生白色沉淀;较 30min 时量少;溶液红色较 3 0min 时
变浅
(资料:Ag+与SCN﹣生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生 Fe3+;
第3页(共4页)假设b:空气中存在O ,由于 (用离子方程式表示),可产生Fe3+;
2
假设c:酸性溶液中NO ﹣具有氧化性,可产生Fe3+;
3
假设d:根据 现象,判断溶液中存在Ag+,可产生Fe3+。
③下列实验Ⅰ可证实假设 a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的 溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液
滴加KSCN 溶液,3min时溶液呈浅红色,30min后溶液几乎无色。
实验Ⅱ:装置如图。其中甲溶液是 ,操作及现象是 。
(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中Fe3+浓度变化的原因: 。
第4页(共4页)