文档内容
2018 年天津市高考化学试卷
一、选择题(共6小题,每小题6分,共36分.每题只有一个正确选项)
1.(6分)以下是中华民族为人类文明进步做出巨大贡献的几个事例,运用化学知识对其
进行的分析不合理的是( )
A.四千余年前用谷物酿造出酒和酯,酿造过程中只发生水解反应
B.商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品
C.汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏土
D.屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作
2.(6分)下列有关物质性质的比较,结论正确的是( )
A.溶解度:Na CO <NaHCO B.热稳定性:HCl<PH
2 3 3 3
C.沸点:C H SH<C H OH D.碱性:LiOH<Be(OH)
2 5 2 5 2
3.(6分)下列叙述正确的是( )
A.某温度下,一元弱酸HA的K 越小,则NaA的K (水解常数)越小
a b
B.铁管镀锌层局部破损后,铁管仍不易生锈
C.反应活化能越高,该反应越易进行
D.不能用红外光谱区分C H OH和CH OCH
2 5 3 3
4.(6分)由下列实验及现象推出的相应结论正确的是( )
实验 现象 结论
A 某溶液中滴加 K [Fe 产生蓝色沉淀 原溶液中有Fe2+,无
3
(CN) ]溶液 Fe3+
6
B 向 C H ONa溶 液 中 溶液变浑浊 酸 性 : H CO >
6 5 2 3
通入CO C H OH
2 6 5
C 向含有 ZnS和 Na S 生成黑色沉淀 K ( CuS) < K
2 sp sp
的 悬 浊 液 中 滴 加 (ZnS)
CuSO 溶液
4
D ①某溶液中加入 Ba①产生白色沉淀 原溶液中有SO 2﹣
4
(NO ) 溶液 ②仍有白色沉淀
3 2
②再加足量盐酸
A.A B.B C.C D.D5.(6分)室温下,向圆底烧瓶中加入1 mol C H OH和含1mol HBr的氢溴酸,溶液中发
2 5
生反应:C H OH+HBr⇌C H Br+H O,充分反应后达到平衡。已知常压下,C H Br和
2 5 2 5 2 2 5
C H OH的沸点分别为38.4℃和78.5℃.下列关叙述错误的是( )
2 5
A.加入NaOH,可增大乙醇的物质的量
B.增大HBr浓度,有利于生成C H Br
2 5
C.若反应物均增大至2mol,则两种反应物平衡转化率之比不变
D.若起始温度提高至60℃,可缩短反应达到平衡的时间
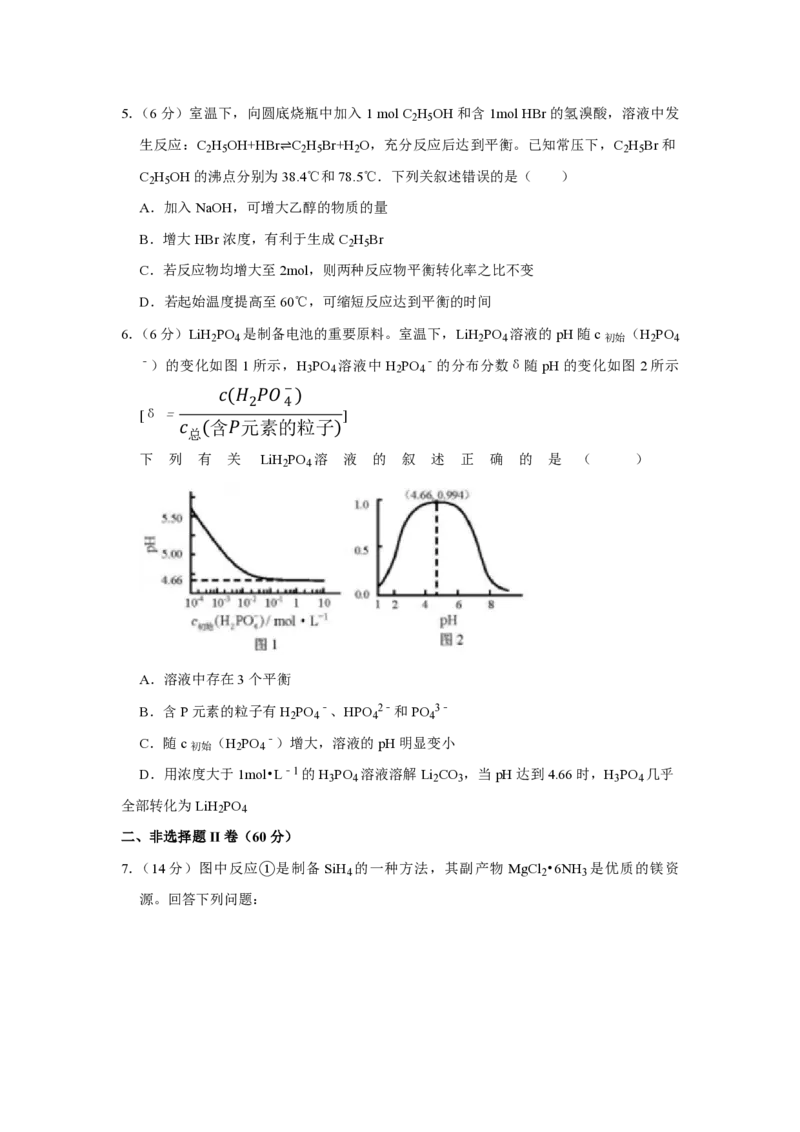
6.(6分)LiH PO 是制备电池的重要原料。室温下,LiH PO 溶液的pH随c (H PO
2 4 2 4 初始 2 4
﹣)的变化如图 1所示,H PO 溶液中 H PO ﹣的分布分数δ随 pH的变化如图 2所示
3 4 2 4
‒
𝑐(𝐻 𝑃𝑂 )
2 4
[δ = ]
𝑐 (含𝑃元素的粒子)
总
下 列 有 关 LiH PO 溶 液 的 叙 述 正 确 的 是 ( )
2 4
A.溶液中存在3个平衡
B.含P元素的粒子有H PO ﹣、HPO 2﹣和PO 3﹣
2 4 4 4
C.随c
初始
(H
2
PO
4
﹣)增大,溶液的pH明显变小
D.用浓度大于1mol•L﹣1的H PO 溶液溶解Li CO ,当pH达到4.66时,H PO 几乎
3 4 2 3 3 4
全部转化为LiH PO
2 4
二、非选择题II卷(60分)
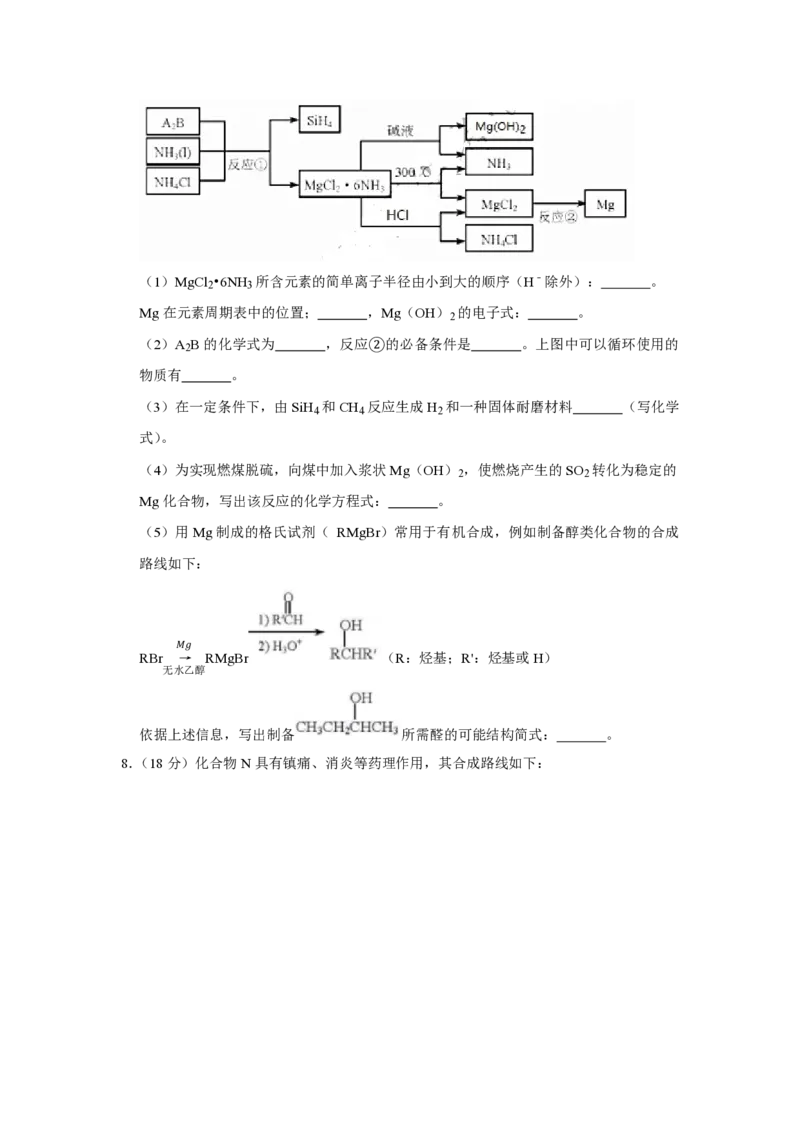
7.(14分)图中反应①是制备 SiH 的一种方法,其副产物 MgCl •6NH 是优质的镁资
4 2 3
源。回答下列问题:(1)MgCl •6NH 所含元素的简单离子半径由小到大的顺序(H﹣除外): 。
2 3
Mg在元素周期表中的位置; ,Mg(OH) 的电子式: 。
2
(2)A B的化学式为 ,反应②的必备条件是 。上图中可以循环使用的
2
物质有 。
(3)在一定条件下,由SiH 和CH 反应生成H 和一种固体耐磨材料 (写化学
4 4 2
式)。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH) ,使燃烧产生的SO 转化为稳定的
2 2
Mg化合物,写出该反应的化学方程式: 。
(5)用Mg制成的格氏试剂( RMgBr)常用于有机合成,例如制备醇类化合物的合成
路线如下:
𝑀𝑔
RBr → RMgBr (R:烃基;R':烃基或H)
无水乙醇
依据上述信息,写出制备 所需醛的可能结构简式: 。
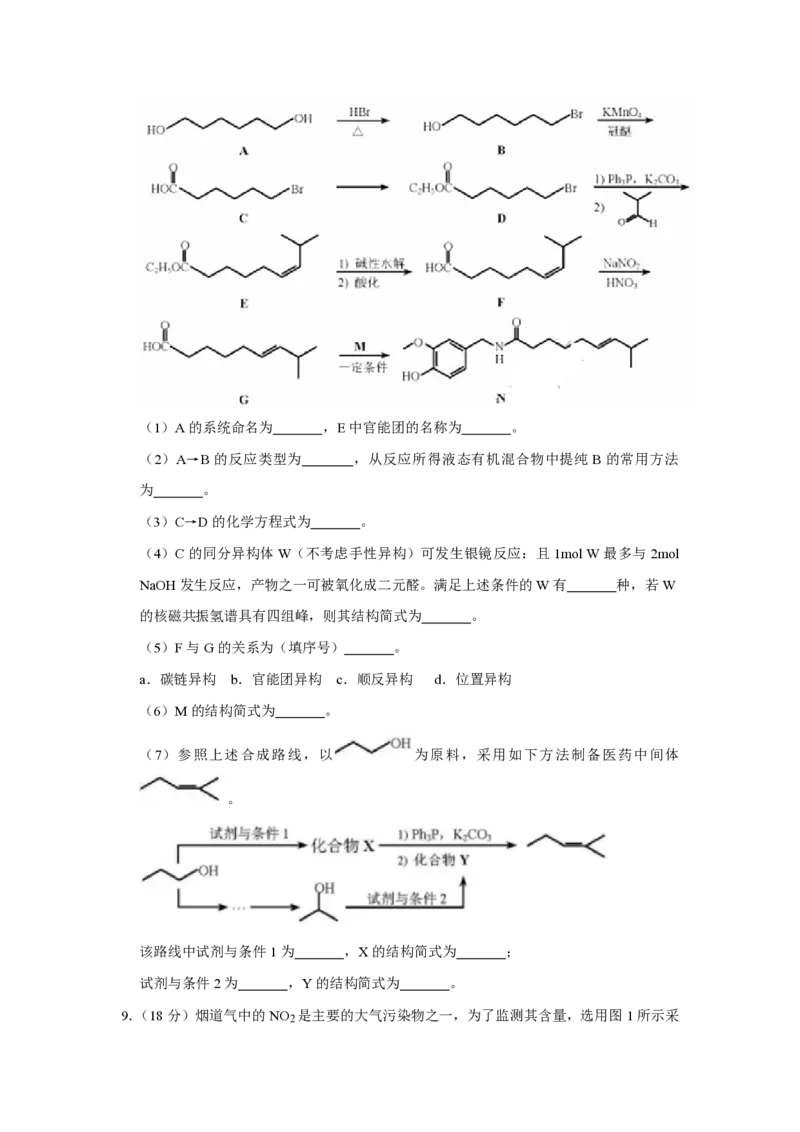
8.(18分)化合物N具有镇痛、消炎等药理作用,其合成路线如下:(1)A的系统命名为 ,E中官能团的名称为 。
(2)A→B的反应类型为 ,从反应所得液态有机混合物中提纯 B的常用方法
为 。
(3)C→D的化学方程式为 。
(4)C的同分异构体W(不考虑手性异构)可发生银镜反应:且1mol W最多与2mol
NaOH发生反应,产物之一可被氧化成二元醛。满足上述条件的W有 种,若W
的核磁共振氢谱具有四组峰,则其结构简式为 。
(5)F与G的关系为(填序号) 。
a.碳链异构 b.官能团异构 c.顺反异构 d.位置异构
(6)M的结构简式为 。
(7)参照上述合成路线,以 为原料,采用如下方法制备医药中间体
。
该路线中试剂与条件1为 ,X的结构简式为 ;
试剂与条件2为 ,Y的结构简式为 。
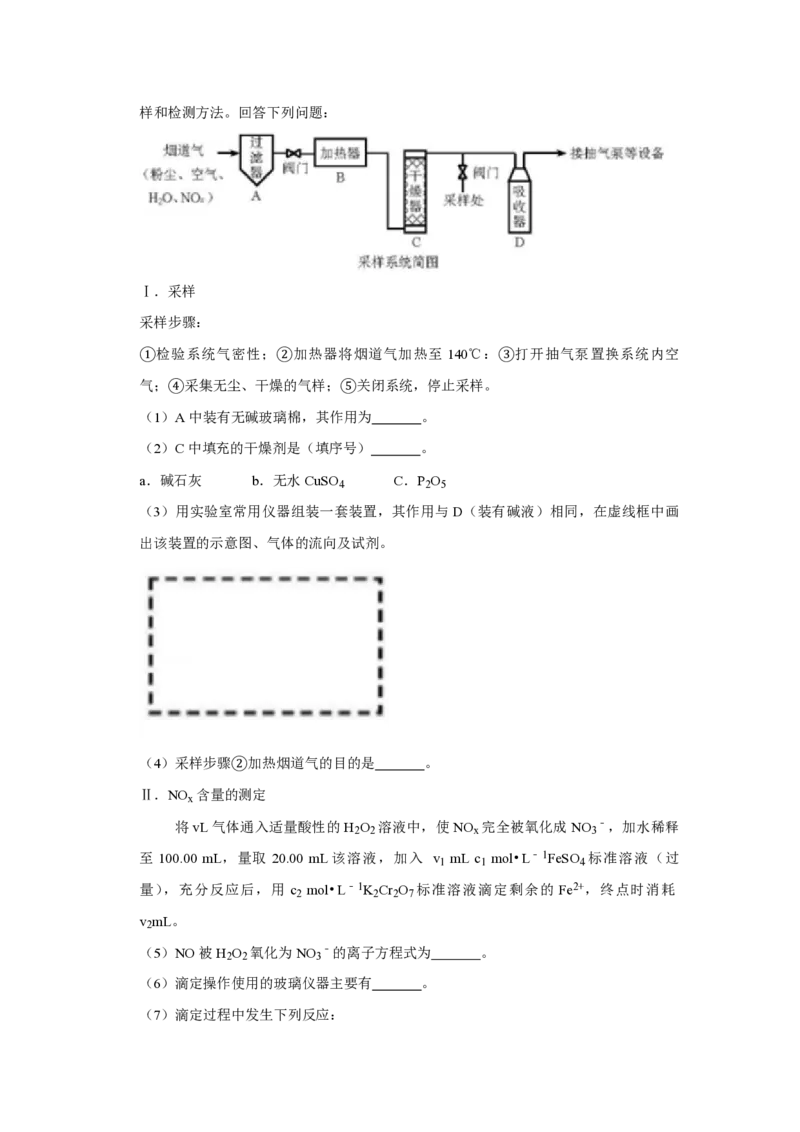
9.(18分)烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用图1所示采
2样和检测方法。回答下列问题:
Ⅰ.采样
采样步骤:
①检验系统气密性;②加热器将烟道气加热至 140℃:③打开抽气泵置换系统内空
气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用为 。
(2)C中填充的干燥剂是(填序号) 。
a.碱石灰 b.无水CuSO C.P O
4 2 5
(3)用实验室常用仪器组装一套装置,其作用与D(装有碱液)相同,在虚线框中画
出该装置的示意图、气体的流向及试剂。
(4)采样步骤②加热烟道气的目的是 。
Ⅱ.NO 含量的测定
x
将vL气体通入适量酸性的H O 溶液中,使NO 完全被氧化成NO ﹣,加水稀释
2 2 x 3
至 100.00 mL,量取 20.00 mL该溶液,加入 v mL c mol•L﹣1FeSO 标准溶液(过
1 1 4
量),充分反应后,用 c mol•L﹣1K Cr O 标准溶液滴定剩余的 Fe2+,终点时消耗
2 2 2 7
v mL。
2
(5)NO被H O 氧化为NO ﹣的离子方程式为 。
2 2 3
(6)滴定操作使用的玻璃仪器主要有 。
(7)滴定过程中发生下列反应:3Fe2++NO ﹣+4H+=NO↑+3Fe3++2H O
3 2
Cr O 2﹣+6Fe2++14H+=2Cr3++6Fe3++7H O
2 7 2
则气样中NO 折合成NO 的含量为 mg•m﹣3。
x 2
(8)判断下列情况对NO 含量测定结果的影响(填“偏高”、“偏低”或“无影响”)
x
若缺少采样步骤③,会使测定结果 。
若FeSO 标准溶液部分变质,会使测定结果 。
4
10.(14分)CO 是一种廉价的碳资源,其综合利用具有重要意义,回答下列问题:
2
(1)CO 可以被NaOH溶液捕获。若所得溶液pH=13,CO 主要转化为 (写
2 2
离子符号);若所得溶液c(HCO ﹣):c(CO 2﹣)=2:1,溶液pH= 。室温
3 3
下,H CO 的K =4×10﹣2;K =5×10﹣11)
2 3 1 2
催化剂
(2)CO 与CH 经催化重整,制得合成气:CH (g)+CO (g) ⇌ 2CO(g)+2H
2 4 4 2 2
(g)
①已知上述反应中相关的化学键键能数据如下:
化学键 C﹣H C=O H﹣H
(CO)
键能/kJ•mol﹣1 413 745 436 1075
则该反应的△H= 。分别在v L恒温密闭容器A(恒容)、B(恒压,容积可变)
中,加入CH 和CO 各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较
4 2
多的是 (填“A”或“B”)
②按一定体积比加入CH 和CO ,在恒压下发生反应,温度对CO和H 产率的影响如
4 2 2
图1所示。此反应优选温度为900℃的原因是 。
(3)O 辅助的 Al﹣CO 电池工作原理如图 2所示。该电池电容量大,能有效利用
2 2CO ,电池反应产物Al (C O ) 是重要的化工原料。
2 2 2 4 3
电池的负极反应式: 。
电池的正极反应式:6O +6e﹣=6O ﹣
2 2
6CO +6O ﹣=3C O 2﹣+6O
2 2 2 4 2
反应过程中O 的作用是 。
2
该电池的总反应式: 。