文档内容
绝密★启用前
2018年普通高等学校招生全国统一考试
理科综合能力测试试题卷(化学)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 P 31 S 32 Fe 56
一、选择题
1. 化学与生活密切相关。下列说法错误的是
A. 泡沫灭火器可用于一般的起火,也适用于电器起火
B. 疫苗一般应冷藏存放,以避免蛋白质变性
C. 家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
D. 电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法
2. 下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
3. 苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是
A. 与液溴混合后加入铁粉可发生取代反应
B. 能使酸性高锰酸钾溶液褪色
C. 与氯化氢反应可以生成氯代苯乙烯
D. 在催化剂存在下可以制得聚苯乙烯
4. 下列实验操作不当的是
A. 用稀硫酸和锌粒制取H 时,加几滴CuSO 溶液以加快反应速率
2 4 [来源:学§科§网Z§X§X§K]
B. 用标准HCl溶液滴定NaHCO 溶液来测定其浓度,选择酚酞为指示剂
3
C. 用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+D. 常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二
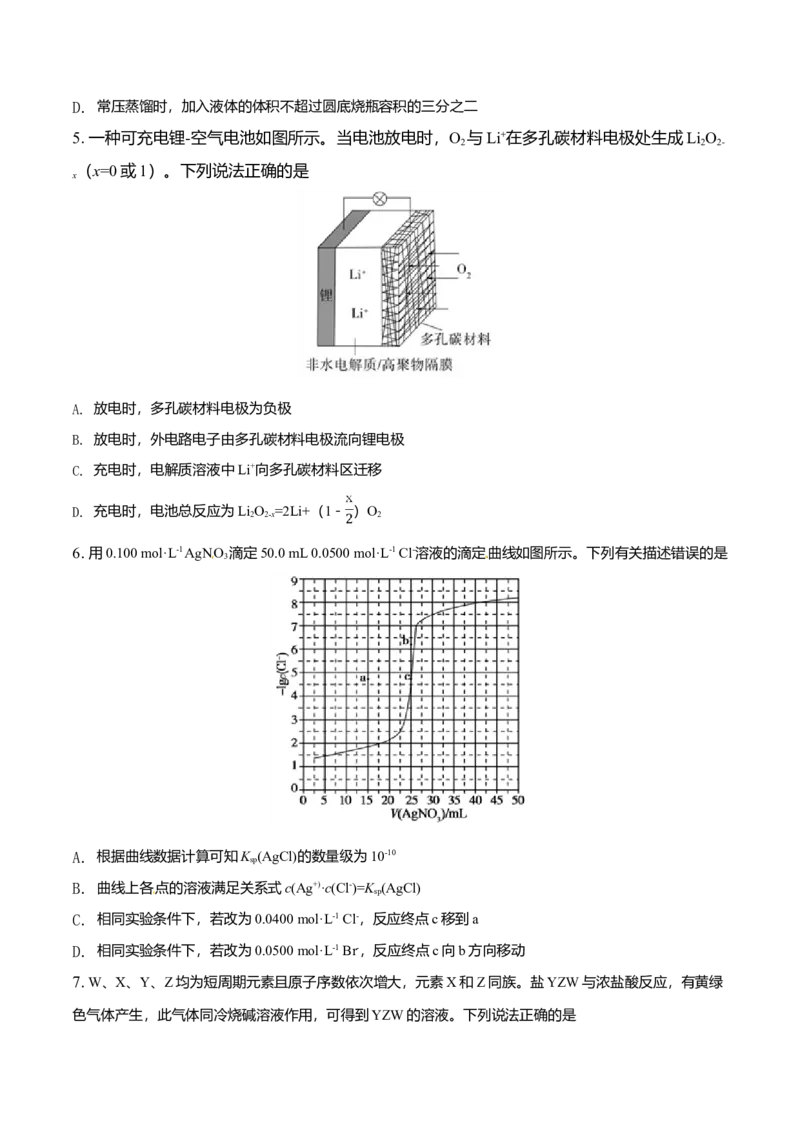
5. 一种可充电锂-空气电池如图所示。当电池放电时,O 与Li+在多孔碳材料电极处生成Li O
2 2 2-
(x=0或1)。下列说法正确的是
x
A. 放电时,多孔碳材料电极为负极
B. 放电时,外电路电子由多孔碳材料电极流向锂电极
C. 充电时,电解质溶液中Li+向多孔碳材料区迁移
D. 充电时,电池总反应为LiO =2Li+(1- )O
2 2-x 2[来源:Z*xx*k.Com]
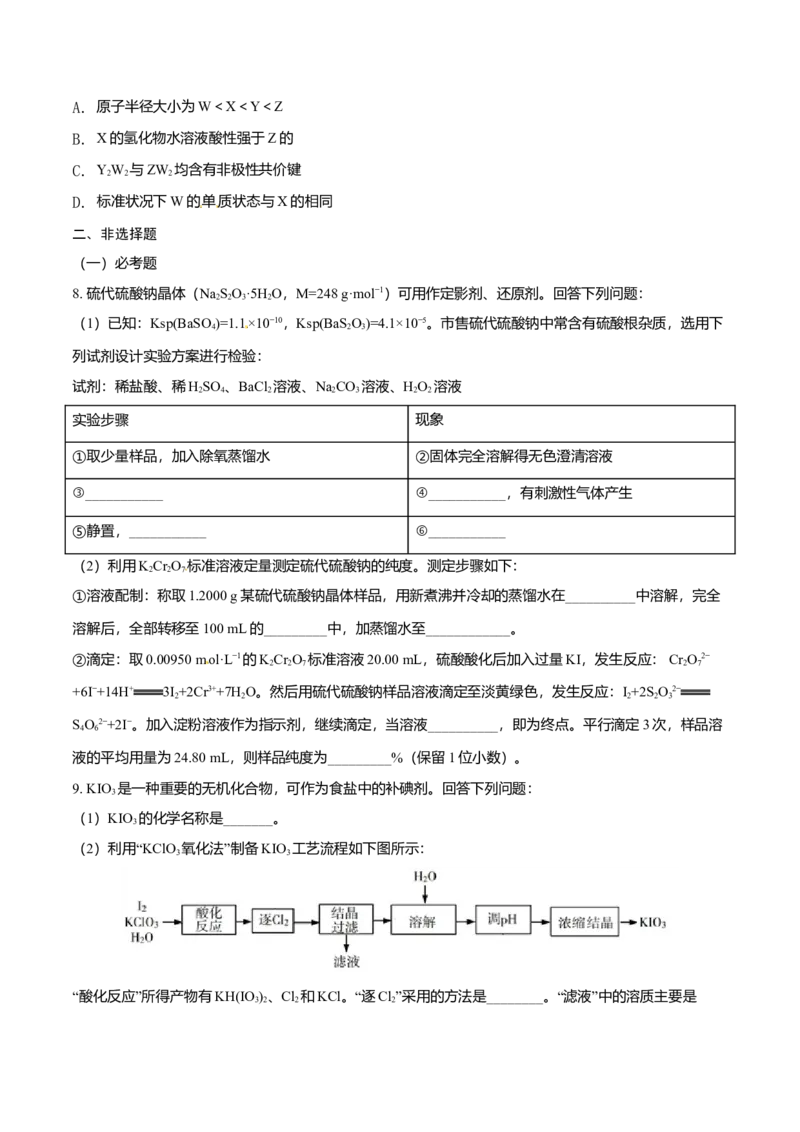
6. 用0.100 mol·L-1 AgNO 滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是
3
A. 根据曲线数据计算可知K (AgCl)的数量级为10-10
sp
B. 曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K (AgCl)
sp
C. 相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D. 相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
7. W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。盐YZW与浓盐酸反应,有黄绿
色气体产生,此气体同冷烧碱溶液作用,可得到YZW的溶液。下列说法正确的是A. 原子半径大小为W<X<Y<Z
B. X的氢化物水溶液酸性强于Z的
C. YW 与ZW 均含有非极性共价键
2 2 2
D. 标准状况下W的单质状态与X的相同
二、非选择题
(一)必考题
8. 硫代硫酸钠晶体(NaSO·5H O,M=248 g·mol−1)可用作定影剂、还原剂。回答下列问题:
2 2 3 2
(1)已知:Ksp(BaSO )=1.1×10−10,Ksp(BaS O)=4.1×10−5。市售硫代硫酸钠中常含有硫酸根杂质,选用下
4 2 3
列试剂设计实验方案进行检验:
试剂:稀盐酸、稀HSO 、BaCl 溶液、NaCO 溶液、HO 溶液
2 4 2 2 3 2 2
实验步骤 现象 [来源:学。科。网]
①取少量样品,加入除氧蒸馏水 ②固体完全溶解得无色澄清溶液
③___________ ④___________,有刺激性气体产生
⑤静置,___________ ⑥___________
(2)利用KCr O 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
2 2 7
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________中溶解,完全
溶解后,全部转移至100 mL的_________中,加蒸馏水至____________。
②滴定:取0.00950 mol·L−1的KCr O 标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应: Cr O2−
2 2 7 2 7
+6I−+14H+ 3I+2Cr3++7H O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I+2S O2−
2 2 2 2 3
SO2−+2I−。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶
4 6
液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
9. KIO 是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
3
(1)KIO 的化学名称是_______。
3
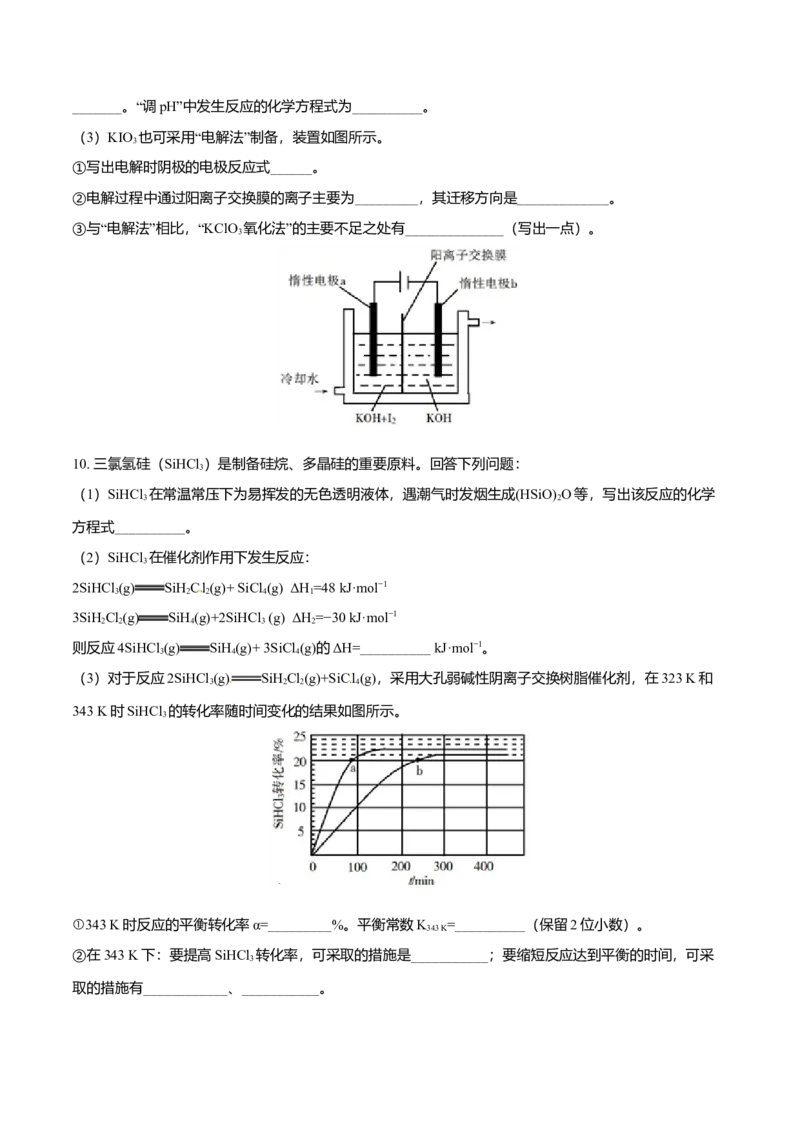
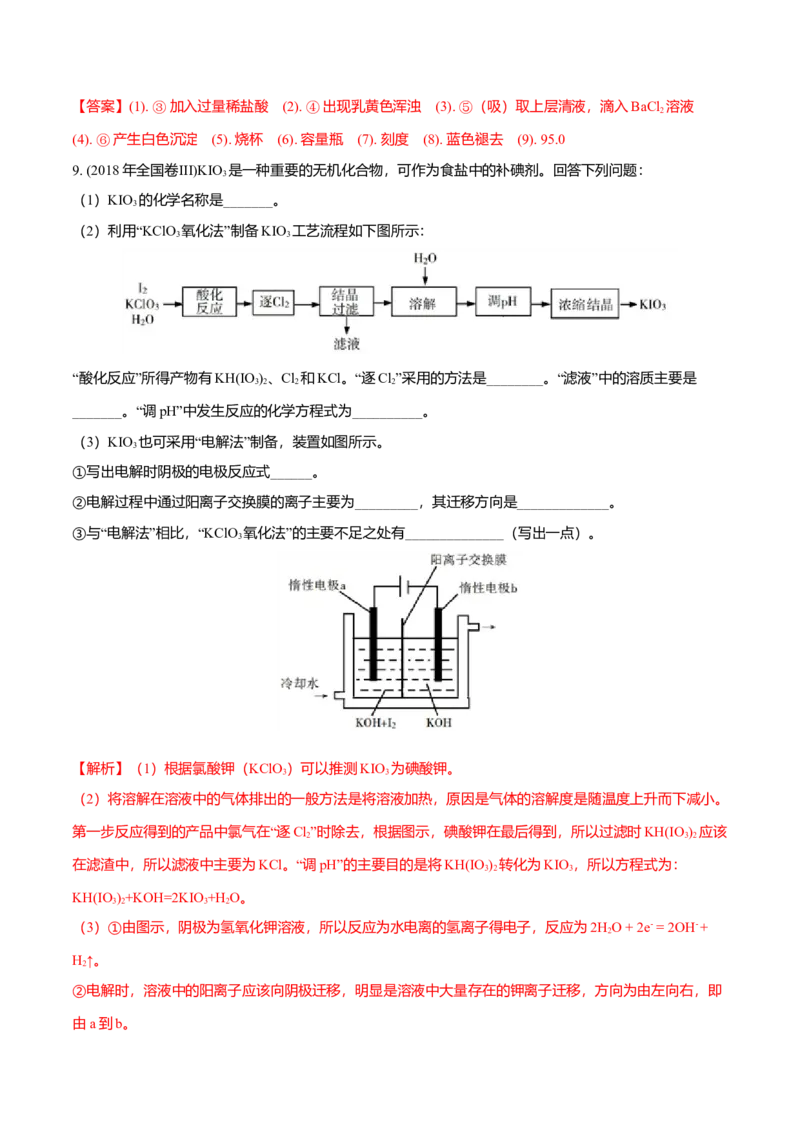
(2)利用“KClO 氧化法”制备KIO 工艺流程如下图所示:
3 3
“酸化反应”所得产物有KH(IO)、Cl 和KCl。“逐Cl”采用的方法是________。“滤液”中的溶质主要是
3 2 2 2_______。“调pH”中发生反应的化学方程式为__________。
(3)KIO 也可采用“电解法”制备,装置如图所示。
3
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO 氧化法”的主要不足之处有______________(写出一点)。
3
10. 三氯氢硅(SiHCl )是制备硅烷、多晶硅的重要原料。回答下列问题:
3
(1)SiHCl 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO) O等,写出该反应的化学
3 2
方程式__________。
(2)SiHCl 在催化剂作用下发生反应:
3
2SiHCl (g) SiHCl(g)+ SiCl (g) ΔH =48 kJ·mol−1
3 2 2 4 1
3SiHCl(g) SiH(g)+2SiHCl (g) ΔH =−30 kJ·mol−1
2 2 4 3 2
则反应4SiHCl (g) SiH(g)+ 3SiCl (g)的ΔH=__________ kJ·mol−1。
3 4 4
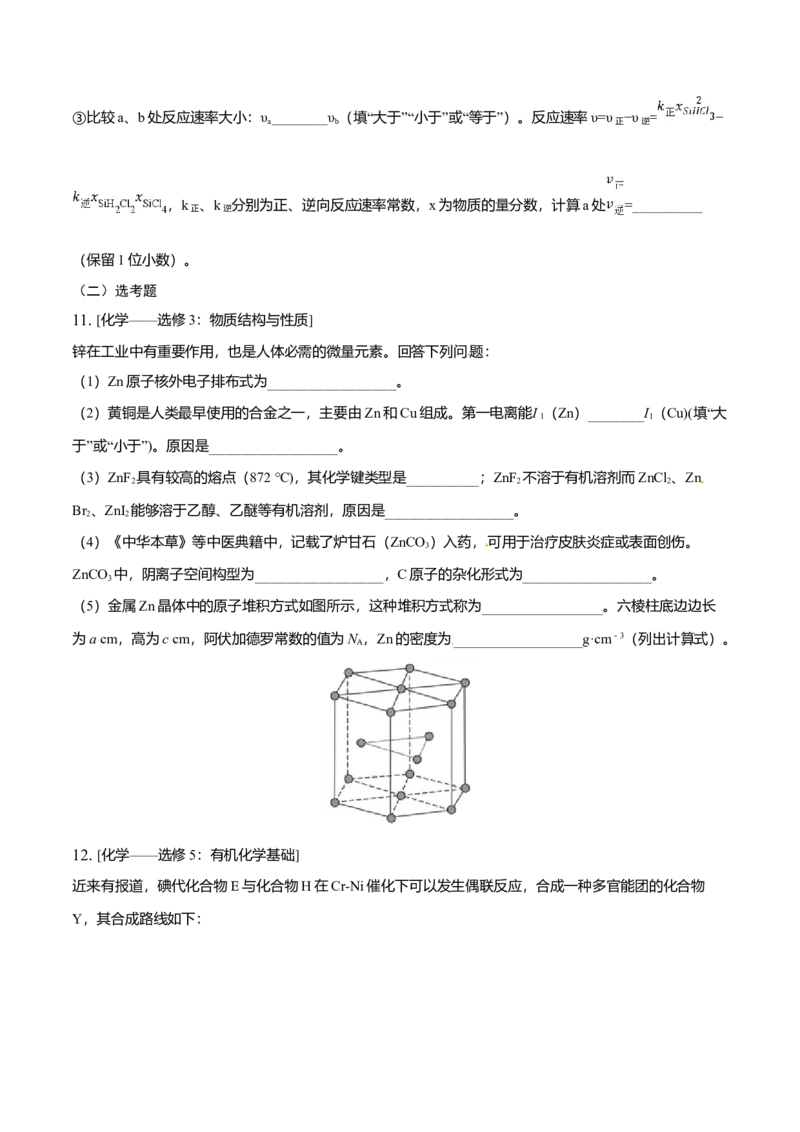
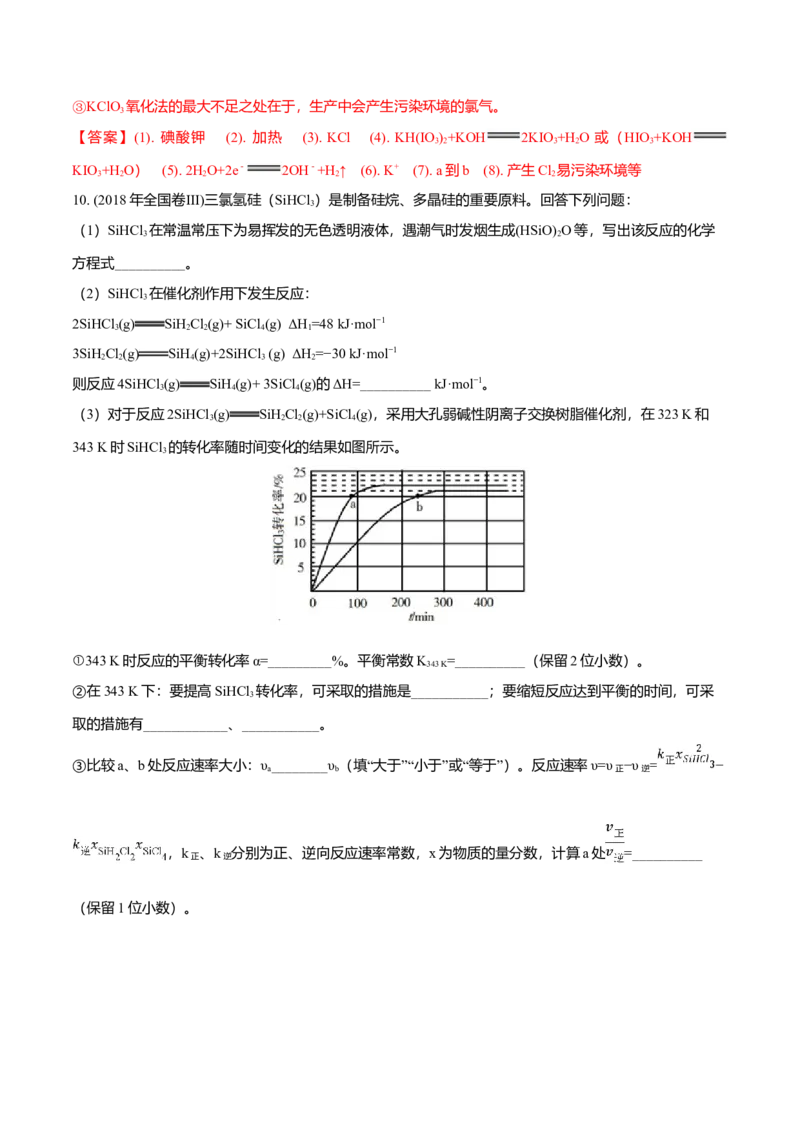
(3)对于反应2SiHCl (g) SiHCl(g)+SiCl(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和
3 2 2 4
343 K时SiHCl 的转化率随时间变化的结果如图所示。
3
①343 K时反应的平衡转化率α=_________%。平衡常数K =__________(保留2位小数)。
343 K
②在343 K下:要提高SiHCl 转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采
3
取的措施有____________、___________。③比较a、b处反应速率大小:υ________υ(填“大于”“小于”或“等于”)。反应速率υ=υ −υ = −
a b 正 逆
,k 、k 分别为正、逆向反应速率常数,x为物质的量分数,计算a处 =__________
正 逆
(保留1位小数)。
(二)选考题
11. [化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ (Zn)_______Ⅰ(Cu)(填“大
1 1
于”或“小于”)。原因是________________。
(3)ZnF 具有较高的熔点(872 ℃),其化学键类型是_________;ZnF 不溶于有机溶剂而ZnCl、Zn
2 2 2
Br 、ZnI 能够溶于乙醇、乙醚等有机溶剂,原因是________________。
2 2
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO )入药,可用于治疗皮肤炎症或表面创伤。
3
ZnCO 中,阴离子空间构型为________________,C原子的杂化形式为________________。
3
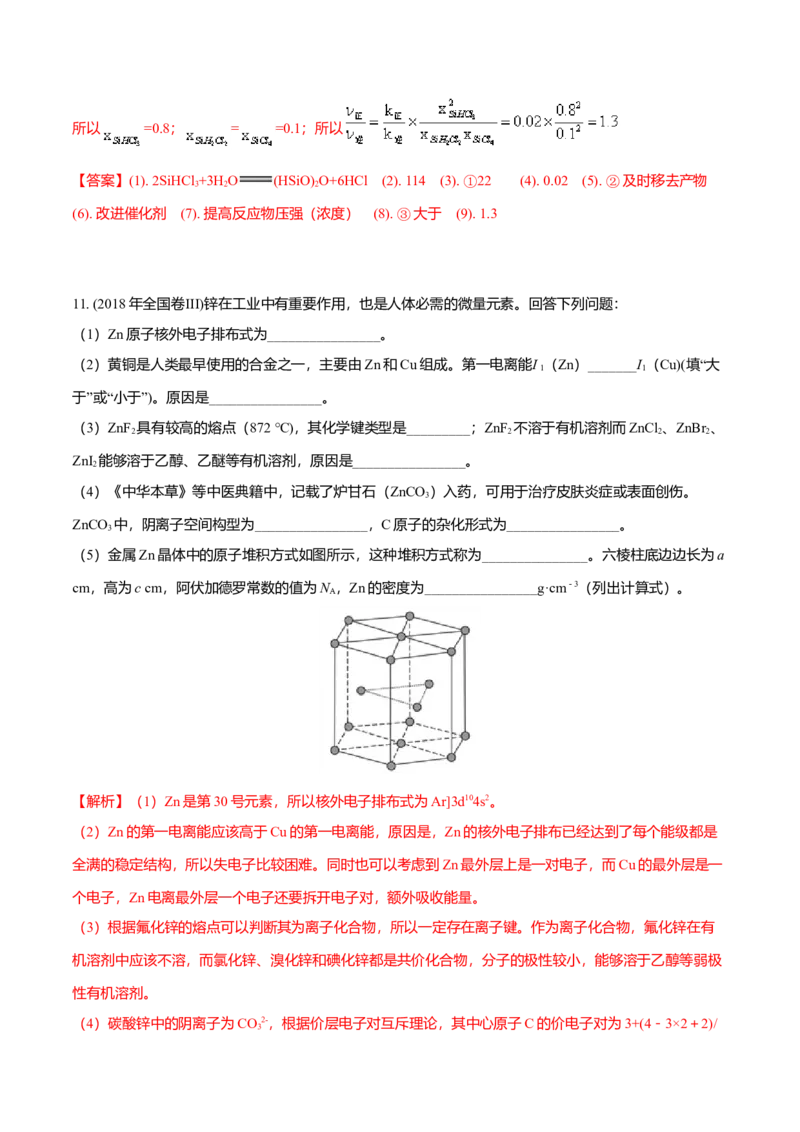
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长
为a cm,高为c cm,阿伏加德罗常数的值为N ,Zn的密度为________________g·cm-3(列出计算式)。
A
12. [化学——选修5:有机化学基础]
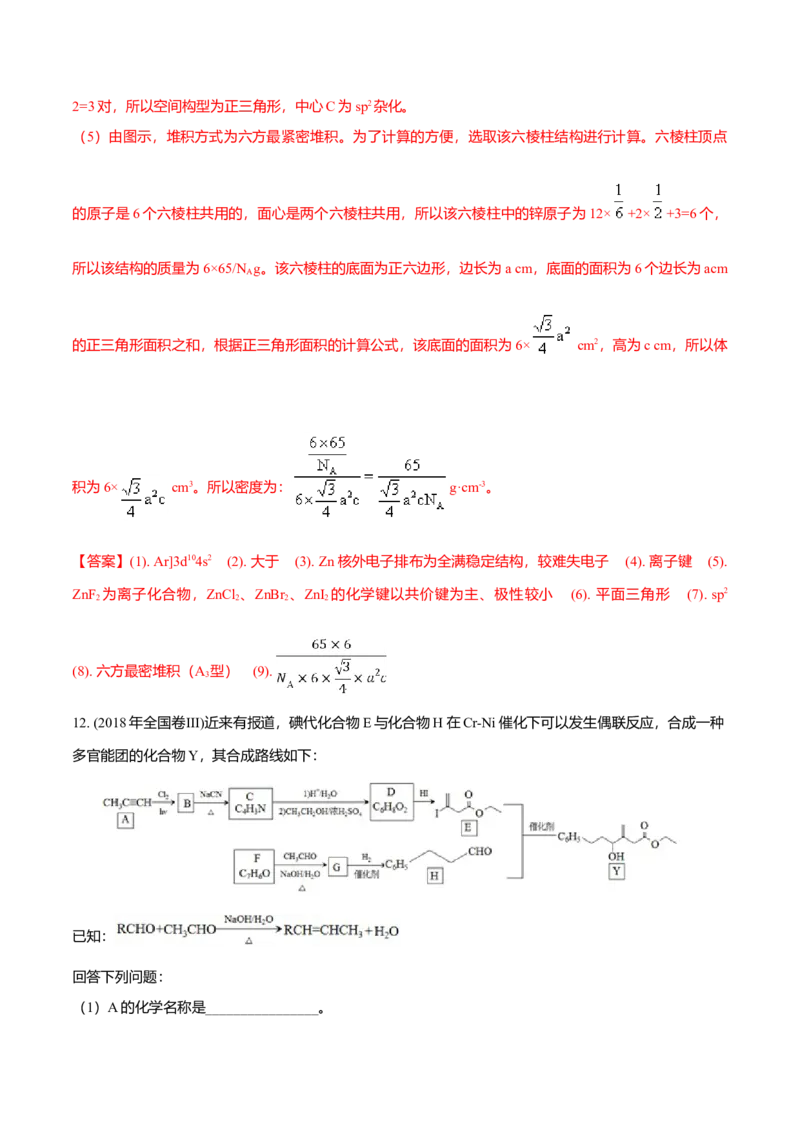
近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物
Y,其合成路线如下:已知:
回答下列问题:
(1)A的化学名称是________________。
(2)B为单氯代烃,由B生成C的化学方程式为________________。
(3)由A生成B、G生成H的反应类型分别是________________、________________。
(4)D的结构简式为________________。
(5)Y中含氧官能团的名称为________________。
(6)E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为________________。
(7)X与D互为同分异构体,且具有完全相同官能团。X的核磁共振氢谱显示三种不同化学环境的氢,
其峰面积之比为3∶3∶2。写出3种符合上述条件的X的结构简式________________。
1. (2018年全国卷III)化学与生活密切相关。下列说法错误的是( )
A. 泡沫灭火器可用于一般的起火,也适用于电器起火
B. 疫苗一般应冷藏存放,以避免蛋白质变性
C. 家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
D. 电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法
【解析】A.泡沫灭火器中加入的主要是碳酸氢钠和硫酸铝溶液,两者混合的时候发生双水解反应,生成
大量的二氧化碳气体泡沫,该泡沫喷出进行灭火。但是,喷出的二氧化碳气体泡沫中一定含水,形成电解
质溶液,具有一定的导电能力,可能导致触电或电器短路,A错误。B.疫苗是指用各类病原微生物制作
的用于预防接种的生物制品。由于疫苗对温度比较敏感,温度较高时,会因为蛋白质变性,而失去活性,所以疫苗一般应该冷藏保存,B正确。
C.油性漆是指用有机物作为溶剂或分散剂的油漆;水性漆是指用水作为溶剂或分散剂的油漆,使用水性
漆可以减少有机物的挥发对人体健康和室内环境造成的影响,C正确。D.电热水器内胆连接一个镁棒,
就形成了原电池,因为镁棒比较活泼所以应该是原电池的负极,从而对正极的热水器内胆(多为不锈钢或
铜制)起到了保护作用,这种保护方法为:牺牲阳极的阴极保护法,D正确。【答案】A
2. (2018年全国卷III)下列叙述正确的是( )
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
【解析】A.1个Mg原子中有12个质子,1个Al原子中有13个质子。24g镁和27g铝各自的物质的量都
是1mol,所以24g镁含有的质子数为12mol,27g铝含有的质子的物质的量为13mol,选项A错误。B.设
氧气和臭氧的质量都是Xg,则氧气(O)的物质的量为 mol,臭氧(O)的物质的量为 mol,所以
2 3
两者含有的氧原子分别为 ×2= mol和 ×3= mol,即此时氧气和臭氧中含有的氧原子是一样多的,
而每个氧原子都含有8个电子,所以同等质量的氧气和臭氧中一定含有相同的电子数,选项B正确。C.
重水为 ,其中 含有1个中子, 含有8个中子,所以1个重水分子含有10个中子,1mol重
水含有10mol中子。水为 ,其中 没有中子, 含有8个中子,所以1个水分子含有8个中子,
1mol水含有8mol中子。两者的中子数之比为10:8=5:4,选项C错误。D.乙烷(C H)分子中有6个C-
2 6
H键和1个C-C键,所以1mol乙烷有7mol共价键。乙烯(C H)分子中有4个C-H键和1个C=C,
2 4
所以1mol乙烯有6mol共价键,选项D错误。【答案】B
3. (2018年全国卷III)苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是( )
A. 与液溴混合后加入铁粉可发生取代反应
B. 能使酸性高锰酸钾溶液褪色C. 与氯化氢反应可以生成氯代苯乙烯
D. 在催化剂存在下可以制得聚苯乙烯
【解析】A.苯乙烯中有苯环,液溴和铁粉作用下,溴取代苯环上的氢原子,所以选项A正确。B.苯乙
烯中有碳碳双键可以被酸性高锰酸钾溶液氧化,所以能使酸性高锰酸钾溶液褪色,选项B正确。C.苯乙
烯与HCl应该发生加成反应,得到的是氯代苯乙烷,选项C错误。
D.乙苯乙烯中有碳碳双键,可以通过加聚反应得到聚苯乙烯,选项D正确。【答案】C
4. (2018年全国卷III)下列实验操作不当的是( )
A. 用稀硫酸和锌粒制取H 时,加几滴CuSO 溶液以加快反应速率
2 4
B. 用标准HCl溶液滴定NaHCO 溶液来测定其浓度,选择酚酞为指示剂
3
C. 用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+
D. 常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二
C.用铂丝蘸取盐溶液在火焰上灼烧,进行焰色反应,火焰为黄色,说明该盐溶液中一定有Na+,选项C正
确。
D.蒸馏时,为保证加热的过程中液体不会从烧瓶内溢出,一般要求液体的体积不超过烧瓶体积的三分之
二,选项D正确。【答案】B
5. (2018年全国卷III)一种可充电锂-空气电池如图所示。当电池放电时,O 与Li+在多孔碳材料电极处生成
2
LiO (x=0或1)。下列说法正确的是( )
2 2-xA. 放电时,多孔碳材料电极为负极
B. 放电时,外电路电子由多孔碳材料电极流向锂电极
C. 充电时,电解质溶液中Li+向多孔碳材料区迁移
D. 充电时,电池总反应为LiO =2Li+(1-)O
2 2-x 2
【解析】A.题目叙述为:放电时,O 与Li+在多孔碳电极处反应,说明电池内,Li+向多孔碳电极移动,
2
因为阳离子移向正极,所以多孔碳电极为正极,选项A错误。B.因为多孔碳电极为正极,外电路电子应
该由锂电极流向多孔碳电极(由负极流向正极),选项B错误。C.充电和放电时电池中离子的移动方向
应该相反,放电时,Li+向多孔碳电极移动,充电时向锂电极移动,选项C错误。D.根据图示和上述分析,
电池的正极反应应该是O 与Li+得电子转化为LiO ,电池的负极反应应该是单质Li失电子转化为Li+,所
2 2 2-X
以总反应为:2Li + (1- )O = LiO ,充电的反应与放电的反应相反,所以为LiO = 2Li + (1-
2 2 2-X 2 2-X
)O ,选项D正确。【答案】D
2
6. (2018年全国卷III)用0.100 mol·L-1 AgNO 滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列
3
有关描述错误的是( )
A. 根据曲线数据计算可知K (AgCl)的数量级为10-10
sp
B. 曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K (AgCl)
sp
C. 相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D. 相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
【解析】A.选取横坐标为50mL的点,此时向50mL 0.05mol/L的Cl-溶液中,加入了50mL 0.1mol/L的
AgNO 溶液,所以计算出此时溶液中过量的Ag+浓度为0.025mol/L(按照银离子和氯离子1:1沉淀,同时不
3要忘记溶液体积变为原来2倍),由图示得到此时Cl-约为1×10-8mol/L(实际稍小),所以K (AgCl)约为
SP
0.025×10-8=2.5×10-10,所以其数量级为10-10,选项A正确。B.由于K (AgCl)极小,所以向溶液滴加硝酸
SP
银就会有沉淀析出,溶液一直是氯化银的饱和溶液,所以c(Ag+)·c(Cl-)=K (AgCl),选项B正确。C.滴定
SP
的过程是用硝酸银滴定氯离子,所以滴定的终点应该由原溶液中氯离子的物质的量决定,将50mL
0.05mol/L的Cl-溶液改为50mL 0.04mol/L的Cl-溶液,此时溶液中的氯离子的物质的量是原来的0.8倍,所
以滴定终点需要加入的硝酸银的量也是原来的0.8倍,因此应该由c点的25mL变为25×0.8=20mL,而a点
对应的是15mL,选项C错误。D.卤化银从氟化银到碘化银的溶解度应该逐渐减小,所以K (AgCl)应该
SP
大于K (AgBr),将50mL 0.05mol/L的Cl-溶液改为50mL 0.05mol/L的Br-溶液,这是将溶液中的氯离子换
SP
为等物质的量的溴离子,因为银离子和氯离子或溴离子都是1:1沉淀的,所以滴定终点的横坐标不变,但
是因为溴化银更难溶,所以终点时,溴离子的浓度应该比终点时氯离子的浓度更小,所以有可能由a点变
为b点。选项D正确。【答案】C
7. (2018年全国卷III)W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。盐YZW与浓
盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到YZW的溶液。下列说法正确的是( )
A. 原子半径大小为W<X<Y<Z
B. X的氢化物水溶液酸性强于Z的
C. YW 与ZW 均含有非极性共价键
2 2 2
D. 标准状况下W的单质状态与X的相同
B.HCl是强酸,HF是弱酸,所以X(F)的氢化物水溶液的酸性弱于Z(Cl)的。选项B错误。C.ClO
2
的中心原子是Cl,分子中只存在Cl和O之间的极性共价键,选项C错误。
D.标准状况下,W的单质O 或O 均为气态,X的单质F 也是气态。选项D正确。
2 3 2
【答案】D
8. (2018年全国卷III)硫代硫酸钠晶体(NaSO·5H O,M=248 g·mol−1)可用作定影剂、还原剂。回答下列
2 2 3 2
问题:(1)已知:Ksp(BaSO )=1.1×10−10,Ksp(BaS O)=4.1×10−5。市售硫代硫酸钠中常含有硫酸根杂质,选用下
4 2 3
列试剂设计实验方案进行检验:
试剂:稀盐酸、稀HSO 、BaCl 溶液、NaCO 溶液、HO 溶液
2 4 2 2 3 2 2
实验步骤 现象
①取少量样品,加入除氧蒸馏水 ②固体完全溶解得无色澄清溶液
③___________ ④___________,有刺激性气体产生
⑤静置,___________ ⑥___________
(2)利用KCr O 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
2 2 7
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________中溶解,完全
溶解后,全部转移至100 mL的_________中,加蒸馏水至____________。
②滴定:取0.00950 mol·L−1的KCr O 标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应: Cr O2−
2 2 7 2 7
+6I−+14H+ 3I+2Cr3++7H O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I+2S O2−
2 2 2 2 3
SO2−+2I−。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶
4 6
液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
【解析】(1)检验样品中的硫酸根离子,应该先加入稀盐酸,再加入氯化钡溶液。但是本题中,硫代硫
酸根离子和氢离子以及钡离子都反应,所以应该排除其干扰,具体过程应该为先将样品溶解,加入稀盐酸
酸化(反应为SO2- + 2H+ = SO↑+S↓+H O),静置,取上层清液中滴加氯化钡溶液,观察到白色沉淀,证
2 3 2 2
明存在硫酸根离子。所以答案为:③加入过量稀盐酸;④有乳黄色沉淀;⑤取上层清液,滴加氯化钡溶液;
⑥有白色沉淀产生。学#
①配制一定物质的量浓度的溶液,应该先称量质量,在烧杯中溶解,在转移至容量瓶,最后定容即可。所
以过程为:将固体再烧杯中加入溶解,全部转移至100mL容量瓶,加蒸馏水至刻度线。
②淡黄绿色溶液中有单质碘,加入淀粉为指示剂,溶液显蓝色,用硫代硫酸钠溶液滴定溶液中的单质碘,
滴定终点时溶液的蓝色应该褪去。根据题目的两个方程式得到如下关系式:Cr O2-~3I~6SO2-,则配制
2 7 2 2 3
的100mL样品溶液中硫代硫酸钠的浓度c= ,含有的硫代硫酸钠为
0.004597mol,所以样品纯度为【答案】(1). ③加入过量稀盐酸 (2). ④出现乳黄色浑浊 (3). ⑤(吸)取上层清液,滴入BaCl 溶液
2
(4). ⑥产生白色沉淀 (5). 烧杯 (6). 容量瓶 (7). 刻度 (8). 蓝色褪去 (9). 95.0
9. (2018年全国卷III)KIO 是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
3
(1)KIO 的化学名称是_______。
3
(2)利用“KClO 氧化法”制备KIO 工艺流程如下图所示:
3 3
“酸化反应”所得产物有KH(IO)、Cl 和KCl。“逐Cl”采用的方法是________。“滤液”中的溶质主要是
3 2 2 2
_______。“调pH”中发生反应的化学方程式为__________。
(3)KIO 也可采用“电解法”制备,装置如图所示。
3
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO 氧化法”的主要不足之处有______________(写出一点)。
3
【解析】(1)根据氯酸钾(KClO)可以推测KIO 为碘酸钾。
3 3
(2)将溶解在溶液中的气体排出的一般方法是将溶液加热,原因是气体的溶解度是随温度上升而下减小。
第一步反应得到的产品中氯气在“逐Cl”时除去,根据图示,碘酸钾在最后得到,所以过滤时KH(IO) 应该
2 3 2
在滤渣中,所以滤液中主要为KCl。“调pH”的主要目的是将KH(IO) 转化为KIO ,所以方程式为:
3 2 3
KH(IO)+KOH=2KIO +H O。
3 2 3 2
(3)①由图示,阴极为氢氧化钾溶液,所以反应为水电离的氢离子得电子,反应为2HO + 2e- = 2OH- +
2
H↑。
2
②电解时,溶液中的阳离子应该向阴极迁移,明显是溶液中大量存在的钾离子迁移,方向为由左向右,即
由a到b。③KClO 氧化法的最大不足之处在于,生产中会产生污染环境的氯气。
3
【答案】(1). 碘酸钾 (2). 加热 (3). KCl (4). KH(IO)+KOH 2KIO +H O 或(HIO +KOH
3 2 3 2 3
KIO +H O) (5). 2HO+2e- 2OH-+H ↑ (6). K+ (7). a到b (8). 产生Cl 易污染环境等
3 2 2 2 2
10. (2018年全国卷III)三氯氢硅(SiHCl )是制备硅烷、多晶硅的重要原料。回答下列问题:
3
(1)SiHCl 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO) O等,写出该反应的化学
3 2
方程式__________。
(2)SiHCl 在催化剂作用下发生反应:
3
2SiHCl (g) SiHCl(g)+ SiCl (g) ΔH =48 kJ·mol−1
3 2 2 4 1
3SiHCl(g) SiH(g)+2SiHCl (g) ΔH =−30 kJ·mol−1
2 2 4 3 2
则反应4SiHCl (g) SiH(g)+ 3SiCl (g)的ΔH=__________ kJ·mol−1。
3 4 4
(3)对于反应2SiHCl (g) SiHCl(g)+SiCl (g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和
3 2 2 4
343 K时SiHCl 的转化率随时间变化的结果如图所示。
3
①343 K时反应的平衡转化率α=_________%。平衡常数K =__________(保留2位小数)。
343 K
②在343 K下:要提高SiHCl 转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采
3
取的措施有____________、___________。
③比较a、b处反应速率大小:υ________υ(填“大于”“小于”或“等于”)。反应速率υ=υ −υ = −
a b 正 逆
,k 、k 分别为正、逆向反应速率常数,x为物质的量分数,计算a处 =__________
正 逆
(保留1位小数)。(3)①由图示,温度越高反应越快,达到平衡用得时间就越少,所以曲线a代表343K的反应。从图中读
出,平衡以后反应转化率为22%。设初始加入的三氯氢硅的浓度为1mol/L,得到:
2SiHCl SiH Cl + SiCl
3 2 2 4
起始: 1 0 0
反应: 0.22 0.11 0.11 (转化率为22%)
平衡: 0.78 0.11 0.11
所以平衡常数K=0.112÷0.782=0.02。
②温度不变,提高三氯氢硅转化率的方法可以是将产物从体系分离(两边物质的量相等,压强不影响平
衡)。缩短达到平衡的时间,就是加快反应速率,所以可以采取的措施是增大压强(增大反应物浓度)、
加入更高效的催化剂(改进催化剂)。
③a、b两点的转化率相等,可以认为各物质的浓度对应相等,而a点的温度更高,所以速率更快,即V>
a
V。根据题目表述得到 , ,当反应达平衡时 ,
b
= ,所以 ,实际就是平衡常数K值,所
以 0.02。a点时,转化率为20%,所以计算出:
2SiHCl SiHCl + SiCl
3 2 2 4
起始: 1 0 0
反应: 0.2 0.1 0.1 (转化率为20%)
平衡: 0.8 0.1 0.1所以 =0.8; = =0.1;所以
【答案】(1). 2SiHCl +3H O (HSiO) O+6HCl (2). 114 (3). ①22 (4). 0.02 (5). ②及时移去产物
3 2 2
(6). 改进催化剂 (7). 提高反应物压强(浓度) (8). ③大于 (9). 1.3
11. (2018年全国卷III)锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ (Zn)_______Ⅰ(Cu)(填“大
1 1
于”或“小于”)。原因是________________。
(3)ZnF 具有较高的熔点(872 ℃),其化学键类型是_________;ZnF 不溶于有机溶剂而ZnCl、ZnBr 、
2 2 2 2
ZnI 能够溶于乙醇、乙醚等有机溶剂,原因是________________。
2
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO )入药,可用于治疗皮肤炎症或表面创伤。
3
ZnCO 中,阴离子空间构型为________________,C原子的杂化形式为________________。
3
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a
cm,高为c cm,阿伏加德罗常数的值为N ,Zn的密度为________________g·cm-3(列出计算式)。
A
【解析】(1)Zn是第30号元素,所以核外电子排布式为Ar]3d104s2。
(2)Zn的第一电离能应该高于Cu的第一电离能,原因是,Zn的核外电子排布已经达到了每个能级都是
全满的稳定结构,所以失电子比较困难。同时也可以考虑到Zn最外层上是一对电子,而Cu的最外层是一
个电子,Zn电离最外层一个电子还要拆开电子对,额外吸收能量。
(3)根据氟化锌的熔点可以判断其为离子化合物,所以一定存在离子键。作为离子化合物,氟化锌在有
机溶剂中应该不溶,而氯化锌、溴化锌和碘化锌都是共价化合物,分子的极性较小,能够溶于乙醇等弱极
性有机溶剂。
(4)碳酸锌中的阴离子为CO2-,根据价层电子对互斥理论,其中心原子C的价电子对为3+(4-3×2+2)/
32=3对,所以空间构型为正三角形,中心C为sp2杂化。
(5)由图示,堆积方式为六方最紧密堆积。为了计算的方便,选取该六棱柱结构进行计算。六棱柱顶点
的原子是6个六棱柱共用的,面心是两个六棱柱共用,所以该六棱柱中的锌原子为12× +2× +3=6个,
所以该结构的质量为6×65/N g。该六棱柱的底面为正六边形,边长为a cm,底面的面积为6个边长为acm
A
的正三角形面积之和,根据正三角形面积的计算公式,该底面的面积为6× cm2,高为c cm,所以体
积为6× cm3。所以密度为: g·cm-3。
【答案】(1). Ar]3d104s2 (2). 大于 (3). Zn核外电子排布为全满稳定结构,较难失电子 (4). 离子键 (5).
ZnF 为离子化合物,ZnCl 、ZnBr 、ZnI 的化学键以共价键为主、极性较小 (6). 平面三角形 (7). sp2
2 2 2 2
(8). 六方最密堆积(A 型) (9).
3
12. (2018年全国卷III)近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种
多官能团的化合物Y,其合成路线如下:
已知:
回答下列问题:
(1)A的化学名称是________________。(2)B为单氯代烃,由B生成C的化学方程式为________________。
(3)由A生成B、G生成H的反应类型分别是________________、________________。
(4)D的结构简式为________________。
(5)Y中含氧官能团的名称为________________。
(6)E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为________________。
(7)X与D互为同分异构体,且具有完全相同官能团。X的核磁共振氢谱显示三种不同化学环境的氢,
其峰面积之比为3∶3∶2。写出3种符合上述条件的X的结构简式________________。
【解析】分析:根据A的结构,第一步进行取代得到B,再将B中的Cl取代为CN,水解后酯化得到D;
根据题目反应得到F的结构,进而就可以推断出结果。
详解:A到B的反应是在光照下的取代,Cl应该取代饱和碳上的H,所以B为 ;B与NaCN
反应,根据C的分子式确定B到C是将Cl取代为CN,所以C为 ;C酸性水解应该得到
,与乙醇酯化得到D,所以D为 ,D与HI加成得到E。
根据题目的已知反应,要求F中一定要有醛基,在根据H的结构得到F中有苯环,所以F一定为
;F与CHCHO发生题目已知反应,得到G,G为 ;G与氢气加成
3
得到H;H与E发生偶联反应得到Y。
(1)A的名称为丙炔。
(2)B为 ,C为 ,所以方程式为:
。
(3)有上述分析A生成B的反应是取代反应,G生成H的反应是加成反应。
(4)D为 。(5)Y中含氧官能团为羟基和酯基。
(6)E和H发生偶联反应可以得到Y,将H换为F就是将苯直接与醛基相连,所以将Y中的苯环直接与
羟基相连的碳连接即可,所以产物为 。
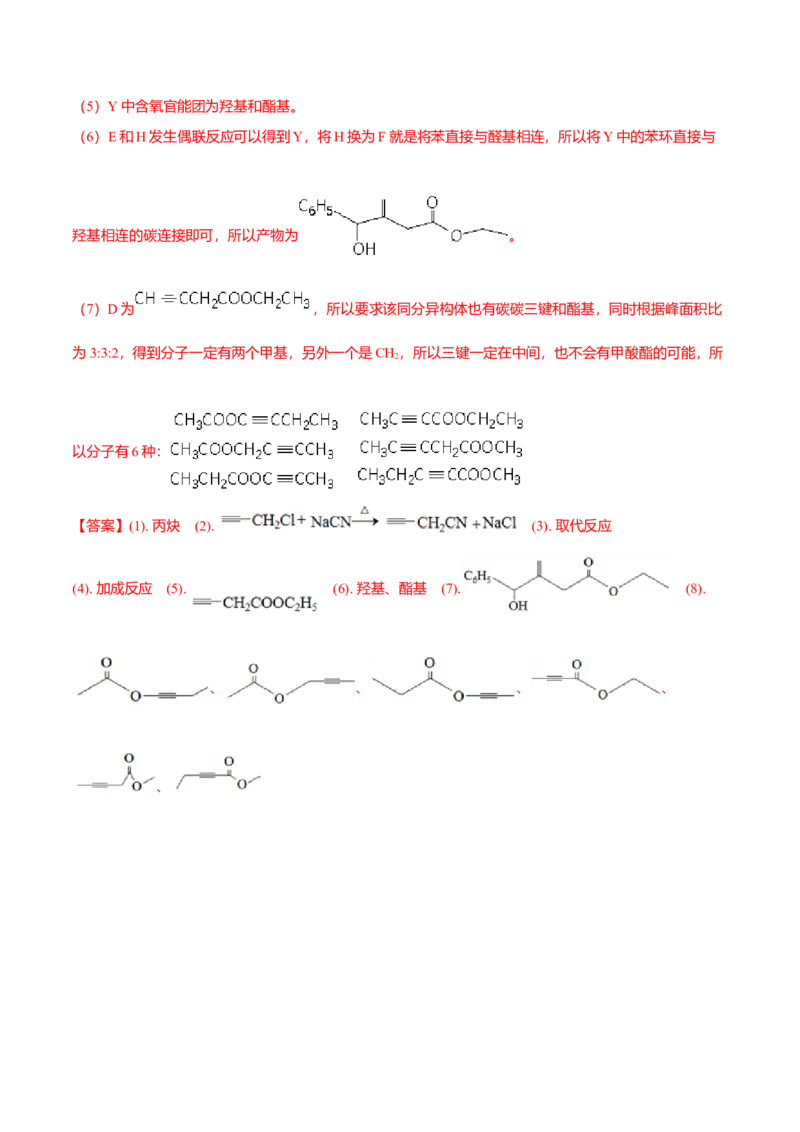
(7)D为 ,所以要求该同分异构体也有碳碳三键和酯基,同时根据峰面积比
为3:3:2,得到分子一定有两个甲基,另外一个是CH,所以三键一定在中间,也不会有甲酸酯的可能,所
2
以分子有6种:
【答案】(1). 丙炔 (2). (3). 取代反应
(4). 加成反应 (5). (6). 羟基、酯基 (7). (8).
、 、 、 、
、