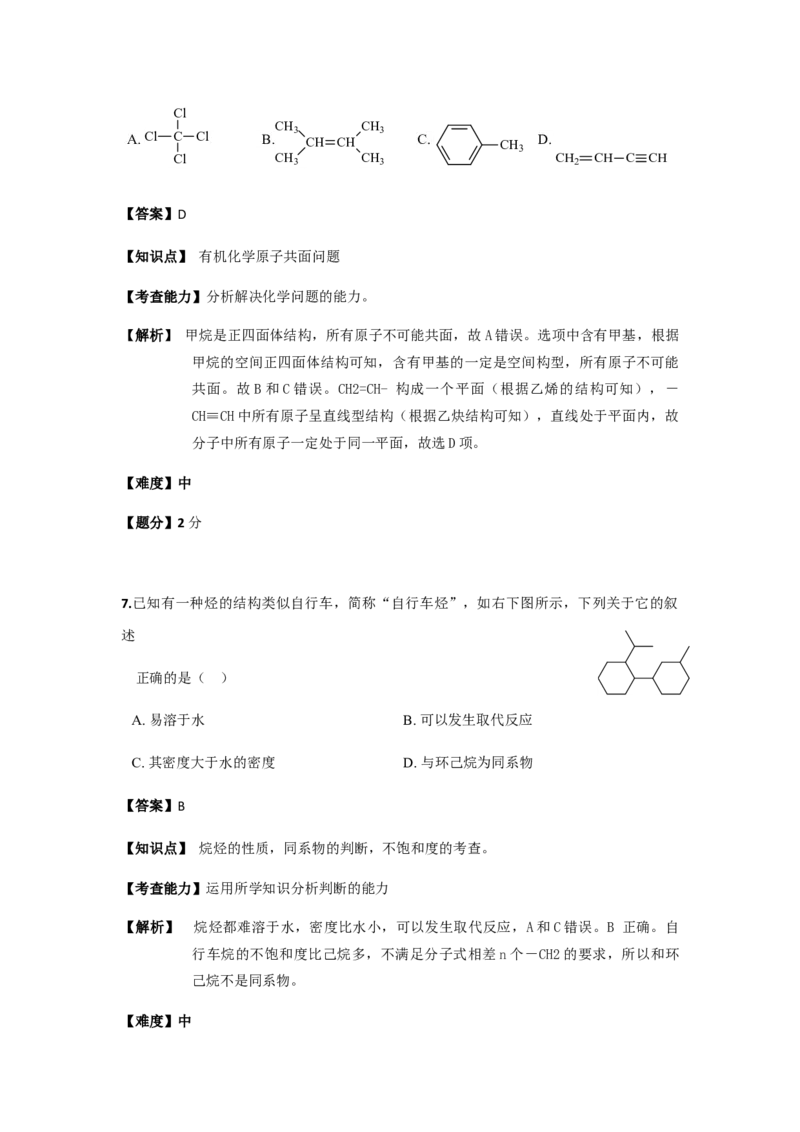2019 年上海市普通高中学业水平等级性考试
化学试卷
相对原子质量:C-12 O-16 S-32
一、选择题(每题只有一个正确答案,每题2分,共计40分)
1. 元素 中文名为(气奥),是一种人工合成的稀有气体元素,下列正确的是( )
A. 核外电子数是118 B. 中子数是295
C. 质量数是117 D. 第六周期0族元素
2. 下列变化中,只涉及物理变化的是( )
A. 次氯酸漂白 B. 盐酸除锈
C. 石油分馏 D. 煤干馏
3. 下列反应只需破坏共价键的是( )
A. 晶体硅熔化 B. 碘升华
C. 熔融Al O D. NaCl溶于水
2 3
4. 下列固体质量增加的是( )
A. Cu加入氯化铁 B. Zn加入硫酸
C. H 通入灼热氧化铜 D. 高温下水蒸气通入Fe
2
5. 25℃时,0.005mol/L Ba(OH) 中H+浓度是( )
2
A. 1× mol/L B. 1× mol/L
C. 5× mol/L D. 5× mol/L6. 所有原子处于同一平面的是( )
Cl
CH CH
3 3
A. Cl C Cl B. CH CH C. CH D.
3
Cl CH 3 CH 3 CH 2 CH C CH
7. 已知有一种烃的结构类似自行车,简称“自行车烃”,如右下图所示,下列关于它的叙
述正确的是( )
A. 易溶于水 B. 可以发生取代反应
C. 其密度大于水的密度 D. 与环己烷为同系物
CH
3
8. 聚异戊二烯 CH C CH CH 的单体是( )
2 2
n
CH
3
A. B.
CH 2 C CH CH 2 (CH 2 ) 2 C CH CH 2
CH
3
C. D.
(CH ) C CH CH CH C CH CH
3 2 2 2 2
9. 下列说法错误的是( )
A. 含有共价键的化合物是共价化合物
B. 含有极性键的分子可能是非极性分子
C. 有电子转移的反应是氧化还原反应
D. 水溶液中能完全电离的电解质是强电解质
10. 用镁带和稀硫酸反应产生氢气来测定氢气的气体摩尔体积,所用的步骤有①冷却至室温,
②调节使水
准管和量气管液面持平,③读数。正确的顺序是( )
A. ①②③ B. ①③②
C. ③①② D. ③②①11. 关于离子化合物NH (H有正价和负价)下列说法正确的是( )
5
A. N为+5价 B. 阴阳离子个数比是1:1
C. 阴离子为8电子稳定结构 D. 阳离子的电子数为11
12. 能证明亚硫酸钠中部分变质所需要的试剂是( )
A. 硝酸钡,稀硫酸 B. 稀盐酸,氯化钡
C. 稀硫酸,氯化钡 D. 稀硝酸,氯化钡
13. 用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法正确的是
( )
A. 可以用酚酞代替指示剂
B. 滴定前用待测液润洗锥形瓶
C. 若氢氧化钠吸收少量CO,不影响滴定结果
2
D. 当锥形瓶内溶液由橙色变为红色,且半分钟内不褪色,即达到滴定终点
14. 下列物质分离(括号内的物质为杂质)的方法错误的是( )
A. 硝基苯(苯)--蒸馏
B. 乙烯(SO )--氢氧化钠溶液
2
C. 己烷(己烯)--溴水,分液
D. 乙酸乙酯(乙醇)--碳酸钠溶液,分液
15. 短周期元素m、n、p、q在元素周期表中的排序如图所示,其中m的气态氢化物与其最
高价氧化物对应的水化物能反应。下列说法正确的是( )
A. 非金属性:m>n
m n
B. 氢化物稳定性:n
qD. 最高价氧化物对应水化物酸性:p>q
16. 在pH为1的100mL 0.1mol/L的AlCl 中,加入300mL 0.1mol/L的氢氧化钠溶液后铝元
3
素的存在形式是( )
A. AlO - B. Al3+ C. Al(OH) D. Al3+、Al(OH)
2 3 3
17. 关于下列装置,叙述错误的是( )
A. 石墨电极反应O+4H++4e→2H O
2 2
B. 鼓入少量空气,会加快Fe的腐蚀
C. 加入少量NaCl,会加快Fe的腐蚀
D. 加入HCl,石墨电极反应式:2H++2e→H
2
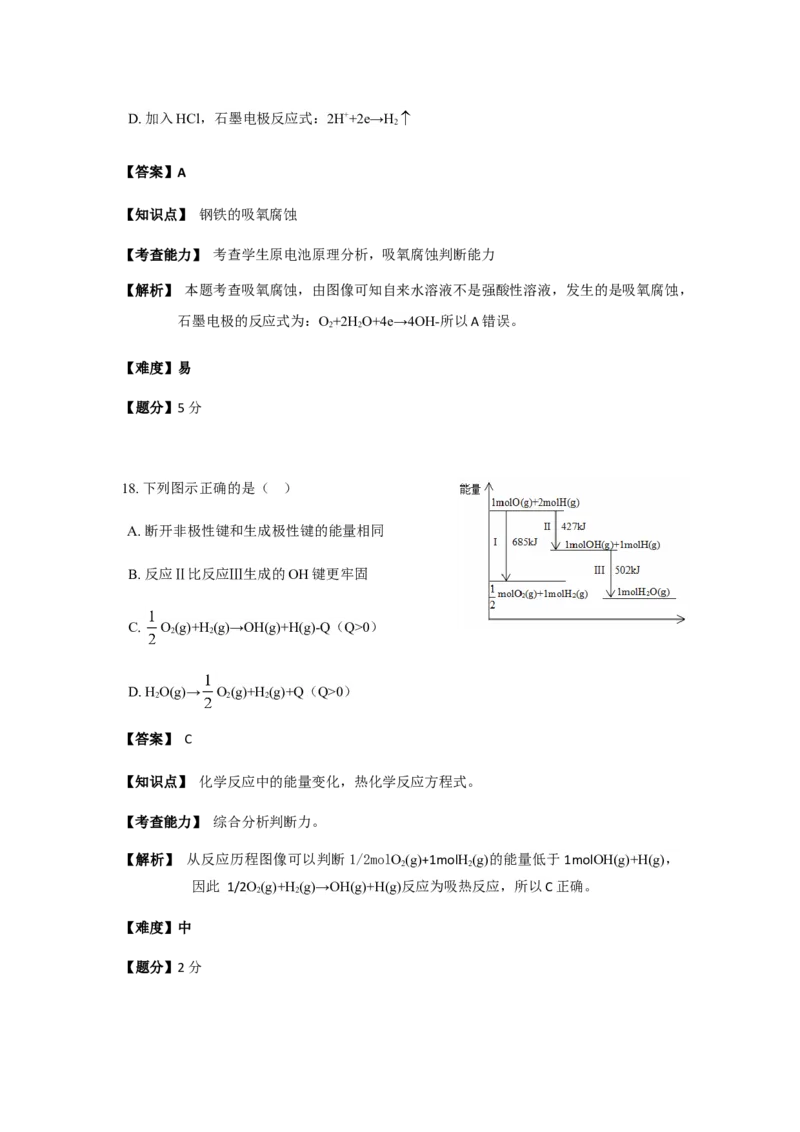
18. 下列图示正确的是( )
A. 断开非极性键和生成极性键的能量相同
B. 反应Ⅱ比反应Ⅲ生成的OH键更牢固
C. O(g)+H(g)→OH(g)+H(g)-Q(Q>0)
2 2
D. H O(g)→ O(g)+H(g)+Q(Q>0)
2 2 2
19. 已 知 反 应 式 : mX(g)+nY(?) pQ(s)+2mZ(g) , 已 知 反 应 已 达 平 衡 , 此 时
c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的 ,c(X)=0.5mol/L,下列说法正
确的是( )
A. 反应向逆方向移动 B. Y可能是固体或液体
C. 系数n>m D. Z的体积分数减小
20. 常温下0.1mol/L ①CH COOH、②NaOH、③CHCOONa,下列叙述正确的是( )
3 3A. ①中[CHCOOH]>[CH COO-]>[H+]>[OH-]
3 3
B. ①②等体积混合后,醋酸根离子浓度小于③的二分之一
C. ①③等体积混合以后,溶液呈酸性,则(Na+)>(CH COO-)>(H+)
3
D. ①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
二、综合分析题(60分)
(一)(15分)氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。
21. 氨态氮肥为何不能与碱性物质混用?_________________________________________
22. 在合成氨工业中,压强通常控制在20~50MP,其原因是
______________________________________。
23. 侯德榜联合制碱法是向饱和食盐水中依次通入足量的氨气与二氧化碳,写出反应的化学
方程式______________________________________________。
24. 烟气中的NO 与尿素[CO(NH)](C的化合价为+4)反应进行脱硝。反应的化学方程式
2 2 2
是2CO(NH)+4NO→4HO+2CO+4N +O 。该反应的氧化产物为__________,若反应
2 2 2 2 2 2 2
过程中有0.15molNO 反应,则电子转移的数目为____________。
2
25. 常温下,在氯化铵溶液中加入一定量的氢氧化钠,使其pH=7,则
c(Na+)____c(NH ·H O)(填“<”、“>”或“=”)。
3 2
(二)(15分)某实验小组同学为了探究铜与浓硫酸的反应,进行了一系列实验。在反应
过程中会发生一些副反应,生成不溶于水和酸的CuS、Cu S。
2
26. 处于安全和绿色化学考虑,在制取硫酸铜时,可选用下列的物质是___________。a. Cu b. CuO c. CuS d. CuSO ·Cu(OH) ∙HO
4 2 2
27. 装置a的作用是________________________。
反应过程中,因为浓硫酸的吸水作用,烧瓶中出现白色固体物质,如何简便检验反应
后圆底烧瓶里有Cu2+存在?
_______________________________________________________________
在实际反应中,由于条件控制不好,容易产生 CuS和Cu2S固体:2CuS
Cu S+S。
2
28. 已知样品质量为ag,得到Cu S是bg,则样品中CuS质量分数是________。如果Cu S
2 2
高温下转化为Cu,则实验测得的值会______(填“偏大”、“偏小”或“不变”)
29. 根据以上信息,说明铜与浓硫酸反应需要控制哪些条件?
______________________________________
(三)(15分)白藜芦醇是一种抗肿瘤的药物,合成它的一种路线如下:
SOCl2
HO CH2Cl
NaCN K2CO3
RO CH2CN
C7H8O3
¢Ù
C8H7NO2
RCl HO OH
A
OH OR
OH
K2CO3
C7H6O2 RO G °×޼«´¼
RCl
B
30. A的结构简式__________。①的反应类型_____________。
31. B的芳香类同分异构体中可以发生水解的结构简式为_________,在酸性条件下水解的
产物为________。
32. 检验官能团G所用的试剂是__________________________。
33. 根据已有知识并结合相关信息,写出以HO-CH-CH-CH-CH-OH和CHOH为原料制
2 2 2 2 3
备CHOOCCH CHCHCHCOOCH 的合成路线流程图(无机试剂任用)。 (已知RCN
3 2 2 2 2 3RCOOH)合成路线流程图如下:(甲————→乙……————→目标产物)
(四)(15分)LiFe (PO ) 作为锂离子电池的负极材料时有良好的放电平台,通过提高材
2 4 3
料的电导率可以有效的改善材料的性能。
34. 配平下列反应的化学方程式。
____LiFe (PO )+1 Fe O+________CO→_______CO+________LiFePO
2 4 3 2 3 2 4
35. CO 的电子式为__________,P原子的核外电子有_____种不同能量的电子。
2
研究CO 与CH 的反应使之转化为H 和CO对减缓燃料危机,减少温室效应具有重大
2 4 2
意义。已知CH(g)+CO (g) 2H(g)+2CO(g)。
4 2 2
36. 该反应的平衡常数K=_________。在2L密闭容器中,通入CO 和CH 的混合气体,
2 4
30min后,CH 的质量减少了4.8g,则v(CH)=________。
4 4
37. 根据下图可得出 n(CO) _____n(CH) (填“>”、“<”和“=”),原因是
2 4
_________________________________________________________________________
______________________________。2019 年上海市普通高中学业水平等级性考试
化学试卷参考答案
一、选择题(每题只有一个正确答案,每题2分,共计40分)
1 2 3 4 5 6 7 8 9 10
A C A D A D B D A A
11 12 13 14 15 16 17 18 19 20
B B C C C D A C C B
二、综合分析题(60分)
(一)(15分)21. 铵态氮肥与碱性物质混合使用时,会使NH +转化为NH 挥发,造成氮
4 3
元素流失,降低肥效
22. 高压能使平衡正向移动,提高反应物转化率;压强过高会增大设备成本
23. CO+NH+NaCl+HO→NH Cl+NaHCO ↓
2 3 2 4 3
24. N 和O;0.6N
2 2 A
25. =
(二)(15分)26. bd
27. 防倒吸;将反应后的溶液沿烧杯壁缓缓倒入水中,若溶液变蓝,则有Cu2+存在
28. 2(a-b)/a;偏大
29. 温度不宜过高,时间不宜过长
HO CH2OH
(三)(15分)30. ;取代
OH
31. HCOO ;HCOOH、 OH32. 新制Cu(OH) 悬浊液
2
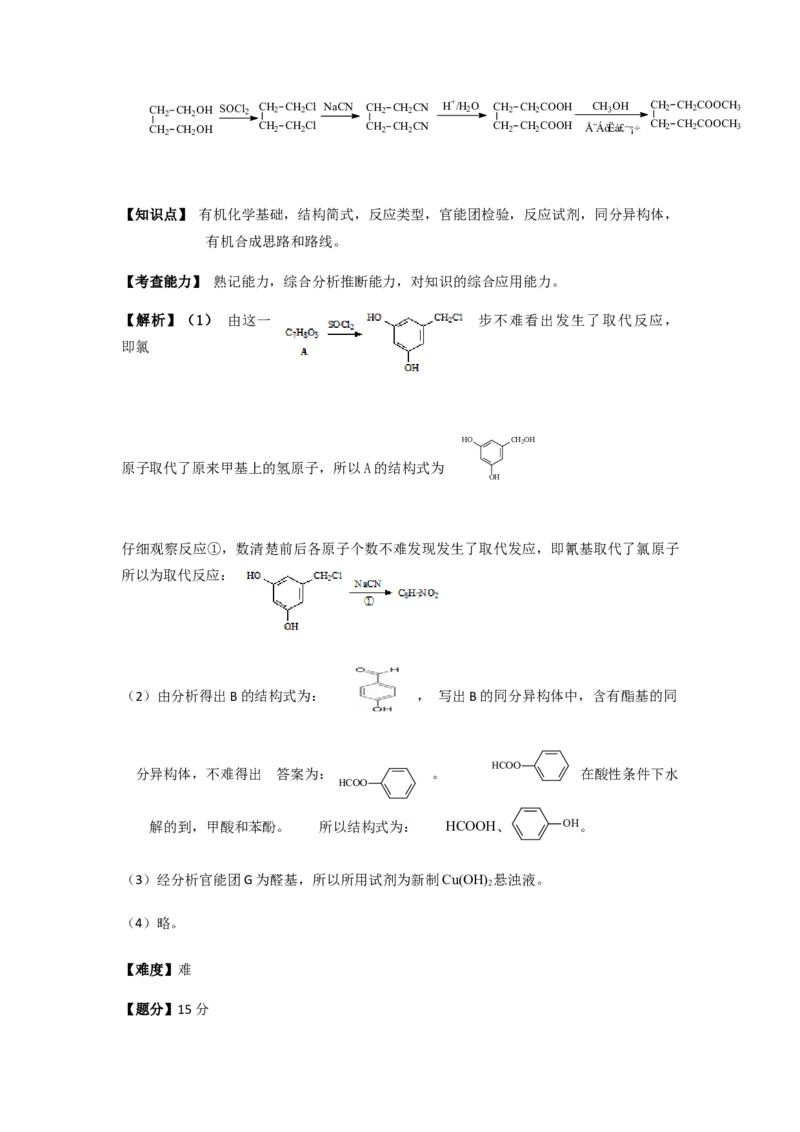
33.
CH 2 CH 2 OH SOCl 2 CH 2 CH 2 Cl NaCN CH 2 CH 2 CN H+/H 2 O CH 2 CH 2 COOH CH 3 OH CH 2 CH 2 COOCH 3
CH 2 CH 2 OH CH 2 CH 2 Cl CH 2 CH 2 CN CH 2 CH 2 COOH ŨÁòËᣬ¡÷ CH 2 CH 2 COOCH 3
(四)(15分)34. 2LiFe (PO )+1 Fe O+3CO→3CO+6LiFePO
2 4 3 2 3 2 4
35. ;5
36. ;0.005mol/(L∙min)
37. >;根据图中信息,有HO生成,平衡时n(H )n
m n
B. 氢化物稳定性:nq
D. 最高价氧化物对应水化物酸性:p>q
【答案】 C
【知识点】元素周期律
【考查能力】分析推理,整合化学信息的能力。
【解析】既有氢化物又有最高价氧化物的水化物的元素一般为非金属元素,非金属的最高
价氧化物水化物为最高价含氧酸。因此其氢化物必须是碱性物质。两者才能反应。
氢化物为碱性的只有氮元素,即为氨气,所以m为N,n为O, p为S, q为Cl.非
金属性O>S,A错误。氢化物稳定性与共价键有关。键长越短,分子越稳定。O
的半径小于S, O-H键比S-H键短,因此稳定性H2O >H₂S,B错误。 S2- 和Cl-
电子层结构相同,核电荷数S2-< Cl-,因此半径S2->Cl-,C正确。S的非金属性弱于Cl,所以最高价氧化物水化物的酸性H2SO40)
2 2
D. H O(g)→ O(g)+H(g)+Q(Q>0)
2 2 2
【答案】 C
【知识点】 化学反应中的能量变化,热化学反应方程式。
【考查能力】 综合分析判断力。
【解析】 从反应历程图像可以判断1/2molO(g)+1molH(g)的能量低于1molOH(g)+H(g),
2 2
因此 1/2O(g)+H(g)→OH(g)+H(g)反应为吸热反应,所以C正确。
2 2
【难度】中
【题分】2分19. 已 知 反 应 式 : mX(g)+nY(?) pQ(s)+2mZ(g) , 已 知 反 应 已 达 平 衡 , 此 时
c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的 ,c(X)=0.5mol/L,下列说法正
确的是( )
A. 反应向逆方向移动 B. Y可能是固体或液体
C. 系数n>m D. Z的体积分数减小
【答案】 C
【知识点】 化学反应平衡移动,勒夏特列原理分析。
【考查能力】理解分析能力
【解析】 已知反应达平衡时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的1/2,如
果化学平衡不移动,c(X)=0.6mol/L,但是题中说c(X)=0.5mol/L说明加压后化
学平衡向正向移动了,故A错误。结合题意可知正反应是气体总体积减少的反
应,如果y为固体或液体,则必须满足m>2m,显然不可能成立。所以有只能
是气体B 错误。要满足m+n>2m,所以n>m。C正确。根据题意化学平衡向右
移动,Z的体积分数是增大的 ,所以D错误。
【难度】中
【题分】2分
20. 常温下0.1mol/L ①CH COOH、②NaOH、③CHCOONa,下列叙述正确的是( )
3 3
A. ①中[CHCOOH]>[CH COO-]>[H+]>[OH-]
3 3
B. ①②等体积混合后,醋酸根离子浓度小于③的二分之一
C. ①③等体积混合以后,溶液呈酸性,则(Na+)>(CH COO-)>(H+)
3
D. ①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
【答案】 B
【知识点】 电解质溶液,微粒大小判断,盐类的水解。弱电解质的电离等知识。【考查能力】 综合分析判断能力。
【 解 析 】 CHCOOH 溶 液 中 的 H+ 来 自 醋 酸 分 子 的 电 离 和 水 的 电 离 , 所 以
3
[CHCOOH]>[H+]>[CH COO-]>[OH-]故A错误。 ①②等体积混合后恰好反应生
3 3
成CHCOONa,体积大约为原来的2倍,如果CH3COO-不水解,浓度约为原
3
来 的 1/2 , CHCOONa 为 弱 酸 强 碱 盐 , 越 稀 越 水 解 , CH3COO-
3
+H2O→CH3COOH+OH-,水解平衡向正向移动,因此CH3COO-浓度小于原来的
1/2.B正确。①③等体积混合以后,溶液呈酸性,说明CHCOOH的电离程度大
3
于CH3COO- 的水解程度,因此(CHCOO-)>(Na+)>(H+),C错误。①②等体积混
3
合以后恰好反应生成CHCOONa,CH3COO- 的水解促进水的电离。①③等体积
3
混合,CHCOOH的电离产生H+抑制水的电离。因此总体上看①②等体积混合
3
后水的电离程度比①③等体积混和后水的电离程度大。D错误。
【难度】难
【题分】2分
二.综合分析题
(一)氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。
21. 氨态氮肥为何不能与碱性物质混用?_________________________________________
22. 在合成氨工业中,压强通常控制在20~50MP,其原因是
______________________________________。
23. 侯德榜联合制碱法是向饱和食盐水中依次通入足量的氨气与二氧化碳,写出反应的化学
方程式______________________________________________。
24. 烟气中的NO 与尿素[CO(NH)](C的化合价为+4)反应进行脱硝。反应的化学方程式
2 2 2
是2CO(NH)+4NO→4HO+2CO+4N +O 。该反应的氧化产物为__________,若反应
2 2 2 2 2 2 2
过程中有0.15molNO 反应,则电子转移的数目为____________。
2
25. 常温下,在氯化铵溶液中加入一定量的氢氧化钠,使其pH=7,则
c(Na+)____c(NH ·H O)(填“<”、“>”或“=”)。
3 2【答案】
(一)21. 铵态氮肥与碱性物质混合使用时,会使NH +转化为NH 挥发,造成氮元素流失
4 3
降低肥效
22. 高压能使平衡正向移动,提高反应物转化率;压强过高会增大设备成本
23. CO+NH+NaCl+HO→NH Cl+NaHCO ↓,2NaHCO3→Na2CO3+H2O+CO2↑
2 3 2 4 3
24. N 和O;0.6N
2 2 A
25. =
【知识点】 铵盐的性质,氧化还原反应的基本概念,电子转移的计算,侯德榜制碱的原理
方程式默写,合成氨的条件,电解质溶液中的电荷守恒和物料守恒。
【考查能力】 理解熟记,分析,综合应用能力。
【解析】 (1)铵盐和碱反应生成氨气逸出,不能被植物吸收,导致肥效降低。考查铵盐
的性质。
(2)合成氨反应N2(g)+3H₂⇌ (g)→2NH₃(g)的条件是高温高压催化剂,正反应为
气体体积减少的反应,根据勒夏特例原理,增大压强化学平衡向正反应方
向移动有利于提高氨气的转化率,但压强不能过高,否则会增加设备等成
本,因此选择20-50MPa的压强。本题从压强对平衡的影响以及从成本的角
度考虑来解决问题。
(3)侯德榜制碱的反应原理为:CO+NH+NaCl+HO→NH Cl+NaHCO ↓,
2 3 2 4 3
2NaHCO3→Na2CO3+H20+CO2↑,考查方程式默写。
(4)氧化产物是化合价升高的产物,本反应化合价升高的元素有两种,一种是氧
元素从-2价升高到0价,生成氧气。另一种是CO(NH)2 的 氮元素从-3
2
价升高为0价的N氮气,因此氧化产物为 N 和O 根据方程式化合价变化
2 2;
情况可以得知4NO2—16e,转移电子数和二氧化氮的比例关系为4:1,因此
吸收0.15molNO2转移的电子数0.15mol×4=0.6mol,即0.6NA个。
(5)根据电荷守恒,c(NH4+) + c(H+)+c(Na+)= c(OH-) + c(Cl-),因为溶液呈
中性,所以c(H+)= c(OH-), 因此可以得出c(NH4+)+c(Na+) =c(Cl-),氯
化铵溶液中的物料守恒守恒为:c(NH4+) + c(NH3.H2O) = c(Cl-) ,所以c(Na+) =c(NH3.H2O)。
【难度】中
【题分】15分
(二)某实验小组同学为了探究铜与浓硫酸的反应,进行了一系列实验。在反应过程中会
发生一些副反应,生成不溶于水和酸的CuS、Cu S。
2
26. 处于安全和绿色化学考虑,在制取硫酸铜时,可选用下列的物质是___________。
a. Cu b. CuO c. CuS d. CuSO ·Cu(OH) ∙HO
4 2 2
27. 装置a的作用是________________________。
反应过程中,因为浓硫酸的吸水作用,烧瓶中出现白色固体物质,如何简便检验反应
后 圆 底 烧 瓶 里 有 Cu2+ 存 在 ?
_______________________________________________________________
28 在实际反应中,由于条件控制不好,容易产生 CuS和Cu2S固体:2CuS
Cu S+S。
2
已知样品质量为 ag,得到Cu S是bg,则样品中 CuS质量分数是________。如果
2
Cu S高温下转化为Cu,则实验测得的值会______(填“偏大”、“偏小”或“不
2
变”)
29. 根 据 以 上 信 息 , 说 明 铜 与 浓 硫 酸 反 应 需 要 控 制 哪 些 条 件 ?
______________________________________【答案】
26. bd
27. 防倒吸;将反应后的溶液沿烧杯壁缓缓倒入水中,若溶液变蓝,则有Cu2+存在。
28. 2(a-b)/a;偏大
29. 温度不宜过高,时间不宜过长。
【知识点】 浓硫酸的性质和稀释问题,铜及其化合物,实验相关知识,误差分析和化学计
算。
【考查能力】 实验综合分析能力,增强环保意识。
【解析】(1) 铜和浓硫酸加热时反应才会制取硫酸铜,同时生成二氧化硫大气污染物,
酸雨气体,故不选A。氧化铜和稀硫酸反应生成硫酸铜和水,无污染物产
生,B正确。 CuS 不溶于酸要想制备硫酸铜先和氧气作用生成氧化铜和二
氧化硫,2CuS + 3O2 →2CuO + 2SO2氧化铜在和稀硫酸作用生成硫酸铜,
在过程中产生二氧化硫大气污染物,故不选C。CuSO ·Cu(OH) ∙HO只需要
4 2 2
和稀硫酸反应可制取硫酸铜,并没有有害物产生,综上分析正确答案选
bd。
(2) 二氧化硫被氢氧化钠溶液吸收,有压强差,很溶液产生倒吸,球形管有比较
大的空间,防止形成过大的负压,可以防止倒吸;由于浓硫酸有吸水性,
所不容易观察溶液颜色,需要将溶液稀释后检验铜离子是否存在,浓硫酸
的稀释应注意酸入水,将原溶液倒入水中进行稀释,如果溶液显蓝色则证
明铜离子存在。
(3) 设样品中CuS xg,Cu S为yg,列方程组,质量守恒:x+y=a,铜原子守恒:
2
(X/96+2y/160)/2=b/160.两个方程联立。可解得x=6a-6b.所以样品中CuS的
质量分数为:6a-6b/a。
Cu S在高温下会转化为Cu,则测的加热后固体的质量b偏小,根据方程式得出
2
CuS的质量分数偏大。(4)根据题意可以得出控制温度不能过高,加热时间不易太长。
【难度】难
【题分】15分
(三)白藜芦醇是一种抗肿瘤的药物,合成它的一种路线如下:
SOCl2
HO CH2Cl
NaCN K2CO3
RO CH2CN
C7H8O3
¢Ù
C8H7NO2
RCl HO OH
A
OH OR
OH
K2CO3
C7H6O2 RO G °×޼«´¼
RCl
B
30. A的结构简式__________。①的反应类型_____________。
31. B的芳香类同分异构体中可以发生水解的结构简式为_________,在酸性条件下水解的
产物为________。
32. 检验官能团G所用的试剂是__________________________。
33. 根据已有知识并结合相关信息,写出以HO-CH-CH-CH-CH-OH和CHOH为原料制
2 2 2 2 3
备CHOOCCH CHCHCHCOOCH 的合成路线流程图(无机试剂任用)。 (已知RCN
3 2 2 2 2 3
RCOOH)合成路线流程图如下:(甲————→乙……————→目标产物)
HO CH2OH
【答案】 30. ;取代
OH
31. HCOO ;HCOOH、 OH
32. 新制Cu(OH) 悬浊液
2
33.CH 2 CH 2 OH SOCl 2 CH 2 CH 2 Cl NaCN CH 2 CH 2 CN H+/H 2 O CH 2 CH 2 COOH CH 3 OH CH 2 CH 2 COOCH 3
CH 2 CH 2 OH CH 2 CH 2 Cl CH 2 CH 2 CN CH 2 CH 2 COOH ŨÁòËᣬ¡÷ CH 2 CH 2 COOCH 3
【知识点】 有机化学基础,结构简式,反应类型,官能团检验,反应试剂,同分异构体,
有机合成思路和路线。
【考查能力】 熟记能力,综合分析推断能力,对知识的综合应用能力。
【解析】(1) 由这一 步不难看出发生了取代反应,
即氯
HO CH2OH
原子取代了原来甲基上的氢原子,所以A的结构式为
OH
仔细观察反应①,数清楚前后各原子个数不难发现发生了取代发应,即氰基取代了氯原子
所以为取代反应:
(2)由分析得出B的结构式为: , 写出B的同分异构体中,含有酯基的同
HCOO
分异构体,不难得出 答案为: 。 在酸性条件下水
HCOO
解的到,甲酸和苯酚。 所以结构式为: HCOOH、 OH。
(3)经分析官能团G为醛基,所以所用试剂为新制Cu(OH) 悬浊液。
2
(4)略。
【难度】难
【题分】15分(四)LiFe (PO ) 作为锂离子电池的负极材料时有良好的放电平台,通过提高材料的电导
2 4 3
率可以有效的改善材料的性能。
34. 配平下列反应的化学方程式。
____LiFe (PO )+1 Fe O+________CO→_______CO+________LiFePO
2 4 3 2 3 2 4
35. CO 的电子式为__________,P原子的核外电子有_____种不同能量的电子。
2
研究CO 与CH 的反应使之转化为H 和CO对减缓燃料危机,减少温室效应具有重大
2 4 2
意义。已知CH(g)+CO (g)→2H(g)+2CO(g)。
4 2 2
36. 该反应的平衡常数K=_________。在2L密闭容器中,通入CO 和CH 的混合气体,
2 4
30min后,CH 的质量减少了4.8g,则v(CH)=________。
4 4
37. 根据下图可得出 n(CO) _____n(CH) (填“>”、“<”和“=”),原因是
2 4
____________________
_____________________________________________________________________________
_______。
【答案】 34. 2LiFe (PO )+1 Fe O+3CO→3CO+6LiFePO
2 4 3 2 3 2 4
35. ;536. ;0.005mol/(L∙min)
37. >;根据图中信息,有HO生成,平衡时n(H )