文档内容
绝密★启用前
2019 年全国统一高考化学试卷(新课标Ⅲ)
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I
127
一、选择题:本题共 13个小题,每小题 6分。共 78分,在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.化学与生活密切相关。下列叙述错误的是
A. 高纯硅可用于制作光感电池
B. 铝合金大量用于高铁建设
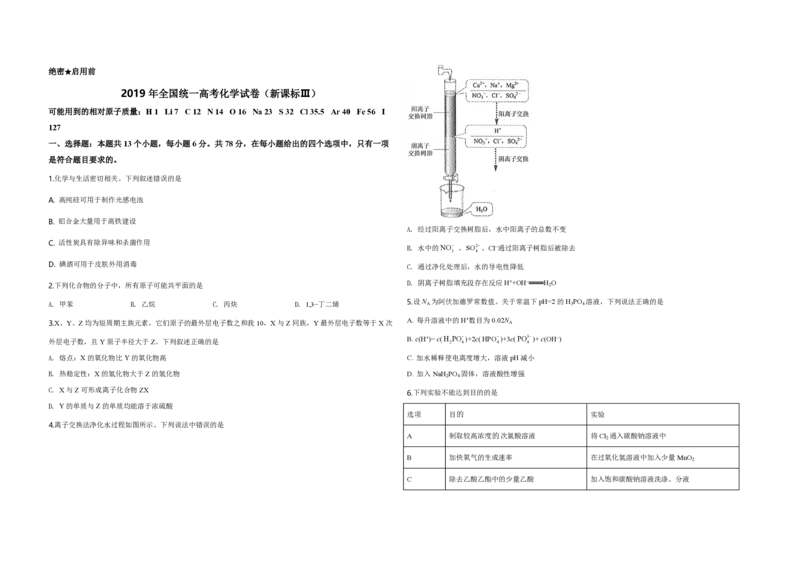
A. 经过阳离子交换树脂后,水中阳离子的总数不变
C. 活性炭具有除异味和杀菌作用
B. 水中的NO 、SO2、Cl−通过阳离子树脂后被除去
3 4
D. 碘酒可用于皮肤外用消毒 C. 通过净化处理后,水的导电性降低
D. 阴离子树脂填充段存在反应H++OH− H O
2.下列化合物的分子中,所有原子可能共平面的是 2
A. 甲苯 B. 乙烷 C. 丙炔 D. 1,3−丁二烯
5.设N
A
为阿伏加德罗常数值。关于常温下pH=2的H
3
PO
4
溶液,下列说法正确的是
A. 每升溶液中的H+数目为0.02N
3.X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和我10,X与Z同族,Y最外层电子数等于X次 A
B. c(H+)= c(H PO)+2c(HPO)+3c(PO3)+ c(OH−)
外层电子数,且Y原子半径大于Z。下列叙述正确的是
2 4 4 4
A. 熔点:X的氧化物比Y的氧化物高 C. 加水稀释使电离度增大,溶液pH减小
B. 热稳定性:X的氢化物大于Z的氢化物 D. 加入NaH PO 固体,溶液酸性增强
2 4
C. X与Z可形成离子化合物ZX
6.下列实验不能达到目的的是
D. Y的单质与Z的单质均能溶于浓硫酸
选项 目的 实验
4.离子交换法净化水过程如图所示。下列说法中错误的是
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸 6 2
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 . 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
A. A B. B C. C D. D
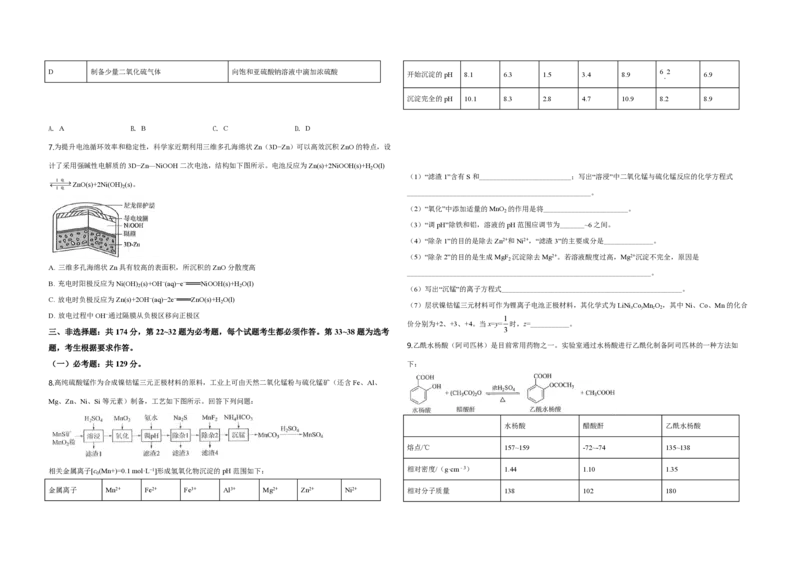
7.为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设
计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H O(l)
2
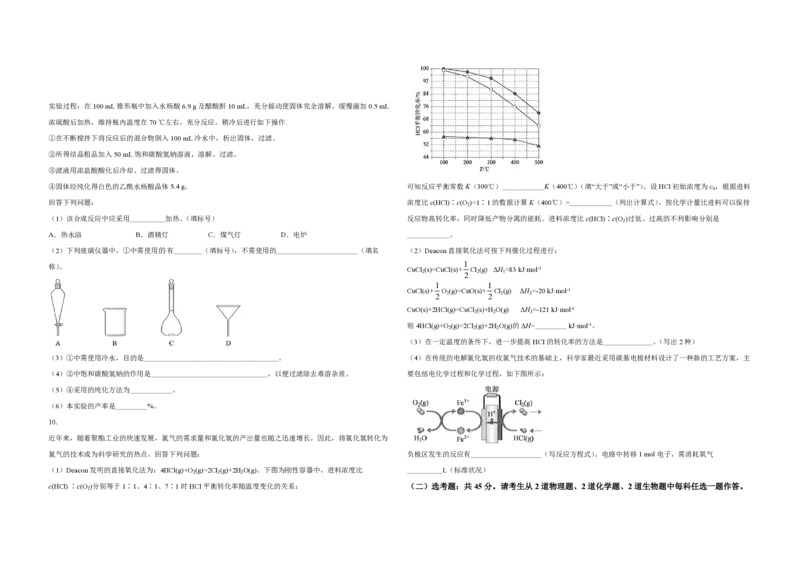
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式
充电 ZnO(s)+2Ni(OH) (s)。
充 电 2
____________________________________________________。
(2)“氧化”中添加适量的MnO 的作用是将________________________。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
2
A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
_____________________________________________________________________。
B. 充电时阳极反应为Ni(OH) (s)+OH−(aq)−e− NiOOH(s)+H O(l)
2 2
(6)写出“沉锰”的离子方程式___________________________________________________。
C. 放电时负极反应为Zn(s)+2OH−(aq)−2e− ZnO(s)+H O(l)
2
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNi Co MnO ,其中Ni、Co、Mn的化合
x y z 2
D. 放电过程中OH−通过隔膜从负极区移向正极区
1
价分别为+2、+3、+4。当x=y= 时,z=___________。
三、非选择题:共 174分,第 22~32 题为必考题,每个试题考生都必须作答。第 33~38 题为选考 3
题,考生根据要求作答。 9.乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如
(一)必考题:共 129分。 下:
8.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、
Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
水杨酸 醋酸酐 乙酰水杨酸
熔点/℃ 157~159 -72~-74 135~138
相关金属离子[c (Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下: 相对密度/(g·cm﹣3) 1.44 1.10 1.35
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+ 相对分子质量 138 102 180实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL
浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作.
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。 可知反应平衡常数K(300℃)____________K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c ,根据进料
0
回答下列问题: 浓度比c(HCl)∶c(O )=1∶1的数据计算K(400℃)=____________(列出计算式)。按化学计量比进料可以保持
2
(1)该合成反应中应采用__________加热。(填标号) 反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O )过低、过高的不利影响分别是
2
A.热水浴 B.酒精灯 C.煤气灯 D.电炉 ____________。
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________________(填名 (2)Deacon直接氧化法可按下列催化过程进行:
1
称)。
CuCl (s)=CuCl(s)+ Cl (g) ΔH =83 kJ·mol-1
2 2 1
2
1 1
CuCl(s)+ O (g)=CuO(s)+ Cl (g) ΔH =-20 kJ·mol-1
2 2 2
2 2
CuO(s)+2HCl(g)=CuCl (s)+H O(g) ΔH =-121 kJ·mol-1
2 2 3
则4HCl(g)+O (g)=2Cl (g)+2H O(g)的ΔH=_________ kJ·mol-1。
2 2 2
(3)在一定温度的条件下,进一步提高HCI的转化率的方法是______________。(写出2种)
(3)①中需使用冷水,目的是______________________________________。 (4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主
(4)②中饱和碳酸氢钠的作用是_________________________________,以便过滤除去难溶杂质。 要包括电化学过程和化学过程,如下图所示:
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。
10.
近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为
氯气的技术成为科学研究的热点。回答下列问题: 负极区发生的反应有____________________(写反应方程式)。电路中转移1 mol电子,需消耗氧气
(1)Deacon发明的直接氧化法为:4HCl(g)+O (g)=2Cl (g)+2H O(g)。下图为刚性容器中,进料浓度比 __________L(标准状况)
2 2 2
c(HCl) ∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系: (二)选考题:共 45分。请考生从 2道物理题、2道化学题、2道生物题中每科任选一题作答。
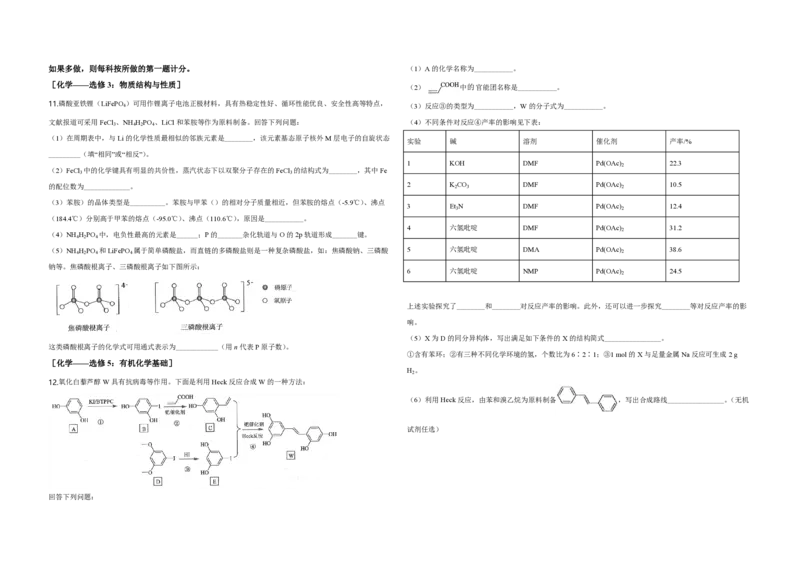
2如果多做,则每科按所做的第一题计分。 (1)A的化学名称为___________。
[化学——选修 3:物质结构与性质]
(2) 中的官能团名称是___________。
11.磷酸亚铁锂(LiFePO
4
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,
(3)反应③的类型为___________,W的分子式为___________。
文献报道可采用FeCl 、NH H PO 、LiCl和苯胺等作为原料制备。回答下列问题: (4)不同条件对反应④产率的影响见下表:
3 4 2 4
(1)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核外M层电子的自旋状态
实验 碱 溶剂 催化剂 产率/%
_________(填“相同”或“相反”)。
1 KOH DMF Pd(OAc) 22.3
2
(2)FeCl 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl 的结构式为________,其中Fe
3 3
的配位数为_____________。 2 K 2 CO 3 DMF Pd(OAc) 2 10.5
(3)苯胺)的晶体类型是__________。苯胺与甲苯()的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点
3 Et N DMF Pd(OAc) 12.4
3 2
(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是___________。
4 六氢吡啶 DMF Pd(OAc) 31.2
2
(4)NH H PO 中,电负性最高的元素是______;P的_______杂化轨道与O的2p轨道形成_______键。
4 2 4
(5)NH 4 H 2 PO 4 和LiFePO 4 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸 5 六氢吡啶 DMA Pd(OAc) 2 38.6
钠等。焦磷酸根离子、三磷酸根离子如下图所示:
6 六氢吡啶 NMP Pd(OAc) 24.5
2
上述实验探究了________和________对反应产率的影响。此外,还可以进一步探究________等对反应产率的影
响。
(5)X为D的同分异构体,写出满足如下条件的X的结构简式________________。
这类磷酸根离子的化学式可用通式表示为____________(用n代表P原子数)。
①含有苯环;②有三种不同化学环境的氢,个数比为6∶2∶1;③1 mol的X与足量金属Na反应可生成2 g
[化学——选修 5:有机化学基础]
H 。
2
12.氧化白藜芦醇W具有抗病毒等作用。下面是利用Heck反应合成W的一种方法:
(6)利用Heck反应,由苯和溴乙烷为原料制备 ,写出合成路线________________。(无机
试剂任选)
回答下列问题: