文档内容
2019 年天津市高考化学试卷
一、选择题(共6小题,每小题6分,满分36分)
1.(6分)化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是
( )
A.利用废弃的秸秆生产生物质燃料乙醇
B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物
D.利用反渗透膜从海水中分离出淡水
2.(6分)下列离子方程式能用来解释相应实验现象的是( )
实验现象 离子方程式
A 向氢氧化镁悬浊液中滴加氯化铵 Mg(OH) +2NH +═Mg2++2NH •H O
2 4 3 2
溶液,沉淀溶解
B 向沸水中滴加饱和氯化铁溶液得 Fe3++3H O═Fe(OH) ↓+3H+
2 3
到红褐色液体
C 二氧化硫使酸性高锰酸钾溶液褪 3SO +2MnO ﹣+4H+═3SO 2﹣+2Mn2++2H O
2 4 4 2
色
D 氧化亚铁溶于稀硝酸 FeO+2H+═Fe2++H O
2
A.A B.B C.C D.D
3.(6分)下列有关金属及其化合物的应用不合理的是( )
A.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
B.铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
C.盐碱地(含较多Na CO 等)不利于作物生长,可施加熟石灰进行改良
2 3
D.无水CoCl 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
2
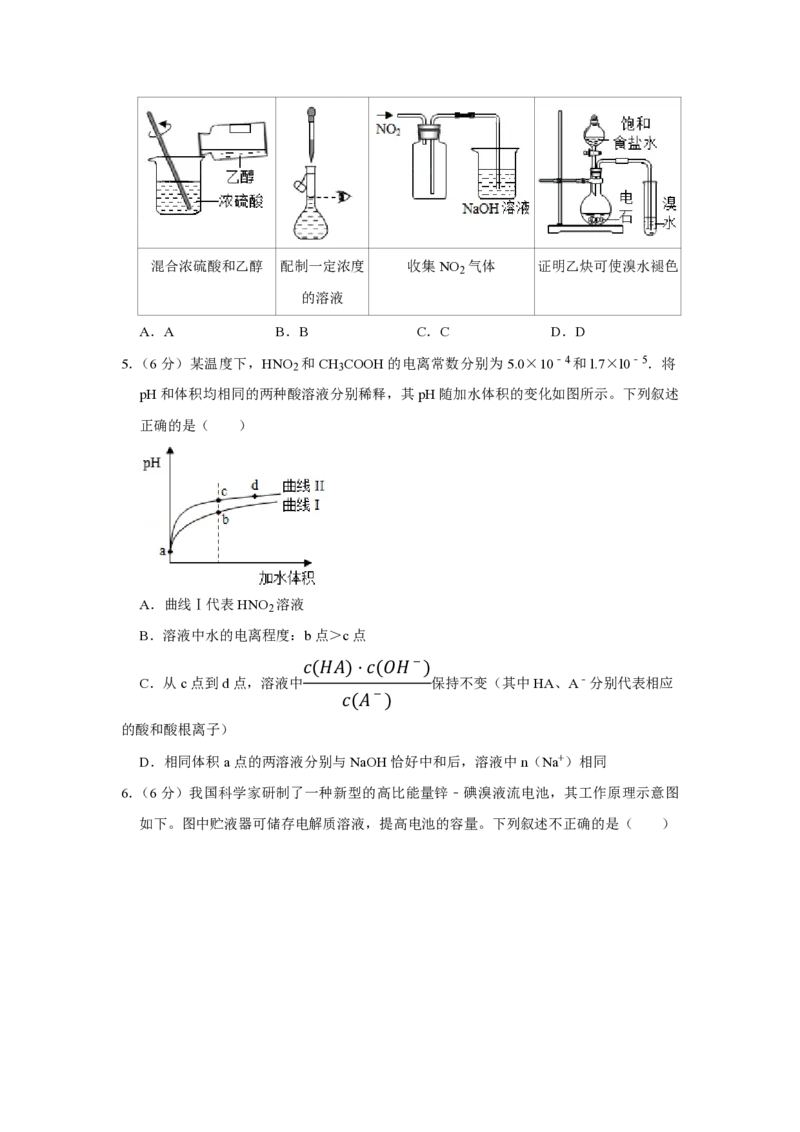
4.(6分)下列实验操作或装置能达到目的是( )
A B C D混合浓硫酸和乙醇 配制一定浓度 收集NO 气体 证明乙炔可使溴水褪色
2
的溶液
A.A B.B C.C D.D
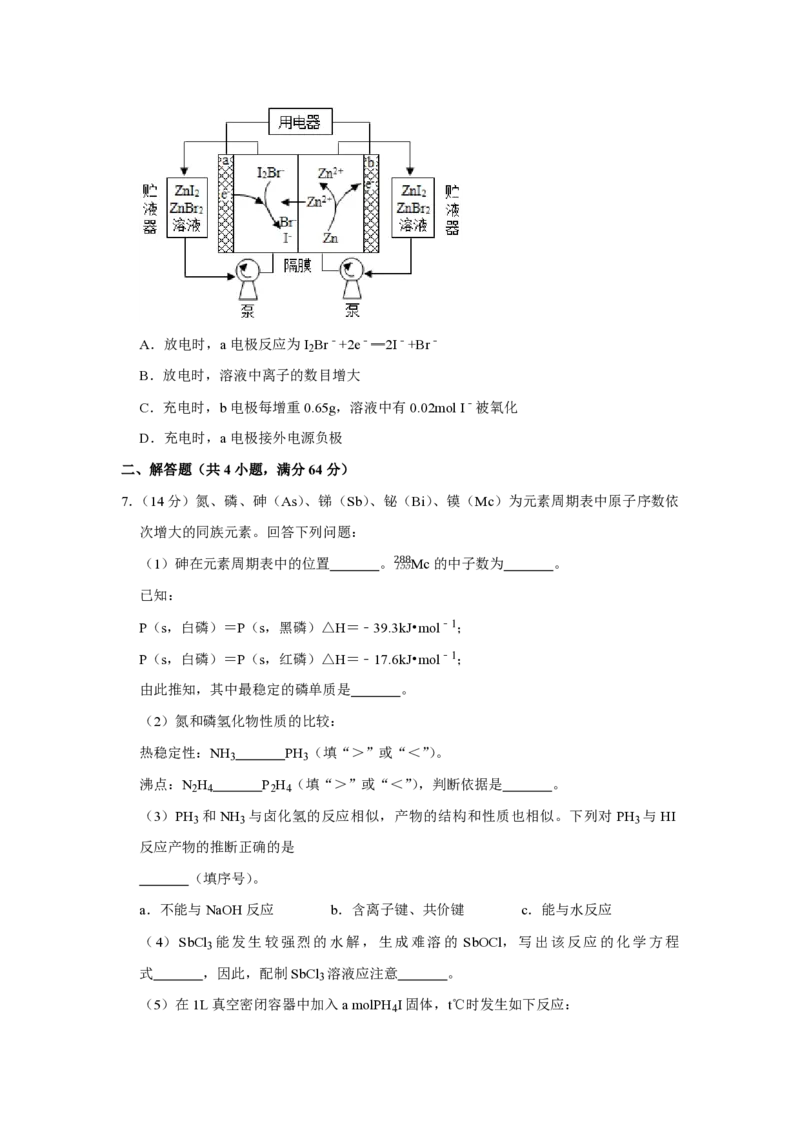
5.(6分)某温度下,HNO 和CH COOH的电离常数分别为5.0×10﹣4和l.7×l0﹣5.将
2 3
pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述
正确的是( )
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
‒
𝑐(𝐻𝐴) ⋅ 𝑐(𝑂𝐻 )
C.从c点到d点,溶液中 保持不变(其中HA、A﹣分别代表相应
‒
𝑐(𝐴 )
的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
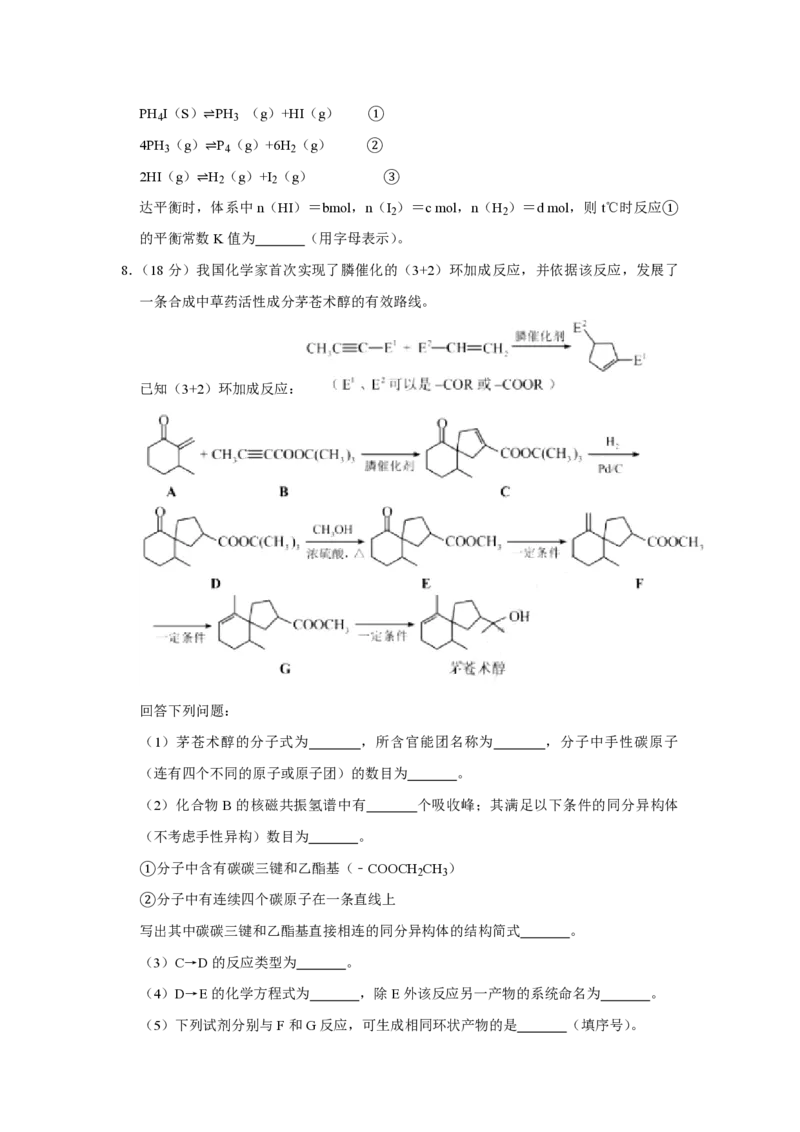
6.(6分)我国科学家研制了一种新型的高比能量锌﹣碘溴液流电池,其工作原理示意图
如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是( )A.放电时,a电极反应为I Br﹣+2e﹣═2I﹣+Br﹣
2
B.放电时,溶液中离子的数目增大
C.充电时,b电极每增重0.65g,溶液中有0.02mol I﹣被氧化
D.充电时,a电极接外电源负极
二、解答题(共4小题,满分64分)
7.(14分)氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依
次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置 。2 15 8 5 8Mc的中子数为 。
已知:
P(s,白磷)=P(s,黑磷)△H=﹣39.3kJ•mol﹣1;
P(s,白磷)=P(s,红磷)△H=﹣17.6kJ•mol﹣1;
由此推知,其中最稳定的磷单质是 。
(2)氮和磷氢化物性质的比较:
热稳定性:NH PH (填“>”或“<”)。
3 3
沸点:N H P H (填“>”或“<”),判断依据是 。
2 4 2 4
(3)PH 和NH 与卤化氢的反应相似,产物的结构和性质也相似。下列对PH 与HI
3 3 3
反应产物的推断正确的是
(填序号)。
a.不能与NaOH反应 b.含离子键、共价键 c.能与水反应
(4)SbCl 能发生较强烈的水解,生成难溶的 SbOCl,写出该反应的化学方程
3
式 ,因此,配制SbCl 溶液应注意 。
3
(5)在1L真空密闭容器中加入a molPH I固体,t℃时发生如下反应:
4PH I(S)⇌PH (g)+HI(g) ①
4 3
4PH (g)⇌P (g)+6H (g) ②
3 4 2
2HI(g)⇌H (g)+I (g) ③
2 2
达平衡时,体系中n(HI)=bmol,n(I )=c mol,n(H )=d mol,则t℃时反应①
2 2
的平衡常数K值为 (用字母表示)。
8.(18分)我国化学家首次实现了膦催化的(3+2)环加成反应,并依据该反应,发展了
一条合成中草药活性成分茅苍术醇的有效路线。
已知(3+2)环加成反应:
回答下列问题:
(1)茅苍术醇的分子式为 ,所含官能团名称为 ,分子中手性碳原子
(连有四个不同的原子或原子团)的数目为 。
(2)化合物B的核磁共振氢谱中有 个吸收峰;其满足以下条件的同分异构体
(不考虑手性异构)数目为 。
①分子中含有碳碳三键和乙酯基(﹣COOCH CH )
2 3
②分子中有连续四个碳原子在一条直线上
写出其中碳碳三键和乙酯基直接相连的同分异构体的结构简式 。
(3)C→D的反应类型为 。
(4)D→E的化学方程式为 ,除E外该反应另一产物的系统命名为 。
(5)下列试剂分别与F和G反应,可生成相同环状产物的是 (填序号)。a.Br b.HBr c.NaOH溶液
2
(6)参考以上合成路线及条件,选择两种链状不饱和酯,通过两步反应合成化合物
M,在方框中写出路线流程图(其他试剂任选)。
9.(18分)环己烯是重要的化工原料。其实验室制备流程如图:
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为 ,现象为 。
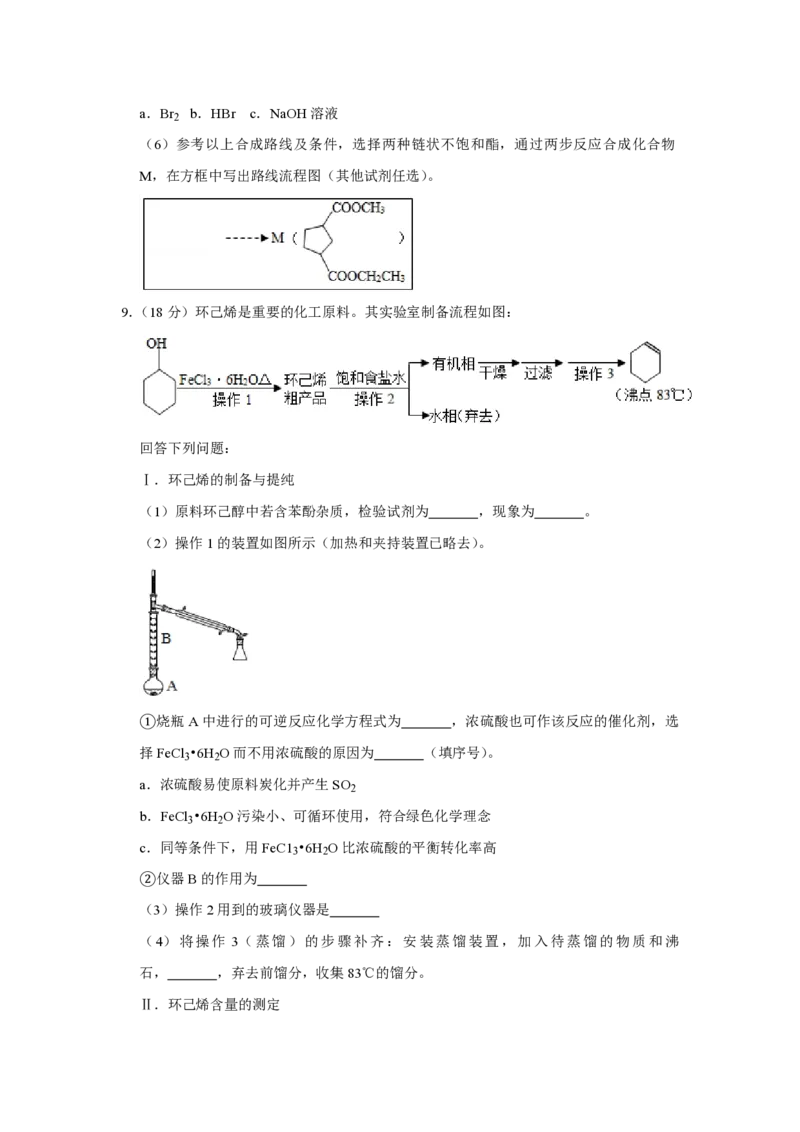
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为 ,浓硫酸也可作该反应的催化剂,选
择FeCl •6H O而不用浓硫酸的原因为 (填序号)。
3 2
a.浓硫酸易使原料炭化并产生SO
2
b.FeCl •6H O污染小、可循环使用,符合绿色化学理念
3 2
c.同等条件下,用FeC1 •6H O比浓硫酸的平衡转化率高
3 2
②仪器B的作用为
(3)操作2用到的玻璃仪器是
(4)将操作 3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸
石, ,弃去前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定在一定条件下,向ag环己烯样品中加入定量制得的bmolBr ,与环己烯充分反应后,剩
2
余的 Br 与足量 KI作用生成 I ,用 cmol•L﹣1的 Na S O 标准溶液滴定,终点时消耗
2 2 2 2 3
Na S O 标准溶液vmL(以上数据均已扣除干扰因素)。
2 2 3
测定过程中,发生的反应如下:
①
②Br +2KI═I +2KBr
2 2
③I +2Na S O ═2NaI+Na S O
2 2 2 3 2 4 6
(5)滴定所用指示剂为 。样品中环己烯的质量分数为 (用字母表示)。
(6)下列情况会导致测定结果偏低的是 (填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.Na S O 标准溶液部分被氧化
2 2 3
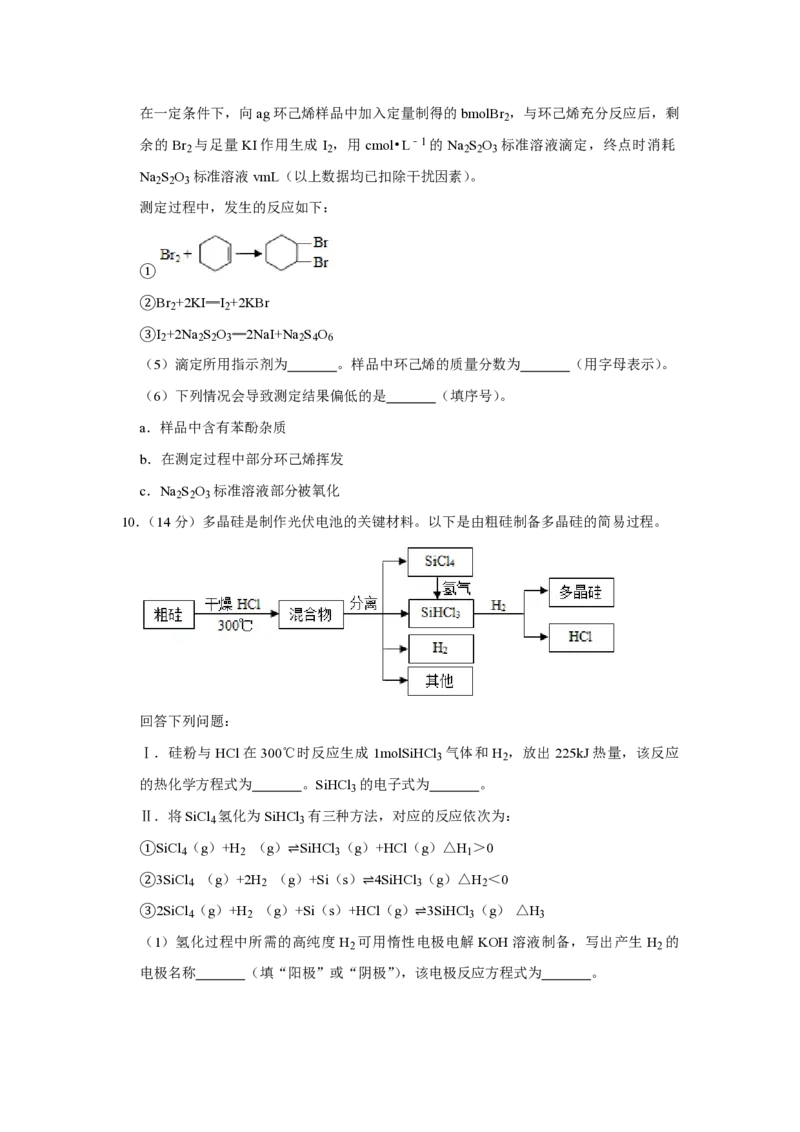
10.(14分)多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
回答下列问题:
Ⅰ.硅粉与HCl在300℃时反应生成1molSiHCl 气体和H ,放出225kJ热量,该反应
3 2
的热化学方程式为 。SiHCl 的电子式为 。
3
Ⅱ.将SiCl 氢化为SiHCl 有三种方法,对应的反应依次为:
4 3
①SiCl (g)+H (g)⇌SiHCl (g)+HCl(g)△H >0
4 2 3 1
②3SiCl (g)+2H (g)+Si(s)⇌4SiHCl (g)△H <0
4 2 3 2
③2SiCl (g)+H (g)+Si(s)+HCl(g)⇌3SiHCl (g) △H
4 2 3 3
(1)氢化过程中所需的高纯度H 可用惰性电极电解KOH溶液制备,写出产生H 的
2 2
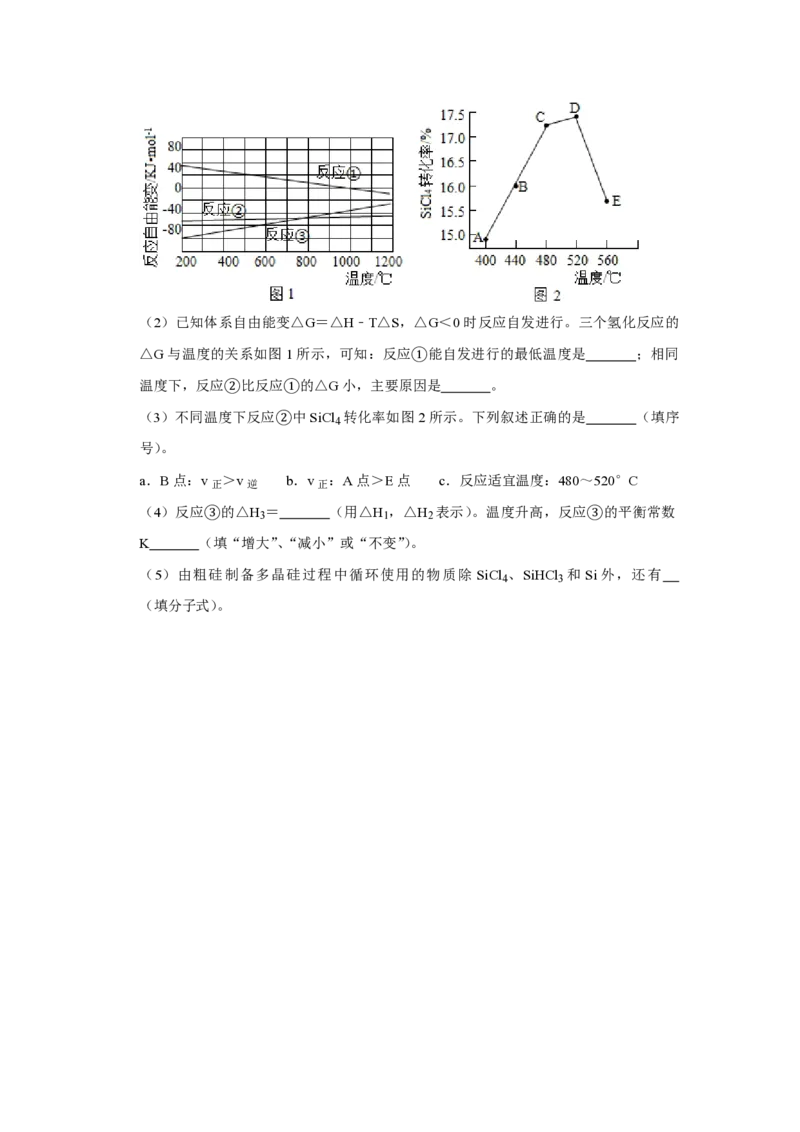
电极名称 (填“阳极”或“阴极”),该电极反应方程式为 。(2)已知体系自由能变△G=△H﹣T△S,△G<0时反应自发进行。三个氢化反应的
△G与温度的关系如图1所示,可知:反应①能自发进行的最低温度是 ;相同
温度下,反应②比反应①的△G小,主要原因是 。
(3)不同温度下反应②中SiCl 转化率如图2所示。下列叙述正确的是 (填序
4
号)。
a.B点:v
正
>v
逆
b.v
正
:A点>E点 c.反应适宜温度:480~520°C
(4)反应③的△H = (用△H ,△H 表示)。温度升高,反应③的平衡常数
3 1 2
K (填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除 SiCl 、SiHCl 和 Si外,还有
4 3
(填分子式)。