文档内容
2019 年江苏省高考化学试卷
一、单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意
1.(2分)糖类是人体所需的重要营养物质。淀粉分子中不含的元素是( )
A.氢 B.碳 C.氮 D.氧
2.(2分)反应NH
4
Cl+NaNO
2
═NaCl+N
2
↑+2H
2
O放热且产生气体,可用于冬天石油开采。下列表示反应中相
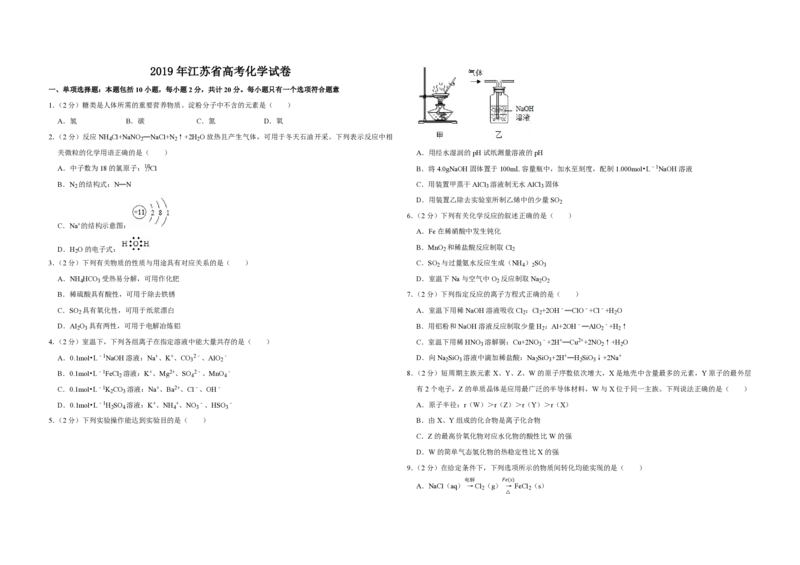
关微粒的化学用语正确的是( ) A.用经水湿润的pH试纸测量溶液的pH
A.中子数为18的氯原子:1
17
8Cl B.将4.0gNaOH固体置于100mL容量瓶中,加水至刻度,配制1.000mol•L﹣1NaOH溶液
B.N 的结构式:N═N C.用装置甲蒸干AlCl 溶液制无水AlCl 固体
2 3 3
D.用装置乙除去实验室所制乙烯中的少量SO
2
6.(2分)下列有关化学反应的叙述正确的是( )
C.Na+的结构示意图:
A.Fe在稀硝酸中发生钝化
D.H 2 O的电子式: B.MnO 2 和稀盐酸反应制取Cl 2
3.(2分)下列有关物质的性质与用途具有对应关系的是( ) C.SO 与过量氨水反应生成(NH ) SO
2 4 2 3
A.NH HCO 受热易分解,可用作化肥 D.室温下Na与空气中O 反应制取Na O
4 3 2 2 2
B.稀硫酸具有酸性,可用于除去铁锈 7.(2分)下列指定反应的离子方程式正确的是( )
C.SO 具有氧化性,可用于纸浆漂白 A.室温下用稀NaOH溶液吸收Cl :Cl +2OH﹣═ClO﹣+Cl﹣+H O
2 2 2 2
D.Al O 具有两性,可用于电解冶炼铝 B.用铝粉和NaOH溶液反应制取少量H :Al+2OH﹣═AlO ﹣+H ↑
2 3 2 2 2
4.(2分)室温下,下列各组离子在指定溶液中能大量共存的是( ) C.室温下用稀HNO 溶解铜:Cu+2NO ﹣+2H+═Cu2++2NO ↑+H O
3 3 2 2
A.0.1mol•L﹣1NaOH溶液:Na+、K+、CO 2﹣、AlO ﹣ D.向Na SiO 溶液中滴加稀盐酸:Na SiO +2H+═H SiO ↓+2Na+
3 2 2 3 2 3 2 3
B.0.1mol•L﹣1FeCl 溶液:K+、Mg2+、SO 2﹣、MnO ﹣ 8.(2分)短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,Y原子的最外层
2 4 4
C.0.1mol•L﹣1K CO 溶液:Na+、Ba2+、Cl﹣、OH﹣ 有2个电子,Z的单质晶体是应用最广泛的半导体材料,W与X位于同一主族。下列说法正确的是( )
2 3
D.0.1mol•L﹣1H SO 溶液:K+、NH +、NO ﹣、HSO ﹣ A.原子半径:r(W)>r(Z)>r(Y)>r(X)
2 4 4 3 3
5.(2分)下列实验操作能达到实验目的是( ) B.由X、Y组成的化合物是离子化合物
C.Z的最高价氧化物对应水化物的酸性比W的强
D.W的简单气态氢化物的热稳定性比X的强
9.(2分)在给定条件下,下列选项所示的物质间转化均能实现的是( )
电解 𝐹𝑒(𝑠)
A.NaCl(aq)→Cl (g) →FeCl (s)
2 2
△石灰乳 煅烧
B.MgCl (aq) → Mg(OH) (s)→MgO(s)
2 2
𝑂 (𝑔) 𝐻 𝑂(𝑙)
2 2
C.S(s) →SO (g) → H SO (aq)
3 2 4
点燃
𝐻 (𝑔) 𝐶𝑂 (𝑔)
2 2
D.N (g) → NH (g) → Na CO (s)
2 3 2 3
高温高压、催化剂 𝑁𝑎𝐶𝑙(𝑎𝑞)
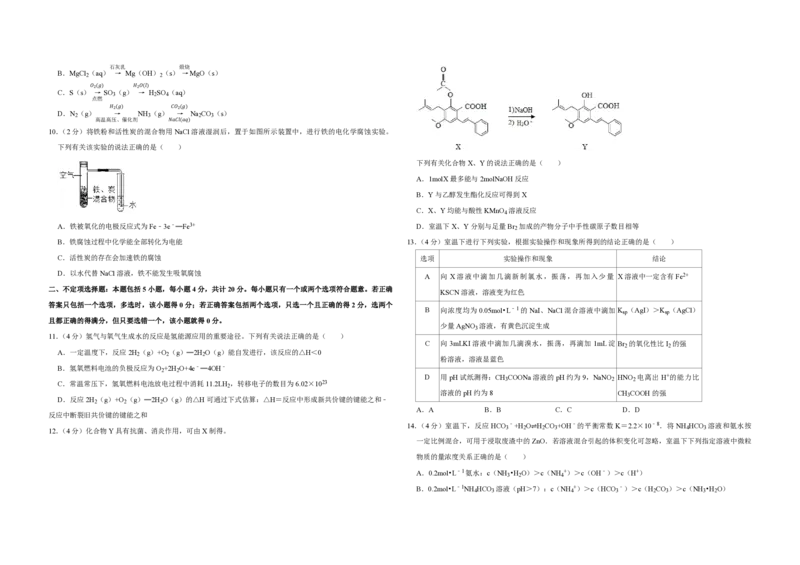
10.(2分)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。
下列有关该实验的说法正确的是( )
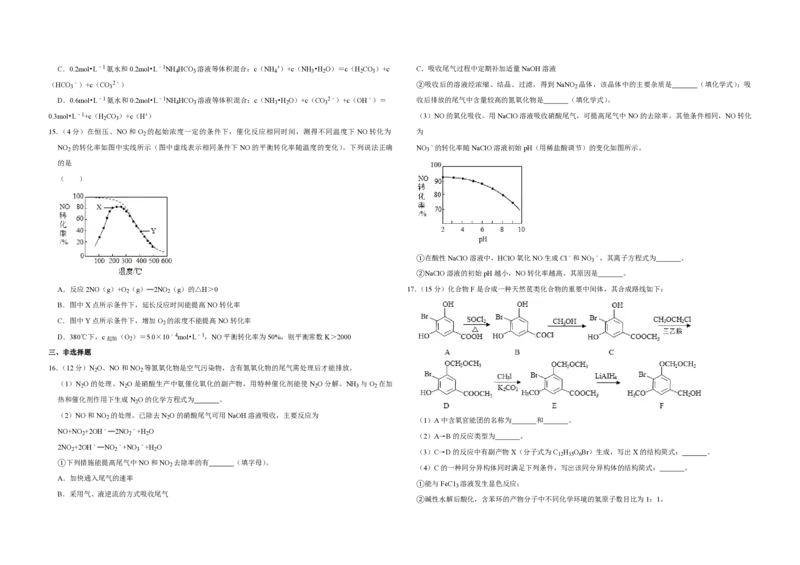
下列有关化合物X、Y的说法正确的是( )
A.1molX最多能与2molNaOH反应
B.Y与乙醇发生酯化反应可得到X
C.X、Y均能与酸性KMnO
4
溶液反应
A.铁被氧化的电极反应式为Fe﹣3e﹣═Fe3+ D.室温下X、Y分别与足量Br 加成的产物分子中手性碳原子数目相等
2
B.铁腐蚀过程中化学能全部转化为电能 13.(4分)室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
C.活性炭的存在会加速铁的腐蚀 选项 实验操作和现象 结论
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
A 向 X溶液中滴加几滴新制氯水,振荡,再加入少量 X溶液中一定含有Fe2+
二、不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确
KSCN溶液,溶液变为红色
答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个
B 向浓度均为 0.05mol•L﹣1的 NaI、NaCl混合溶液中滴加 K (AgI)>K (AgCl)
sp sp
且都正确的得满分,但只要选错一个,该小题就得0分。
少量AgNO 溶液,有黄色沉淀生成
3
11.(4分)氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是( )
C 向 3mLKI溶液中滴加几滴溴水,振荡,再滴加 1mL淀 Br 的氧化性比I 的强
2 2
A.一定温度下,反应2H (g)+O (g)═2H O(g)能自发进行,该反应的△H<0
2 2 2
粉溶液,溶液显蓝色
B.氢氧燃料电池的负极反应为O +2H O+4e﹣═4OH﹣
2 2
D 用pH试纸测得:CH COONa溶液的pH约为9,NaNO HNO 电离出 H+的能力比
3 2 2
C.常温常压下,氢氧燃料电池放电过程中消耗11.2LH ,转移电子的数目为6.02×1023
2
溶液的pH约为8 CH COOH的强
3
D.反应2H (g)+O (g)═2H O(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和﹣
2 2 2
A.A B.B C.C D.D
反应中断裂旧共价键的键能之和
14.(4分)室温下,反应HCO ﹣+H O⇌H CO +OH﹣的平衡常数K=2.2×10﹣8.将NH HCO 溶液和氨水按
3 2 2 3 4 3
12.(4分)化合物Y具有抗菌、消炎作用,可由X制得。
一定比例混合,可用于浸取废渣中的ZnO.若溶液混合引起的体积变化可忽略,室温下下列指定溶液中微粒
物质的量浓度关系正确的是( )
A.0.2mol•L﹣1氨水:c(NH •H O)>c(NH +)>c(OH﹣)>c(H+)
3 2 4
B.0.2mol•L﹣1NH HCO 溶液(pH>7):c(NH +)>c(HCO ﹣)>c(H CO )>c(NH •H O)
4 3 4 3 2 3 3 2C.0.2mol•L﹣1氨水和0.2mol•L﹣1NH HCO 溶液等体积混合:c(NH +)+c(NH •H O)=c(H CO )+c C.吸收尾气过程中定期补加适量NaOH溶液
4 3 4 3 2 2 3
(HCO ﹣)+c(CO 2﹣) ②吸收后的溶液经浓缩、结晶、过滤,得到NaNO 晶体,该晶体中的主要杂质是 (填化学式);吸
3 3 2
D.0.6mol•L﹣1氨水和0.2mol•L﹣1NH HCO 溶液等体积混合:c(NH •H O)+c(CO 2﹣)+c(OH﹣)= 收后排放的尾气中含量较高的氮氧化物是 (填化学式)。
4 3 3 2 3
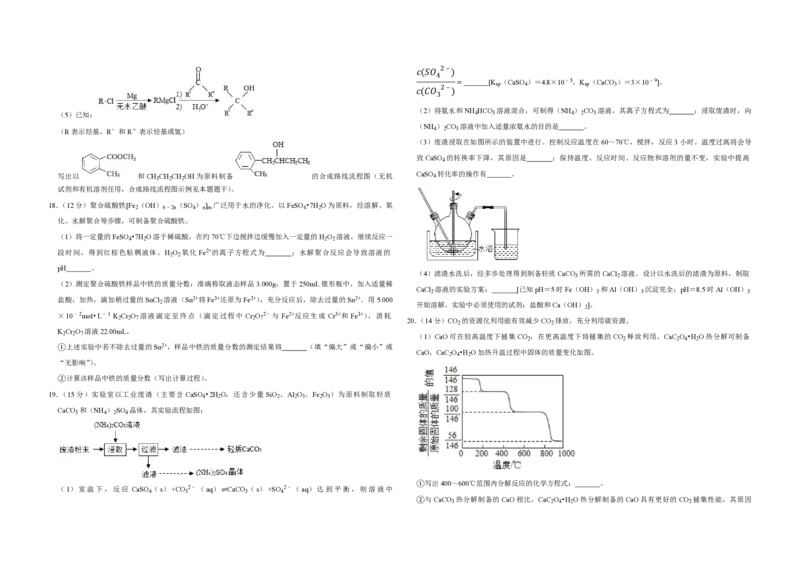
0.3mol•L﹣1+c(H CO )+c(H+) (3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化
2 3
15.(4分)在恒压、NO和 O 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下 NO转化为 为
2
NO 的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确 NO ﹣的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
2 3
的是
( )
①在酸性NaClO溶液中,HClO氧化NO生成Cl﹣和NO ﹣,其离子方程式为 。
3
②NaClO溶液的初始pH越小,NO转化率越高。其原因是 。
A.反应2NO(g)+O (g)═2NO (g)的△H>0 17.(15分)化合物F是合成一种天然茋类化合物的重要中间体,其合成路线如下:
2 2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O 的浓度不能提高NO转化率
2
D.380℃下,c
起始
(O
2
)=5.0×10﹣4mol•L﹣1,NO平衡转化率为50%,则平衡常数K>2000
三、非选择题
16.(12分)N O、NO和NO 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
2 2
(1)N O的处理。N O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N O分解。NH 与O 在加
2 2 2 3 2
热和催化剂作用下生成N O的化学方程式为 。
2
(2)NO和NO 的处理。已除去N O的硝酸尾气可用NaOH溶液吸收,主要反应为
2 2 (1)A中含氧官能团的名称为 和 。
NO+NO +2OH﹣═2NO ﹣+H O
2 2 2 (2)A→B的反应类型为 。
2NO +2OH﹣═NO ﹣+NO ﹣+H O
2 2 3 2 (3)C→D的反应中有副产物X(分子式为C H O Br)生成,写出X的结构简式: 。
12 15 6
①下列措施能提高尾气中NO和NO 去除率的有 (填字母)。
2 (4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
A.加快通入尾气的速率
①能与FeC1 溶液发生显色反应;
3
B.采用气、液逆流的方式吸收尾气
②碱性水解后酸化,含苯环的产物分子中不同化学环境的氢原子数目比为1:1。2‒
𝑐(𝑆𝑂 )
4
= [K (CaSO )=4.8×10﹣5,K (CaCO )=3×10﹣9]。
sp 4 sp 3
2‒
𝑐(𝐶𝑂 )
3
(2)将氨水和NH HCO 溶液混合,可制得(NH ) CO 溶液,其离子方程式为 ;浸取废渣时,向
(5)已知: 4 3 4 2 3
(NH ) CO 溶液中加入适量浓氨水的目的是 。
(R表示烃基,R′和R″表示烃基或氢) 4 2 3
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70℃,搅拌,反应3小时。温度过高将会导
致CaSO 的转换率下降,其原因是 ;保持温度、反应时间、反应物和溶剂的量不变,实验中提高
4
写出以 和 CH CH CH OH为原料制备 的合成路线流程图(无机 CaSO 4 转化率的操作有 。
3 2 2
试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
18.(12分)聚合硫酸铁[Fe (OH) (SO ) ] 广泛用于水的净化。以FeSO •7H O为原料,经溶解、氧
2 6﹣2n 4 n m 4 2
化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO •7H O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H O 溶液,继续反应一
4 2 2 2
段时间,得到红棕色粘稠液体。H O 氧化 Fe2+的离子方程式为 ;水解聚合反应会导致溶液的
2 2
pH 。
(4)滤渣水洗后,经多步处理得到制备轻质CaCO 所需的CaCl 溶液。设计以水洗后的滤渣为原料,制取
3 2
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀
CaCl 溶液的实验方案: [已知pH=5时Fe(OH) 和Al(OH) 沉淀完全;pH=8.5时Al(OH)
2 3 3 3
盐酸,加热,滴加稍过量的SnCl 溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+.用5.000
2
开始溶解。实验中必须使用的试剂:盐酸和Ca(OH) ]。
2
×10﹣2mol•L﹣1 K Cr O 溶液滴定至终点(滴定过程中 Cr O 2﹣与 Fe2+反应生成 Cr3+和 Fe3+),消耗
2 2 7 2 7 20.(14分)CO 的资源化利用能有效减少CO 排放,充分利用碳资源。
2 2
K Cr O 溶液22.00mL。
2 2 7
(1)CaO可在较高温度下捕集 CO ,在更高温度下将捕集的 CO 释放利用。CaC O •H O热分解可制备
2 2 2 4 2
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将 (填“偏大”或“偏小”或
CaO,CaC O •H O加热升温过程中固体的质量变化如图。
2 4 2
“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)。
19.(15分)实验室以工业废渣(主要含 CaSO •2H O,还含少量 SiO 、Al O 、Fe O )为原料制取轻质
4 2 2 2 3 2 3
CaCO 和(NH ) SO 晶体,其实验流程如图:
3 4 2 4
①写出400~600℃范围内分解反应的化学方程式: 。
(1)室温下,反应 CaSO (s)+CO 2﹣(aq)⇌CaCO (s)+SO 2﹣(aq)达到平衡,则溶液中
4 3 3 4
②与 CaCO 热分解制备的 CaO相比,CaC O •H O热分解制备的 CaO具有更好的 CO 捕集性能,其原因
3 2 4 2 2是 。 ①温度高于300℃,CO 平衡转化率随温度升高而上升的原因是 。
2
(2)电解法转化CO 可实现CO 资源化利用。电解CO 制HCOOH的原理示意图如图。 ②220℃时,在催化剂作用下CO 与H 反应一段时间后,测得CH OCH 的选择性为48%(图中A点)。不
2 2 2 2 2 3 3
改变反应时间和温度,一定能提高CH OCH 选择性的措施有 。
3 3
【选做题】本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评
分。A.[物质结构与性质]
21.(12分)Cu O广泛应用于太阳能电池领域。以CuSO 、NaOH和抗坏血酸为原料,可制备Cu O。
2 4 2
(1)Cu2+基态核外电子排布式为 。
(2)SO 2﹣的空间构型为 (用文字描述);Cu2+与OH﹣反应能生成[Cu(OH) ]2﹣,[Cu(OH) ]2﹣
4 4 4
中的配位原子为 (填元素符号)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为 ;推测抗坏血酸在水中的溶
①写出阴极CO 还原为HCOO﹣的电极反应式: 。 解性: (填“难溶于水”或“易溶于水”)。
2
②电解一段时间后,阳极区的KHCO 溶液浓度降低,其原因是 。
3
(3)CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下列反应:
2 2
反应Ⅰ:CO (g)+H (g)=CO(g)+H O(g)△H=41.2kJ•mol﹣1
2 2 2
反应Ⅱ:2CO (g)+6H (g)=CH OCH (g)+3H O(g)△H=﹣122.5kJ•mol﹣1
2 2 3 3 2
在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CH OCH 的选择性随温度的变化如
2 2 2 3 3
图。其中:
(4)一个Cu O晶胞(如图2)中,Cu原子的数目为 。
2
[实验化学]
22.丙炔酸甲酯(CH≡C﹣COOCH )是一种重要的有机化工原料,沸点为103﹣105℃.实验室制备少量丙炔
3
浓𝐻 𝑆𝑂
2 4
酸甲酯的反应为CH≡C﹣COOH+CH OH → CH≡C﹣COOCH +H O
3 3 2
△
实验步骤如下:
步骤1:在反应瓶中,加入14g丙炔酸、50mL甲醇和2mL浓硫酸,搅拌,加热回流一段时间。
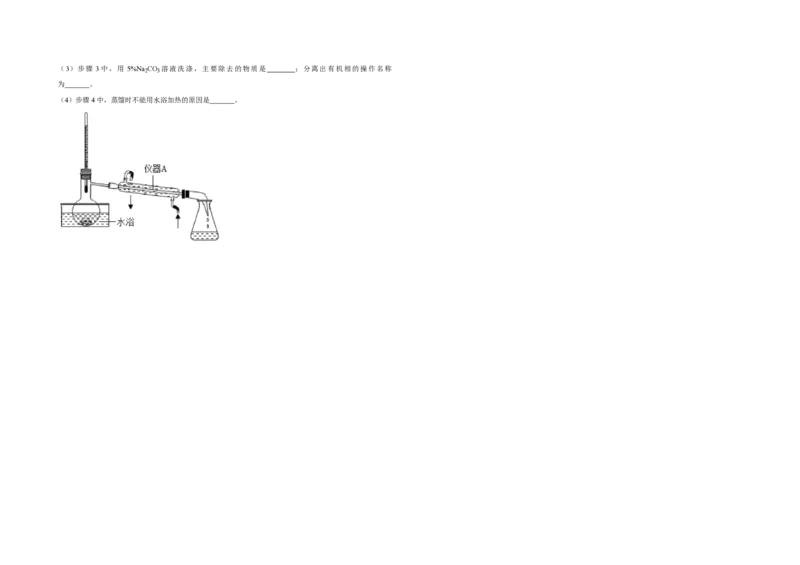
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na CO 溶液、水洗涤。分离出有机相。
2 3
步骤4:有机相经无水Na
2
SO
4
干燥、过滤、蒸馏,得丙炔酸甲酯。
2 × 𝐶𝐻 𝑂𝐶𝐻 的物质的量
3 3 (1)步骤1中,加入过量甲醇的目的是 。
CH OCH 的选择性 = ×100%
3 3
反应的𝐶𝑂 的物质的量
2
(2)步骤2中,如图所示的装置中仪器A的名称是 ;蒸馏烧瓶中加入碎瓷片的目的是 。(3)步骤 3中,用 5%Na CO 溶液洗涤,主要除去的物质是 ;分离出有机相的操作名称
2 3
为 。
(4)步骤4中,蒸馏时不能用水浴加热的原因是 。