文档内容
2019 年 1 月浙江省学业水平测试化学试卷
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Fe 6 Cu 64 Ba 137
一、选择题(本大题共25小题,每小题2分,共50分。每小题列出的四个备选项中只有一
个是符合题目要求的,不选、多选、错选均不得分)
1.水的分子式是
A.H B O C H O D CO
2 2 2 2
2.根据物质的组成与性质进行分类,MgO属于
A.氧化物 B.酸 C碱 D.盐
3.仪器名称为“胶头滴管”的是
4.冰毒有剧毒,人体摄入后将严重损害心脏、大脑组织甚至导致死亡,严禁吸食。它的分
子式为C H N,其中的氮元素在周期表中处于
10 11
A.第ⅡA族 B.第ⅢA族 C.第ⅣA族 C.第VA族
5.萃取碘水中的碘单质,可作萃取剂的是
A.水 B四氯化碳 C.酒精 D.食醋
6.反应2Na+2H O=2NaOH+H ↑中,氧化剂是
2 2
A. Na B. H O C. NaOH D.H
2 2
7.下列属于弱电解质的
A.NH ·H O B. NaOH C. NaCl D. CH CH OH
3 2 3 2
8.下列表示不正确的是
A.甲烷分子的比例模型
B.乙烷的结构简式为CH CH
3 3
C.磷原子的结构示意图为
D.MgCl2的电子式为:9.下列说法不正确的是
A16O和18O互为同位素
B.金刚石和足球烯互为同素异形体
C.C H 和C H 互为同系物
2 4 3 6
D.C H OH和 CH OCH 互为同分异构体
2 5 3 3
10.下列说法不正确的是
A.石灰石、纯碱、石英可作为制备水泥的主要原料
B.燃煤烟气的脱硫过程可以得到副产品石膏和硫酸铵
C.硫酸钡可作高档油漆、油墨、塑料、橡胶的原料及填充剂
D.在催化剂作用下,用玉米、高梁为原料经水解和细菌发酵可制得乙醇
11.四种短周期主族元素X、Y、Z和M在周期表中的位置如图所示。下列说法正确的是
A.原子半径(r):r(X)>r(Z)
B.元素的非金属性:Y>M
C.Y元素的最高化合价为+7价
D.Z的最高价氧化物的水化物为强酸
12.下列方程式不正确的是
A.碳与热的浓硫酸反应的化学方程式:C+2H SO (浓) CO↑+2SO ↑+2H O
2 4 2 2
B.乙炔燃烧的化学方程式:2C H +5O 点燃4CO +2H O
2 2 2 2 2
C.氯化氢在水中的电离方程式:HCl=H++Cl-
D.氯化铵水解的离子方程式:NH ++H O=NH ·H O+H+
4 2 3 2
13.下列实验操作对应的现象不符合事实的是A.用铂丝蘸取 NaCl溶 B.将少量银氨溶液加 C.饱和食盐水通电一 D.将胆矾晶体悬挂盛
液置于酒精灯火焰上 入盛有淀粉和硫酸的 段时间后,湿润的KI- 有浓 H SO 的密闭试
2 4
灼烧,火焰成黄色 试管中加热,产生光 淀粉试纸遇 b处气体 管中蓝色晶体逐渐变
亮的银镜 变蓝色 为白色
14.下列说法不正确的是
A.苯与溴水、酸性高锰酸钾溶液不反应,说明苯分子中碳碳原子间只存在单键
B.煤是由有机物和无机物所组成的复杂的混合物
C.天然气的主要成分是甲烷,甲烷可在高温下分解为炭黑和氢气
D.乙烯为不饱和烃,分子中6个原子处于同一平面
15. 下列说法不正确的
A.油脂是一种营养物质,也是一种重要的工业原料,用它可以制造肥皂和油漆等
B.饱和Na SO 溶液加入蛋白质溶液中,可使蛋白质析出
2 4
C.碱性条件下,葡萄糖与新制氢氧化铜混合、加热,生成砖红色沉淀
D.每个氨基酸分子中均只有一个羧基和一个氨基
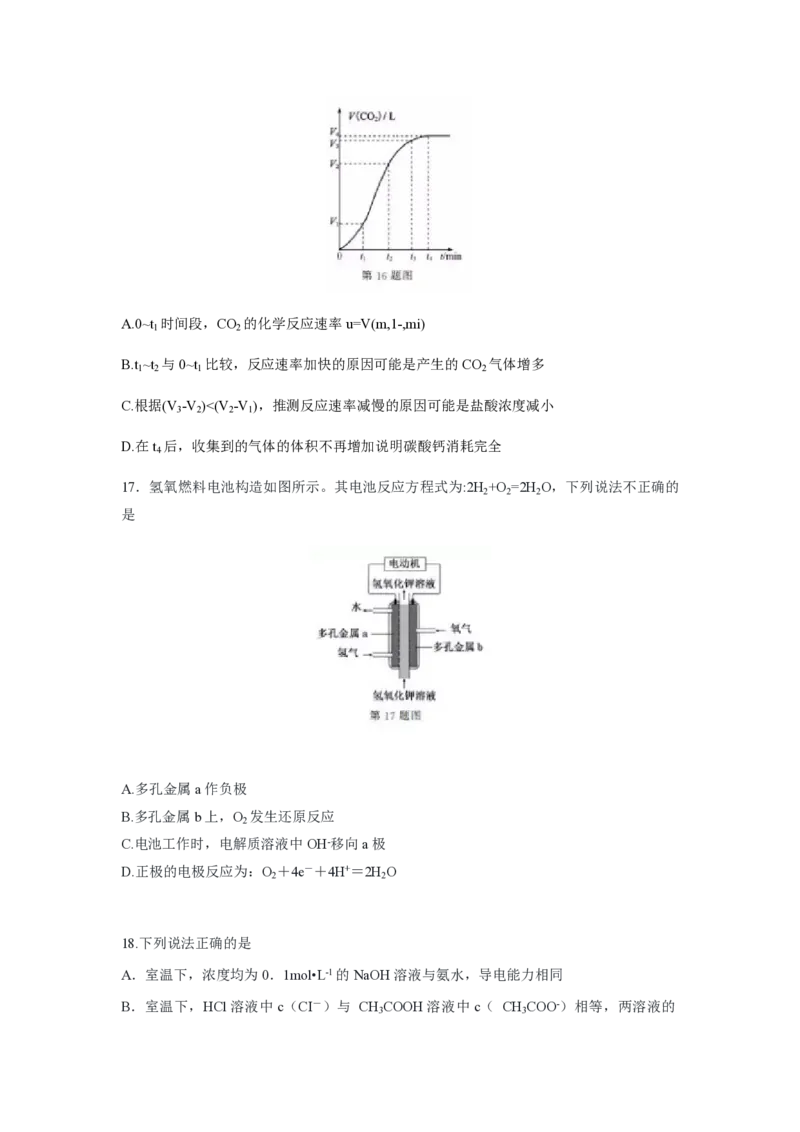
16.为了探究反应速率的影响因素某同学通过碳酸钙与稀盐酸的反以应,绘制出收集到的
CO 体积与反应时间的关系图(0~t 、t ~t ~t 的时间间隔相等)。下列说法正确的是
2 1 1 2 3A.0~t 时间段,CO 的化学反应速率u=V(m,1-,mi)
1 2
B.t ~t 与0~t 比较,反应速率加快的原因可能是产生的CO 气体增多
1 2 1 2
C.根据(V -V )<(V -V ),推测反应速率减慢的原因可能是盐酸浓度减小
3 2 2 1
D.在t 后,收集到的气体的体积不再增加说明碳酸钙消耗完全
4
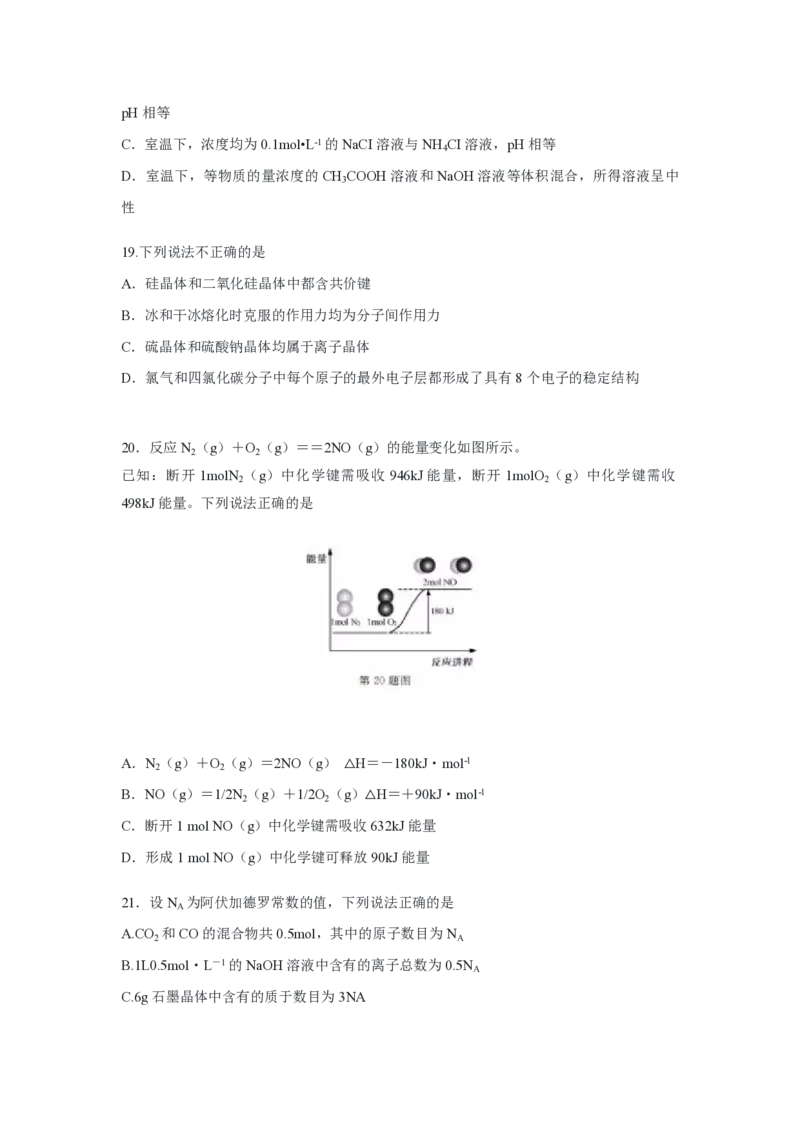
17.氢氧燃料电池构造如图所示。其电池反应方程式为:2H +O =2H O,下列说法不正确的
2 2 2
是
A.多孔金属a作负极
B.多孔金属b上,O 发生还原反应
2
C.电池工作时,电解质溶液中OH-移向a极
D.正极的电极反应为:O +4e-+4H+=2H O
2 2
18.下列说法正确的是
A.室温下,浓度均为0.1mol•L-1的NaOH溶液与氨水,导电能力相同
B.室温下,HCl溶液中c(CI-)与 CH COOH溶液中c( CH COO-)相等,两溶液的
3 3pH相等
C.室温下,浓度均为0.1mol•L-1的NaCI溶液与NH CI溶液,pH相等
4
D.室温下,等物质的量浓度的CH COOH溶液和NaOH溶液等体积混合,所得溶液呈中
3
性
19.下列说法不正确的是
A.硅晶体和二氧化硅晶体中都含共价键
B.冰和干冰熔化时克服的作用力均为分子间作用力
C.硫晶体和硫酸钠晶体均属于离子晶体
D.氯气和四氯化碳分子中每个原子的最外电子层都形成了具有8个电子的稳定结构
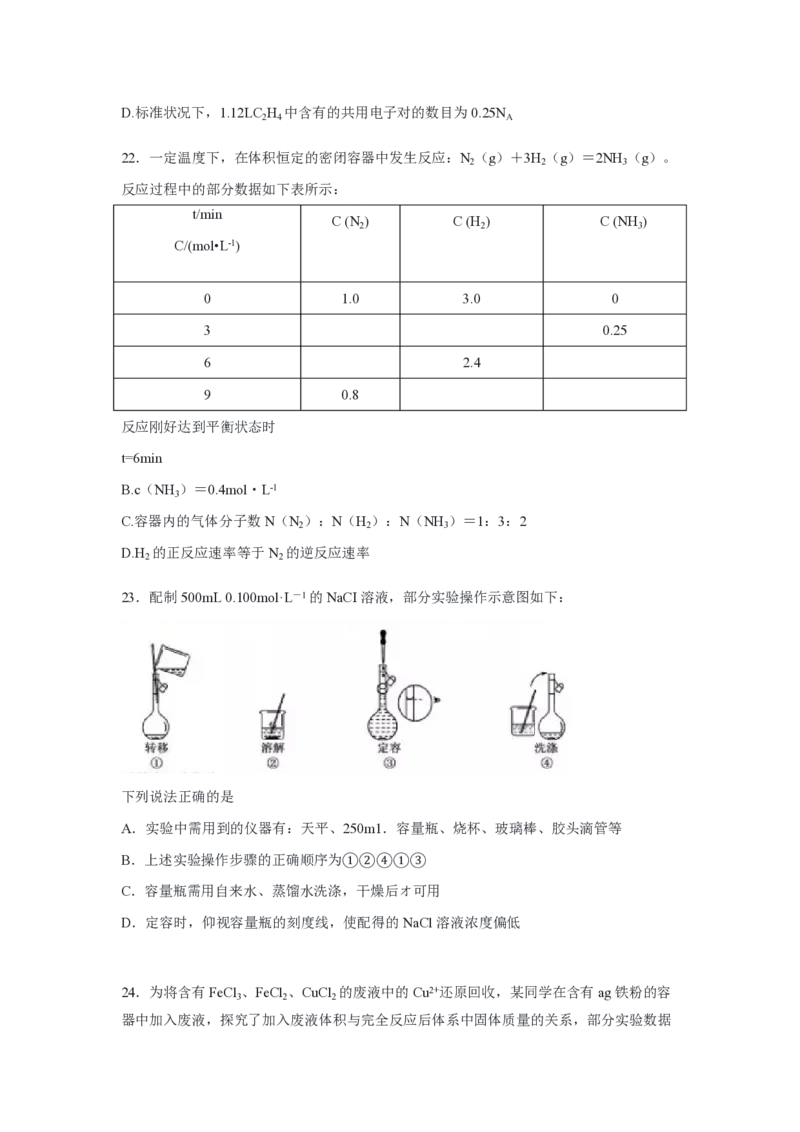
20.反应N (g)+O (g)==2NO(g)的能量变化如图所示。
2 2
已知:断开 1molN (g)中化学键需吸收 946kJ能量,断开 1molO (g)中化学键需收
2 2
498kJ能量。下列说法正确的是
A.N (g)+O (g)=2NO(g) △H=-180kJ・mol-1
2 2
B.NO(g)=1/2N (g)+1/2O (g)△H=+90kJ・mol-1
2 2
C.断开1 mol NO(g)中化学键需吸收632kJ能量
D.形成1 mol NO(g)中化学键可释放90kJ能量
21.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.CO 和CO的混合物共0.5mol,其中的原子数目为N
2 A
B.1L0.5mol・L-1的NaOH溶液中含有的离子总数为0.5N
A
C.6g石墨晶体中含有的质于数目为3NAD.标准状况下,1.12LC H 中含有的共用电子对的数目为0.25N
2 4 A
22.一定温度下,在体积恒定的密闭容器中发生反应:N (g)+3H (g)=2NH (g)。
2 2 3
反应过程中的部分数据如下表所示:
t/min
C (N ) C (H ) C (NH )
2 2 3
C/(mol•L-1)
0 1.0 3.0 0
3 0.25
6 2.4
9 0.8
反应刚好达到平衡状态时
t=6min
B.c(NH )=0.4mol・L-1
3
C.容器内的气体分子数N(N ):N(H ):N(NH )=1:3:2
2 2 3
D.H 的正反应速率等于N 的逆反应速率
2 2
23.配制500mL 0.100mol·L-1的NaCI溶液,部分实验操作示意图如下:
下列说法正确的是
A.实验中需用到的仪器有:天平、250m1.容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为①②④①③
C.容量瓶需用自来水、蒸馏水洗涤,干燥后オ可用
D.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
24.为将含有FeCl 、FeCl 、CuCl 的废液中的Cu2+还原回收,某同学在含有ag铁粉的容
3 2 2
器中加入废液,探究了加入废液体积与完全反应后体系中固体质量的关系,部分实验数据如下表所示。已知:废液中c(Cu2+)=0.7mol・L;废液体积大于0.5L,充分反应后才
能检测出Cu2+,
废液体积/L ≤0.5 1 2 3 ≥4
固体质量/g a 6 4 2 0
a a a
7 7 7
下列说法不正确的是
A.当铁粉与0.25废液反应完全后,固体成分为Fe与Cu
B.当铁粉与1L废液反应完全后,再加入废液时发生的离子反应为Fe+2Fe3++=3Fe2+
C.废液中c(Fe3+)=0.2mol·L-1
D.要将1L废液中的Cu全部还原,则至少需要铁粉44.8g
25为确定试样xNa CO▪yNaHCO 的组成,某同学将质量为ag的试样加水溶解后,所得试
2 3
样溶液进行如下实验
注: NaHCO 溶液pH约为8.3,饱和H CO 溶液pH约为4.0。
3 2 3
下列说法正确的是
A.当pH=8.3时,溶液中只存在Na+、H+、HCO -、CI-、OH-
3
B.溶液pH由8.3变成4.0过程中,发生反应:CO 2-+2H+=CO ↑+H O
3 2 2
C.若V =2V ,则x=y
2 1
8.4103V
D.试样中, NaHCO 的质量分数 2 1000
3 0
a
二、非选择题(本大題共5小题,共20分)
26.(4分)
(1)①写出Na O的名称
2
②写出葡萄糖的分子式:
(2) 写出氯气与溴化钾溶液反应的化学方程式:
25.(4分)已知:X为具有浓郁香味、不易溶于水的油状液体,食醋中约含有3%~5%
的D,其转化关系如下图所示。请回答:
(1)X的结构简式是
(2)A→B的化学方程式是
(3)下列说法不正确的是
A.A+D→X的反应属于取代反应
B.除去X中少量D杂质可用饱和Na CO 溶液
2 3
C.A与金属钠反应比水与金属钠反应要剧烈得多
D.等物质的量的A、B、D完全燃烧消耗O 的量依次减小
2
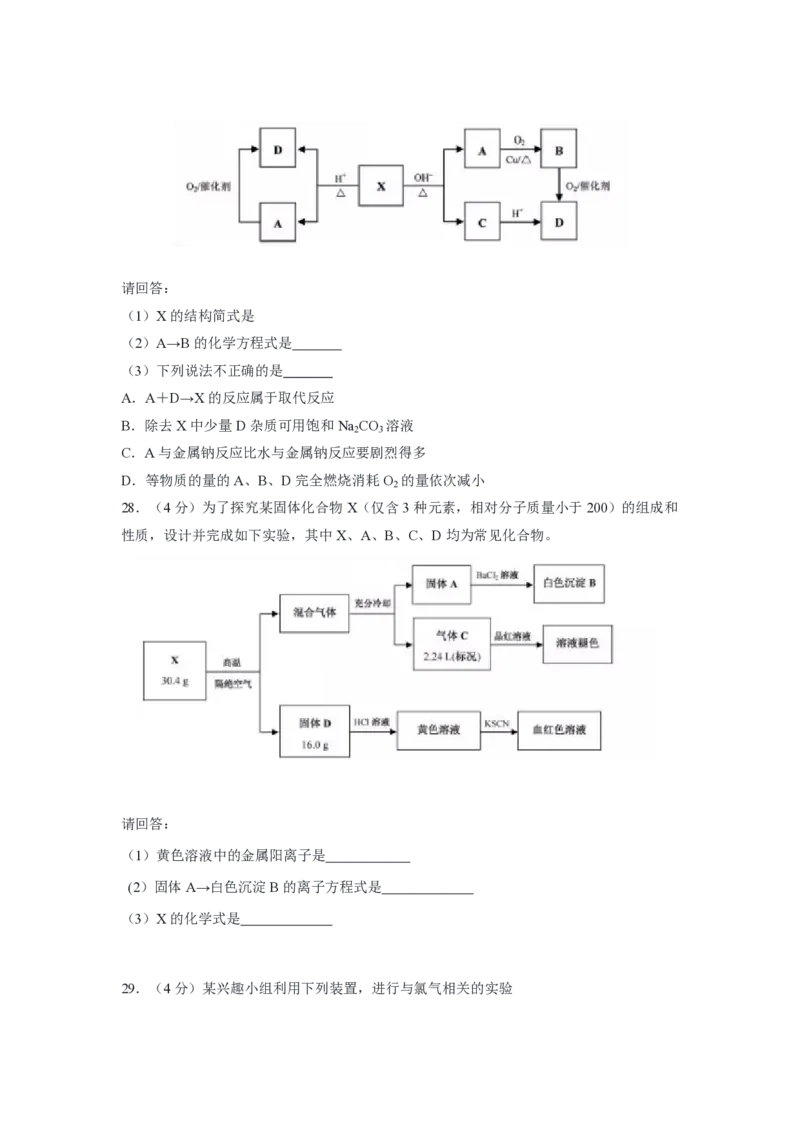
28.(4分)为了探究某固体化合物X(仅含3种元素,相对分子质量小于200)的组成和
性质,设计并完成如下实验,其中X、A、B、C、D均为常见化合物。
请回答:
(1)黄色溶液中的金属阳离子是
(2)固体A→白色沉淀B的离子方程式是
(3)X的化学式是
29.(4分)某兴趣小组利用下列装置,进行与氯气相关的实验(1)装置④中NaOH溶液的作用是
(2)实验结束后,取装置③中的溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得
到FeCl •6H O晶体。在蒸发浓缩操作中,不需要的仪器是
3 2
A.蒸发皿 B.漏斗 C.玻璃棒 D.酒精灯
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl
2
请说明理由
30.(4分)为探究某铜的硫化物的组成,取一定量的硫化物在氧气中充分灼烧,将生成
的气体全部通入盛有足量的H O 和BaCl 的混合液中,得到白色沉淀11.65g;将灼烧后的
2 2 2
固体(仅含铜与氧2种元素)溶于过量的H SO 中过滤,得到1.60g红色固体,将滤液稀释
2 4
至150mL,测得c(Cu2+)=0.50mo•lL-1。
已知:CuO+H SO ==CuSO +Cu+H O
2 4 4 2
请计算:
(1)白色沉淀的物质的量为 mol
(2)该铜的硫化物中铜与硫的原子个数比N(Cu):N(S)=