文档内容
绝密★考试结束前 B.可用精密pH试纸区分pH=5.1和pH=5.6的两种NH Cl溶液
4
C.用加水后再分液的方法可将苯和四氯化碳分离
2019年4月浙江省普通高校招生 选考 科目考试
D.根据燃烧产生的气昧,可区分棉纤绵和蛋白质纤维
10.下列说法正确的是
化学试题
A.18O 和16O 互为同位素
2 2
姓名:____________ 准考证号:____________ B.正己烷和2,2−二甲基丙烷互为同系物
本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。其中加试题部分为 C.C 和C 是具有相同质子数的不同核素
60 70
30分,用【加试题】标出。考生注意: D.H NCH COOCH 和CH CH NO 是同分异构体
2 2 3 3 2 2
1.答题前,请务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔分别填写在试题卷和答题纸
11.针对下列实验现象表述不正确的是
规定的位置上。
2.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上 A.用同一针筒先后抽取80 mL氯气、20 mL水,振荡,气体完全溶解,溶液变为黄绿色
的作答一律无效。 B.在表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,固体由蓝色变白色
3.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可先使用 C.向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀
2B铅笔,确定后必须使用黑色字迹的签字笔或钢笔描黑,答案写在本试题卷上无效。 D.将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成
4.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Ca 40 Fe 12.化学电源在日常生活和高科技领域中都有广泛应用。
56 Cu 64 Ba 137
选择题部分
一、选择题(本大题共25小题,每小题2分,共50分。每个小题列出的四个备选项中只有一个是符合题
目要求的,不选、多选、错选均不得分)
l.下列属于碱的是
A.C H OH B.Na CO C.Ca(OH) D.Cu (OH) CO
2 5 2 3 2 2 2 3
下列说法不正确的是
2.下列属于强电解质的是
A.硫酸钡 B.食盐水 C.二氧化硅 D.醋酸 A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
3.下列图示表示过滤的是 B.乙:正极的电极反应式为Ag O+2e−+H O===2Ag+2OH−
2 2
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
13.不能正确表示下列变化的离子方程式是
A. B. C. D. A.二氧化硫与酸性高锰酸钾溶液反应:5SO +2H O+2MnO===2Mn2++5SO+4H+
2 2
4.下列属于置换反应的是 B.酸性碘化钾溶液中滴加适量双氧水:2I−+2H++H O ===I +2H O
2 2 2 2
A.4NH 2 +5O 2 =======4NO+6H 2 O B.2Na 2 SO 3 +O 2 ===2Na 2 SO 4 C.硅酸钠溶液和盐酸反应:SiO+2H+===H SiO ↓
2 3
C.2Na O +2CO ===2Na CO +O D.2KI+Cl ===2KCl+I
2 2 2 2 3 2 2 2 D.硫酸铜溶液中加少量的铁粉:3Cu2++2Fe===2Fe3++3Cu
5.下列溶液呈碱性的是
A.NH NO B.(NH ) SO C.KCl D.K CO 14.2019年是门捷列夫提出元素周期表150周年。根据元素周期律和元素周期表,下列推断不合理的是
4 3 4 2 4 2 3
6.反应8NH +3Cl ===N +6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比为
3 2 2 4 3 2 A.第35号元素的单质在常温常压下是液体 B.位于第四周期第ⅤA族的元素为非金属元素
A.2∶3 B.8∶3 C.6∶3 D.3∶2
C.第84号元素的最高化合价是+7 D.第七周期0族元素的原子序数为118
7.下列表示不正确的是
15.下列说法不正确的是
A.正丁烷的沸点比异丁烷的高,乙醇的沸点比二甲醚的高
A.次氯酸的电子式 B.丁烷的球棍模型
B.甲烷、苯、葡萄糖均不能使溴水或酸性高锰酸钾溶液褪色
C.乙烯的结构简式CH =CH D.原子核内有8个中子的碳原子C
C.羊毛、蚕丝、塑料、合成橡胶都属于有机高分子材料
2 2
D.天然植物油没有恒定的熔沸点,常温下难溶于水
8.下列说法不正确的是 16.下列表述正确的是
A.液氯可以储存在钢瓶中 B.天然气的主要成分是甲烷的水合物 A.苯和氯气生成C 6 H 6 Cl 6 的反应是取代反应 B.乙烯与溴水发生加成反应的产物是CH 2 CH 2 Br 2
C.天然石英和水晶的主要成分都是二氧化硅 D.硫元素在自然界的存在形式有硫单质、硫化物和
C.等物质的量的甲烷与氯气反应的产物是CH
3
Cl
D.硫酸作催化剂,CH CO18OCH CH 水解所锝乙醇分子中有18O
硫酸盐等 3 2 3
9.下列说法不正确的是
17.下列说法正确的是
A.蒸馏时可通过加碎瓷片防暴沸
A.H(g)+I
2
(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变B.C(s)+H O(g) H (g)+CO(g),碳的质量不再改变说明反应已达平衡 B.生成聚合硫酸铁后,水溶液的pH增大
2 2
C.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C不能同时是气体 C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水 D.在相同条件下,Fe3+比[Fe(OH)]2+的水解
D.1 mol N 和3 mol H 反应达到平衡时H 转化率为10%,放出热量Q ;在相同温度和压强下, 能力更强
2 2 2 1
当2 mol NH 分解为N 和H 的转化率为10%时,吸收热至Q ,Q 不等于Q 25.白色固体混合物A,含有KCl、CaCO 、Na CO 、Na SiO 、CuSO ,中的几种,常温常压下进行如下
3 2 2 2 2 1 3 2 3 2 3 4
实验。
18.下列说法不正确的是
A.纯碱和烧碱熔化时克服的化学键类型相同 B.加热蒸发氯化钾水溶液的过程中有分子间作用
力的破坏
C.CO 溶于水和干冰升华都只有分子间作用力改变
2
D.石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
下列推断不正确的是
19.设N 为阿伏加德罗常数的值,下列说法不正确的是
A A.无色溶液B的pH≥7 B.白色固体F的主要成分是H SiO
2 3
A.1 mol CH =CH 分子中含有的共价键数为6N B.500 mL 0.5 mol·L−1的NaCl溶液中微粒 C.混合物A中有Na SiO 、CuSO 和CaCO
2 2 A 2 3 4 3
数大于0.5N D.在无色溶液B中加HNO 酸化,无沉淀;再滴加AgNO ,若有白色沉淀生成,说明混合物A中
A 3 3
C.30 g HCHO与CH COOH混合物中含C原子数为N 有KCl
3 A
D.2.3 g Na与O 完全反应,反应中转移的电子数介于0.1N 和0.2N 之间
2 A A 非选择题部分
20.在温热气候条件下,浅海地区有厚层的石灰石沉积,而深海地区却很少。下列解析不正确的是
二、非选择题(本大题共7小题,共50分)
A.与深海地区相比,浅海地区水温较高,有利于游离的CO 增多、石灰石沉积 26.(6分)以煤、天然气和生物质为原料制取有机化合物日益受到重视。E是两种含有碳碳双键的酯的混
2
B.与浅海地区相比,深海地区压强大,石灰石岩层易被CO 溶解,沉积少 合物。相关物质的转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):
2
C.深海地区石灰石岩层的溶解反应为:CaCO (s)+H O(l)+CO (aq)===Ca(HCO ) (aq)
3 2 2 3 2
D.海水里弱酸性,大气中CO 浓度增加,会导致海水中CO浓度增大
2
21.室温下,取20 mL 0.1 mol·L−1某二元酸H A,滴加0.2 mol·L−1 NaOH溶液。
2
已知:H A===H++HA−,HA− H++A2−。下列说法不正确的是
2 请回答:(1) A→B的反应类型________,C中含氧官能团的名称________。
A.0.1 mol·L−1 H A溶液中有c(H+)-c(OH−)-c(A2−)=0.1 mol·L−1 (2) C与D反应得到E的化学方程式____________________________________________。
2
B.当滴加至中性时,溶液中c(Na+)=c(HA−)+2c(A2−),用去NaOH溶液的体积小于10 mL (3) 检验B中官能团的实验方法__________________________________________________。
C.当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2−)=c(H+)-c(OH−) 27.(6分)固体化合物X由3种元素组成。某学习小组进行了如下实验:
D.当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA−)+2c(A2−)
22.高温高压液态水具有接近常温下弱酸的c(H+)或弱碱的c(OH−),油脂在其中能以较快的反应速率水
解。与常温常压水相比,下列说法不正确的是
A.高温高压液态水中,体系温度升高,油脂水解反应速率加快
B.高温高压液态水中,油脂与水的互溶能力增强,油脂水解反应速率加快
C.高温高压液态水中,c(H+)增大,可催化油脂水解反应,且产生的酸进一步催化水解 请回答:(1) 由现象1得出化合物X含有________元素(填元素符号)。
D.高温高压液态水中的油脂水解,相当于常温下在体系中加入了相同c(H+)的酸或相同c(OH−)的 (2) 固体混合物Y的成分________(填化学式)。
碱的水解 (3) X的化学式________。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反
23.MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg): 应的化学方程式是________。
3 3
M2+(g)+CO(g) ———→ M2+(g)+O2−(g)+CO (g) 28.(4分)某同学设计如图装置(气密性已检查)制备Fe(OH) 白色沉淀。
2 2
MCO3(s) ———→ MO(s)+CO2(g)
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A.ΔH (MgCO )>ΔH (CaCO )>0 B.ΔH (MgCO )=ΔH (CaCO )>0
1 3 1 3 2 3 2 3
C.ΔH (CaCO )-ΔH (MgCO )=ΔH (CaO)-ΔH (MgO) D.对于MgCO 和CaCO ,ΔH +ΔH
1 3 1 3 3 3 3 3 1 2
>ΔH
3
24.聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和KClO 在水溶液中反应
4 n 4 2 3 请回答:
(1) 仪器1的名称________。装置5的作用________。
得到。下列说法不正确的是
(2) 实验开始时,关闭K ,打开K ,反应一段时间后,再打开K ,关闭K ,发现3中溶液不能进
2 1 2 1
A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗6/n mol KClO
3 4 n 3 入4中。请为装置作一处改进,使溶液能进入4中________。(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有 ①阳极的电极反应式是__________________________。②制备H O 的总反应方程式是
2 2
产生白色沉淀的原因________。 ______________。
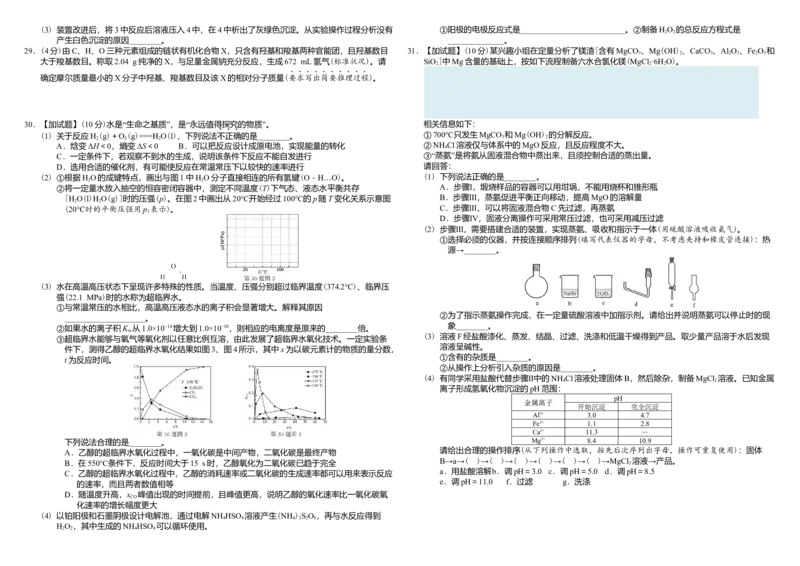
29.(4分)由C、H、O三种元素组成的链状有机化合物X,只含有羟基和羧基两种官能团,且羟基数目 31.【加试题】(10分)某兴趣小组在定量分析了镁渣[含有MgCO 、Mg(OH) 、CaCO 、Al O 、Fe O 和
3 2 3 2 3 2 3
大于羧基数目。称取2.04 g纯净的X,与足量金属钠充分反应,生成672 mL氢气(标准状况)。请 SiO ]中Mg含量的基础上,按如下流程制备六水合氯化镁(MgCl ·6H O)。
2 2 2
确定摩尔质量最小的X分子中羟基、羧基数目及该X的相对分子质量(要求写出简要推理过程)。
30.【加试题】(10分)水是“生命之基质”,是“永远值得探究的物质”。 相关信息如下:
(1) 关于反应H
2
(g)+O
2
(g)===H
2
O(l),下列说法不正确的是________。 ①700℃只发生MgCO
3
和Mg(OH)
2
的分解反应。
A.焓变ΔH<0,熵变ΔS<0 B.可以把反应设计成原电池,实现能量的转化 ②NH
4
Cl溶液仅与体系中的MgO反应,且反应程度不大。
C.一定条件下,若观察不到水的生成,说明该条件下反应不能自发进行 ③“蒸氨”是将氨从固液混合物中蒸出来,且须控制合适的蒸出量。
D.选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行 请回答:
(2) ①根据H O的成键特点,画出与图1中H O分子直接相连的所有氢键(O-H…O)。 (1) 下列说法正确的是________。
2 2
②将一定量水放入抽空的恒容密闭容器中,测定不同温度(T)下气态、液态水平衡共存 A.步骤Ⅰ,煅烧样品的容器可以用坩埚,不能用烧杯和锥形瓶
[H O(l)H O(g)]时的压强(p)。在图2中画出从20℃开始经过100℃的p随T变化关系示意图 B.步骤Ⅲ,蒸氨促进平衡正向移动,提高MgO的溶解量
2 2
(20℃时的平衡压强用p 表示)。 C.步骤Ⅲ,可以将固液混合物C先过滤,再蒸氨
1
D.步骤Ⅳ,固液分离操作可采用常压过滤,也可采用减压过滤
(2) 步骤Ⅲ,需要搭建合适的装置,实现蒸氨、吸收和指示于一体(用硫酸溶液吸收氨气)。
①选择必须的仪器,并按连接顺序排列(填写代表仪器的字母,不考虑夹持和橡皮管连接):热
源→________。
(3) 水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2℃)、临界压
强(22.1 MPa)时的水称为超临界水。
①与常温常压的水相比,高温高压液态水的离子积会显著增大。解释其原因
②为了指示蒸氨操作完成,在一定量硫酸溶液中加指示剂。请给出并说明蒸氨可以停止时的现
____________________。
②如果水的离子积K 从1.0×10−14增大到1.0×10−10,则相应的电离度是原来的________倍。
象________。
w
(3) 溶液F经盐酸漆化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。取少量产品溶于水后发现
③超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条
溶液呈碱性。
件下,测得乙醇的超临界水氧化结果如图3、图4所示,其中x为以碳元素计的物质的量分数,
①含有的杂质是________。
t为反应时间。
②从操作上分析引入杂质的原因是________。
(4) 有同学采用盐酸代替步骤Ⅱ中的NH Cl溶液处理固体B,然后除杂,制备MgCl 溶液。已知金属
4 2
离子形成氢氧化物沉淀的pH范围:
pH
金属离子
开始沉淀 完全沉淀
Al3+ 3.0 4.7
Fe3+ 1.1 2.8
Ca2+ 11.3 -
下列说法合理的是________。 Mg2+ 8.4 10.9
A.乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物
请给出合理的操作排序(从下列操作中选取,按先后次序列出字母,操作可重复使用):固体
B.在550℃条件下,反应时间大于15 s时,乙醇氧化为二氧化碳已趋于完全
B→a→( )→( )→( )→( )→( )→( )→MgCl
2
溶液→产品。
a.用盐酸溶解b.调pH=3.0 c.调pH=5.0 d.调pH=8.5
C.乙醇的超临界水氧化过程中,乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应
e.调pH=11.0 f.过滤 g.洗涤
的速率,而且两者数值相等
D.随温度升高,x 峰值出现的时间提前,且峰值更高,说明乙醇的氧化速率比一氧化碳氧
CO
化速率的增长幅度更大
(4) 以铂阳极和石墨阴极设计电解池,通过电解NH HSO 溶液产生(NH ) S O ,再与水反应得到
4 4 4 2 2 8
H O ,其中生成的NH HSO 可以循环使用。
2 2 4 432.【加试题】(10分)某研究小组拟合成除草剂苯达松和染料中间体X。
已知信息:①+RCOOR′—————→
②RCH COOR′+R′′COOR′′′—————→
2
(1) 下列说法正确的是________。
A.化合物B到C的转变涉及到取代反应
B.化合物C具有两性
C.试剂D可以是甲醇
D.苯达松的分子式是C H N O S
10 10 2 3
(2) 化合物F的结构简式是________。
(3) 写出E+G→H的化学方程式________。
(4) 写出C H NO 同时符合下列条件的同分异构体的结构简式________。
6 13 2
①分子中有一个六元环,且成环原子中最多含2个非碳原子;
②1H−NMR谱和IR谱检测表明分子中有4种化学环境不同的氢原子。有N-O键,没有过氧键
(-O-O-)。
(5) 设计以CH CH OH和 原料制备X( )的合成路线(无机试剂任选,合
3 2
成中须用到上述①②两条已知信息,用流程图表示)________。②
化学试题参考答案
一、选择题(本大题共25小题,每小题2分,共50分。每个小题列出的四个备选项中只有一个是符合题
目要求的,不选、多选、错选均不得分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C A C D D A A B C B
题号 11 12 13 14 15 16 17 18 19 20
(3) ①水的电离为吸热过裎,升高温度有利于电离(压强对电离平
答案 A A D C B D B C D D
衡影响不大)
题号 21 22 23 24 25
②100
答案 B D C A C
③ABD
二、非选择题(本大题共7小题,共50分)
(4) ①2HSO-2e−===S O+2H+或2SO-2e−===S O
2 2
26.(6分)
②2H O=====H O +H ↑
2 2 2 2
(1) 氧化反应
31.(10分)
羧基
(1) ABD
(2) +CH =CHCOOH————→+H O
2 2 (2) ①a→d→f→c
+CH =CHCOOH————→+H O
2 2 ②甲基橙,颜色由红色变橙色
(3) 加过量银氨溶液,加热,出现银镜,说明有醛基;用盐酸酸
(3) ①碱式氯化镁(氢氧化镁)
化,过滤,滤液中加入溴水,若溴水褪色,说明有碳碳双键
②过度蒸发导致氯化镁水解
27.(6分)
(4) c→f→e→f→g→a
(1) O
32.(10分)
(2) Cu和NaOH
(1) BC
(3) NaCuO
2 (2) (CH ) CHNH
2NaCuO +8HCl===2NaCl+2CuCl+Cl ↑+4H O 3 2 2
2 2 2 (3)
28.(4分)
+(CH ) CHNHSO Cl
3 2 2
(1) 滴液漏斗(分液漏斗)
液封,防止空气进入装置4
+HCl
(2) 在装置2、3之间添加控制开关
(4)
(3) 装置4内的空气没有排尽
29.(4分)
n(H )=0.03 mol,设X中羟基和羧基的总数为m个(m≥2)
2
则n(X)=(0.03×2)/m=0.06/m mol,M(X)=2.04m/0.06=34m (5) CH CH OH——→CH COOH——————
3 2 3
g·mol−1 →CH COOCH CH ————→ CH COCH COOCH CH
3 2 3 3 2 2 3
m=4,M(X)=136 g·mol−1,含有3个羟基和1个羧基,相对分子质
量为136。 ——————→
说明:1.文档中可逆符号均使用ZBFH字体,显示异常请下载字体或对应PDF。
2019 年 4 月浙江省普通高校招生选考科目考试
2.制图使用Chem Draw和MS Visio。
30.(10分)
(1) C
化学试题
(2) ①
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Ca 40 Fe 56 Cu
64 Ba 137
选择题部分
一、选择题(本大题共25小题,每小题2分,共50分。每个小题列出的四个备选项中只有一个是符合题
目要求的,不选、多选、错选均不得分)
1.下列属于碱的是
A. C HOH B. NaCO C. Ca(OH) D. Cu (OH) CO
2 5 2 3 2 2 2 3【答案】C 【解析】
【解析】 【详解】置换反应是指一个单质和一个化合物反应生成另一个单质和化合物,属于氧化还原反应,前者在后者的概念范
【详解】A. C HOH是有机物,属于醇类,A不合题意; 围内;
2 5
B. Na CO 属于无机盐,B不合题意; A.该反应属于氧化还原反应,但不是置换反应,A不合题意;
2 3
C. Ca(OH) 是二元强碱,C符合题意; B.该反应是化合反应,B不合题意;
2
D. Cu (OH) CO 是碱式盐,D不合题意。 C.该反应属于氧化还原反应,但不是置换反应,C不合题意;
2 2 3
故答案选C。 D.该反应符合置换反应定义,属于非金属单质之间的置换反应,活泼性强的非金属单质置换出活泼性较弱的非金属单质,
2.下列属于强电解质的是 D符合题意。
A. 硫酸钡 B. 食盐水 C. 二氧化硅 D. 醋酸 故答案选D。
【答案】A 5.下列溶液呈碱性的是
【解析】 A. NH NO B. (NH )SO C. KCl D. KCO
4 3 4 2 4 2 3
【详解】按强电解质的定义可知,强电解质指在水中完全电离的电解质,包含强酸、强碱、大部分盐等。所以对四个选
【答案】D
项进行物质分类考查: 【解析】
A.可知硫酸钡是强电解质,A项正确; 【分析】
B.食盐水为混合物,不在强电解质的概念内,B项错误; 盐类水解是指弱酸阴离子或弱碱阳离子发生水解,导致溶液的酸碱性发生变化,本题四个选项均涉及盐类水解。
C.二氧化硅是非电解质,C项错误; 【详解】A.该盐属于强酸弱碱盐,NH ++H O⇌NH ·H O+H+,溶液显酸性,A不合题意;
4 2 3 2
D.醋酸在水中不完全电离,为弱电解质,D项错误。 B.同A,NH +发生水解,使得溶液显酸性,B不合题意;
4
故答案选A。 C.该盐属于强酸强碱盐,不发生水解,溶液显中性,C不合题意;
3.下列图示表示过滤的是 D.该盐属于强碱弱酸盐,CO2-+H O⇌HCO -+OH-,HCO -+H O⇌HCO+OH-,溶液显碱性,D项符合题意。
3 2 3 3 2 2 3
故答案选D。
【点睛】关于正盐的酸碱性可利用口诀速度判断:“谁强显谁性,都强显中性,都弱须看电离程度大小”。
A. B. C. D.
6.反应8NH +3Cl N+6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比为
3 2 2 4 3 2
A. 2∶3 B. 8∶3 C. 6∶3 D. 3∶2
【答案】C
【答案】A
【解析】
【解析】
【详解】A.该操作是分液,A不合题意;
B.该操作是配制一定物质的量浓度溶液中定容步骤,B不合题意;
【详解】该氧化还原反应用双线桥表示为 ,可知实际升价的N原子为2个,所以2个NH 被氧
3
C.该操作是过滤,C符合题意;
D.该操作是配制一定物质的量浓度溶液中转移溶液步骤,D不合题意。
故答案选C。 化,同时Cl 全部被还原,观察计量数,Cl 为3个,因而被氧化的NH 与被还原的Cl 的物质的量之比为2:3。
2 2 3 2
4.下列属于置换反应的是 故答案选A。
7.下列表示不正确的是
A. 4NH +5O 4NO+6HO B. 2NaSO +O 2NaSO
3 2 2 2 3 2 2 4
C. 2NaO+2CO 2NaCO+O D. 2KI+Cl 2KCl+I
2 2 2 2 3 2 2 2 A. 次氯酸的电子式 B. 丁烷的球棍模型
【答案】DC. 乙烯的结构简式CH=CH D. 原子核内有8个中子的碳原子14C A. 18O 和16O 互为同位素
2 2 6 2 2
【答案】A B. 正己烷和2,2−二甲基丙烷互为同系物
【解析】 C. C 和C 是具有相同质子数的不同核素
60 70
【详解】A.次氯酸中Cl最外层为7个电子,为达到8电子稳定结构,需要拿出一个电子与其他原子形成一个共用电子对, D. HNCH COOCH 和CHCHNO 是同分异构体
2 2 3 3 2 2
O原子最外层为6个电子,为达到8电子稳定结构,需要拿出两个电子与其他原子形成两对共用电子对,因而次氯酸的 【答案】B
【解析】
电子式为 ,A项错误。B、C、D等3个选项均正确。 【详解】A. 18O 和16O 是指相对分子质量不同的分子,而同位素指具有相同质子数,但中子数不同的元素互称同位素,
2 2
故答案选A。 A项错误;
8.下列说法不正确的是 B. 正己烷的分子式C 6 H 14 ,2,2−二甲基丙烷即新戊烷分子式是C 5 H 12 ,两者同属于烷烃,且分子式差一个CH 2 ,属于同系
A. 液氯可以储存在钢瓶中 物,B项正确;
B. 天然气的主要成分是甲烷的水合物 C.核素表示具有一定的质子数和中子数的原子,C 60 和C 70 是由一定数目的碳原子形成的分子,显然,C项错误;
C. 天然石英和水晶的主要成分都是二氧化硅 D. H 2 NCH 2 COOCH 3 和CH 3 CH 2 NO 2 是分子式分别为C 3 H 7 O 2 N和C 2 H 5 O 2 N,分子式不同,显然不是同分异构体,D项错误。
D. 硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等 故答案选B。
【答案】B 11.针对下列实验现象表述不正确的是
【解析】 A. 用同一针筒先后抽取80 mL氯气、20 mL水,振荡,气体完全溶解,溶液变为黄绿色
【详解】A.液氯就是液态的氯气,与钢瓶不反应,可以储存在钢瓶中,A项正确; B. 在表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,固体由蓝色变白色
B.天然气的主要成分是甲烷,可燃冰的主要成分是甲烷的水合物,B项错误; C. 向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀
C.石英、水晶、硅石、沙子的主要成分均为二氧化硅,C项正确; D. 将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成
D.硫在地壳中主要以硫化物、硫酸盐等形式存在,火山口处有硫单质,D项正确。 【答案】A
故答案选B。 【解析】
9.下列说法不正确的是 【详解】A.氯气可溶于水,在常温时,1体积水大约能溶解2体积氯气,因而20mL水大约能溶解40mL氯气,气体大约
A. 蒸馏时可通过加碎瓷片防暴沸 剩余40mL未溶解,A项错误;
B. 可用精密pH试纸区分pH=5.1和pH=5.6的两种NH Cl溶液 B.胆矾指的是五水合硫酸铜(CuSO ·5H O),其显蓝色,而浓硫酸具有吸水性,CuSO ·5H O变为CuSO ,CuSO 为白
4 4 2 4 2 4 4
C. 用加水后再分液的方法可将苯和四氯化碳分离 色固体,B项正确;
D. 根据燃烧产生的气味,可区分棉纤绵和蛋白质纤维 C.双氧水将SO 氧化,离子方程式为HO+SO =SO2-+2H+,氯化钡溶液中Ba2+与SO 2-生成BaSO 白色沉淀,C项正确;
2 2 2 2 4 4 4
【答案】C
D.将点燃后的镁条伸入充满二氧化碳的集气瓶,发生反应的化学方程式为 ,MgO为白色固体,C
【解析】
【详解】A.加热液体至沸腾时,必须要在反应容器内加碎瓷片,防止暴沸,否则出现暴沸将会很危险,A项正确; 是黑色固体,D项正确。
B.精密pH试纸可以将pH值精确到小数点后一位,所以可以区分pH=5.1和pH=5.6的两种NH Cl溶液,B项正确; 故答案选A。
4
C.苯和四氯化碳互相溶解,均难溶于水,因而加水不影响苯和四氯化碳的互溶体系,不可以分液,可采用蒸馏分离,C 12.化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
项错误;
D. 棉纤绵成分是纤维素,蛋白质纤维成分是蛋白质,蛋白质燃烧时会产生烧焦羽毛的气味,因而可以用燃烧法区别,D
A. Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
项正确。
故答案选C。
10.下列说法正确的是B. 位于第四周期第ⅤA族的元素为非金属元素
C. 第84号元素的最高化合价是+7
B. 正极的电极反应式为Ag O+2e−+HO 2Ag+2OH−
2 2
D. 第七周期0族元素的原子序数为118
【答案】C
【解析】
【详解】A.35号元素是溴元素,单质Br 在常温常压下是红棕色的液体,A项合理;
C. 锌筒作负极,发生氧化反应,锌筒会变薄 2
B.位于第四周期第ⅤA族的元素是砷元素(As),为非金属元素,B项合理;
C.第84号元素位于第六周期ⅥA族,为钋元素(Po),由于最高正价等于主族序数,所以该元素最高化合价是+6,C
项不合理;
D. 使用一段时间后,电解质溶液的酸性减弱,导电能力下降 D.第七周期0族元素是第七周期最后一个元素,原子序数为118,D项合理。
故答案选C。
15.下列说法不正确的是
【答案】A
A. 正丁烷的沸点比异丁烷的高,乙醇的沸点比二甲醚的高
【解析】
B. 甲烷、苯、葡萄糖均不能使溴水或酸性高锰酸钾溶液褪色
【详解】A.Zn较Cu活泼,做负极,Zn失电子变Zn2+,电子经导线转移到铜电极,铜电极负电荷变多,吸引了溶液中的
C. 羊毛、蚕丝、塑料、合成橡胶都属于有机高分子材料
阳离子,因而Zn2+和H+迁移至铜电极,H+氧化性较强,得电子变H,因而c(H+)减小,A项错误;
2
D. 天然植物油没有恒定的熔、沸点,常温下难溶于水
B. Ag O作正极,得到来自Zn失去的电子,被还原成Ag,结合KOH作电解液,故电极反应式为Ag O+2e−+HO 2Ag
2 2 2
【答案】B
+2OH−,B项正确;
【解析】
C.Zn为较活泼电极,做负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,锌溶解,因而锌筒会变薄,C项正确;
【详解】A.对于分子式相同的烷烃,支链越多,沸点越低,因而正丁烷的沸点比异丁烷的高。而对于相对分子质量相近
的有机物,含羟基越多,沸点越高,原因在于-OH可形成分子间的氢键,使得沸点升高,因而乙醇的沸点比二甲醚的高,
D.铅蓄电池总反应式为PbO + Pb + 2H SO 2PbSO + 2H O,可知放电一段时间后,HSO 不断被消耗,因而
2 2 4 4 2 2 4
A项正确;
电解质溶液的酸性减弱,导电能力下降,D项正确。 B.葡萄糖为多羟基醛,含有醛基,能使溴水或者酸性高锰酸钾溶液褪色,甲苯也可使酸性高锰酸钾溶液褪色,B项错误;
故答案选A。 C.羊毛、蚕丝主要成分是蛋白质,为天然高分子化合物,塑料、合成橡胶都属于人工合成的高分子材料,C项正确;
13.不能正确表示下列变化的离子方程式是 D.天然植物油是混合物,无固定熔、沸点,另外,植物油常温下难溶于水,D项正确。
A. 二氧化硫与酸性高锰酸钾溶液反应:5SO +2HO+2MnO - 2Mn2++5SO +4H+ 故答案选B。
2 2 4
B. 酸性碘化钾溶液中滴加适量双氧水:2I−+2H++HO I+2HO 16.下列表述正确的是
2 2 2 2
C. 硅酸钠溶液和盐酸反应:SiO2-+2H+ HSiO↓ A. 苯和氯气生成C HCl 的反应是取代反应
3 2 3 6 6 6
D. 硫酸铜溶液中加少量的铁粉:3Cu2++2Fe 2Fe3++3Cu B. 乙烯与溴水发生加成反应的产物是CHCHBr
2 2 2
【答案】D C. 等物质的量的甲烷与氯气反应的产物是CHCl
3
【解析】 D. 硫酸作催化剂,CHCO18OCH CH 水解所得乙醇分子中有18O
3 2 3
【详解】D.Fe3+氧化性大于Cu2+,所以Cu2+只能将Fe氧化到Fe2+,因而硫酸铜溶液中加少量的铁粉的离子方程式为 【答案】D
Cu2++Fe Fe2++Cu,D项错误。其他3个选项的离子方程式都是正确的。 【解析】
故答案选D。
14.2019年是门捷列夫提出元素周期表150周年。根据元素周期律和元素周期表,下列推断不合理的是 【详解】A.苯和氯气生成农药六六六,其反应方程式为 ,反应类型是加成反应,A项错误;
A. 第35号元素的单质在常温常压下是液体B.乙烯与溴水发生加成反应的产物是CHBrCHBr,B项错误; A. 1 mol CH =CH 分子中含有的共价键数为6N
2 2 2 2 A
C.甲烷和氯气反应为连续反应,甲烷和氯气生成CHCl和HCl,接着CHCl和氯气生成CHCl 和HCl,之后生成CHCl B. 500 mL 0.5 mol·L−1的NaCl溶液中微粒数大于0.5N
3 3 2 2 3 A
和CCl ,,因而产物除了4种有机物,还有HCl,C项错误; C. 30 g HCHO与CHCOOH混合物中含C原子数为N
4 3 A
D.酯类水解断裂C-18O单键,该18O原子结合水中H,即生成乙醇H18OCH CH,因而,D项正确。 D. 2.3 g Na与O 完全反应,反应中转移的电子数介于0.1N 和0.2N 之间
2 3 2 A A
故答案选D。 【答案】D
17.下列说法正确的是 【解析】
A. H(g)+I 2 (g) ⇌ 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变 【详解】A.1个乙烯分子中碳碳双键含两个共价键,4个碳氢键合为4个共价键,总计6个共价键,因而1mol CH 2 =CH 2
B. C(s)+HO(g) ⇌ H(g)+CO(g),碳的质量不再改变说明反应已达平衡 分子中含有的共价键数为6N ,A项正确;
2 2 A
C. 若压强不再随时间变化能说明反应2A(?)+B(g) ⇌ 2C(?)已达平衡,则A、C不能同时是气体 B.n(Na+)=n(Cl-)=0.5L×0.5mol·L-1=0.25mol,n(Na+)+n(Cl-)=0.5mol,因而钠离子和氯离子总计0.5N 个,但水会电离出极少
A
D. 1 mol N 和3 mol H 反应达到平衡时H 转化率为10%,放出的热量为Q;在相同温度和压强下,当2 mol NH 分解为 量的H+和OH-,因而NaCl溶液中微粒数大于0.5N ,B项正确;
2 2 2 1 3 A
N 和H 的转化率为10%时,吸收的热量为Q,Q 不等于Q C.HCHO与CHCOOH的最简式为CHO,原混合物相当于30gCHO,n(CHO)=1mol,因而C原子数为N ,C项正确;
2 2 2 2 1 3 2 2 2 A
【答案】B D.不管钠和氧气生成氧化钠还是过氧化钠,钠元素的化合价由0变为+1,因而2.3gNa(2.3gNa为0.1mol)转移电子数为
【解析】 0.1mol×1×N =0.1N ,D项错误。
A A
【详解】A.该可逆反应的反应前后气体计量数不发生变化,当缩小反应容器体积,相当于加压,正逆反应速率同等程度 故答案选D。
增加,A项错误; 20.在温热气候条件下,浅海地区有厚层的石灰石沉积,而深海地区却很少。下列解析不正确的是
B.在建立平衡前,碳的质量不断改变,达到平衡时,质量不变,因而碳的质量不再改变说明反应已达平衡,B项正确; A. 与深海地区相比,浅海地区水温较高,有利于游离的CO 增多、石灰石沉积
2
C.若压强不再改变说明反应达到平衡,表明反应前后气体的计量数不等,故A、C不可能均为气体,C项错误; B. 与浅海地区相比,深海地区压强大,石灰石岩层易被CO 溶解,沉积少
2
D.易知N
2
(g)+3H
2
(g)⇌2NH
3
(g) ΔH,合成氨气实际参与反应n(H
2
)=3×10%=0.3mol,因而Q
1
=0.3/3×|ΔH|=0.1|ΔH|,分解氨 C. 深海地区石灰石岩层的溶解反应为:CaCO
3
(s)+H
2
O(l)+CO
2
(aq) Ca(HCO
3
)
2
(aq)
气时实际消耗的n(NH )=2×10%=0.2mol,Q=0.2/2×|ΔH|=0.1|ΔH|,则Q=Q ,D项错误。 D. 海水呈弱酸性,大气中CO 浓度增加,会导致海水中CO 浓度增大
3 2 1 2 2
故答案选B。 【答案】D
18.下列说法不正确的是 【解析】
A. 纯碱和烧碱熔化时克服的化学键类型相同 【分析】
B. 加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏 石灰岩的形成是 CaCO 3 的沉积结果,海水中溶解一定量的 CO 2 ,因此CaCO 3 与CO 2 ,H 2 O之间存在着下列平衡:
C. CO 溶于水和干冰升华都只有分子间作用力改变 CaCO (s)+CO(g)+HO(l)⇌Ca(HCO )(aq)。
2 3 2 2 3 2
D. 石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏 【详解】A.海水中CO 的溶解度随温度的升高而减小,随压力的增大而增大,在浅海地区,海水层压力较小,同时水温
2
【答案】C 比较高,因而CO 的浓度较小,即游离的CO 增多,根据平衡移动原理,上述平衡向生成CaCO 方向移动,产生石灰石
2 2 3
【解析】
沉积,A项正确;
【详解】A.烧碱和纯碱均属于离子化合物,熔化时须克服离子键,A项正确;
B.与A恰恰相反,石灰石岩层易被CO 溶解,沉积少,B项正确;
2
B.加热蒸发氯化钾水溶液,液态水变为气态水,水分子之间的分子间作用力被破坏,B项正确;
C.在深海地区中,上述平衡向右移动,且倾向很大,故溶解反应为CaCO (s)+HO(l)+CO(aq) Ca(HCO )(aq),C项
3 2 2 3 2
C.CO 溶于水发生反应:CO+H O⇌HCO,这里有化学键的断裂和生成,C项错误;
2 2 2 2 3 正确;
D.石墨属于层状结构晶体,每层石墨原子间为共价键,层与层之间为分子间作用力,金刚石只含有共价键,因而石墨转
D. 海水温度一定时,大气中CO 浓度增加,海水中溶解的CO 随之增大,导致CO2-转化为HCO -,CO2-浓度降低,D
2 2 3 3 3
化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏,D项正确。
项错误。
故答案选C。
故答案选D。
19.设N
A
为阿伏加德罗常数的值,下列说法不正确的是
21.室温下,取20 mL 0.1 mol·L−1某二元酸HA,滴加0.1 mol·L−1 NaOH溶液。已知:HA H++HA−,HA−⇌H++A2−。
2 2下列说法不正确的是 故答案选D。
A. 0.1 mol·L−1 HA溶液中有c(H+)-c(OH−)-c(A2−)=0.1 mol·L−1 23.MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
2 3 3
B. 当滴加至中性时,溶液中c(Na+)=c(HA−)+2c(A2−),用去NaOH溶液的体积小于10 mL M2+(g)+CO2-(g) M2+(g)+O2−(g)+CO(g)
3 2
C. 当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2−)=c(H+)-c(OH−)
D. 当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA−)+2c(A2−)
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
【答案】B
A. ΔH(MgCO )>ΔH(CaCO)>0
【解析】 1 3 1 3
B. ΔH(MgCO )=ΔH(CaCO)>0
【分析】 2 3 2 3
C. ΔH(CaCO)-ΔH(MgCO )=ΔH(CaO)-ΔH(MgO)
由于该二元酸HA,第一步电离完全,第二步部分电离,可以把20 mL 0.1 mol·L−1二元酸HA看做20 mL 0.1 mol·L−1HA- 1 3 1 3 3 3
2 2
D. 对于MgCO 和CaCO ,ΔH+ΔH>ΔH
一元弱酸和0.1mol/LH+溶液,注意该溶液是不存在HA微粒。 3 3 1 2 3
2
【答案】C
【详解】A. 0.1 mol·L−1HA 溶液存在电荷守恒,其关系为 c(H+)=c(OH−)+2c(A2−)+ c(HA−),因而 c(H+)-c(OH−)-c(A2−)=
2
【解析】
c(A2−)+c(HA−)=0.1mol·L−1,A项正确;
【详解】根据盖斯定律,得 ΔH=ΔH+ΔH +ΔH ,又易知 Ca2+半径大于 Mg2+半径,所以 CaCO 的离子键强度弱于
1 2 3 3
B.若NaOH用去10ml,反应得到NaHA溶液,由于HA−⇌H++A2−,溶液显酸性,因而滴加至中性时,需要加入超过
MgCO ,CaO的离子键强度弱于MgO。
3
10ml的NaOH溶液,B项错误;
A. ΔH 表示断裂CO2-和M2+的离子键所吸收的能量,离子键强度越大,吸收的能量越大,因而ΔH(MgCO )>
1 3 1 3
C.当用去NaOH溶液体积10 mL时,得到NaHA溶液,溶液的pH<7,存在质子守恒,其关系为c(A2−)=c(H+)-
ΔH(CaCO)>0,A项正确;
1 3
c(OH−),C项正确;
B. ΔH 表示断裂CO2-中共价键形成O2−和CO 吸收的能量,与M2+无关,因而ΔH(MgCO )=ΔH(CaCO)>0,B项正确;
2 3 2 2 3 2 3
D.当用去NaOH溶液体积20 mL时,得到NaA溶液,根据物料守恒有:c(Na+)=2c(HA−)+2c(A2−),D项正确。
2
C.由上可知ΔH(CaCO)-ΔH (MgCO )<0,而ΔH 表示形成MO离子键所放出的能量,ΔH 为负值,CaO的离子键强度弱
1 3 1 3 3 3
故答案选B。
于MgO,因而ΔH(CaO)>ΔH(MgO),ΔH(CaO)-ΔH (MgO)>0,C项错误;
22.高温高压液态水具有接近常温下弱酸的c(H+)或弱碱的c(OH−),油脂在其中能以较快的反应速率水解。与常温常压水 3 3 3 3
D.由上分析可知ΔH+ΔH >0,ΔH<0,故ΔH+ΔH>ΔH,D项正确。
1 2 3 1 2 3
相比,下列说法不正确的是
故答案选C。
A. 高温高压液态水中,体系温度升高,油脂水解反应速率加快
24.聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和KClO 在水溶液中反应得到。下列说法不
4 n 4 2 3
B. 高温高压液态水中,油脂与水的互溶能力增强,油脂水解反应速率加快
正确的是
C. 高温高压液态水中,c(H+)增大,可催化油脂水解反应,且产生的酸进一步催化水解
A. KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗6/n mol KClO
D. 高温高压液态水中的油脂水解,相当于常温下在体系中加入了相同c(H+)的酸或相同c(OH−)的碱的水解 3 4 n 3
B. 生成聚合硫酸铁后,水溶液的pH增大
【答案】D
C. 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
【解析】
D. 在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
【详解】A.对于任何化学反应,体系温度升高,均可加快反应速率,A项正确;
【答案】A
B.由于高温高压液态水中,c(H+)和c(OH−)增大,油脂水解向右移动的倾向变大,因而油脂与水的互溶能力增强,反应速
【解析】
率加快,B项正确;
【详解】A.根据题干中信息,可利用氧化还原配平法写出化学方程式:6nFeSO +nKClO +3nH O=6[Fe(OH)SO ]n+nKCl,
4 3 2 4
C.油脂在酸性条件下水解,以H+做催化剂,加快水解速率,因而高温高压液态水中,c(H+)增大,可催化油脂水解反应,
可知KClO 做氧化剂,同时根据计量数关系亦知每生成1 mol [Fe(OH)SO ] 消耗n/6 mol KClO ,A项错误;
3 4 n 3
且产生的酸进一步催化水解,C项正确;
B.绿矾溶于水后,亚铁离子水解使溶液呈酸性,当其转系为聚合硫酸铁后,亚铁离子的浓度减小,因而水溶液的pH增
D.高温高压液态水中的油脂水解,其水环境仍呈中性,因而不能理解成相当于常温下在体系中加入了相同c(H+)的酸或
大,B项错误;
相同c(OH−)的碱的水解,而是以体系升温、增加水和油脂的互溶以及提高水中H+浓度的方式,促进油脂的水解,D项不
C.聚合硫酸铁可在水中形成氢氧化铁胶体,胶体粒子吸附杂质微粒引起聚沉,因而净水,C项正确;
正确。
D.多元弱碱的阳离子的水解是分步进行的。[Fe(OH)]2+的水解相当于Fe3+的二级水解,由于其所带的正电荷比Fe3+少,因而在相同条件下,其结合水电离产生的OH-的能力较弱,故其水解能力不如Fe3+,即在相同条件下,一级水解的程度大 (1) A→B的反应类型________,C中含氧官能团的名称________。
于二级水解,D项正确。 (2) C与D反应得到E的化学方程式________。
故答案选A。 (3) 检验B中官能团的实验方法________。
25.白色固体混合物A,含有KCl、CaCO 、NaCO、NaSiO、CuSO 中的几种,常温常压下进行如下实验。
3 2 3 2 3 4
【答案】 (1). 氧化反应 (2). 羧基 (3). +CH=CHCOOH +HO +
2 2
下列推断不正确的是
A. 无色溶液B的pH≥7 CH=CHCOOH +HO (4). 加过量银氨溶液,加热,出现银镜,说明有醛基;用盐酸酸化,
2 2
B. 白色固体F的主要成分是HSiO
2 3
C. 混合物A中有NaSiO、CuSO 和CaCO
2 3 4 3 过滤,滤液中加入溴水,若溴水褪色,说明有碳碳双键
D. 在无色溶液B中加HNO 酸化,无沉淀;再滴加AgNO,若有白色沉淀生成,说明混合物A中有KCl
3 3 【解析】
【答案】C
【分析】
【解析】
B到C发生氧化反应,醛基被氧化成羧基,C为 ,油脂在酸性条件下水解得到高级脂肪酸和甘油,
【分析】
白色固体混合物A加水得无色溶液B和固体C,B中肯定不含Cu2+,但结合固体C加过量硝酸,产生蓝色溶液,说明A
到B的过程中Cu2+转化为沉淀,A中必含有CuSO ,又结合固体C中加过量硝酸后得到白色固体F,说明A中必含有
4
NaSiO ,而且固体C与硝酸反应可得无色气体,该气体只能是 CO ,可能是CaCO 和硝酸反应,也可能是Cu2+和CO2- 结合D的分子式,可知D为甘油 ,C和D发生酯化反应得到E,结合E的分子式可知-OH和-COOH发生1:1
2 3 2 3 3
双水解得到的碱式碳酸铜与硝酸反应生成的,因此,不能确定碳酸钙和碳酸钠是否一定存在,但两者至少存在一种。
【详解】A.无色溶液B成分复杂,若B中只含有KCl,则 pH=7;若含有NaCO 或硅酸钠或两者均有,则CO2-和硅酸
2 3 3
根离子水解使溶液显碱性,pH>7,故无色溶液pH≥7,A项正确;
B.白色固体F难溶于硝酸,说明F为HSiO,B项正确;
2 3
酯化,混合物E的结构简式为 和 。
C.固体C加入硝酸得无色气体,该气体只能是CO,可能是CaCO 生成的,也可能是NaCO 与硫酸铜反应生成的碱式
2 3 2 3
碳酸铜再与硝酸反应生成的CO,因此,固体C中不一定含有CaCO ,C项错误;
2 3
D.检验Cl-可用硝酸酸化的AgNO 溶液,所以证明A含有KCl,证明Cl-即可,D项正确。
3 【详解】(1)根据分子组成的变化,即去氢加氧,A到B的反应类型为氧化反应,C中的含氧官能团为羧基。
故答案选C。
非选择题部分
(2)由上分析混合物E的结构简式,可知C和D的酯化反应得到两种有机产物,因而化学方程式分别为 +CH
2
二、非选择题(本大题共7小题,共50分)
26.以煤、天然气和生物质为原料制取有机化合物日益受到重视。E是两种含有碳碳双键的酯的混合物。相关物质的转化
关系如下(含有相同官能团的有机物通常具有相似的化学性质):
=CHCOOH +HO和 +CH=CHCOOH +HO。
2 2 2
(3)B中含有碳碳双键和醛基,两者都易被氧化,其中醛基能被弱氧化剂氧化,因而需要先检验醛基,可采用银氨溶
请回答:
液检验,注意这里需要加过量的银氨溶液以便将醛基全部氧化,然后用盐酸酸化,原因在于银氨溶液呈碱性,能和溴水反应,然后将过滤后的滤液加入溴水,观察现象。因而答案为加过量银氨溶液,加热,出现银镜,说明有醛基;用盐酸 (3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原
酸化,过滤,滤液中加入溴水,若溴水褪色,说明有碳碳双键。 因________。
27.固体化合物X由3种元素组成。某学习小组进行了如下实验: 【答案】 (1). 滴液漏斗(分液漏斗) (2). 液封,防止空气进入装置4 (3). 在装置2、3之间添加控制开关
(4). 装置4内的空气没有排尽
【解析】
【分析】
该装置制备Fe(OH) 白色沉淀的思路是在排尽空气的气氛中,先将铁屑和稀硫酸反应得到 FeSO ,再利用气体产生的气
2 4
压把FeSO 溶液压至装置4中与NaOH反应,得到Fe(OH) ,注意所需试剂也需要加热除掉溶解氧。
4 2
请回答:
【详解】(1)观察仪器1特征可知是分液漏斗或者滴液漏斗,该反应需要置于无氧环境,注意这里跟防倒吸无关,可
(1) 由现象1得出化合物X含有________元素(填元素符号)。
知装置5的作用是液封,防止空气进入装置4。
(2) 固体混合物Y的成分________(填化学式)。
(2)实验开始时,关闭K,打开K,反应一段时间后,再打开K,关闭K,发现3中溶液不能进入4中。如此操作,
2 1 2 1
(3) X的化学式________。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反应的化学方程式是
不行的原因在于仪器1产生的H 从左侧导管溢出,那么没有足够的压强不能将FeSO 溶液挤出,因而在装置2、3之间
2 4
________。
添加控制开关即可。
【答案】 (1). O (2). Cu和NaOH (3). NaCuO (4). 2NaCuO +8HCl 2NaCl+2CuCl +Cl↑+4HO
2 2 2 2 2
(3)灰绿色沉淀产生的原因是Fe(OH) 被空气氧化,因为装置4中空气没有完全排尽。
【解析】 2
29.由C、H、O三种元素组成的链状有机化合物X,只含有羟基和羧基两种官能团,且羟基数目大于羧基数目。称取
【分析】
2.04 g纯净的X,与足量金属钠充分反应,生成672 mL氢气(标准状况)。请确定摩尔质量最小的X分子中羟基、羧基数
固体混合物Y溶于水,得到固体单质为紫红色,说明是Cu,产生碱性溶液,焰色反应呈黄色说明含有钠元素,与盐酸
HCl中和,说明为NaOH(易算出为0.02mol),混合气体能使CuSO 变蓝,说明有水蒸汽。
目及该X的相对分子质量(要求写出简要推理过程)。
4
【详解】(1)CuSO 4 由白色变为蓝色,说明有水生成,根据元素守恒分析,必定含有O元素。 【答案】n(H 2 )=0.03 mol,设X中羟基和羧基的总数为m个(m≥3)则n(X)=(0.03×2)/m=0.06/m mol,M(X)=2.04m/0.06
(2)现象2获得紫色单质,说明Y含有Cu,现象3焰色反应为黄色说明有Na元素,与HCl发生中和反应说明有 =34m g·mol−1 m=4,M(X)=136 g·mol−1,含有3个羟基和1个羧基,相对分子质量为136。
NaOH,故答案填Cu和NaOH。 【解析】
(3)NaOH为0.02mol,易算出m(Na)=0.02×23g=0.46g,m(O)=m-m(Na)-m(Cu)=2.38-0.46-1.28=0.46g,N(Na):N(Cu): 【分析】
利用X和足量金属钠反应计算羟基和羧基的总数目,其关系为 2-OH~H 、H~2-COOH,进而推理出摩尔质量最小的
2 2
0.46 1.28 0.64
N(O)= : : =1:1:2,故化学式为NaCuO ,X与浓盐酸反应,根据反应现象,产物有Cl,和CuCl 蓝色
23 64 16 2 2 2 X。
V(H )
溶液,因而化学方程式为2NaCuO 2 +8HCl 2NaCl+2CuCl 2 +Cl 2 ↑+4H 2 O 【详解】n(H 2 )= 2 mol=0.03 mol,由于2-OH~H 2 、2-COOH ~H 2 ,设X中羟基和羧基的总数为m个(m>2,且为整
22.4
28.某同学设计如图装置(气密性已检查)制备Fe(OH) 白色沉淀。
2
m(X) 2.04g
0.03×2 0.06 M(X)= = =
数),则n(X)= mol= mol, n(X) 0.06mol 34m g/mol。当m=3,M(X)=102g/mol, 羟基数目
m m
m
大于羧基数目,说明含有2个羟基和1个羧基,说明X分子式有4个O,碳和氢的摩尔质量=102-16×4=38g/mol,分子式
为C HO , 2个羟基和1个羧基就占了3个H原子,可知这个分子式不合理,m=3不成立;当m=4,M(X)=136g/mol,
3 2 4
说明含有 3 个羟基和 1 个羧基,同上分析可知分子式为 C HO ,该分子式合理,例如可能的结构简式为
4 8 5
请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K 2 ,打开K 1 ,反应一段时间后,再打开K 2 ,关闭K 1 ,发现3中溶液不能进入4中。请为装置作 。故答案是:含有3个羟基和1个羧基,相对分子质量为136。
一处改进,使溶液能进入4中________。【点睛】注意当C原子数很少时,氢原子很多,就会不符碳原子4价键原则,即当C原子为n时,在烃的含氧衍生物中 ①阳极的电极反应式是________。
H原子最多为2n+2。 ②制备H 2 O 2 的总反应方程式是________。
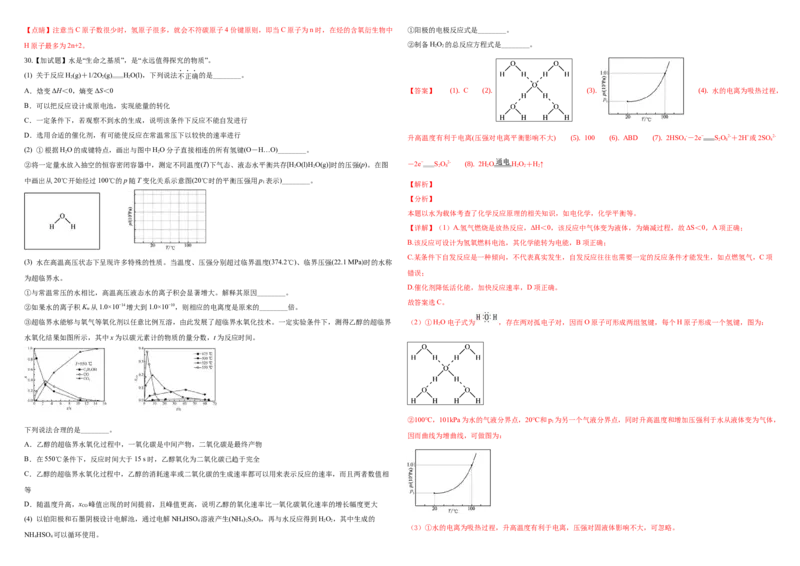
30.【加试题】水是“生命之基质”,是“永远值得探究的物质”。
(1) 关于反应H(g)+1/2O (g) HO(l),下列说法不正确的是________。
2 2 2
A.焓变ΔH<0,熵变ΔS<0 【答案】 (1). C (2). (3). (4). 水的电离为吸热过裎,
B.可以把反应设计成原电池,实现能量的转化
C.一定条件下,若观察不到水的生成,说明该条件下反应不能自发进行
D.选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行
升高温度有利于电离(压强对电离平衡影响不大) (5). 100 (6). ABD (7). 2HSO --2e− SO2-+2H+或2SO 2-
4 2 8 4
(2) ①根据HO的成键特点,画出与图中HO分子直接相连的所有氢键(O-H…O)________。
2 2
②将一定量水放入抽空的恒容密闭容器中,测定不同温度(T)下气态、液态水平衡共存[H O(l)H O(g)]时的压强(p)。在图 -2e− SO2- (8). 2HO HO+H↑
2 2 2 8 2 2 2 2
中画出从20℃开始经过100℃的p随T变化关系示意图(20℃时的平衡压强用p 表示)________。
1 【解析】
【分析】
本题以水为载体考查了化学反应原理的相关知识,如电化学,化学平衡等。
【详解】(1)A.氢气燃烧是放热反应,ΔH<0,该反应中气体变为液体,为熵减过程,故ΔS<0,A项正确;
B.该反应可设计为氢氧燃料电池,其化学能转为电能,B项正确;
C.某条件下自发反应是一种倾向,不代表真实发生,自发反应往往也需要一定的反应条件才能发生,如点燃氢气,C项
(3) 水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2℃)、临界压强(22.1 MPa)时的水称
错误;
为超临界水。
D.催化剂降低活化能,加快反应速率,D项正确。
①与常温常压的水相比,高温高压液态水的离子积会显著增大。解释其原因________。
故答案选C。
②如果水的离子积K 从1.0×10−14增大到1.0×10−10,则相应的电离度是原来的________倍。
w
③超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条件下,测得乙醇的超临界 (2)①HO电子式为 ,存在两对孤电子对,因而O原子可形成两组氢键,每个H原子形成一个氢键,图为:
2
水氧化结果如图所示,其中x为以碳元素计的物质的量分数,t为反应时间。
②100℃,101kPa为水的气液分界点,20℃和p 为另一个气液分界点,同时升高温度和增加压强利于水从液体变为气体,
1
下列说法合理的是________。
因而曲线为增曲线,可做图为:
A.乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物
B.在550℃条件下,反应时间大于15 s时,乙醇氧化为二氧化碳已趋于完全
C.乙醇的超临界水氧化过程中,乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应的速率,而且两者数值相
等
D.随温度升高,x 峰值出现的时间提前,且峰值更高,说明乙醇的氧化速率比一氧化碳氧化速率的增长幅度更大
CO
(4) 以铂阳极和石墨阴极设计电解池,通过电解NH HSO 溶液产生(NH )SO,再与水反应得到HO,其中生成的
4 4 4 2 2 8 2 2
(3)①水的电离为吸热过裎,升高温度有利于电离,压强对固液体影响不大,可忽略。
NH HSO 可以循环使用。
4 4②c(H+)=❑√K ,当K =1.0×10-14,c(H+)=10-7mol/L,当K =1.0×10-10,c(H+)=10-5mol/L,易知后者是前者的100倍,所以
w w 1 w 2
相应的电离度是原来的100倍。
③A.观察左侧x-t图像可知,CO先增加后减少,CO 一直在增加,所以CO为中间产物,CO 为最终产物,A项正确;
2 2
B.观察左侧x-t图像,乙醇减少为0和CO最终减少为0的时间一致,而右图x -t图像中550℃,CO在15s减为0,说明
CO
乙醇氧化为CO 趋于完全,B项正确;
2
②为了指示蒸氨操作完成,在一定量硫酸溶液中加指示剂。请给出并说明蒸氨可以停止时的现象________。
C.乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应的速率,但两者数值不相等,比值为化学计量数之比,等
(3) 溶液F经盐酸酸化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。取少量产品溶于水后发现溶液呈碱性。
于1:2,C项错误;
①含有的杂质是________。
D.随着温度的升高,乙醇的氧化速率和一氧化碳氧化速率均增大,但CO是中间产物,为乙醇不完全氧化的结果,CO
②从操作上分析引入杂质的原因是________。
峰值出现的时间提前,且峰值更高,说明乙醇氧化为CO和CO 速率必须加快,且大于CO的氧化速率,D项正确。
2 (4) 有同学采用盐酸代替步骤Ⅱ中的NH Cl溶液处理固体B,然后除杂,制备MgCl 溶液。已知金属离子形成氢氧化物
4 2
故答案选ABD。
沉淀的pH范围:
(4)①电解池使用惰性电极,阳极本身不参与反应,阳极吸引HSO -(或SO 2-)离子,并放电生成SO2-,因而电极反
4 4 2 8
pH
应式为2HSO --2e−=S O2-+2H+或2SO 2--2e−=S O2- 。 金属离子
4 2 8 4 2 8
开始沉淀 完全沉淀
②通过电解NH HSO 溶液产生(NH )SO 和H。由题中信息可知,生成的NH HSO 可以循环使用,说明(NH )SO 与水
4 4 4 2 2 8 2 4 4 4 2 2 8
Al3+ 3.0 4.7
反应除了生成HO,还有NH HSO 生成,因而总反应中只有水作反应物,产物为HO 和H,故总反应方程式为2HO
2 2 4 4 2 2 2 2
Fe3+ 1.1 2.8
HO+H↑。
2 2 2 Ca2+ 11.3 -
31.某兴趣小组在定量分析了镁渣[含有MgCO 、Mg(OH) 、CaCO 、Al O、Fe O 和SiO]中Mg含量的基础上,按如下
3 2 3 2 3 2 3 2 Mg2+ 8.4 10.9
流程制备六水合氯化镁(MgCl ·6H O)。
2 2
请给出合理的操作排序(从下列操作中选取,按先后次序列出字母,操作可重复使用):固体B→a→( )→( )→
( )→( )→( )→( )→MgCl 溶液→产品。
2
a.用盐酸溶解 b.调pH=3.0 c.调pH=5.0 d.调pH=8.5
e.调pH=11.0 f.过滤 g.洗涤
相关信息如下:
【答案】 (1). ABD (2). a→d→f→c (3). 甲基橙,颜色由红色变橙色 (4). 碱式氯化镁(氢氧化镁) (5).
①700℃只发生MgCO 和Mg(OH) 的分解反应。
3 2
过度蒸发导致氯化镁水解 (6). c (7). f (8). e (9). f (10). g (11). a
②NH Cl溶液仅与体系中的MgO反应,且反应程度不大。
4
【解析】
③“蒸氨”是将氨从固液混合物中蒸出来,且须控制合适的蒸出量。
【详解】(1)A.煅烧固体样品需用坩埚,烧杯和锥形瓶用来加热液体,A项正确;
请回答:
B.氯化铵水解方程式为NH Cl+H O⇌NH ·H O+HCl,氧化镁和HCl反应,蒸氨即一水合氨分解,平衡向右移动,HCl浓
4 2 3 2
(1) 下列说法正确的是________。
度变大,促进了氧化镁的溶解,B项正确;
A.步骤Ⅰ,煅烧样品的容器可以用坩埚,不能用烧杯和锥形瓶
C.根据信息②NH Cl溶液仅与体系中的MgO反应,且反应程度不大,不能先过滤,否则氧化镁损耗很大,C项错误;
4
B.步骤Ⅲ,蒸氨促进平衡正向移动,提高MgO的溶解量
D.固液分离操作均可采用常压过滤,使用减压过滤加快过滤速度,也可行,D项正确。
C.步骤Ⅲ,可以将固液混合物C先过滤,再蒸氨
故答案选ABD。
D.步骤Ⅳ,固液分离操作可采用常压过滤,也可采用减压过滤
(2)①先选发生装置为a,然后连接回流装置d,生成的氨气有水蒸气,需要干燥,然后连接干燥管f,氨气是碱性气
(2) 步骤Ⅲ,需要搭建合适的装置,实现蒸氨、吸收和指示于一体(用硫酸溶液吸收氨气)。
体,需要用酸吸收,最后连接c。故答案填a→d→f→c。
①选择必须的仪器,并按连接顺序排列(填写代表仪器的字母,不考虑夹持和橡皮管连接):热源→________。
②硫酸和氨气恰好完全反应生成硫酸铵((NH )SO ),硫酸铵显酸性,因而选择在酸性范围内变色的指示剂:甲基橙,
4 2 4其颜色变化是红色变为橙色。
(3)溶液F经盐酸酸化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。①溶液仍呈碱性,注意不可能是氨气的影响, +HCl (4). (5). CHCHOH CHCOOH
3 2 3
由于氯化镁水解使溶液呈酸性,故溶液的碱性是由杂质引起的。考虑到氯化镁易水解,所以含有的杂质可能是
Mg(OH)Cl或者Mg(OH) 。
2
②升高温度会促进水解的进行,因而必然是蒸发阶段导致,即过度蒸发导致氯化镁水解。
(4)根据各离子完全沉淀的pH值,加酸后溶液呈酸性,可逐步提高pH,同时以沉淀形式除掉不同离子,因而先将pH
调至5,除掉Al3+和Fe3+,然后过滤其沉淀,然后将pH调至11.0使得Mg2+变为Mg(OH) 2 沉淀,过滤并洗涤,得到纯净的 CH 3 COOCH 2 CH 3 CH 3 COCH 2 COOCH 2 CH 3
Mg(OH) 沉淀,然后加入盐酸得到氯化镁溶液。故答案依次填cfefga。
2
32.某研究小组拟合成除草剂苯达松和染料中间体X。
【解析】
【分析】
以A和F为原料制备苯达松,观察苯达松结构简式,易知 A中有苯环,便可推出A为 ,根据A到B的反应
已知信息:① +RCOOR′
条件(HNO 和 HSO )可知该反应为硝化反应,继续观察苯达松可知其苯环上为邻位二取代侧链,因而 B 为
3 2 4
②RCHCOOR′+R′′COOR′′′
2
,继续观察苯达松侧链有羰基和亚氨基,说明B到C的两步反应为甲基被氧化为羧基和硝基被还原为氨基,
(1)下列说法正确的是________。
A.化合物B到C的转变涉及到取代反应
B.化合物C具有两性
C.试剂D可以是甲醇
D.苯达松的分子式是C H NOS C 为 ,根据反应条件易知 C 和 D 反应为酯化反应,然后结合 E 的分子式可推出 D 是甲醇,E 为
10 10 2 3
(2)化合物F的结构简式是________。
(3)写出E+G→H的化学方程式________。
(4)写出C H NO 同时符合下列条件的同分异构体的结构简式________。
6 13 2
①分子中有一个六元环,且成环原子中最多含2个非碳原子; ,最后结合苯达松右侧碳链部分和F的分子式可知氨基接在碳链中的2号碳上,F为 ,从
②1H−NMR谱和IR谱检测表明分子中有4种化学环境不同的氢原子。有N-O键,没有过氧键(-O-O-)。
(5)设计以CHCHOH和 原料制备X( )的合成路线(无机试剂任选,合成中须用到上述
3 2
而G为 。
①②两条已知信息,用流程图表示)________。
【详解】(1)A.B到C的两步反应分别是甲基的氧化反应和硝基的还原反应,不涉及取代反应,A项错误;
【答案】 (1). BC (2). (CH)CHNH (3). +(CH)CHNHSO Cl
3 2 2 3 2 2 B.C为邻氨基苯甲酸,其官能团为氨基和羧基,氨基具有碱性,羧基具有酸性,因而C有两性,B项正确;
C.C和D发生酯化反应生成E,结合C和E的分子式,易推出D为甲醇,C项正确;
D.苯达松的分子式是C H NOS,D项错误。
10 12 2 3
故答案选BC。(2)结合苯达松右侧杂环上的碳链可知,氨基接在碳链中2号碳的位置,F的结构简式为(CH)CHNH 。
3 2 2
(3)G的氯原子和E氨基上的氢原子偶联脱去HCl生成H,因而化学方程式为 +(CH)CHNHSO Cl
3 2 2
+HCl。
(4)根据分子式C H NO 算出不饱和度为1,结合信息,说明存在一个六元环,无不饱和键(注意无硝基)。结合环
6 13 2
内最多含有两个非碳原子,先分析六元环:①六元环全为碳原子;②六元环中含有一个O;③六元环中含有一个N;④六
元环中含有一个N和一个O;若六元环中含有2个O,这样不存在N-O键,不符合条件。同时核磁共振氢谱显示有4中
氢原子,该分子具有相当的对称性,可推知环上最少两种氢,侧链两种氢,这种分配比较合理。最后注意有N-O键,无
O-O键。那么基于上述四种情况分析可得出4种同分异构体,结构简式分别为 、 、
和 。
(5)基于逆合成分析法,观察信息①,X可从肽键分拆得 和CHCOCH COOR,那么关键在于合成
3 2
CHCOCH COOR,结合信息②可知利用乙酸某酯CHCOOR做原料合成制得。另一个原料是乙醇,其合成乙酸某酯,
3 2 3
先将乙醇氧化为乙酸,然后乙酸与乙醇反应,可得乙酸乙酯。以上分析便可将整个合成路线设计为:CHCHOH
3 2
CHCOOH CHCOOCH CH CHCOCH COOCH CH
3 3 2 3 3 2 2 3 。