文档内容
福建省 2023 年高考化学试题
1. 唐代陆羽《茶经·三之造》中记载茶叶制作过程:“晴采之,蒸之,捣之,拍之,焙之,穿之,封之,茶
之干矣”。以下操作中最不可能引起化学变化的是
A. 蒸 B. 捣 C. 焙 D. 封
2. 抗癌药物 的结构如图。关于该药物的说法错误的是
A. 能发生水解反应 B. 含有2个手性碳原子
C. 能使 的 溶液褪色 D. 碳原子杂化方式有 和
第3题暂未征集到
3. 某含锰着色剂的化学式为 ,Y、X、Q、Z为原子序数依次增大的短周期元素,其中
具有正四面体空间结构, 结构如图所示。下列说法正确的是
A. 键角: B. 简单氢化物沸点:
的
C. 第一电离能: D. 最高价氧化物对应 水化物酸性:
4. 我国新一代载人飞船使用的绿色推进剂硝酸羟胺 在催化剂作用下可完全分解为
和 。 为阿伏加德罗常数的值,下列说法正确的是
A. 含有的质子数为
B. 固态硝酸羟胺含有的离子数为
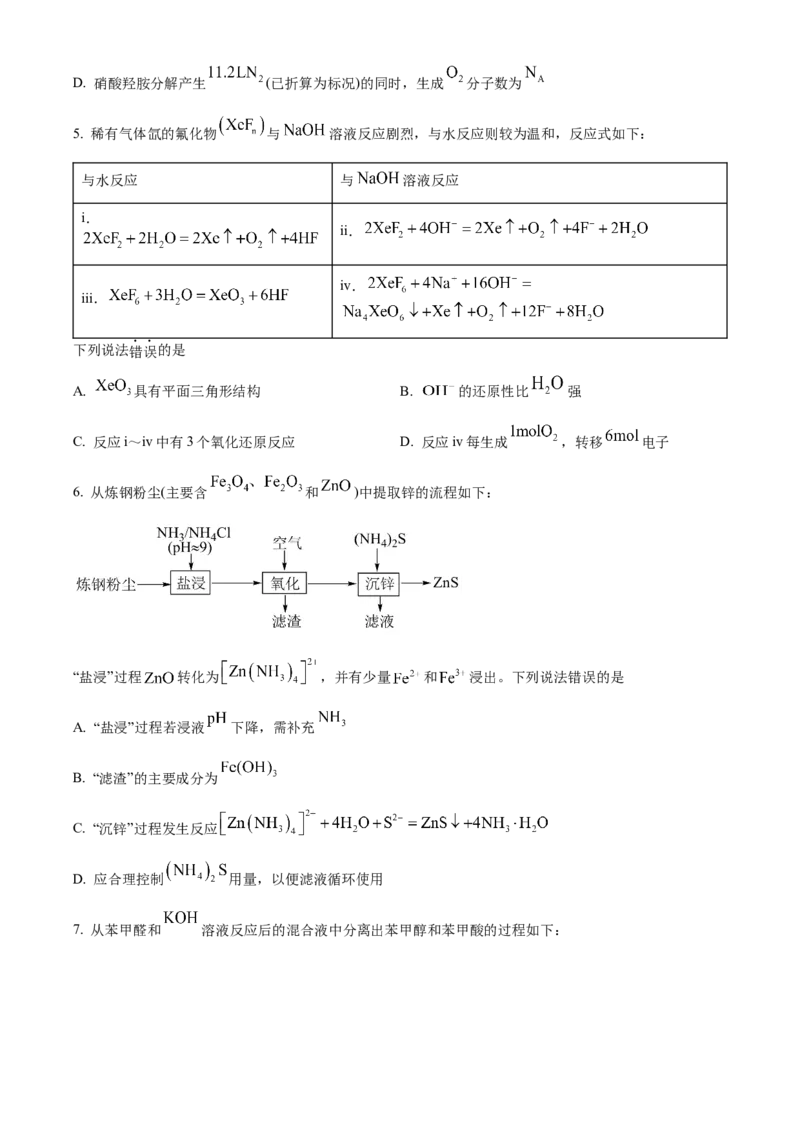
C. 硝酸羟胺含有的 键数为D. 硝酸羟胺分解产生 (已折算为标况)的同时,生成 分子数为
5. 稀有气体氙的氟化物 与 溶液反应剧烈,与水反应则较为温和,反应式如下:
与水反应 与 溶液反应
i.
ii.
iv.
iii.
下列说法错误的是
A. 具有平面三角形结构 B. 的还原性比 强
C. 反应i~iv中有3个氧化还原反应 D. 反应iv每生成 ,转移 电子
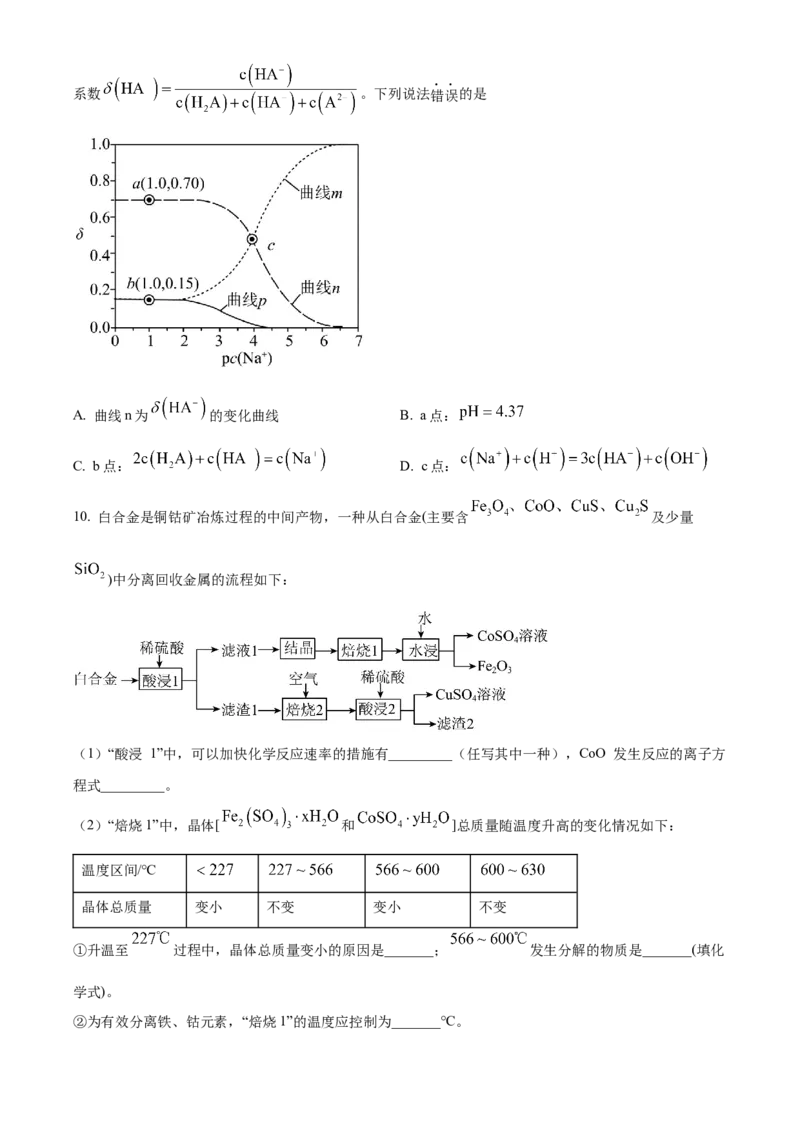
6. 从炼钢粉尘(主要含 和 )中提取锌的流程如下:
“盐浸”过程 转化为 ,并有少量 和 浸出。下列说法错误的是
A. “盐浸”过程若浸液 下降,需补充
B. “滤渣”的主要成分为
C. “沉锌”过程发生反应
D. 应合理控制 用量,以便滤液循环使用
7. 从苯甲醛和 溶液反应后的混合液中分离出苯甲醇和苯甲酸的过程如下:已知甲基叔丁基醚的密度为 。下列说法错误的是
A. “萃取”过程需振荡、放气、静置分层
B. “有机层”从分液漏斗上口倒出
C. “操作X”为蒸馏,“试剂Y”可选用盐酸
D. “洗涤”苯甲酸,用乙醇的效果比用蒸馏水好
8. 一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由 和
形成熔点为 的共熔物),其中氯铝酸根 起到结合或释放 的作用。电池总
反应: 。下列说法错误的是
A. 含 个 键
B. 中同时连接2个 原子 的原子有 个
C. 充电时,再生 单质至少转移 电子
D. 放电时间越长,负极附近熔融盐中n值小的 浓度越高
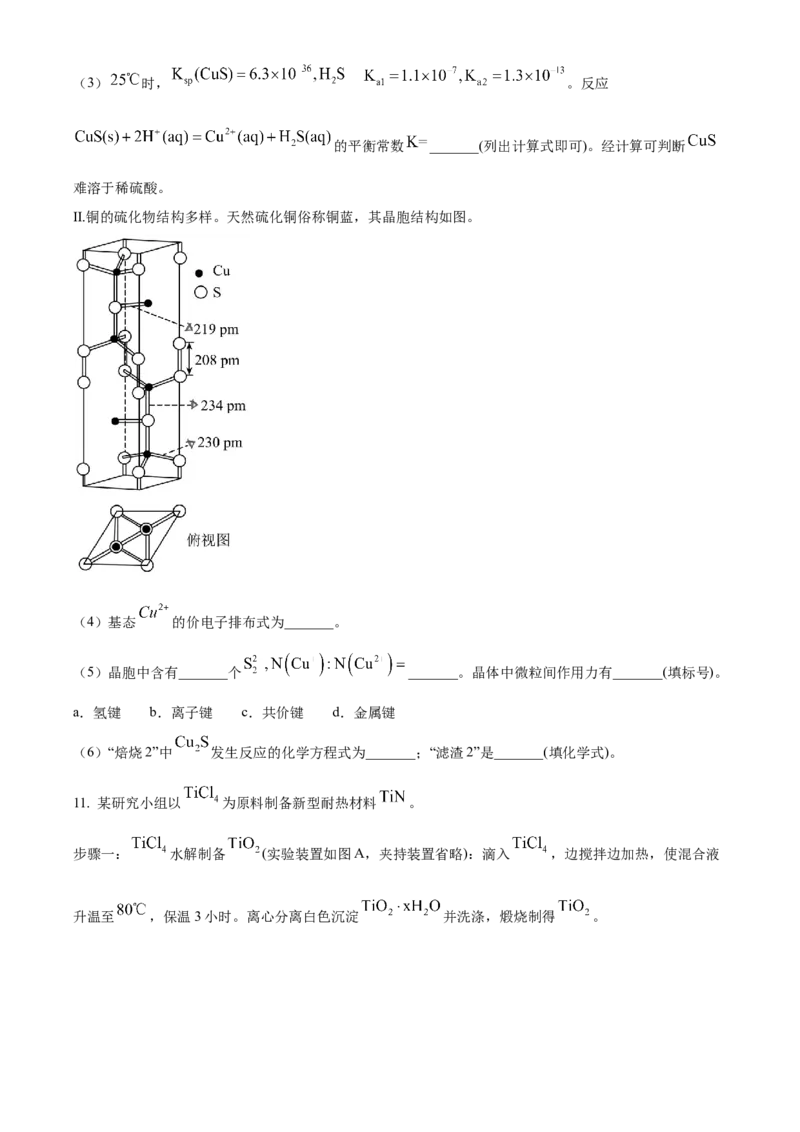
9. 时,某二元酸 的 、 。 溶液稀释过程中
与 的关系如图所示。已知 的分布系数 。下列说法错误的是
A. 曲线n为 的变化曲线 B. a点:
C. b点: D. c点:
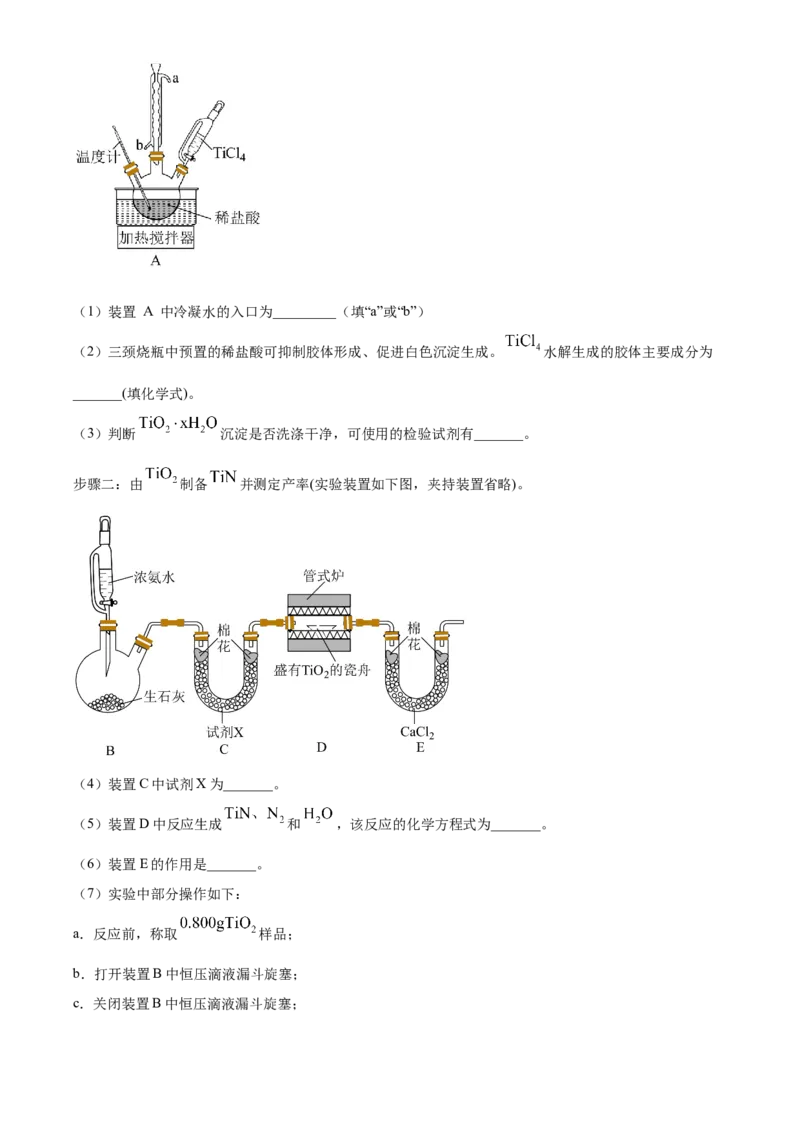
10. 白合金是铜钴矿冶炼过程的中间产物,一种从白合金(主要含 及少量
)中分离回收金属的流程如下:
(1)“酸浸 1”中,可以加快化学反应速率的措施有_________(任写其中一种),CoO 发生反应的离子方
程式_________。
(2)“焙烧1”中,晶体[ 和 ]总质量随温度升高的变化情况如下:
温度区间/℃
晶体总质量 变小 不变 变小 不变
①升温至 过程中,晶体总质量变小的原因是_______; 发生分解的物质是_______(填化
学式)。
②为有效分离铁、钴元素,“焙烧1”的温度应控制为_______℃。(3) 时, 的。反应
的平衡常数 _______(列出计算式即可)。经计算可判断
难溶于稀硫酸。
II.铜的硫化物结构多样。天然硫化铜俗称铜蓝,其晶胞结构如图。
(4)基态 的价电子排布式为_______。
(5)晶胞中含有_______个 _______。晶体中微粒间作用力有_______(填标号)。
a.氢键 b.离子键 c.共价键 d.金属键
(6)“焙烧2”中 发生反应的化学方程式为_______;“滤渣2”是_______(填化学式)。
11. 某研究小组以 为原料制备新型耐热材料 。
步骤一: 水解制备 (实验装置如图A,夹持装置省略):滴入 ,边搅拌边加热,使混合液
升温至 ,保温3小时。离心分离白色沉淀 并洗涤,煅烧制得 。(1)装置 A 中冷凝水的入口为_________(填“a”或“b”)
(2)三颈烧瓶中预置的稀盐酸可抑制胶体形成、促进白色沉淀生成。 水解生成的胶体主要成分为
_______(填化学式)。
(3)判断 沉淀是否洗涤干净,可使用的检验试剂有_______。
步骤二:由 制备 并测定产率(实验装置如下图,夹持装置省略)。
(4)装置C中试剂X为_______。
(5)装置D中反应生成 和 ,该反应的化学方程式为_______。
(6)装置E的作用是_______。
(7)实验中部分操作如下:
a.反应前,称取 样品;
b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;d.打开管式炉加热开关,加热至 左右;
e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为 。
①正确的操作顺序为:a→_______→f(填标号)。
② 的产率为_______。
12. 探究甲醇对丙烷制丙烯的影响。丙烷制烯烃过程主要发生的反应有
ⅰ.
ⅱ.
ⅲ.
已知: 为用气体分压表示的平衡常数,分压=物质的量分数×总压。在 下,丙烷单独进料
时,平衡体系中各组分的体积分数 见下表。
物质 丙烯 乙烯 甲烷 丙烷 氢气
体积分数(%) 21 23.7 55.2 0.1 0
(1)比较反应自发进行(∆G=∆H-T∆S<0)的最低温度,反应 ⅰ_____反应 ⅱ(填“>”或“<”)。
(2)①在该温度下,Kp 远大于 Kp ,但φ(C H)和φ(C H)相差不大,说明反应 ⅲ 的正向进行有利于
2 1 3 6 2 4
反应 ⅰ 的__________反应和反应 ⅱ 的_________反应(填“正向”或“逆向”)。
②从初始投料到达到平衡,反应 ⅰ、ⅱ、ⅲ 的丙烷消耗的平均速率从大到小的顺序为:__________。
③平衡体系中检测不到 ,可认为存在反应: ,下列相关说法正
的
确 是_______(填标号)。
a.
b.
c.使用催化剂,可提高丙烯的平衡产率d.平衡后再通入少量丙烷,可提高丙烯的体积分数
④由表中数据推算:丙烯选择性 _______(列出计算式)。
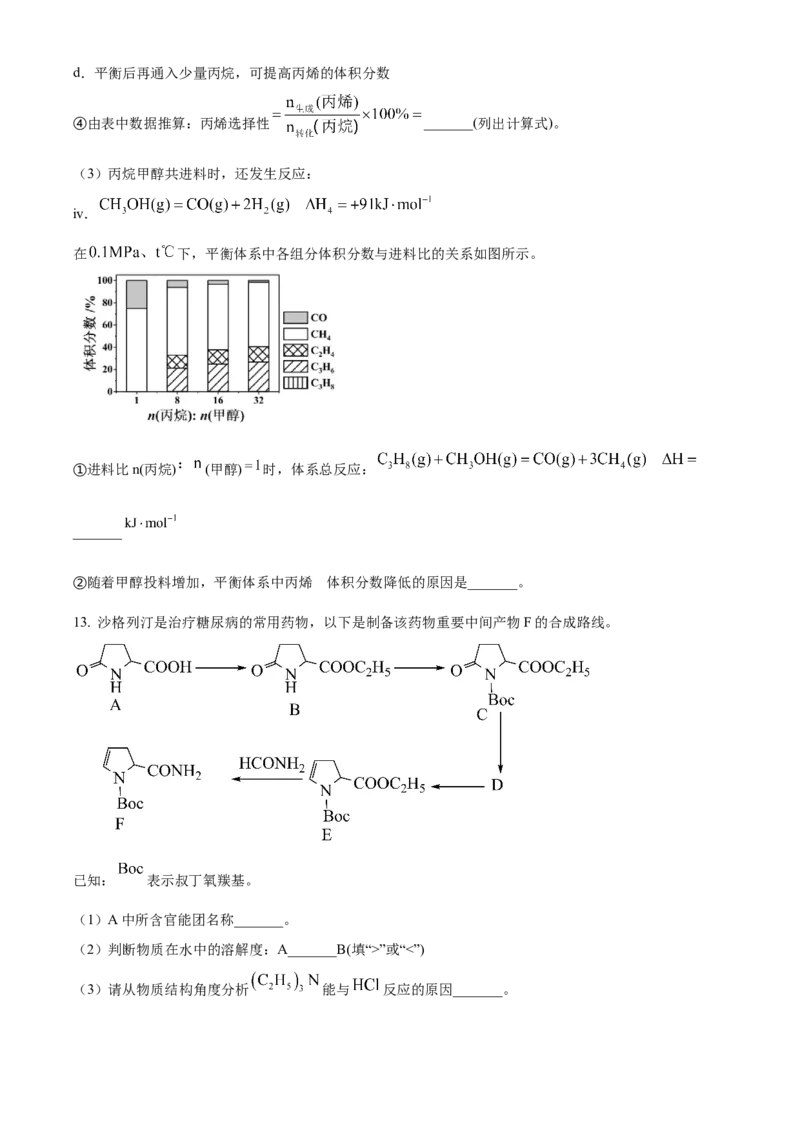
(3)丙烷甲醇共进料时,还发生反应:
ⅳ.
在 下,平衡体系中各组分体积分数与进料比的关系如图所示。
①进料比n(丙烷) (甲醇) 时,体系总反应:
_______
的
②随着甲醇投料增加,平衡体系中丙烯 体积分数降低的原因是_______。
13. 沙格列汀是治疗糖尿病的常用药物,以下是制备该药物重要中间产物F的合成路线。
已知: 表示叔丁氧羰基。
(1)A中所含官能团名称_______。
(2)判断物质在水中的溶解度:A_______B(填“>”或“<”)
(3)请从物质结构角度分析 能与 反应的原因_______。(4) 的反应类型_______。
(5)写出D的结构简式_______。
(6)写出 的化学反应方程式_______。
(7)A的其中一种同分异构体是丁二酸分子内脱水后的分子上一个H被取代后的烃的衍生物,核磁共振
氢谱图的比例为 ,写出该同分异构体的结构简式_______。(只写一种)