文档内容
2024 年江西省新高考化学试卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项符合题目要求。
1. 景德镇青花瓷素有“国瓷”的美誉。是以黏土为原料,用含钴、铁的颜料着色,上釉后一次性高温烧制而
成的青蓝色彩瓷。下列关于青花瓷说法正确的是
A. 青蓝色是由于生成了单质钴 B. 表面的釉属于有机高分子膜
C. 主要成分为铝硅酸盐 D. 铁元素的存在形式只有Fe O
2 3
【答案】C
【解析】
【详解】A.青花瓷上的蓝色花纹是由于使用了含有氧化钴的“青料”绘制而成,与单质钴无直接关系,A
错误;
B.釉是一种覆盖在陶瓷表面的物质,通常由无机物质组成,如硅酸盐、氧化物等,B错误;
C.青花瓷是一种釉面瓷,其材质属于无机非金属材料,主要成分为铝硅酸盐,C正确;
D.青花瓷呈现青蓝色,不能确定铁元素的具体存在形式,Fe O ,D错误;
2 3呈红色
故选C。
2. 科学家发现宇宙中存在100多种星际分子。下列关于星际分子说法正确的是
A. 分子的极性:SiH>NH B. 键的极性:H—Cl>H—H
4 3
C. 键角:HO>CH D. 分子中三键的键长:HC≡N>HC≡CH
2 4
【答案】B
【解析】
【详解】A.SiH 中四条Si—H键完全相同,均为极性键,但由于SiH 为正四面体结构,故为非极性分子,
4 4
NH 为三角锥形结构,3条N—H键的极性不能抵消,故为极性分子,故A错误;
3
B.H—H为非极性键,H—Cl为极性键,则键的极性:H—Cl>H—H,故B正确;
C.水分子为V形结构,含两对孤对电子,甲烷为正四面体结构,不含孤对电子,孤对电子对成键电子对
斥力较大,则键角:HO<CH,故C错误;
2 4
D.原子半径C>N,分子中三键的键长:HC≡N<HC≡CH,故D错误;
故选B。
3. “稀土之父”徐光宪先生提出了稀土串级萃取理论,其基本操作是利用有机络合剂把稀土离子从水相富
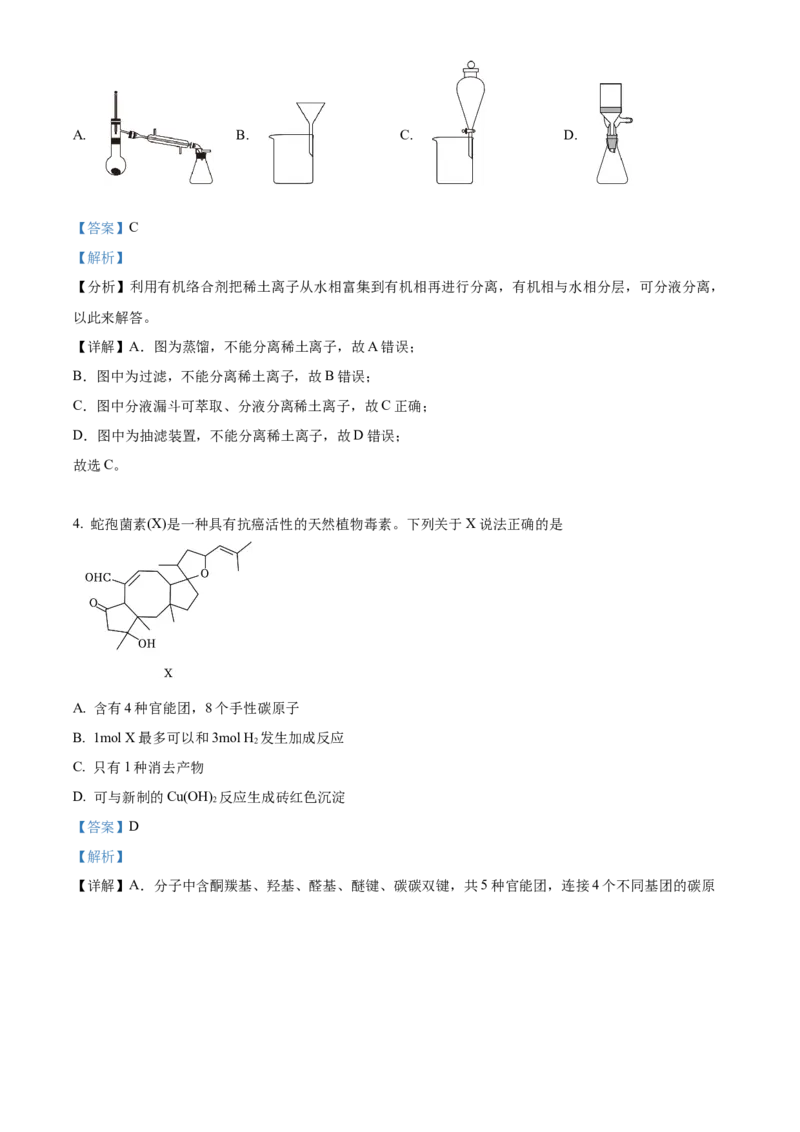
集到有机相再进行分离。分离时可用的玻璃装置是A. B. C. D.
【答案】C
【解析】
【分析】利用有机络合剂把稀土离子从水相富集到有机相再进行分离,有机相与水相分层,可分液分离,
以此来解答。
【详解】A.图为蒸馏,不能分离稀土离子,故A错误;
B.图中为过滤,不能分离稀土离子,故B错误;
C.图中分液漏斗可萃取、分液分离稀土离子,故C正确;
D.图中为抽滤装置,不能分离稀土离子,故D错误;
故选C。
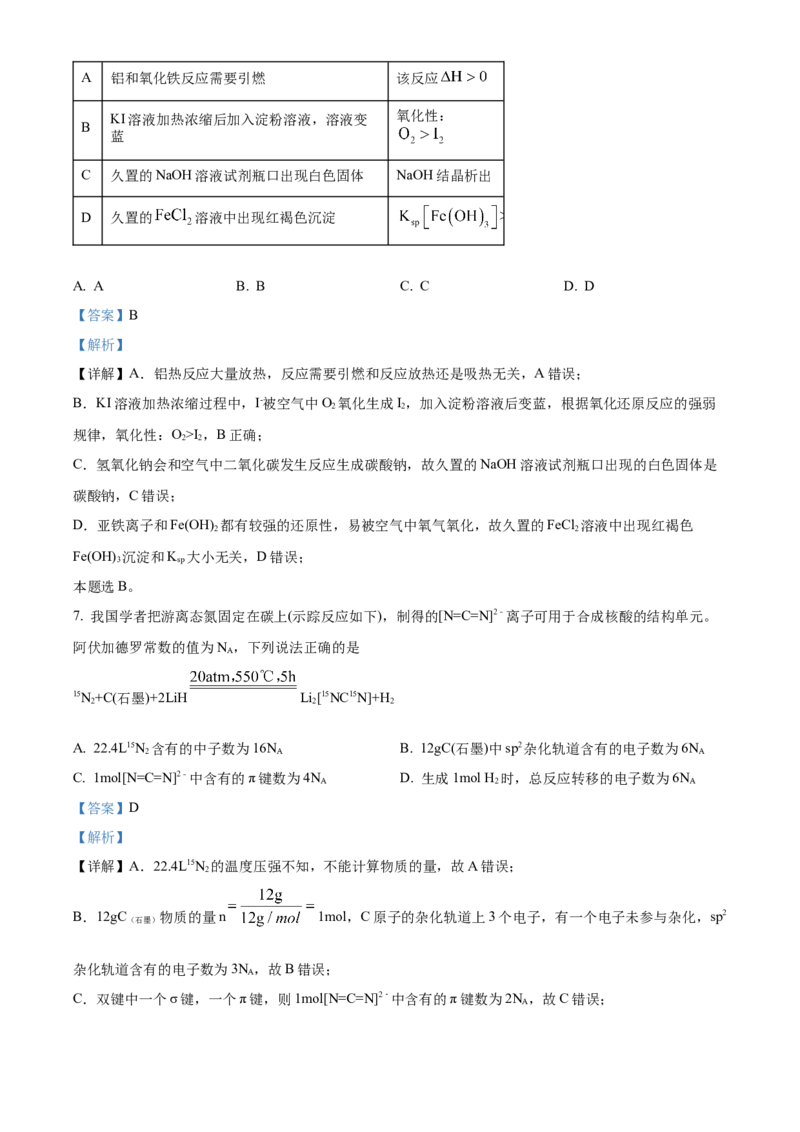
4. 蛇孢菌素(X)是一种具有抗癌活性的天然植物毒素。下列关于X说法正确的是
A. 含有4种官能团,8个手性碳原子
B. 1mol X最多可以和3mol H 发生加成反应
2
C. 只有1种消去产物
D. 可与新制的Cu(OH) 反应生成砖红色沉淀
2
【答案】D
【解析】
【详解】A.分子中含酮羰基、羟基、醛基、醚键、碳碳双键,共5种官能团,连接4个不同基团的碳原子为手性碳原子,分子中含8个手性碳原子, 故A错误;
B.酮羰基、醛基、碳碳双键均与氢气发生加成反应,则1mol X最多可以和4mol H 发生加成反应,故B
2
错误;
C.与羟基相连碳的邻位碳原子上有H原子可发生消去反应,与左侧甲基、亚甲基上H原子可发生消去反
应,则有2种消去产物,故C错误;
D.分子中含醛基,可与新制的Cu(OH) 反应生成砖红色沉淀,故D正确;
2
故选D。
5. 某新材料阳离子为W X YZM+。W、X、Y、Z和M是原子序数依次增大的前20号主族元素,前四周
36 18 2 6
期中M原子半径最大,X、Y、Z同周期。XW 分子含有大π键( ),XZ 分子呈直线形。下列说法正确
6 6 2
的是
A. WYZ 是强酸 B. MZW是强碱 C. MZ 是共价化合物 D. XW 是离子化合物
2 2 2 2 2
【答案】B
【解析】
【分析】W、X、Y、Z和M是原子序数依次增大的前20号主族元素,前四周期中M原子半径最大,M为
K元素,X、Y、Z同周期,XW 分子含有大π键( ),说明XW 是苯,X为C元素,W为H元素,XZ
6 6 6 6 2
分子呈直线形,为CO,Z为O元素,Y为N元素,以此解答。
2
【详解】A.由分析可知,W为H元素、Y为N元素、Z为O元素,HNO 是弱酸,不是强酸,A错误;
2
B.由分析可知,M为K元素、Z为O元素,W为H元素,KOH是强碱,B正确;
C.由分析可知,M为K元素、Z为O元素,KO 中存在K+和 ,属于离子化合物,C错误;
2 2
D.由分析可知,X为C元素、W为H元素,C H 为乙炔的分子式,乙炔中没有离子键,属于共价化合物,
2 2
D错误;
故选B。
6. 由下列实验事实得出的结论正确的是
实验事实 结论A 铝和氧化铁反应需要引燃 该反应
KI溶液加热浓缩后加入淀粉溶液,溶液变 氧化性:
B
蓝
C 久置的NaOH溶液试剂瓶口出现白色固体 NaOH结晶析出
D 久置的 溶液中出现红褐色沉淀
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.铝热反应大量放热,反应需要引燃和反应放热还是吸热无关,A错误;
B.KI溶液加热浓缩过程中,I-被空气中O 氧化生成I,加入淀粉溶液后变蓝,根据氧化还原反应的强弱
2 2
规律,氧化性:O>I ,B正确;
2 2
C.氢氧化钠会和空气中二氧化碳发生反应生成碳酸钠,故久置的NaOH溶液试剂瓶口出现的白色固体是
碳酸钠,C错误;
D.亚铁离子和Fe(OH) 都有较强的还原性,易被空气中氧气氧化,故久置的FeCl 溶液中出现红褐色
2 2
Fe(OH) 沉淀和K 大小无关,D错误;
3 sp
本题选B。
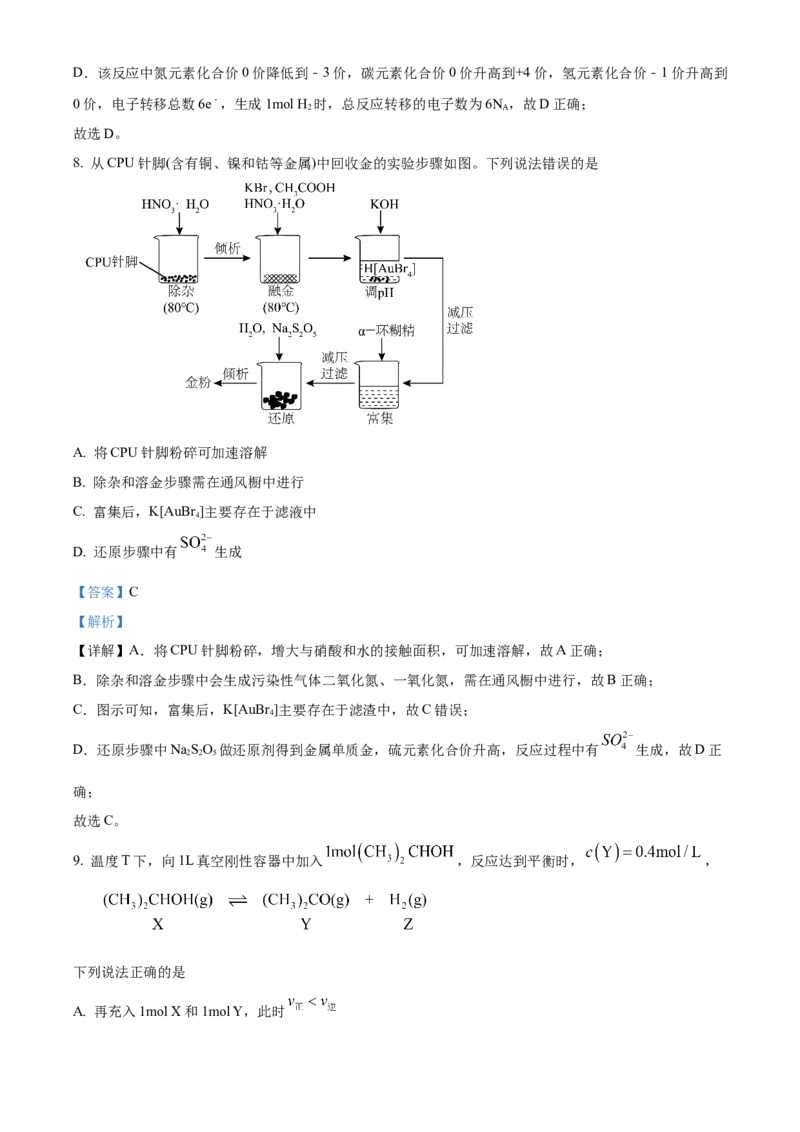
7. 我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2﹣离子可用于合成核酸的结构单元。
阿伏加德罗常数的值为N ,下列说法正确的是
A
15N+C(石墨)+2LiH Li[15NC15N]+H
2 2 2
A. 22.4L15N 含有的中子数为16N B. 12gC(石墨)中sp2杂化轨道含有的电子数为6N
2 A A
C. 1mol[N=C=N]2﹣中含有的π键数为4N D. 生成1mol H 时,总反应转移的电子数为6N
A 2 A
【答案】D
【解析】
【详解】A.22.4L15N 的温度压强不知,不能计算物质的量,故A错误;
2
B.12gC 物质的量n 1mol,C原子的杂化轨道上3个电子,有一个电子未参与杂化,sp2
(石墨)
杂化轨道含有的电子数为3N ,故B错误;
A
C.双键中一个σ键,一个π键,则1mol[N=C=N]2﹣中含有的π键数为2N ,故C错误;
AD.该反应中氮元素化合价0价降低到﹣3价,碳元素化合价0价升高到+4价,氢元素化合价﹣1价升高到
0价,电子转移总数6e﹣,生成1mol H 时,总反应转移的电子数为6N ,故D正确;
2 A
故选D。
8. 从CPU针脚(含有铜、镍和钴等金属)中回收金的实验步骤如图。下列说法错误的是
A. 将CPU针脚粉碎可加速溶解
B. 除杂和溶金步骤需在通风橱中进行
C. 富集后,K[AuBr ]主要存在于滤液中
4
D. 还原步骤中有 生成
【答案】C
【解析】
【详解】A.将CPU针脚粉碎,增大与硝酸和水的接触面积,可加速溶解,故A正确;
B.除杂和溶金步骤中会生成污染性气体二氧化氮、一氧化氮,需在通风橱中进行,故B正确;
C.图示可知,富集后,K[AuBr ]主要存在于滤渣中,故C错误;
4
D.还原步骤中NaSO 做还原剂得到金属单质金,硫元素化合价升高,反应过程中有 生成,故D正
2 2 5
确;
故选C。
9. 温度T下,向1L真空刚性容器中加入 ,反应达到平衡时, ,
下列说法正确的是
A. 再充入1mol X和1mol Y,此时B. 再充入1mol X,平衡时
C. 再充入 ,平衡向右移动
D. 若温度升高,X的转化率增加,则上述反应
【答案】A
【解析】
【分析】由题意可知,平衡时Y的浓度为0.4mol/L,由方程式可知,X的浓度为1mol/L—0.4mol/L=0.6
mol/L,Z的浓度为0.4mol/L,则反应的平衡常数K= ≈0.27。
【详解】A.向真空刚性容器中再充入1mol X和1mol Y时,反应的浓度熵Q= =0.35>K,则反
c
应向逆反应方向进行,正反应速率小于逆反应速率,故A正确;
B.向真空刚性容器中再充入1mol X相当于增大压强,该反应是气体体积增大的反应,增大压强,平衡向
逆反应方向移动,则平衡时,Y的浓度小于0.8mol/L,故B错误;
C.向真空刚性容器中再充入不参与反应的1mol氮气,反应体系中各物质浓度不变,平衡不移动,故C错
误;
D.温度升高,X的转化率增加,说明平衡向正反应方向移动,该反应为焓变大于0的吸热反应,故D错
误;
故选A。
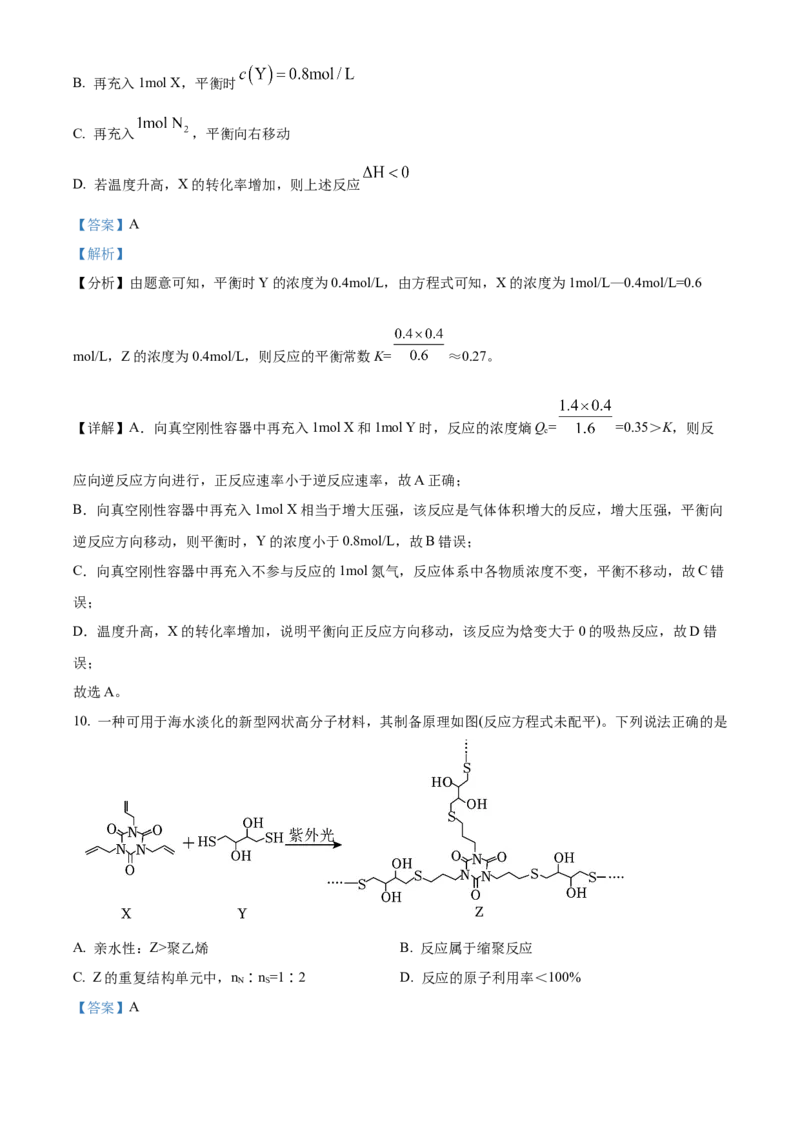
10. 一种可用于海水淡化的新型网状高分子材料,其制备原理如图(反应方程式未配平)。下列说法正确的是
A. 亲水性:Z>聚乙烯 B. 反应属于缩聚反应
C. Z的重复结构单元中,n ∶n =1∶2 D. 反应的原子利用率<100%
N S
【答案】A【解析】
【详解】A.Z含多个羟基,易与水分子形成氢键,聚乙烯不溶于水,则亲水性:Z>聚乙烯,故A正确;
B.X中碳碳双键转化为单键,且生成高分子,该反应为加聚反应,故B错误;
C.X中碳碳双键与H-S键发生加成,X中含3个氮原子,且3个碳碳双键发生加成反应,则Z的重复结构
单元中也含有3个硫原子,可知Z的重复结构单元中,n ∶n =1∶1,故C错误;
N S
D.该反应中生成物只有一种,为化合反应,反应的原子利用率为100%,故D错误;
故选:A。
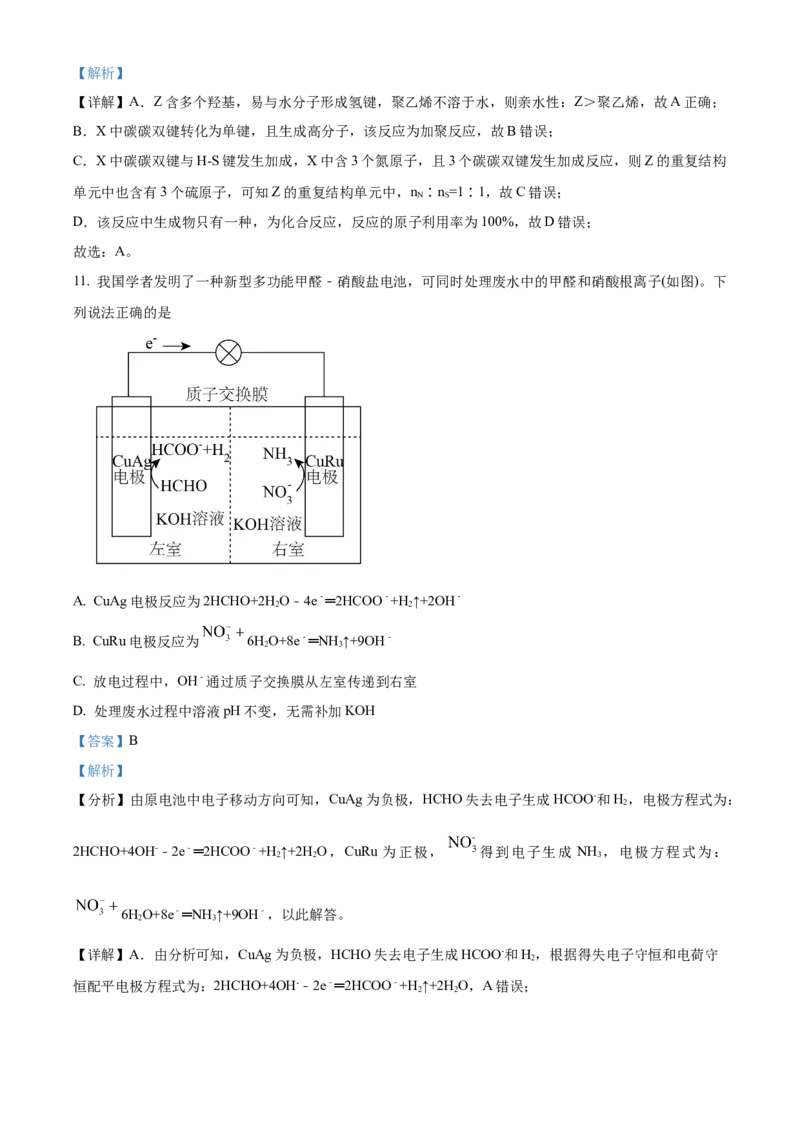
11. 我国学者发明了一种新型多功能甲醛﹣硝酸盐电池,可同时处理废水中的甲醛和硝酸根离子(如图)。下
列说法正确的是
A. CuAg电极反应为2HCHO+2H O﹣4e﹣═2HCOO﹣+H ↑+2OH﹣
2 2
B. CuRu电极反应为 6HO+8e﹣═NH ↑+9OH﹣
2 3
C. 放电过程中,OH﹣通过质子交换膜从左室传递到右室
D. 处理废水过程中溶液pH不变,无需补加KOH
【答案】B
【解析】
【分析】由原电池中电子移动方向可知,CuAg为负极,HCHO失去电子生成HCOO-和H ,电极方程式为:
2
2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,CuRu 为正极, 得到电子生成 NH ,电极方程式为:
2 2 3
6HO+8e﹣═NH ↑+9OH﹣,以此解答。
2 3
【详解】A.由分析可知,CuAg为负极,HCHO失去电子生成HCOO-和H,根据得失电子守恒和电荷守
2
恒配平电极方程式为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,A错误;
2 2B.由分析可知,CuRu为正极, 得到电子生成NH ,根据得失电子守恒和电荷守恒配平电极方程式
3
为: 6HO+8e﹣═NH ↑+9OH﹣,B正确;
2 3
C.质子交换膜只允许H+通过,C错误;
D.由分析可知,负极电极方程式为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,正极电极方程式为:
2 2
6HO+8e﹣═NH ↑+9OH﹣,总反应为8HCHO+ 7OH-=NH +8HCOO-+4 H ↑+2H O,处理废
2 3 3 2 2
水过程中消耗OH-,溶液pH减小,需补加 KOH,D错误;
故选B。
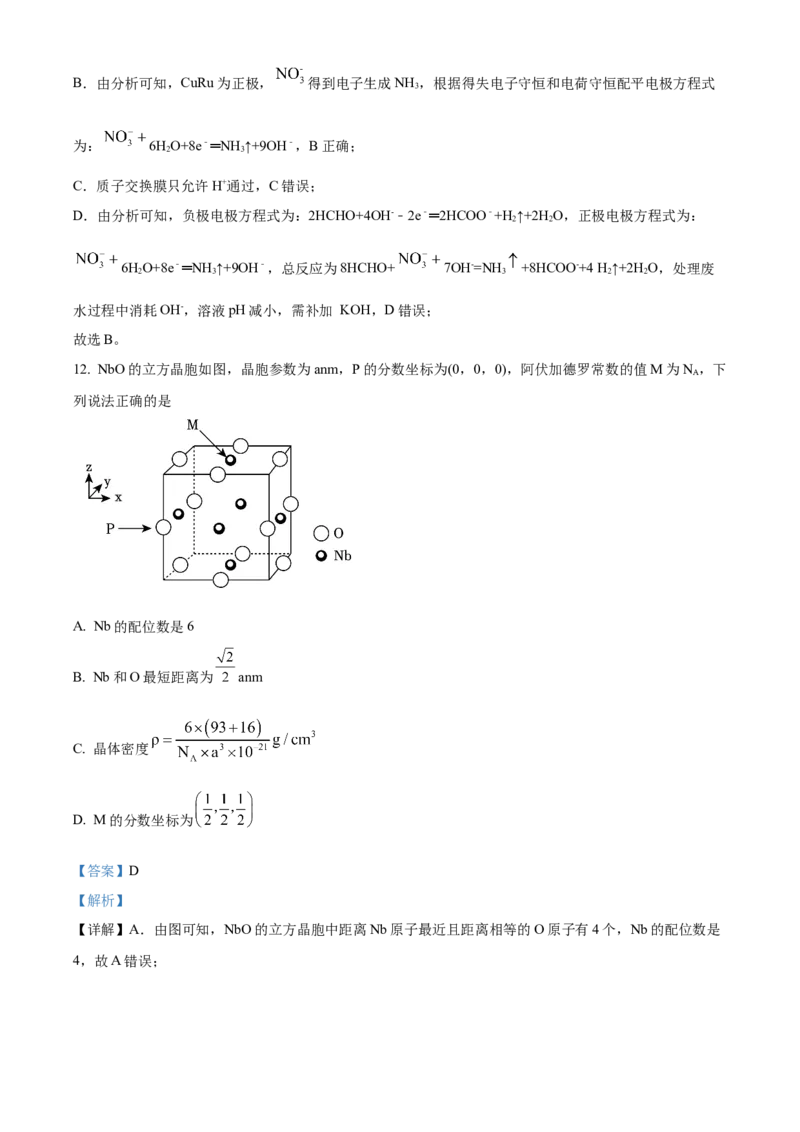
12. NbO的立方晶胞如图,晶胞参数为anm,P的分数坐标为(0,0,0),阿伏加德罗常数的值M为N ,下
A
列说法正确的是
A. Nb的配位数是6
B. Nb和O最短距离为 anm
C. 晶体密度
D. M的分数坐标为
【答案】D
【解析】
【详解】A.由图可知,NbO的立方晶胞中距离Nb原子最近且距离相等的O原子有4个,Nb的配位数是
4,故A错误;B.由图可知,Nb和O最短距离为边长的 ,晶胞参数为anm,Nb和O最短距离为 anm,故B错误;
C.根据均摊法计算可知,Nb的个数为6× =3,O的个数为12× =3,即晶胞中含有3个NbO,晶胞密度
为ρ= ,故C错误;
D.P 的分数坐标为(0,0,0),M位于正方体的面心,M的分数坐标为( , , ),故D正确;
故选:D。
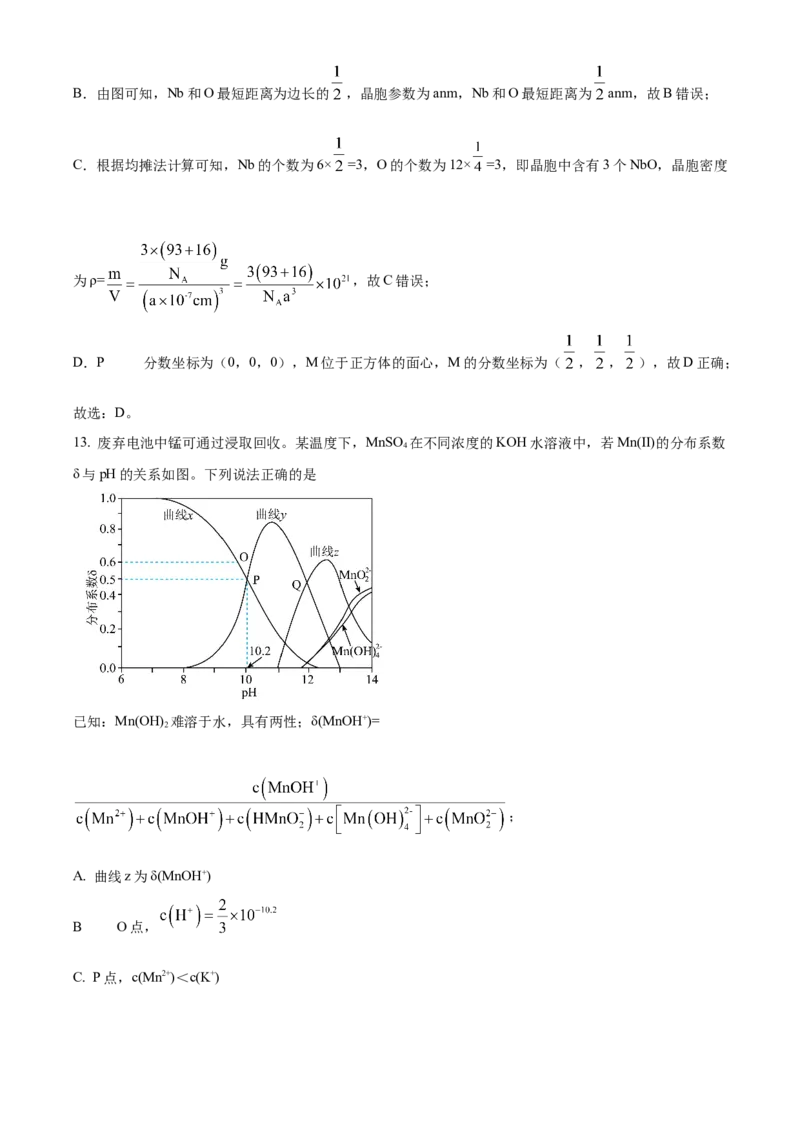
13. 废弃电池中锰可通过浸取回收。某温度下,MnSO 在不同浓度的KOH水溶液中,若Mn(Ⅱ)的分布系数
4
δ与pH的关系如图。下列说法正确的是
已知:Mn(OH) 难溶于水,具有两性;δ(MnOH+)=
2
;
A. 曲线z为δ(MnOH+)
.
B O点,
C. P点,c(Mn2+)<c(K+)D. Q点,c( )=2c(MnOH+)+2c( )
【答案】C
【解析】
【分析】Mn(OH) 难溶于水,具有两性,某温度下,MnSO 在不同浓度的KOH水溶液中,若Mn(Ⅱ)的分
2 4
布系数δ与pH的关系如图,结合曲线变化和分布分数可知,pH较小时,Mn元素存在形式为Mn2+,则曲
线x为Mn2+,曲线y为MnOH+,曲线z为 ,结合图象变化分析判断选项。
【详解】A.分析可知,z表示δ( ),故A错误;
B.图中 O 点存在电离平衡 Mn2++OH﹣⇌MnOH+,在 P 点时 c(Mn2+)=c(MnOH+),pH=10.2,K
103.8,O点δ(Mn2+)=0.6时,δ(MnOH+)=0.4,则
c(OH﹣) 10﹣3.8mol/L 10﹣3.8mol/L,则 ,故B错误;
C.P 点时 δ(Mn2+)=δ(MnOH+)=0.5,溶液中含 Mn 元素微粒只有这两种,根据物料守恒有 c(Mn2+)
+c(MnOH+)=c( ) , 且 c(Mn2+) = c(MnOH+)① 即 2c(Mn2+)=c( )② , 根 据 电 荷 守 恒 有
③ , 将 ① 和 ② 代 入 ③ 得 到
,此时pH=10.2, 则c(Mn2+)<c(K+),故C正确;
D.Q点时,根据图像溶液中存在,物料守恒:c( )=c(Mn2+)+c(MnOH+)+c( )+c( )+c[
],且c(MnOH+)=c( ),c( )=c[ ],则c( )=c(Mn2+)+2c(MnOH+)
+2c( ) ,故c( )>2c(MnOH+)+2c( ) ,故D错误;
故选C。
14. 白色固体样品X,可能含有AgNO、NH NO 、BaCl 、KCl、NaSO 、NaCO、Al O 之中的几种或全
3 4 3 2 2 3 2 3 2 3部。在三个烧杯中各加入适量X。分别加入足量以下三种试剂并微热使之充分反应,实验记录为:
编号 试剂 反应后的不溶物 生成的气体
Ⅰ 蒸馏水 白色 无色、有刺激性气味
Ⅱ 稀盐酸 白色 无色、无味
Ⅲ NaOH溶液 无不溶物 无色、有刺激性气味
依据实验现象,下列说法正确的是
A. 可能含Al O B. 含BaCl C. 含NaSO D. 不含KCl
2 3 2 2 3
【答案】A
【解析】
【分析】白色固体样品X,可能含有AgNO 、NH NO 、BaCl 、KCl、NaSO 、NaCO 、Al O 之中的几种
3 4 3 2 2 3 2 3 2 3
或全部,在三个烧杯中各加入适量X,分别加入足量以下三种试剂并微热使之充分反应,Ⅰ.加入蒸馏水,
微热生成无色有刺激性气味的气体,是微热条件下铵根离子和弱酸根离子发生的双水解反应生成了氨气和
气体,说明一定含NH NO ,反应生成白色沉淀,白色沉淀可能为氧化铝,也可能为 AgNO 和NaSO 、
4 3 3 2 3
NaCO 反应生成的Ag SO 或Ag CO 沉淀,或BaCl 和NaSO 、NaCO 反应生成的BaSO 、BaCO 沉淀,
2 3 2 3 2 3 2 2 3 2 3 3 3
Ⅱ.加入稀盐酸反应后的不溶物为白色沉淀,同时生成的气体为无色无味气体,为二氧化碳气体,说明一
定含NaCO ,一定不含NaSO ,白色沉淀可能为AgNO 生成的AgCl,可能含AgNO 、BaCl ,可能存在
2 3 2 3 3 3 2
Al O ;Ⅲ.加入NaOH溶液,无沉淀,有无色刺激性气味的气体生成,说明一定含 NH NO ,可能含
2 3 4 3
AgNO、BaCl 、KCl、NaSO 、NaCO、Al O,据此分析判断。
3 2 2 3 2 3 2 3
【详解】A.分析可知,可能含Al O,故A正确;
2 3
B.分析可知,固体中可能含BaCl ,故B错误;
2
C.加入盐酸生成气体为无色无味,说明不含NaSO ,故C错误;
2 3
D.上述过程中的分析可知,KCl的存在不能确定,故D错误;
故选A。
二、非选择题:本题共4小题,共58分。
15. 稀土是国家的战略资源之一。以下是一种以独居石【主要成分为CePO 含有Th(PO )、UO 和少量镭
4. 3 4 4 3 8
杂质】为原料制备CeCl •nH O的工艺流程图。
3 2已知:ⅰ.K [Th(OH) ]=4.0×10﹣45,K [Ce(OH) ]=1.6×10﹣20,K [Ce(OH) ]=2.0×10﹣48
sp 4 sp 3 sp 4
ⅱ.镭为第ⅡA族元素
回答下列问题:
(1)关于独居石的热分解,以下说法正确的是 _______(填标号)。
a.降低压强,分解速率增大 b.降低温度,分解速率降低
c.反应时间越长,分解速率越大 d.提高搅拌速度,分解速率降低
(2)NaUO 中铀元素的化合价为 _______,热分解阶段UO 生成NaUO 的化学反应方程式为 _______。
2 2 7 3 8 2 2 7
(3)浓缩结晶后,得到的晶体产物化学式为 _______,滤液可用于 _______阶段循环利用,避免产生大
量的高碱度废水。
(4)溶解阶段,将溶液pH先调到1.5~2.0,反应后再回调至4.5。
①盐酸溶解Ce(OH) 的离子方程式为 _______。
4
②当溶液pH=4.5时,c(Th4+)=_______mol/L,此时完全转化为氢氧化钍沉淀。
(5)以BaSO 为载体形成共沉淀,目的是去除杂质 _______。
4
【答案】(1)b (2) ①. +6 ②. 2UO+O +6NaOH=3NaUO+3H O
3 8 2 2 2 7 2
(3) ①. NaPO •12HO ②. 热分解
3 4 2
(4) ①. 2Ce(OH) +8H++2Cl﹣=2Ce3++Cl↑+8H O ②. 4×10﹣7
4 2 2
(5)RaSO
4
【解析】
【分析】独居石的主要成分为CePO ,含有Th(PO ) 、UO 和少量镭杂质,加入55~60%的NaOH进行热
4 3 4 4 3 8
分解,UO 发生反应:2UO+O +6NaOH=3NaUO+3H O,转化为NaUO ,CePO 中的Ce被氧化为
3 8 3 8 2 2 2 7 2 2 2 7 4
Ce(OH) ,将热分解后的物质加水稀释后过滤,得到的滤液中含有Na+、 ,滤液浓缩结晶后,得到的
4
晶体化学式为:NaPO •12H O,滤液可用于热分解阶段循环利用,避免产生大量的高碱度废水,过滤得到
3 4 2
的固体产物中加入盐酸和凝聚剂,Ce(OH) 具有氧化性,与盐酸发生反应:2Ce(OH) +8H++2Cl﹣=2Ce3+
4 4
+Cl↑+8H O,废气为Cl ,调节pH,使铀和Th进入沉淀,向滤液中加入硫酸铵和氯化钡,使 BaSO 和
2 2 2 4
RaSO 形成共沉淀,得到含有Ce3+的溶液,经过一系列操作,得到CeCl •nH O,据此分析作答。
4 3 2
【小问1详解】
a.降低压强,分解速率降低,故a错误;
b.降低温度,分解速率降低,故b正确;
c.反应时间越长,分解速率逐渐变慢,故c错误;
d.提高搅拌速度,分解速率加快,故d错误;
故答案为b;【小问2详解】
NaUO 中Na为+1价,O为﹣2价,根据化合价代数和为0,则铀元素的化合价为+6价,热分解阶段UO
2 2 7 3 8
生成NaUO 的化学反应方程式为:2UO+O +6NaOH=3NaUO+3H O
2 2 7 3 8 2 2 2 7 2
【小问3详解】
稀释过滤后的滤液中含有Na+、 ,滤液浓缩结晶后,得到的晶体产物化学式为:NaPO •12HO,滤液
3 4 2
可用于热分解阶段循环利用,避免产生大量的高碱度废水;
【小问4详解】
①根据后续流程可知,生成+3价Ce,则盐酸溶解Ce(OH) 发生氧化还原反应,其离子方程式为:
4
2Ce(OH) +8H++2Cl﹣=2Ce3++Cl↑+8H O;
4 2 2
②当溶液 pH=4.5 时,c(H+)=1×10﹣4.5mol/L,c(OH﹣)=1×10﹣9.5mol/L,c(Th4+)×c4(OH﹣)=4.0×10﹣45,则
c(Th4+)=4×10﹣7 mol/L,此时完全转化为氢氧化钍沉淀;
【小问5详解】
以BaSO 为载体形成共沉淀,目的是去除杂质RaSO,RaSO 的溶解度更小。
4 4 4
的
16. 石油开采 天然气含有HS。综合利用天然气制氢是实现“碳中和”的重要途径。CH 和HS重整
2 4 2
制氢的主要反应如下:
反应Ⅰ:CH(g)+2HS(s) CS(g)+4H(g) ΔH =+260kJ/mol
4 2 2 2 1
反应Ⅱ:CH
4
(g) C(s)+2⇌H
2
(g) ΔH
2
=+90kJ/mol
反应Ⅲ:2H
2
S(g⇌) S
2
(g)+2H
2
(g) ΔH
3
=+181kJ/mol
回答下列问题:⇌
(1)HS分子的电子式为 _______。
2
(2)反应Ⅳ:CS(g)⇌S(g)+C(s)ㅤΔH=_______kJ/mol。
2 2 4
(3)保持反应器进料口总压为100kPa.分别以8kPaCH、24kPaHS(He作辅气)与25kPaCH、75kPaHS进
4 2 4 2
料。CH 平衡转化率与温度的关系如图1,含有He的曲线为 _______,理由是 _______。
4
(4)假设在10L的恒温刚性容器中,通入0.3mol CH 和0.15mol H S发生反应Ⅰ、Ⅱ和Ⅲ,起始总压为
4 2P CH 和HS的转化率与时间的关系如图2,0~5min内H 的化学反应速率为 _______mol/(L•min);5min
0. 4 2 2
时,容器内总压为 _______。
(5)假设HS和CH 的混合气体在某固体催化剂上的吸附服从Langmuir等温吸附(吸附分子彼此不发生相
2 4
互作用,且气体分子为单分子层吸附)。吸附等温式为: 。其中
a是气体的吸附系数,V 是气体在固体表面的饱和吸附量(标态),P是气体的分压,V是气体分压为P时的
m
平衡吸附量(标态)。在一定温度下,HS的吸附系数是CH 的4倍,当HS的分压为2MPa及4MPa,CH
2 4 2 4
和HS的分压相同时,HS平衡吸附量分别为0.6m3/kg和0.8m3/kg(已换算成标态),则HS的吸附系数为
2 2 2
_______MPa﹣1。
(6)与传统天然气制氢中需要脱硫将HS转化为硫黄和水相比,上述方法优点是 _______。
2
【答案】(1) (2)+11
(3) ①. M ②. 总压一定,充入氦气,反应物分压减小,相当于减压,反应Ⅰ、Ⅱ均正向移动,
CH 平衡转化率增大
4
(4) ①. 1.2×10-3 ②. P
0
(5)0.4 (6)HS得到了综合利用,3步反应均生成了H
2 2
【解析】
【小问1详解】
HS为共价化合物,其电子式为 ;
2
【小问2详解】
根据盖斯定律可知,反应Ⅱ+Ⅲ﹣Ⅰ=Ⅳ,则CS
2
(g)⇌S
2
(g)+C(s)ㅤΔH
4
=ΔH
2
+ΔH
3
﹣ΔH
1
=(90+181-260)kJ/mol=+11kJ/mol;
【小问3详解】
保持反应器进料口总压为100kPa。分别以8kPaCH、24kPaHS(He作辅气)与25kPaCH、75kPaHS进料。
4 2 4 2
CH 平衡转化率与温度的关系如图1,含有He的曲线为M,理由是总压一定,充入氦气,反应物分压减小,
4
相当于减压,反应Ⅰ、Ⅱ均正向移动,CH 平衡转化率增大
4
【小问4详解】
由图可知,0~5min内消耗的CH 为0.3mol×5%=0.015mol,消耗的HS为0.15mol×20%=0.03mol,根据
4 2
氢原子守恒,则生成H 的物质的量为n(H )=2×0.015mol+0.03=0.06mol,0~5min内H 的化学反应速率为
2 2 2
v(H ) 1.2×10-3mol/(L•min);
2
设反应Ⅰ转化了xmolCH ,则反应Ⅱ转化了(0.015-x)molCH ,反应Ⅰ转化了2xmolH S,反应Ⅲ转化了(0.03-
4 4 2
2x) molHS,列三段式有
2
,5min时,n(CH)=0.285mol,n(H S)=0.12mol,
4 2
n(H )=0.06mol,n(CS)=xmol,n(S )=(0.015-x)mol,n(总)=0.48mol,起始总压为P,气体总量为0.45mol,
2 2 2 0
根据压强之比等于物质的量之比,可得5min时,容器内总压为 ×P = P;
0 0
【小问5详解】根据题意可知方程:① ,②
,联立方程①与②,解得:α =0.4MPa﹣1;
1
【小问6详解】
与传统天然气制氢中需要脱硫将HS转化为硫黄和水相比,上述方法优点是HS得到了综合利用,3步反
2 2
应均生成了H。
2
17. 一种可用于温度传感的红色配合物Z,其制备实验步骤及传感原理如图(反应物均按化学计量数之比进
行投料):
Ⅰ.将Ni(NO )•6H O和去离子水加入圆底烧瓶中,搅拌至完全溶解,再依次加入乙酰丙酮(HY)、无水
3 2 2
NaCO 和N,N,N'﹣三甲基乙二胺(X)溶液,继续搅拌5min;
2 3
Ⅱ.加入NaB(C H) 溶液,立即生成红色沉淀,室温下继续反应35min;
6 5 4
Ⅲ.减压过滤,用去离子水洗涤3次,烘干,重结晶,得到配合物Z;
Ⅳ.室温下,将适量Z溶于丙酮(L),温度降至15℃,溶液经混合色逐渐转为蓝绿色,得到配合物W的溶
液。
回答下列问题:
(1)已知配合物Z中Ni、N和O五个原子共平面,Ni2+的杂化方式 _______(填“是”或“不是”)sp3。
(2)步骤Ⅰ中,加入NaCO 的目的是 _______。
2 3
(3)步骤Ⅱ中,为避免沉淀包裹反应物共沉,可采取的操作是 _______。
(4)步骤Ⅲ中,洗涤去除的无机盐产物是 _______。
(5)采用EDTA配位滴定法测定Ni的含量。实验步骤如下:
ⅰ.准确称取mg的配合物Z;
ⅱ.加入稀硝酸使样品完全消解,再加入去离子水,用20%醋酸钠溶液调节pH至4~5;
ⅲ.以PAN为指示剂,用cmol/LEDTA标准溶液滴定,平行测定三次,平均消耗EDTA体积VmL。
已知:EDTA与Ni2+化学计量数之比为1:1①除了滴定管外,上述测定实验步骤中,使用的仪器有 _______(填标号)。
②Ni的质量百分含量为 _______%。
(6)利用上述配合物的变色原理(温差约10℃时,颜色有明显变化),设计一种实用温度传感装置 _______。
【答案】(1)不是 (2)中和X与HY反应生成的 ,使平衡正向移动,有利于Z的生成
(3)充分搅拌、剧烈振荡
(4)
(5) ①. bcd ②.
的
(6)具有温度指示功能 水杯,水杯外壁涂有配位化合物W(含少量丙酮)并以透明材料密封,并附有
比色卡,水温可通过所示颜色与比色卡比较,大致判断,是否适合饮用
【解析】
【 分 析 】 红 色 配 合 物 Z 的 制 备 实 验 步 骤 及 传 感 原 理 为 :
, 将
Ni(NO )•6H O和去离子水加入圆底烧瓶中,搅拌至完全溶解,再依次加入乙酰丙酮(HY)、无水NaCO 和
3 2 2 2 3
N,N,N'﹣三甲基乙二胺(X)溶液,继续搅拌5min,加入 的目的是中和X与HY反应生成的 ,
使平衡正向移动,有利于Z的生成,加入NaB(C H) 溶液,立即生成红色沉淀,室温下继续反应35min,
6 5 4
再经过减压过滤、洗涤、干燥得到配合物Z。
【小问1详解】
已知配合物Z中Ni、N和O五个原子共平面, 的杂化方式为 杂化,不是 杂化。【
小问2详解】
步骤Ⅰ中,加入 的目的是中和X与HY反应生成的 ,使平衡正向移动,有利于Z的生成。
【小问3详解】
步骤Ⅱ中,为避免沉淀包裹反应物共沉,可采取的操作是充分搅拌、剧烈振荡。
【小问4详解】
步骤Ⅰ和Ⅱ中,引入了 和 ,则步骤Ⅲ中,洗涤去除的无机盐产物是 。
【小问5详解】
①称取mg的配合物Z需要电子天平,加去离子水可以使用洗瓶,滴定过程需要用到滴定管和锥形瓶,所
以上述测定实验步骤中,使用的仪器除了滴定管外,还有天平、锥形瓶、洗瓶;故选bcd;
②根据题意有关系式: ,则 ,所以Ni的质量百
分含量为 。
【小问6详解】
利用上述配合物的变色原理(温差约 时,颜色有明显变化),设计一种实用温度传感装置,该装置可
以是具有温度指示功能的水杯,水杯外壁涂有配位化合物W(含少量丙酮)并以透明材料密封,并附有比色
卡,水温可通过所示颜色与比色卡比较,大致判断,是否适合饮用。
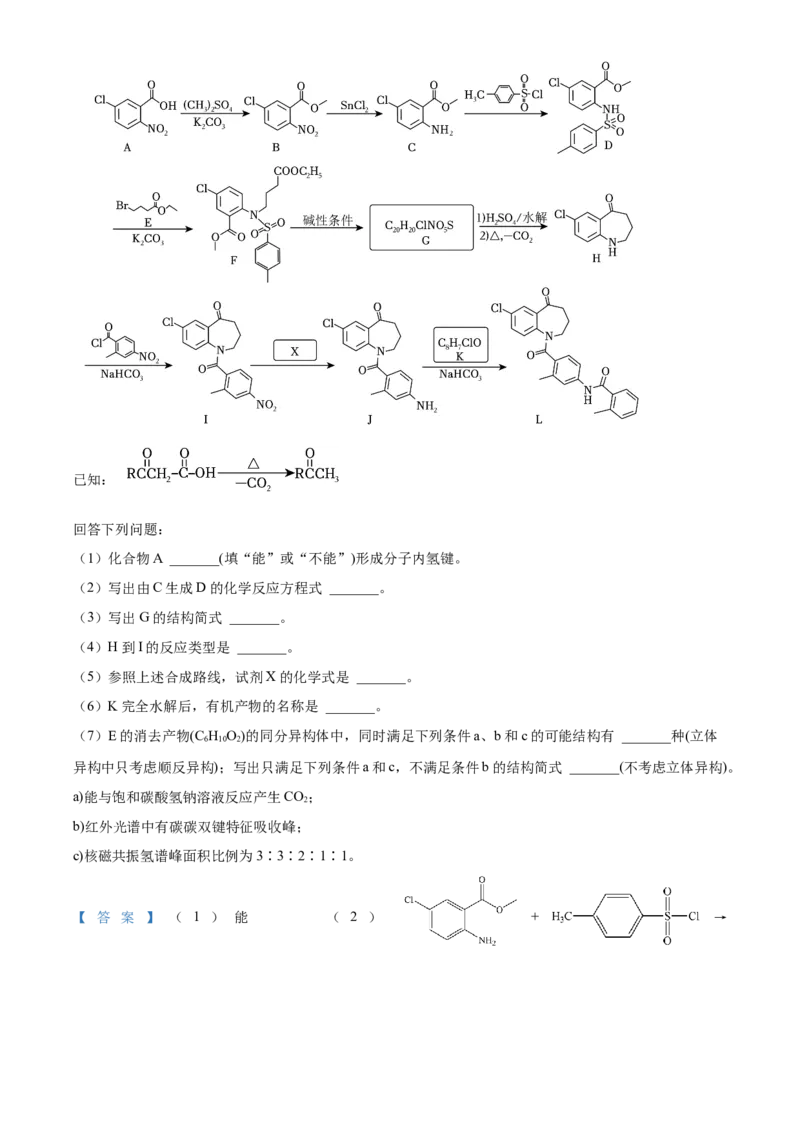
18. 托伐普坦是一种治疗心血管疾病的药物,其前体(L)合成步骤如图(部分试剂和条件略去)。已知:
回答下列问题:
(1)化合物A _______(填“能”或“不能”)形成分子内氢键。
(2)写出由C生成D的化学反应方程式 _______。
(3)写出G的结构简式 _______。
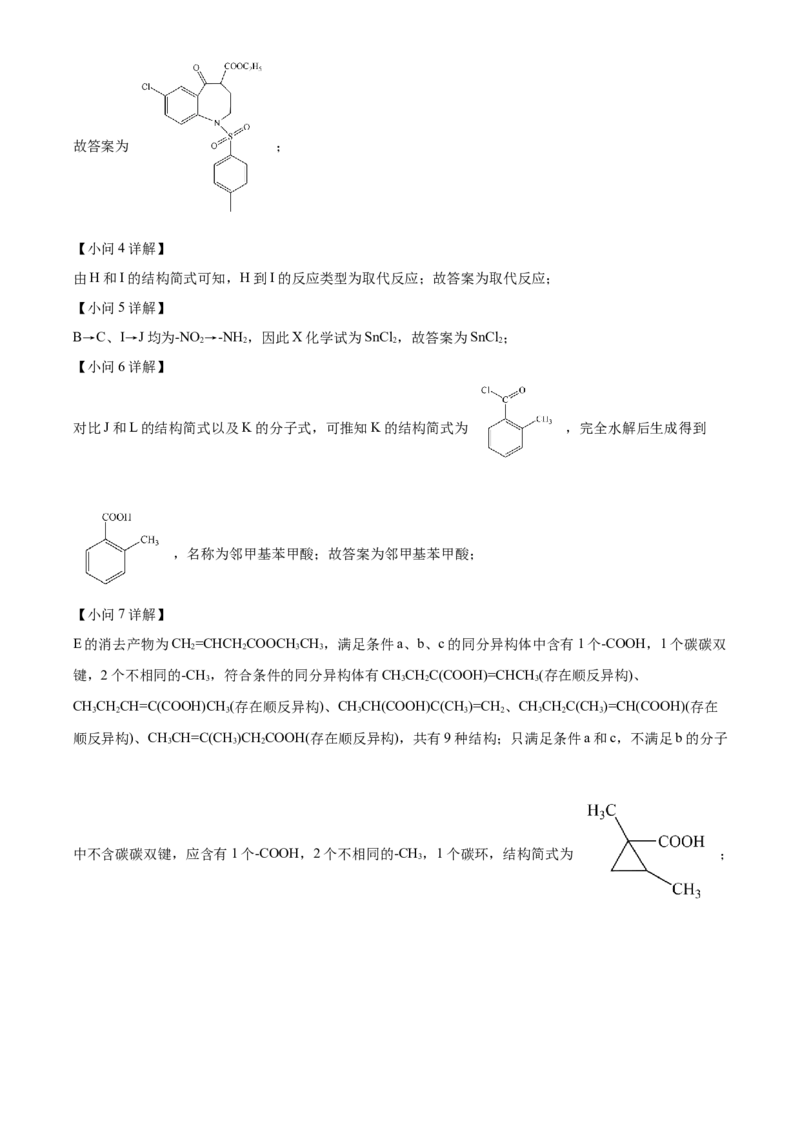
(4)H到I的反应类型是 _______。
(5)参照上述合成路线,试剂X的化学式是 _______。
(6)K完全水解后,有机产物的名称是 _______。
(7)E的消去产物(C H O)的同分异构体中,同时满足下列条件a、b和c的可能结构有 _______种(立体
6 10 2
异构中只考虑顺反异构);写出只满足下列条件a和c,不满足条件b的结构简式 _______(不考虑立体异构)。
a)能与饱和碳酸氢钠溶液反应产生CO;
2
b)红外光谱中有碳碳双键特征吸收峰;
c)核磁共振氢谱峰面积比例为3∶3∶2∶1∶1。
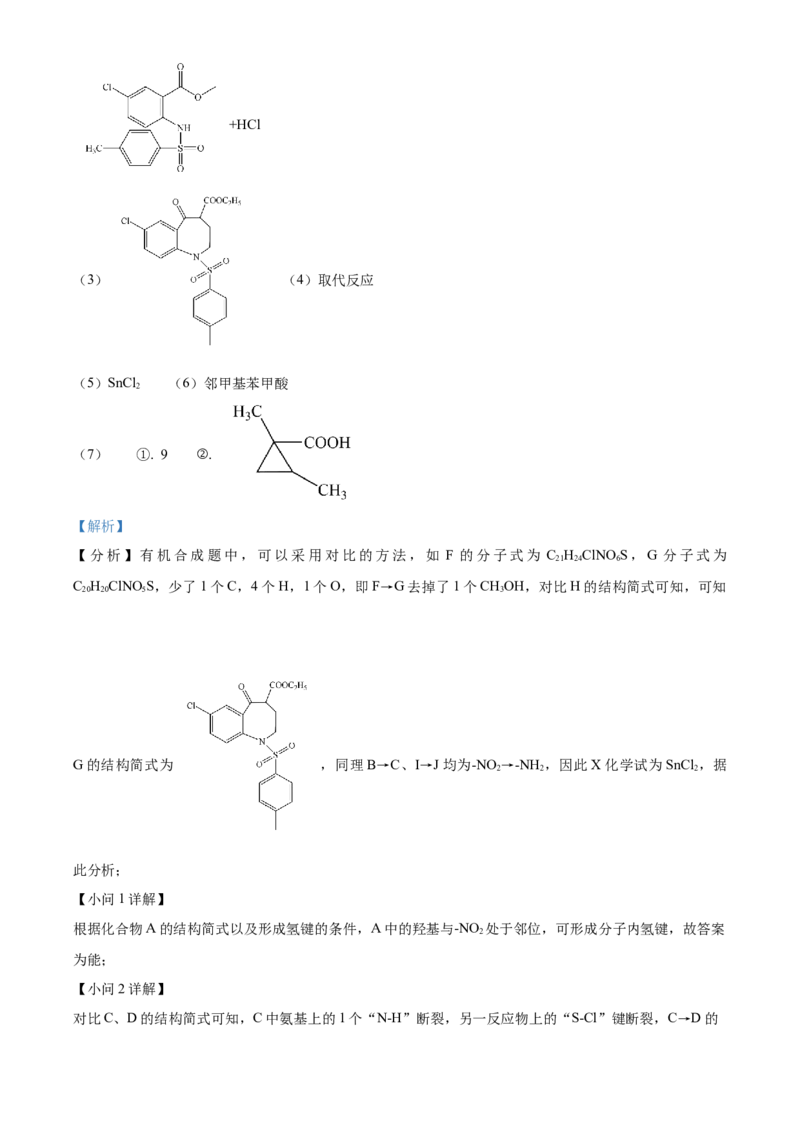
【 答 案 】 ( 1 ) 能 ( 2 ) + →+HCl
(3) (4)取代反应
(5)SnCl (6)邻甲基苯甲酸
2
(7) ①. 9 ②.
【解析】
【分析】有机合成题中,可以采用对比的方法,如 F 的分子式为 C H ClNOS,G 分子式为
21 24 6
C H ClNOS,少了1个C,4个H,1个O,即F→G去掉了1个CHOH,对比H的结构简式可知,可知
20 20 5 3
G的结构简式为 ,同理B→C、I→J均为-NO →-NH ,因此X化学试为SnCl ,据
2 2 2
此分析;
【小问1详解】
根据化合物A的结构简式以及形成氢键的条件,A中的羟基与-NO 处于邻位,可形成分子内氢键,故答案
2
为能;
【小问2详解】
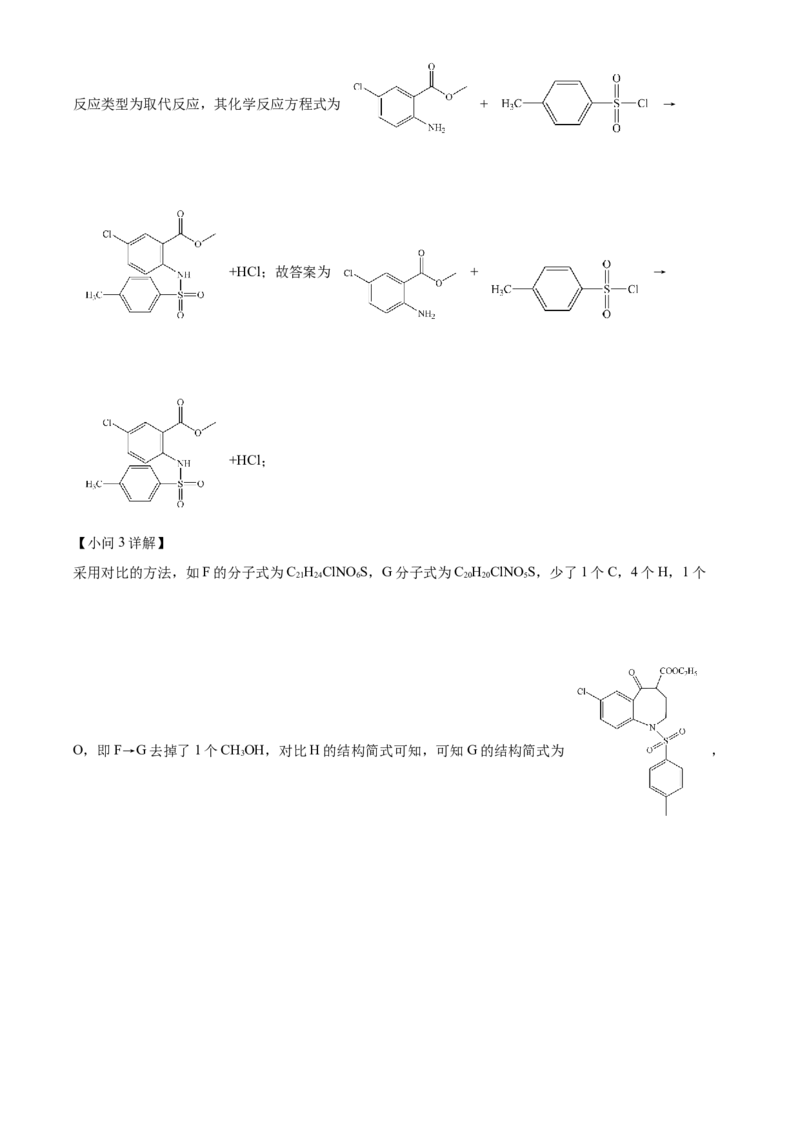
对比C、D的结构简式可知,C中氨基上的1个“N-H”断裂,另一反应物上的“S-Cl”键断裂,C→D的反应类型为取代反应,其化学反应方程式为 + →
+HCl;故答案为 + →
+HCl;
【小问3详解】
采用对比的方法,如F的分子式为C H ClNOS,G分子式为C H ClNOS,少了1个C,4个H,1个
21 24 6 20 20 5
O,即F→G去掉了1个CHOH,对比H的结构简式可知,可知G的结构简式为 ,
3故答案为 ;
【小问4详解】
由H和I的结构简式可知,H到I的反应类型为取代反应;故答案为取代反应;
【小问5详解】
B→C、I→J均为-NO →-NH ,因此X化学试为SnCl ,故答案为SnCl ;
2 2 2 2
【小问6详解】
对比J和L的结构简式以及K的分子式,可推知K的结构简式为 ,完全水解后生成得到
,名称为邻甲基苯甲酸;故答案为邻甲基苯甲酸;
【小问7详解】
E的消去产物为CH=CHCHCOOCH CH,满足条件a、b、c的同分异构体中含有1个-COOH,1个碳碳双
2 2 3 3
键,2个不相同的-CH,符合条件的同分异构体有CHCHC(COOH)=CHCH (存在顺反异构)、
3 3 2 3
CHCHCH=C(COOH)CH (存在顺反异构)、CHCH(COOH)C(CH )=CH 、CHCHC(CH)=CH(COOH)(存在
3 2 3 3 3 2 3 2 3
顺反异构)、CHCH=C(CH )CHCOOH(存在顺反异构),共有9种结构;只满足条件a和c,不满足b的分子
3 3 2
中不含碳碳双键,应含有1个-COOH,2个不相同的-CH,1个碳环,结构简式为 ;
3故答案为9; 。